
- •Бабенко м. О.
- •Тема 4. Механіка твердого тіла.
- •Тема 5. Закони збереження.
- •Тема 6. Механічні коливання.
- •Тема 7. Механічні хвилі.
- •Тема 8. Спеціальна теорія відносності.
- •Тема 1. Вступ до молекулярної фізики і термодинаміки.
- •Тема 7. Властивості реальних газів, рідин, твердих тіл.
- •Тема 8. Фазові переходи.
- •Задачі для самостійного розв’язування
- •Кінематика обертального руху.
- •Використання законів динаміки для знаходження прискорення точки
- •Теоретичні відомості
- •Задачі для самостійного розв’язування
- •Тема 3 Динаміка руху точки по колу. Рух тіла зі змінною масою Теоретичні відомості
- •Задачі для самостійного розв’язування
- •Закон збереження механічної енергії.
- •Консервативні і неконсервативні сили
- •Теоретичні відомості
- •Задачі для самостійного розв’язування
- •Тема 5 Закон збереження імпульсу. Теорія пружних і непружних зіткнень Теоретичні відомості
- •Задачі для самостійного розв’язування
- •Тема 6 Динаміка обертального руху тіла. Умови рівноваги тіла Теоретичні відомості
- •Задачі для самостійного розв’язування
- •Механічні властивості твердих тіл. Закон Гука.
- •Елементи гідродинаміки. Закон Бернуллі
- •Теоретичні відомості
- •Задачі для самостійного розв’язування
- •Тема 8 Перший закон термодинаміки. Внутрішня енергія і засоби її зміни. Теоретичні відомості
- •Задачі для самостійного розв’язування
- •Тема 9 Теплові двигуни та холодильні машини Теоретичні відомості
- •Задачі для самостійного розв’язування
- •Тема 10 Основне рівняння мкт. Явища переносу Теоретичні відомості
- •Задачі для самостійного розв’язування
- •Приклади розв’язування задач
- •Питання до заліку
- •Правила оформлення контрольної роботи
- •Завдання до контрольної роботи
- •Список рекомендованої літератури
Задачі для самостійного розв’язування
Густина ρ суміші азоту й водню при температурі t=47ºС і тиску p=2,05 кПа становить 0,3 кг/м3. Яка концентрація водню Н2 в суміші?
Атмосферне повітря містить переважно кисень, азот і аргон. Визначити кількість молекул n цих газів та їхні маси в одиниці об’єму за нормальних умов, коли відомо, що кількість молекул азоту в 4 рази більша, а аргону в 20 разів менша від кількості молекул кисню.
У посудині місткістю V=2 л знаходиться m=2 г гідриду урану UH3. При нагріванні до температури Т=673 К гідрид повністю розпадається на уран, відносна атомна маса якого Аr=238, та атомний водень. Визначити тиск водню посудині при цій температурі.
У циліндрі під поршнем міститься газ за нормальних умов. Спочатку при Т=const об’єм газу збільшили у β=5 разів, потім газ нагріли при р=const до температури t=127ºC. Визначити концентрацію n в кінцевому стані.
До якої температури Т потрібно нагріти ідеальний газ при р=const, щоб його густина зменшилась у два рази порівняно з густиною цього газу, коли t0=0 С°?
Електрична лампа розжарювання, об’єм якої V=500 м3 наповнена азотом під тиском р=9∙104 Па. Яка маса води m увійде в лампу, якщо в ній зробити отвір під водою при нормальному атмосферному тиску?
У відкритій посудині при t1=20°С міститься m1=150 г повітря. На яке значення Δm зменшиться маса повітря в посудині уразі нагрівання її до t2=100°С? Зміною розмірів посудини під час нагрівання нехтувати.
Суміш газів, що перебуває під тиском p=1,02∙105 Па, містить m1=16 г кисню та m2=4 г гелію. Температура суміші Т=280 К. Обчислити концентрацію n молекул суміші та її густину ρ.
Швидкість відкачування роторного масляного насоса Q=1,5∙10–4 м3/с. Який час потрібен для того, щоб повітря в посудині місткістю V=5 л відкачати від нормального атмосферного тиску до тиску р=1,33 Па?
У посудині, об’єм якої V=20 л, міститься m1=5 г водню та m2=10 г азоту при температурі Т=290 К. Визначити тиск у посудині, молярну масу та густину суміші газів.
На дні озера, глибина якого h=20 м, температура води t1=7°С. Бульбашка повітря, яка на дні озера має об’єм V1=2 мм3, повільно піднімається. Який об’єм V матиме бульбашка повітря біля поверхні води, якщо атмосферний тиск нормальний, а температура біля поверхні води t2=19°С? Тиском, що мовлений поверхневим натягом, нехтувати.
Приклади розв’язування задач
Задача 1. Рівняння руху тіла масою m мають вигляд:
![]()
де A, B, C, D – постійні величини.
Визначити значення швидкості υ, прискорення a, сили F і кінетичної енергії Ek у момент часу t = τ.
Розв’язок.
Значення
швидкості тіла:
![]()
![]() ,
,
![]()
Прискорення:
![]() ,
,![]()
![]()
![]() .
.
Сила,
що діє на тіло:
![]()
![]() ,
,![]()
![]() .
.
Кінетична
енергія тіла:
![]() ,
,
![]() .
.
Задача 2. Обруч (куля, циліндр), що має масу m і радіус R котиться без прослизання зі швидкість υ. Визначити його кінетичну енергію. Тертям катання зневажити.
Розв’язок. Кінетична енергія тіла в даному випадку визначається по теоремі Кьоніга:
![]() ,
,
де
![]() - момент інерції тіла щодо осі, що
проходить через центр інерції, коефіцієнтk
залежить від форми тіла. У даному випадку:
k
=1 – для обруча,
k
=
- момент інерції тіла щодо осі, що
проходить через центр інерції, коефіцієнтk
залежить від форми тіла. У даному випадку:
k
=1 – для обруча,
k
=![]() - для кулі,
k
=
- для кулі,
k
=![]() – для циліндра.
– для циліндра.
![]() .
.
Кутова
і лінійна швидкості зв'язані співвідношенням:
![]() ,
отже: для обруча
,
отже: для обруча
![]()
![]() ,
для кулі
,
для кулі
![]()
![]() ,
для циліндра
,
для циліндра![]() .
.
Задача 3. У судині обсягом V знаходиться суміш m1 газу з молярною масою M 1 і m2 гази з молярною масою M2 при температурі T . Визначити тиск p і молярну масу суміші газів M . Універсальна газова постійна R = 8,31 Дж/(моль·К).
Розв’язок. Запишемо рівняння Менделєєва – Клапейрона для кожного з газів:
![]() ,
,
![]() ,
,
де
![]() - парціальний тиск першого газу,
- парціальний тиск першого газу,![]() - другого. За законом Дальтона тиск
суміші дорівнює сумі парціальних тисків
складову суміш газів:
- другого. За законом Дальтона тиск
суміші дорівнює сумі парціальних тисків
складову суміш газів:![]() ,
,
![]() ;
;
![]() .
.
Молярна
маса суміші:
![]() ,
де
,
де![]() - число молів першого газу,
- число молів першого газу,![]() - другого. Молярна маса суміші:
- другого. Молярна маса суміші:
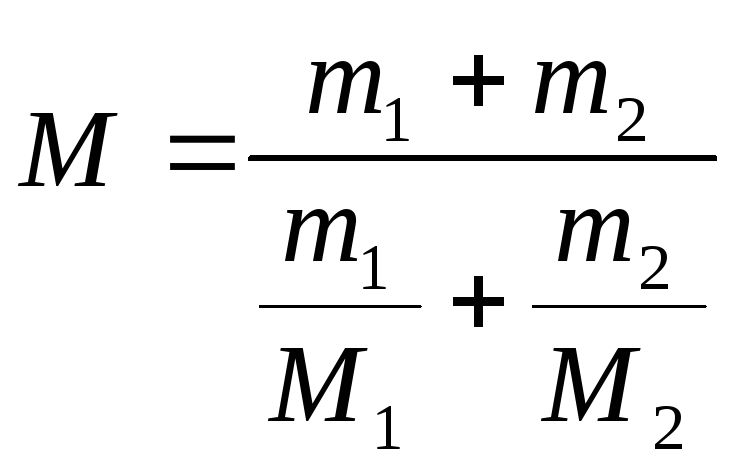 .
.
Задача 4. Обсяг газу, що знаходиться при тиску p1, збільшився від значення V1 до значення V2. Знайти зміна внутрішньої енергії газу, якщо розширення відбулося:
изобарически; 2) адиабатически.
Розв’язок. По першому початку термодинаміки кількість теплоти Q , передане системі, витрачається на збільшення її внутрішньої енергії ΔU і роботу A, чинену газом проти зовнішніх тіл:
![]() ,
,
![]() ,
,
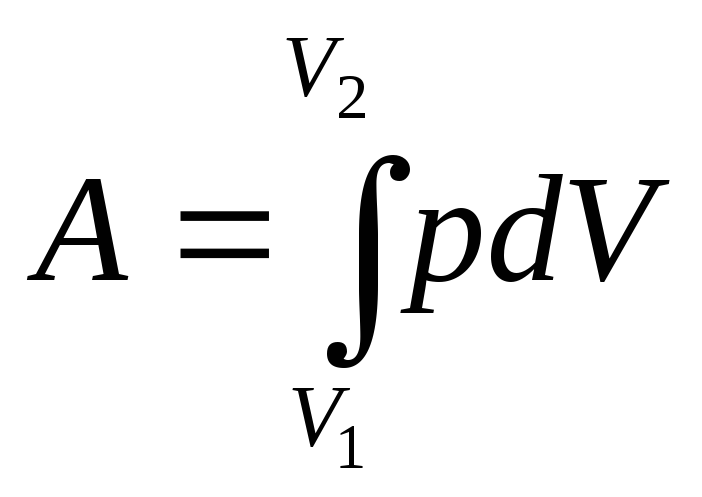 .
.
Число ступенів волі молекули i дорівнює i =3 для одноатомних молекул, i=5 для двохатомних молекул, i=6 для більш складних молекул.
Ізобаричний процес. У цьому випадку тиск постійний
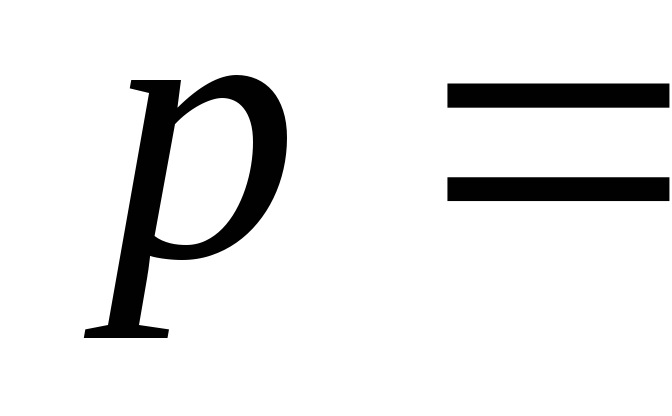 const
=
const
= .
Запишемо рівняння Менделєєва –
Клапейрона для початкового і кінцевого
стану:
.
Запишемо рівняння Менделєєва –
Клапейрона для початкового і кінцевого
стану:
![]() ,
,
![]() .
.
Звідси
випливає:
![]() ,
,
![]() .
.
2)
Адіабатичний
процес. У
цьому випадку теплообмін з навколишнім
середовищем відсутня
![]() Робота відбувається газом за рахунок
убули ег внутрішньої енергії
Робота відбувається газом за рахунок
убули ег внутрішньої енергії![]()
Робота в адіабатичному процесі:

де
![]() - показник адіабати, дорівнює відношенню
молярних (або питомих) теплоємкостей
газу при постійному тиску
- показник адіабати, дорівнює відношенню
молярних (або питомих) теплоємкостей
газу при постійному тиску![]() і постійному обсязі
і постійному обсязі![]() .
.
Оскільки
![]() ,
та зміна внутрішньої енергії:
,
та зміна внутрішньої енергії:
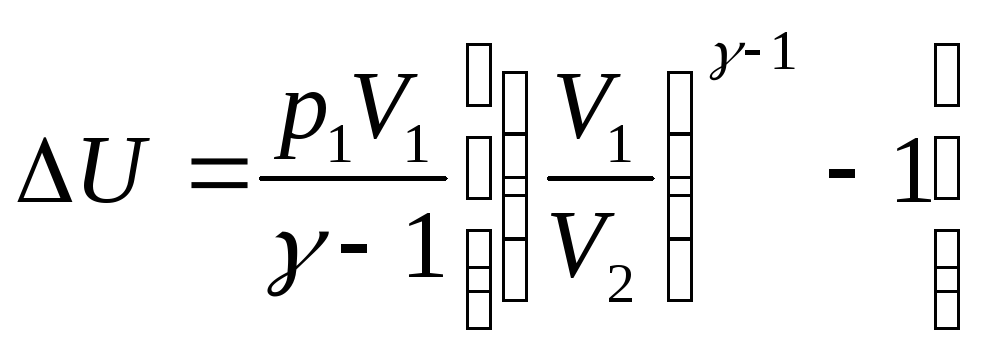 .
.
