
02_Молекулярная_физика
.pdf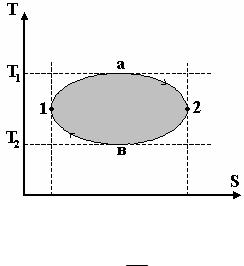
81
Теплообмен в изолированной системе протекает единственным образом: тепло передается от тела с большей температурой к телу с меньшей температурой.
п.2 Максимальный КПД тепловой машины
Рассмотрим цикл в координатах (TS). Разобьем его на участки 12 и 21.
Запишем
dS = dQT , dQ = TdS ,
Q = ∫TdS.
На участке 12 энтропия возрастает, следовательно
Q = ∫2 TdS > 0 ,
1
2
Q1 = ∫TdS ,
1
где Q1 - количество теплоты, полученное рабочим телом. На участке 21 очевидно, что
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Q = ∫TdS < 0 , |
|
|
|
|
|
|||||||||||||||
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Q2 |
= ∫1 |
TdS , |
|
|
|
|
|
|||||||||||||
|
|
|
|
2 |
|
|
|
|
|
|
|
|
. |
|
|
|
|
|
||||
|
|
Q2 |
= − |
|
Q2 |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
Работа, совершаемая за цикл равна |
|
|
|
|
|
|
|
|
|
|
. |
|
|
|
|
|
||||||
КПД цикла равен |
|
A = Q1 − |
|
Q2 |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
Q1 − |
|
Q2 |
|
|
|
|
|
|
|
|
Q2 |
|
|
|||||||
η = |
A |
= |
|
|
=1 |
− |
|
|
. |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Q |
|
Q |
|
|
|
|
|
|
|
Q |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
1 |
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|||

82
Для увеличения КПД нужно уменьшать Q2 и увеличивать Q1 . Пусть T1 , T2 - температуры нагревателя и холодильника. Величина Q1 численно равна площади, ограниченной кривой 1а2. Чтобы ее увеличить, нужно чтобы участок 1а2 шел по прямой T1 . Величина Q2 численно равна площади под кривой 2в1. Для ее уменьшения необходимо, чтобы график шел по прямой T2 . В результате приходим к циклу: 12341.
Участки 12 и 34 это T1 = const и T2 = const , т.е. изотермическое расширение и сжатие. На участках 23 и 41 имеем
dS = 0 , dQ = TdS = 0 ,
dQ = 0 .
Следовательно, это участки адиабатического расширения и сжатия. График 12341 соответствует циклу Карно. Найдем КПД цикла
2 |
2 |
(S2 −S1 )> 0 , |
Q1 = ∫TdS = T1 |
∫dS = T1 |
|
1 |
1 |
|
Q2 = ∫4 TdS = T2 ∫4 dS = T2 (S4 −S3 )= T2 (S1 −S2 )< 0 ,
3 |
3 |
|
= T2 (S2 −S1 ), |
||||||||
|
|
Q2 |
|
||||||||
|
|
|
|||||||||
|
η =1− |
|
Q2 |
|
|
=1− |
T2 |
. |
|||
|
|
|
|||||||||
|
|
|
|||||||||
|
|
Q |
|
||||||||
|
|
|
|
|
|
|
T |
||||
|
|
|
|
|
1 |
|
|
1 |
|
||
Теорема Нернста
Рассмотрим идеальный газ при 0К.
T= 0 ,
ε= 2i kT = 0 .
Все молекулы неподвижны. Каждой молекуле в фазовом пространстве соответствует одна фазовая ячейка, которую данная молекула не может покинуть.
Статистический вес молекулы равен единице
83
Г1 =1.
Статистический вес N молекул
Г = Г1 Г2 Г3 ...ГN =1 1 1...1 =1.
Энтропия системы
S = k lnГ = k ln1 = 0 .
При температуре 0 K энтропия всякой системы равна нулю. Это третье начало термодинамики или теорема Нернста.

84
ГЛАВА 7. ВЕРОЯТНОСТЬ СОСТОЯНИЯ
Математическая вероятность и вероятность состояния
Рассмотрим идеальный газ из N одинаковых молекул, находящихся в объеме V . Разделим этот объем на одинаковые объемы V′.
Обозначим ω′(1) - вероятность того, что одна молекула находится в этом объеме V′. Если все объемы V′ одинаковые, то ω′(1) - вероятность нахождения молекулы в любом объеме V′. Вероятность тог, что молекула находится в одном из объемов V′ равна ω′(1)+ω′(1)+...+ω′(1)= kω′(1),
k = VV′.
На событие, заключающееся в том, что молекула находится в одном из объемов V′, принадлежащих объему V , есть достоверное событие, значит
kω′(1)=1.
Величина в левой части имеет смысл времени, в течение которого N молекул соберутся в одной половине сосуда
t = ∆t ln(1−ωn (N)). ln 1− 21N
Для того чтобы считать такое событие возможным, положим
ωn (N)= 0.9 .
Кроме того, пусть выполняется условие
21N <<1.
Для этого достаточно, чтобы N > 5
ln(1± x)≈ ±x, x <<1,

85
ln 1− 21N ≈ −21N ,
|
|
t = ∆t |
ln0.1 |
= −∆t 2N ln0.1 = ∆t 2N ln10 , |
|
||||||||||||
|
|
|
|
||||||||||||||
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
− |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
2N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
t =2N ∆t ln10 =2N ∆t . |
|
|
|
|
||||||||
Обозначим t - время, в течение которого все N молекул окажутся в одной |
|||||||||||||||||
половине сосуда. Пусть время измерения ∆t =1c . Расчеты даны |
|
||||||||||||||||
N |
|
5 |
|
|
10 |
|
|
|
100 |
|
|
105 |
1019 |
||||
t,c |
|
32 |
|
|
103 |
|
|
|
1032 |
|
|
2105 |
21019 |
||||
|
|
|
|
|
|
|
|
V |
ω′(1)=1, |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
′ |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
V |
|
′ |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
′ |
|
V |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Обозначим |
′ |
|
|
|
ω(1)= V . |
|
|
|
|
|
|||||||
ω(N) - вероятность того, что все N молекул находятся в |
|||||||||||||||||
одном объеме V′. По теореме умножения вероятностей |
|
||||||||||||||||
|
|
ω(N) |
= ω |
(1) ω(1)...ω(1)= |
[ω(1)] |
, |
|
||||||||||
|
|
|
′ |
|
′ |
|
|
′ |
|
′ |
′ |
N |
|
|
|
||
ω′(N)= V′ N .V
Обозначим ω′(N1, N2 )- вероятность того, что N1 молекул находятся в объеме V′, а N2 молекул в остальном объеме (V − V′). Очевидно, что
|
|
V′ N1 |
|
V − V′ N2 |
||
ω′(N1 |
, N2 )= |
|
|
|
|
. |
|
V |
|||||
|
|
V |
|
|
||
Вероятности ω′(1), ω′(N), ω′(N1, N2 ) |
|
есть |
математическая вероятность |
|||
определенного события. Рассмотрим систему, в которой, например, 4 одинаковые молекулы. Пронумеруем их: 1,2,3,4.… Найдем вероятность того, что в объеме V′- одна любая молекула, а в объеме (V − V′) остальные три.
|
|
′ 1 |
|
′ |
3 |
||
|
V V −V |
|
|||||
′ |
|
|
|
|
|
. |
|
|
|
|
|
||||
ω(1,3)= |
|
V |
|
||||
|
|
V |
|
|
|
||
Проанализируем возможные распределения молекул по объемам V′ и (V −V′). Каждое распределение характеризуется вероятностью ω′(1,3).
Поскольку все молекулы одинаковые, то если рассматривать макросостояние данной системы, то совершенно неважно, какие именно молекулы находятся в объемах V′ и (V −V′).
Таким образом, макросостоянию, которое можно обозначить (1,3) соответствует 4 комбинации, при которых в объемах V′ и (V −V′) находятся 1 и 3 молекулы.

86
Обозначим ω(1,3) - вероятность макросостояния (состояния), при котором
в объеме V |
′ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
′ |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
одна молекула, а в объеме (V −V ) тир молекулы. |
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
ω(1,3) |
|
|
′ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
= ω(1,3) 4 . |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
Обобщим результат. Рассмотрим макросостояние, при котором в объеме |
||||||||||||||||||||||||||||||||||
V |
′ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
′ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
находится N1 молекул, а в объеме (V −V ) соответственно N2 молекул. |
|||||||||||||||||||||||||||||||||||
Обозначим z(N1, N2 ) - число комбинаций, |
|
|
при которых в объемах V |
′ |
′ |
|||||||||||||||||||||||||||||||
|
|
|
и (V −V ) |
|||||||||||||||||||||||||||||||||
находятся соответственно N1 и N2 |
любых молекул. |
|
|
|
|
|||||||||||||||||||||||||||||||
Обозначим ω(N1, N2 ) - вероятность данного состояния. |
|
|
|
|||||||||||||||||||||||||||||||||
|
|
Тогда |
ω(N1, N2 ) |
= |
|
|
′ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
ω |
(N1, N2 ) z(N1, N2 ), |
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
z(N1, N2 )= |
(N1 + N2 )! |
= |
|
|
|
N! |
|
|
|
, |
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
N !N |
! |
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
N !N |
2! |
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
1 |
|
|
2 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
V′ N1 V |
−V′ N2 |
|
|
|
|
N! |
|
|
|
|||||||||||||||||||||
|
|
|
|
ω(N1, N2 )= |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
, |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
V |
|
|
|
|
N1!N2! |
|
|
|||||||||||||||||||
|
|
|
|
|
|
V |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
N = N1 + N2 . |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
Наиболее вероятное распределение молекул |
|
|
||||||||||||||||||||||||||||||
|
|
Разделим объем V пополам. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
V′ = |
V |
, (V − V′)= |
, |
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
ω(N1, N2 )= |
|
1 N1 |
|
|
1 N2 |
|
|
N! |
|
|
|
. |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
N1!N2! |
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
2 |
|
|
|
|
|
|
|
|||||||||||||||
|
|
Найдем значение N1 , при котором ω(N1, N2 ) имеем максимум. |
|
|
||||||||||||||||||||||||||||||||
|
|
Проинтегрируем ω(N1, N2 ) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
1 N1 |
|
|
|
1 |
N2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
ln ω(N1, N2 )= ln |
|
|
|
+ln |
|
|
|
+lnN!−lnN!1 −lnN2!. |
|
|
||||||||||||||||||||||
|
|
|
|
|
|
2 |
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
Логарифм есть положительная функция. Поэтому если ω(N1, N2 ) имеет |
||||||||||||||||||||||||||||||||||
максимум, |
|
то и ln ω(N1, N2 ) также |
|
имеет |
|
максимум. Применим |
формулу |
|||||||||||||||||||||||||||||
Стирлинга.
lnN!= N lnN .
Запишем
N2 = N − N1 ,

87
ln ω(N1, N − N1 )= −N1 ln2 −(N − N1 )ln2 + N lnN − N1 lnN1 −(N − N1 )ln(N − N1 ).
Продифференцируем по N1 |
с учетом того, что |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
N = const , |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
d lnω(N1, N − N1 ) |
= 0 , |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
N |
|
|
|
dN1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
(−1) |
|
|
|
|
|
|||||||
−ln2 +ln2 −lnN1 − |
|
+ln(N − N1 )−(N − N1 ) |
|
|
= 0 , |
||||||||||||||||||||||||||||||
|
1 |
|
|
|
|
||||||||||||||||||||||||||||||
|
N |
(N − N ) |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
ln(N − Ni )= ln N1 , |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
N − Ni |
= N1 , |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
N1 |
= |
N |
, |
|
N2 = |
|
|
N |
. |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
Найдем ω(N1, N2 )max |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
N |
|
1 |
N |
|
|
|
N! |
|
|
|
|
|
|
|
1 |
|
|
|
N! |
|
|
|
|
|
||||||||
ω(N1, N2 ) |
2 |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
, |
|||||||||||||
= |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
N |
N |
2N |
|
N |
N |
|||||||||||||||||||||||||||
max |
2 |
|
|
2 |
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
! |
|
! |
|
|
|
|
|
! |
|
! |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
2 |
|
|
|
|
2 |
2 |
|
||||||||||
|
|
|
N! |
|
|
|
|
N |
|||
ln |
|
|
|
|
|
|
|
= lnN!−2ln |
|
!= |
|
|
N |
N |
2 |
||||||||
|
|
|
|||||||||
|
|
|
! |
|
|
! |
|
|
|
||
|
2 |
|
2 |
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
N |
|
N |
|
N |
|
N |
= N ln2 = ln2 |
N |
|
N lnN − 2 |
|
ln |
|
= N lnN − N ln |
|
= N lnN −ln |
|
|
|
|
2 |
2 |
2 |
2 |
|
||||||
|
|
|
|
|
|
|
||||
ω(N1, N2 )max = 21N 2N =1,
ω(N1, N2 )max = ω N , N =1.
2 2
Молекулы в одной половине сосуда
Разделим сосуд на две одинаковые части и будем наблюдать за одной из них. Пусть всего в сосуде находится N молекул.
|
|
1 |
N |
1 |
0 |
N! |
|
||||||
ω(N1, N2 )= ω1 |
(N,0)= |
|
|
|
|
|
|
|
|
, |
|||
2 |
2 |
N!0! |
|||||||||||
|
|
|
|
|
|
|
|
||||||
|
0!=1, |
|
|
|
|
|
|
|
|
|
|
||
|
ω1 = |
1 |
. |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||
|
|
2N |
|
|
|
|
|
|
|
|
|
||
Обозначим ω- вероятность того, что в соседней половине нет ни одной молекулы. Очевидно, что
ω1 +ω =1 ,
ω=1−ω1 ,
ω=1− 21N .
Обозначим
n - количество опытов по измерению тела молекул в обеих половинах сосуда. ωn(0) - вероятность того, что в n опытах в половине сосуда не окажется ни одной
молекулы.
88
Очевидно, что
ωn(0) = ω ω ω...ω = 1− 21N n .
Обозначим ωn(N) - вероятность того, что в опытах в другой половине сосуда находится N молекул.
ωn(N) =1−ωn(0) =1− 1− 21N n ,
1− 21N n =1−ωn (N),
n ln 1− 21N = ln(1−ωn (N)),
n = ln(1−ωn (N)). ln 1− 12N
Пусть каждый опыт продолжается ∆t секунд. Умножим обе части на ∆t ,
∆t n = ln(1−ωn (N)) ∆t . ln 1− 1
2N

89
ГЛАВА 8. ЯВЛЕНИЕ ПЕРЕНОСА В ГАЗАХ
Столкновение молекул
В идеальном газе происходят столкновения между двумя молекулами. Одновременными столкновениями между тремя и большим числом молекул пренебречь.
Молекулы в газе могут сближаться на достаточно малые расстояния, при котором между ними возникают силы отталкивания. Молекулы при этом нужно представлять как упругие сферы радиусами r1 и r2 .
Столкновение молекул возможно только в случае, если центры молекул сблизятся на расстояние равное сумме радиусов (r1 + r2 ).
Минимальное расстояние между центрами двух молекул называется эффективным диаметром молекулы.
Характеристики соударений
Столкновения молекул являются случайными событиями. При столкновении скорость молекулы изменяется случайным образом, как по направления, так и по величине. Следовательно, в общем случае в промежутках между столкновениями молекула пролетает различные отрезки пути.
Расстояние, которое молекула проходит двумя последовательными столкновениями называется длиной свободного пробега.
Обозначим эту величину буквой l . Из вышесказанного следует, что l является случайной величиной и характеризуется функцией распределения.
f (l)= |
1 |
|
|
l |
|
|
exp |
− |
|
. |
|
λ |
|
||||
|
|
|
λ |
||
Вычислим среднее значение длины свободного пробега
∞ |
∞ |
1 |
|
|
l |
|
l = ∫l f (l)dl = ∫l |
|
exp |
− |
|
dl = λ . |
|
λ |
|
|||||
0 |
0 |
|
|
λ |
||
Параметр λ в функции распределения f (l) имеет смысл средней длины свободного пробега молекулы.
Очевидно, что значение λ должно зависеть как от размеров молекул, так и от их тела.
Расчет дает
90
λ = 2π1d2n ,
где d - эффективный диаметр молекулы
n- концентрация молекул.
При нормальных условиях в газах
λ≈10−7 .
Промежуток времени между двумя последовательными столкновениями молекулы называется временем свободного пробега.
Эта величина также является случайной и можно определить среднее время свободного пробега τ. Расчет дает
τ = λυ ,
где υ - средняя арифметическая скорость молекул газа.
Частота столкновений (среднее число столкновений) молекулы есть величина равная среднему количеству столкновений молекулы в единицу времени.
Обозначим частоту столкновений z .
Запишем:
z = |
1 |
= |
|
1 |
|
= |
υ |
= |
|
υ |
|
|
= 2πd2n υ , |
|
τ |
|
λ |
|
λ |
|
1 |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
2 |
n |
|
|
|
|
|
|
υ |
|
|
|
2 πd |
|
||||
z =  2πd2n υ .
2πd2n υ .
Диффузия в газах
Диффузией называется процесс самопроизвольного выравнивания концентрации вещества в системе. Пусть концентрация молекул газа n изменяется вдоль некоторого направления z .
Очевидно, что |
dn |
≠ 0 . |
|
|
|
|||
dz |
|
|
|
|||||
|
dn(z) |
|
|
|
|
|
||
Если |
≠ 0 , |
то |
существует |
градиент |
концентрации n вдоль |
|||
|
||||||||
|
dz |
|
|
|
|
|
||
направления |
оси |
z . |
Проведем |
мысленно |
плоскую поверхность |
|||
перпендикулярную оси z и выделим участок поверхности, площадь которого обозначим dS .
