
3. Класифікація амінокислот
Амінокислоти, які входять до складу білків, часто класифікують за кількістю аміно- і карбоксильних груп та будовою основного ланцюга. Зараз також широко використовується класифікація амінокислот; яка ґрунтується на полярності їх радикалів. За цією ознакою амінокислоти поділяють на чотири класи: з неполярними радикалами, з незарядженими полярними радикалами, з негативно зарядженими полярними радикалами і з позитивно зарядженими полярними радикалами.
Нижче наводиться класифікація амінокислот за першою ознакою.
Ациклічні амінокислоти. Цю групу амінокислот залежно від кількості амінних і карбоксильних груп поділяють на чотири класи:
Моноаміномонокарбонові кислоти. До цього класу входять амінокислоти, які містять одну амінну і одну карбоксильну групу.
L (+) аланін (α-амінопропіонова кислота)
Н2N – CH – COOH
│
СН3
Ця амінокислота часто зустрічається у складі білків рослин і тварин, а також знаходиться у вільному стані. Крім α-аланіну в організмі виявлено також β-аланін. Однак до складу білків останній не входить. β-Аланін бере участь в утворенні структури пептидів, зокрема дипептидів карнозину та ансерину, які містяться у м'язовій тканині більшості хребетних тварин, та входить до складу вітаміну В3.
L (-) серин (α-аміно-β-оксипропіонова кислота)
CH2 – CH – COOH
I I
OH NH2
Синтезується в організмах людини і тварин, є складовою частиною багатьох білків. Серин входить до складу активних центрів таких ферментів, як трипсин, холінестераза; бере участь у синтезі окремих амінокислот.
L (-) цистеїн (α-аміно-β-тіопропіонова кислота)
CH2 – CH – COOH
I I
SH NH2
Характерною особливістю цієї амінокислоти є те, що її сульфгідрильна група легко окислюється. При цьому дві молекули цистеїну взаємодіють між собою й утворюють диамінодикарбонову кислоту – цистин (β,β-дитіо-α,α-диамінопропіонову кислоту):
L (-) метіонін (α-аміно-γ-метилтіомасляна кислота)
CH2 – CH2 – CH – COOH
I I
S – CH3 NH2
В організмі відіграє надзвичайно важливу роль як донор метильних груп для забезпечення процесів синтезу холіну, адреналіну, бере участь у процесах утворення цистеїну та інших біологічно активних речовин. В організмі людини і тварин не синтезується.
L (-) треонін (α-аміно-β-оксимасляна кислота)
CH3 – CH – CH – COOH
I I
OH NH2
Входить до складу багатьох рослинних і тваринних білків. Значна кількість треоніну міститься в таких білках, як пепсин, фібрин та ін. В організмі людини і тварин треонін не синтезується.
L (+) валін (α-аміно-β-метилмасляна кислота)
CH3 – CH – CH – COOH
I I
СН3 NH2
В організмі тварин і рослин валін входить до складу білків та зустрічається у вільному стані. Значна кількість валіну (4-15%) міститься у білках – міоглобіні, казеїні і еластині. В організмі людини і тварин валін не синтезується, і тому для забезпечення нормальних фізіологічних процесів він повинен постійно надходити з продуктами харчування.
L (-) лейцин (α-аміно-γ-метилвалеріанова кислота)
CH3 – CH – СН2 – CH – COOH
I I
СН3 NH2
Входить до складу багатьох білків тваринного і рослинного походження. Значна кількість його міститься у пророслому зерні злакових культур. В організмі людини і тварин лейцин не синтезується, належить до незамінних амінокислот.
L (+) ізолейцин (α-аміно-β-метилвалеріанова кислота)
CH3 – CH2 – СН – CH – COOH
I I
СН3 NH2
У складі білків міститься в незначних кількостях, належить, як і лейцин, до незамінних амінокислот.
2.Моноамінодикарбонові кислоти. Цей клас амінокислот містить одну амінну і дві карбоксильні групи, тому їх водні розчини мають кислотний характер:
L (+) аспарагінова кислота (аміноянтарна)
HOOС – CH2 – CH – COOH
I
NH2
Особливо високий вміст її було виявлено в соці спаржі (звідси і походить її назва). Аспарагінова кислота синтезується в організмах людини і тварин, входить до складу багатьох білків рослинного і тваринного походження. Вона використовується в процесах синтезу азотистих основ нуклеїнових кислот і сечовини, знешкодження аміаку, переамінування амінокислот та ін.
L (+) глутамінова кислота (α-аміноглутарова)
HOOС – CH2 – СН2 – CH – COOH
I
NH2
Глутамінову
кислоту вперше було виділено у 1866 р. з
гідролізату клейковини пшеничного
зерна. Вона знаходиться як у складі
білків, так і у вільному стані. Зокрема,
високим вмістом глутамінової кислоти
характеризуються альбуміни і глобуліни
крові, колаген та інші
 білки. Глутамінова кислота, як і
аспарагінова, бере участь у багатьох
обмінних процесах організму – в
дезамінуванні, переамінуванні,
декарбоксилюванні амінокислот. З неї
утворюється важливий медіатор нервової
системи – γ-аміномасляна кислота та
інші важливі сполуки, зокрема глютамін.
Натрієва сіль глутамінової кислоти
широко використовується в харчовій
промисловості для підсилення смакових
якостей харчових продуктів.
білки. Глутамінова кислота, як і
аспарагінова, бере участь у багатьох
обмінних процесах організму – в
дезамінуванні, переамінуванні,
декарбоксилюванні амінокислот. З неї
утворюється важливий медіатор нервової
системи – γ-аміномасляна кислота та
інші важливі сполуки, зокрема глютамін.
Натрієва сіль глутамінової кислоти
широко використовується в харчовій
промисловості для підсилення смакових
якостей харчових продуктів.
Ці амінокислоти входять до складу білків також у вигляді амідів – аспарагіну і глутаміну
Н2NОC – CH2 – CH – COOH
I
NH2
H2NOС – CH2 – СН2 – CH – COOH
I
NH2
Аспарагін і глутамін відіграють важливу роль у процесах обміну в організмі, окрема у процесах зв'язування аміаку і транспорту його до місця синтезу сечовини. Особливо багато аспарагіну нагромаджується в паростках бобових рослин.
3. Диаміномонокарбонові кислоти. Амінокислоти цього класу мають у своєму складі дві аміногрупи і одну карбоксильну, тому їх водні розчини проявляють лужні властивості.
L (+) аргінін (α-аміно-δ-гуанідинвалеріанова кислота)
NH = C – NH – CH2 – CH2 – CH2 – CH – COOH
I I
NH2 NH2
Високий вміст аргініну (до 84% загальної маси амінокислот) виявлено в спермі риб. Аргінін відіграє досить важливу роль в обміні речовин, зокрема в процесах утворення сечовини, креатину та інших речовин. Аргінін постійно синтезується в організмі людини і тварин.
L (+) лізин (α,ε-диамінокапронова кислота)
СН2 – CH2 – CH2 – CH2 – CH – COOH
I I
NH2 NH2
Входить до складу всіх білків; в організмах людини і тварин не синтезується і належать до незамінних амінокислот. Багато лізину міститься в білках ядер – протамінах і гістонах.
Зараз лізин добувають у результаті хімічного та мікробіологічного синтезу, його використовують для підвищення продуктивності сільськогосподарських тварин.
4. Диамінодикарбонові кислоти. Існує одна амінокислота цього класу – цистин (β,β-дитіо-α,α-диамінопропіонова кислота)
СН2 – S – S – CH2
I I
CH – NH2 CH – NH2
I I
COOH COOH
При відновленні цистину відбувається розщеплення його на дві молекули цистеїну. Отже, ці амінокислоти відіграють важливу роль в окислювально-відновних процесах організму. У значних кількостях цистеїн входить до складу багатьох білків, зокрема білків волосся, нігтів, пір'я та ін.
Циклічні амінокислоти. Цю групу амінокислот поділяють на два класи.
1. Карбоциклічні амінокислоти
L (-) фенілаланін (α-аміно-β-фенілпропіонова кислота)
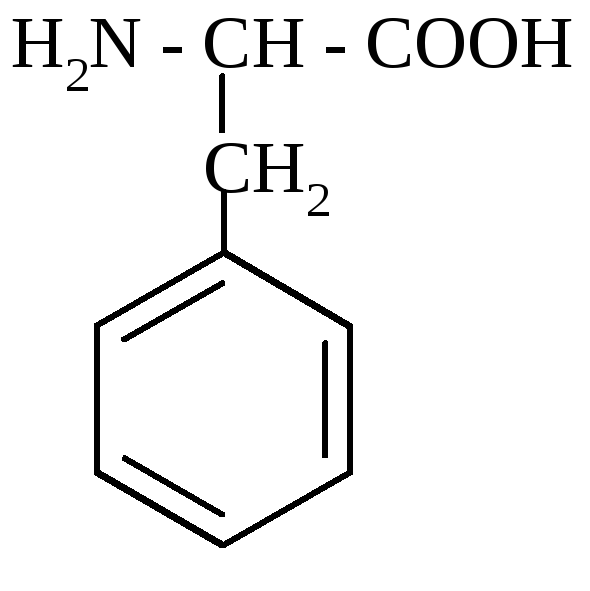
В організмі людини і тварин не синтезується. Використовується в процесах синтезу адреналіну і тироксину.
L (-) тирозин (α-аміно-β-параоксифенілпропіонова кислота)
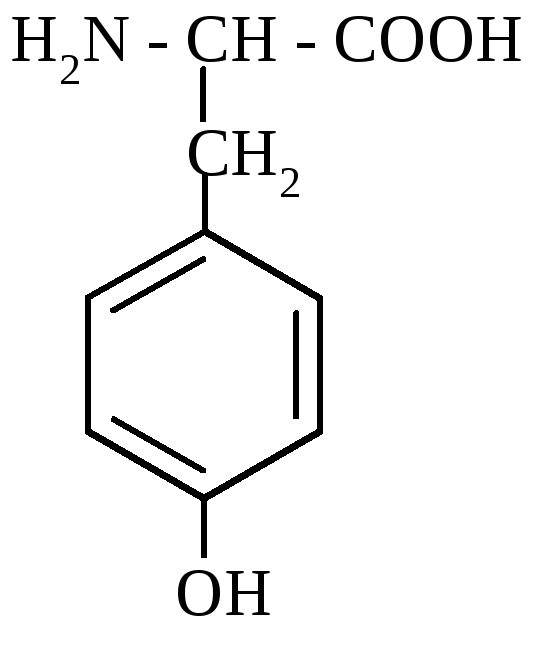
Входить до складу різних білків, особливо велика кількість його є в інсуліні великої рогатої худоби (до 12,5%) і пепсині (до 8,5%). У організмі людини і тварин тирозин утворюється при окисненні фенілаланіну і використовується у процесах синтезу гормонів – тироксину, адреналіну і норадреналіну тощо.
2. Гетероциклічні амінокислоти
L (-) триптофан (α-аміно-β-індолілпропіонова кислота)
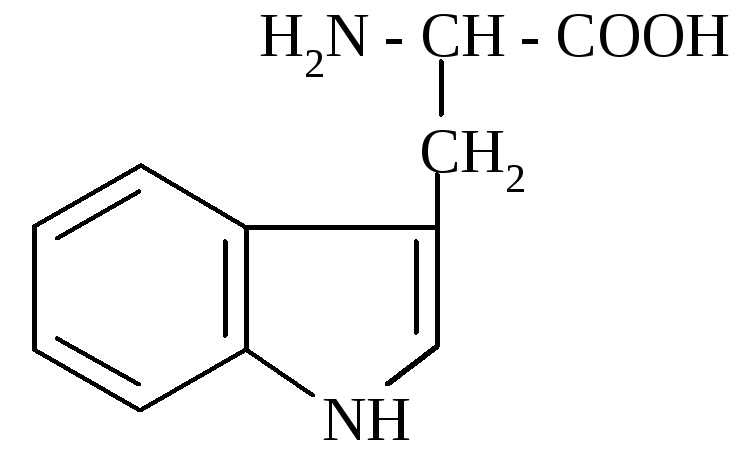
Вперше виділено у 1901 р. з продуктів гідролізу казеїну. Міститься в білках рослинного і тваринного походження. В організмі людини і тварин не синтезується і належить до незамінних амінокислот.
L (-) гістидин (α-аміно-β-імідазолпропіонова кислота)
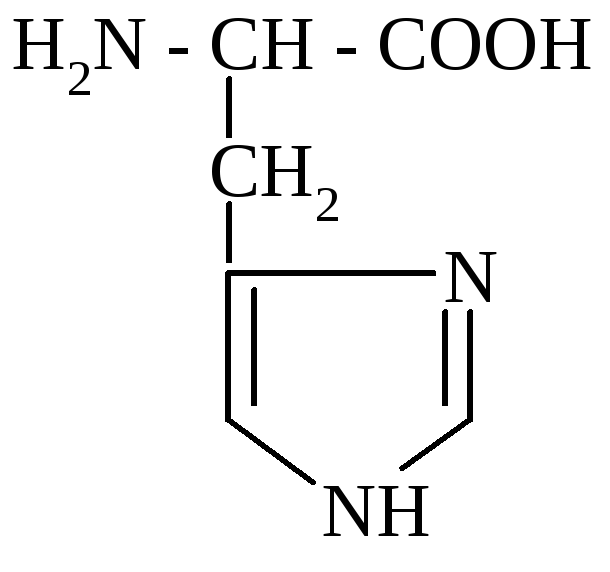
У значних кількостях гістидин міститься в тканинах печінки, нирок та в гемоглобіні крові. З гістидину при його декарбоксилюванні утворюється важливий біогенний амін – гістамін, який сприяє розширенню кровоносних судин та секреції соляної кислоти в шлунку.
Амінокислоти відіграють дуже важливу роль в організмі у синтезі важливих фізіологічно активних сполук, а також у забезпеченні деяких властивостей харчової сировини і продуктів. Тирозин відповідає за забарвлення волосся, шкіри, очей, потемніння харчових продуктів: хліба, фруктів, картоплі у процесі обробки. Глутамінова кислота утворює пролін, який відіграє важливу роль у формуванні структури колагену і білків клейковини пшениці, утворюючи у молекулах згини. Дисульфідні зв’язки цистеїну придають клейковині пружні властивості.
