
- •Министерство образования и науки украины
- •1. Строение атома
- •1.2. Некоторые сведения из квантовой механики
- •1.3. Уравнение Шредингера для атома водорода
- •1.4. Спин электрона
- •1.5. Атомная орбиталь
- •1.6. Принцип Паули
- •1.7. Многоэлектронные атомы
- •2. Химическая связь
- •2.1. Основные характеристики химической связи
- •2.1. Составление химических уравнений
- •2.3. Стехиометрические расчеты в химии
- •2.5. Номенклатура неорганических соединений
- •2.5. Скорость химических реакций.
- •3. Кристаллохимия
- •3.1. Ионные кристаллы
- •3.2. Ковалентные связи в кристаллах
- •3.3. Металлическая связь
- •3.4. Слабая (ван-дер-ваальсовая) связь в кристаллах
- •3.5. Кристаллохимические параметры
- •4. Кристаллография (1 часть)
- •4.1. Предмет кристаллографии
- •4.4. Сетка Вульфа. Сферические координаты
- •4.5. Элементы симметрии кристалла
- •5. Кристаллография (2 часть)
- •5.1. Сингонии. Решетки Бравэ
- •5.2. Некоторые наиболее распространенные типы решеток
- •5.3. Пространственная решетка
- •5.4. Индицирование направления
- •5.5. Индицирование плоскостей (hkl)
- •5.6. Индицирование гексагональных кристаллов (граней)
- •5.7. Термины в кристаллографии
- •6. Дефекты кристаллической решетки
- •6.1. Точечные дефекты
- •6.2. Миграция точечных дефектов
- •6.3. Диффузия в твердых телах
- •6.4. Дислокации в кристаллах
- •7. Макро-, микро- и наноструктура материалов
- •7.1. Макроскопический анализ
- •7.2. Микроскопический анализ
- •7.3. Принцип работы металлографического микроскопа
- •7.4. Определение балла зерна
- •7.5 Фазовый анализ
- •7.6. Наноструктура
- •7.7. Рентгеноструктурный анализ материалов
- •8. Механические свойства твердых материалов
- •8.1. Разновидности механических свойств материалов
- •8.3. Упругая линейная продольная деформация
- •8.4. Сдвиг. Упругая деформация сдвига
- •8.5. Взаимосвязь между деформациями растяжения (сжатия) и сдвига
- •9. Всесторонняя деформация сжатия
- •9.1. Закон Гука для всесторонней деформации
- •9.2. Закон Гука для деформации вдоль одной стороны
- •9.3. Связь между модулем всестороннего сжатия и
- •9.4. Напряжения при ударе
- •9.5. Упругое последствие
- •10. Изгиб и кручение материалов
- •10.1. Изгиб. Упругая изгибная деформация
- •10.2. Прогиб и поворот сечения балки
- •10.3. Прогиб балки на двух опорах
- •10.4. Кручение материалов. Деформация кручения
- •11. Пластичность. Твердость. Ударная вязкость
- •11.1. Пластическая деформация твердых тел
- •11.2. Физическая сущность пластической деформации
- •11.3. Пластическая деформация поликристаллов
- •11.4. Основные характеристики деформации и разрушения
- •11.5. Твердость материалов
- •12. Разрушение материалов. Пути повышения прочности
- •12.1. Прочность. Виды разрушений
- •12.2. Ползучесть материалов
- •12.3. Другие механические свойства
- •12.4. Пути повышения прочности материалов
- •13. Тепловые свойства твердых тел
- •13.1. Колебания атомов в кристаллах
- •13.2. Теплоемкость твердых тел
- •13.3. Теплопроводность твердых тел
- •13.4. Тепловое расширение твердых тел
- •13.5. Зависимость механических напряжений от температуры
- •13.6. Повышение механических свойств материалов под действием температуры
- •14. Жидкое состояние вещества
- •14.3. Вязкость жидкостей
- •14.4. Поверхностное натяжение
- •14.5. Явления смачивания
- •14.6. Жидкие растворы
- •14.9. Осмотическое давление
- •15. Структура полимеров
- •15.1. Молекулярное строение полимеров
- •15.2. Классификация полимеров
- •15.3. Превращения в полимерах
- •15.4. Надмолекулярная структура полимеров
- •16. Механические свойства полимеров
- •16.1 Высокоэластическое состояние полимеров
- •16.2. Модель Максвелла для линейных полимеров
- •16.3. Модель Кельвина-Фогта для сетчатых полимеров
- •17. Термодинамика фазовых превращений
- •17.1. Фазовые превращения. Правило фаз
- •17.2. Термодинамические функции и параметры
- •Свойства термодинамических функций:
- •17.3. Связь между основными термодинамическими функциями и параметрами
- •17.4. Химический потенциал
- •18. Фазовые переходы I рода. Плавление и
- •18.1. Фазовые переходы I рода
- •18.2. Уравнение Клапейрона-Клаузиуса
- •18.3. Плавление и кристаллизация
- •18.4. Термический анализ
- •19. Фазовые превращения в твердом состоянии
- •19.1. Изоморфизм и полиморфизм вещества
- •19.2. Полиморфные превращения
- •19.3. Бездиффузионные и диффузионные превращения
- •19.4 Кинетика твердофазных превращений
- •19. 5 Упорядочение и разупорядочение в сплавах
- •19.6. Диаграмма состояния сплавов с учетом твердофазных превращений
- •19.7. Эвтектоидные превращения
- •19. 8. Рекристаллизация
- •20. Сплавы
- •20.1. Классификация сплавов
- •20.2. Зависимость свободной энергии Гиббса от температуры и
- •20.3. Система с неограниченной растворимостью компонентов в жидком и твердом состояниях
- •20.4. Построение диаграмм состояния методом термического
- •21. Диаграммы состояния бинарных систем
- •21.1. Система с ограниченной взаимной растворимостью
- •21.2. Анализ диаграммы состояния для сплавов с эвтектическим
- •21.3. Анализ диаграммы состояния для сплавов с перитектическим превращением.
- •21.4. Диаграммы состояния для сплавов, когда компоненты образуют химические соединения
- •22. Изучение диаграмм состояния
- •22.1. Построение и расшифровка диаграмм состояния тройных сплавов
- •22.2. Основные типы диаграмм состояния трехкомпонентных
- •II. Изотермические и политермические сечения тройных диаграмм.
- •23. Определение концентрации компонентов
- •Бинарные сплавы
- •Найти молярную массу бинарного раствора м при известных ,,м1 и м2.
- •24.2. Неорганическое стекло
- •24.3. Механические и тепловые свойства стекла
- •24.6. Оптические свойства стекла
- •24.5. Применение технических стекол.
- •25. Дисперсные системы
- •25.1. Введение
- •25.2. Свойства малых частиц
- •25.3. Коагуляция частиц
- •26. Электрические свойства материалов
- •26.1. Элементы зонной теории твердого тела
- •26.2. Электропроводность твердых тел
- •26.2. Поляризация диэлектрика
- •26.4. Сверхпроводники
- •26.5. Электрический ток в жидкостях
- •27. Магнитные свойства твердых тел
- •27.1. Магнитные моменты атомов
- •27.2. Намагничивание. Диа- и парамагнетики
- •27.3. Ферромагнетики
21. Диаграммы состояния бинарных систем
РАЗНОГО ТИПА
21.1. Система с ограниченной взаимной растворимостью
компонентов в твердом состоянии
Рассмотрим построение равновесной диаграммы состояния в том случае, когда компоненты А и В имеют близкие атомные диаметры, аналогичную или близкую валентность, но различную кристаллическую структуру. Такие металлы полностью растворяются друг в друге в жидком состоянии и ограниченно — в твердом. При температуре Т1, когда существует только жидкая фаза, соответствующая диаграмма в координатах G-x имеет вид, показанный на рис. 21.1,а или б.

Рис. 21.1. Кривые свободной энергии при температуре Т1 для систем с ограниченной растворимостью компонентов в твердом состоянии. SA и SB - твердые растворы на основе компонентов А и В соответственно.

Рис. 21.2. Кривые свободной энергии при температуре Т2 для систем с ограниченной растворимостью компонентов в твердом состоянии. Показано равновесие между жидкой и твердой фазами.
Из
рис. 21.1, а
видно, что минимум на кривой свободной
энергии для жидкой фазы располагается
между минимумами на кривых свободной
энергии для твердых растворов на основе
компонентов А
и В.
Согласно рис. 21.1,б,
минимум на кривой свободной энергии
для жидкой фазы находится вне этого
интервала, т. е. по одну сторону от
минимумов на кривых свободной энергии
твердых растворов. В случае рис. 21.1,а
по мере понижения температуры наступает
такое состояние (при Т2),
когда кривая свободной энергии жидких
растворов пересекает сразу две к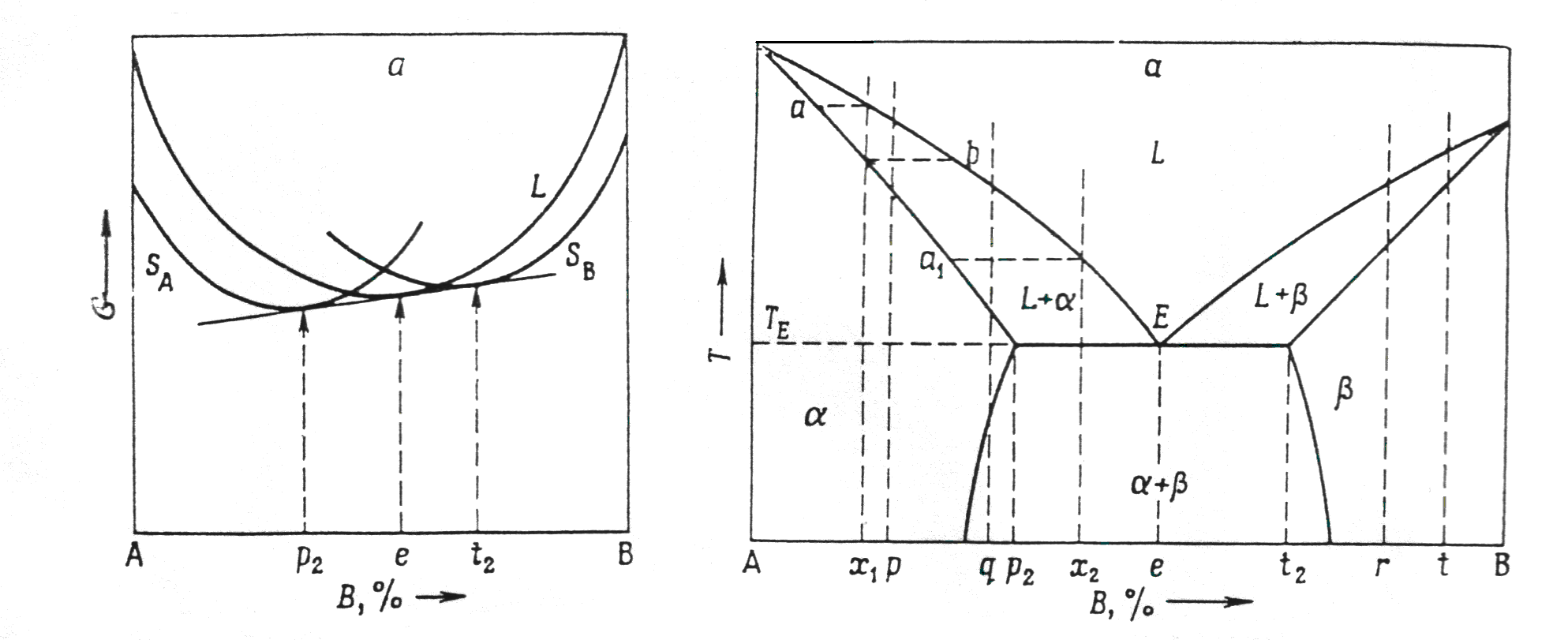 ривые
свободной энергии твердых растворов
на основе компонентовА
и В
(рис. 2
ривые
свободной энергии твердых растворов
на основе компонентовА
и В
(рис. 2 1.2,а).
1.2,а).
Рис. 21.3. Относительное распо- Рис. 21.4. Равновесные диаграммы
ложение кривых свободной состояния с ограниченной растворимостью
энергии для систем с огра- компонентов в твердом состоянии: а - система
ниченной растворимостью эвтектического типа, соответствующая
компонентов в твердом состо- кривым свободной энергии на рис. 21.4,а;
янии: а - при эвтектической б - система перитектического типа,
температуре ТЕ; б - при пери- соответствующая кривым свободной энергии на
тектической температуре Тр. рис. 21.4,б.
Поэтому при температуре Т2 сплавы, расположенные по составу между чистым компонентом А и сплавом состава р, состоят из кристаллов твердого раствора, богатого компонентом А, а сплавы, расположенные между точками p и q, являются двухфазными и состоят из твердого и жидкого растворов, составы которых изображаются соответственно точками p и q. В интервале концентраций qr все сплавы находятся в жидком состоянии; в интервале rt сплавы являются двухфазными и состоят соответственно из жидкой и твердой фаз, и, наконец, в интервале tВ сплавы представляют собой твердые растворы, богатые компонентом В.
Дальнейшее понижение температуры приводит к тому, что все сплавы заканчивают кристаллизацию и они становятся твердыми. При температуре TЕ наблюдается состояние, изображенное на рис. 21.3,а. Согласно этому рисунку, при температуре Tе все три кривые свободной энергии имеют одну общую касательную; отсюда следует, что при этой температуре жидкость состава е находится в равновесии с -твердым раствором состава p2 и -твердым раствором состава t2. Данное трехфазное равновесие может наблюдаться только при строго определенной температуре.
Равновесная диаграмма состояния, отвечающая всем положениям кривых свободной энергии на рис. 21.1,а — 21.3,а, представлена на рис. 21.4,а. Сплав состава точки Е называют эвтектическим. Жидкость этого состава кристаллизуется при эвтектической температуре TЕ, образуя смесь кристаллов двух твердых растворов составов р2 и t2 соответственно; отношение весовых количеств этих твердых фаз измеряется отношением отрезков et2/p2e. В равновесных условиях температура остается постоянной до тех пор, пока не закончится кристаллизация всей жидкости эвтектического состава; система, состоящая из трех фаз, находящихся в равновесии друг с другом, не имеет степеней свободы, т.е. является нонвариантной.
Если кривые свободной энергии для рассматриваемой системы расположены, как показано на рис. 21.1,б, то изменения состояния системы при понижении температуры, будут изображаться рис. 21.2,б и 21.3,б. На рис. 21.2,б в отличие от рис. 21.2,а жидкость состава q находится в равновесии с -твердым раствором состава р, а -твердый раствор при этой температуре не находится в равновесии с этими фазами. Промежуточное состояние, показанное на рис. 21.3б, несколько отличается от состояния на рис. 21.3,а. При этой особой температуре Тр (и никакой другой) в равновесии снова оказываются три фазы; жидкая фаза состава р0 находится в равновесии с - и -твердыми растворами составов р2 и t2 соответственно. Соответствующая диаграмма состояния показана на рис. 21.4,б. Точку р называют перитектической; значение этой диаграммы состояния заключается в том, что при температуре Тр жидкость состава р0 реагирует с кристаллами -твердого раствора состава р2, в результате чего образуются кристаллы -твердого раствора состава t2. В равновесных условиях температура остается постоянной и равной Тр до тех пор, пока не закончится перитектическая реакция; такая система является нонвариантной.
Примерами таких диаграмм состояния являются диаграммы состояния таких систем как Bi-Sn, Bi-Pb, Cd-Sn, Pb-Sb, Cd-In и др.
