- •Айала ф., Кайгер Дж. Современная генетика: в 3-х т. Т. 1. Пер. С англ.: – м.: Мир, 1987. – 295 с.
- •Электронное оглавление
- •9. Методы работы с днк 260
- •Предисловие редактора перевода
- •Предисловие
- •Структура книги
- •Особенности книги
- •Организация и передача генетического материала
- •I. Введение
- •Прокариоты: бактерии и сине-зеленые водоросли
- •Одноклеточные и многоклеточныеэукариоты
- •МейозIi
- •Значение мейоза
- •Литература
- •2.Менделевскаягенетика Первые представленияо наследственности
- •Открытие законов наследственности
- •Методы Менделя
- •Доминантность и рецессивность
- •Расщепление
- •Гены - носители наследственности
- •Независимое комбинирование
- •Тригибридные скрещивания
- •27 Гладкие желтые пурпурные
- •Множественные аллели
- •Генотип и фенотип
- •Литература
- •3. Хромосомныеосновы наследственности Гены и хромосомы
- •Наследование, сцепленное с полом
- •Нерасхождение х-хромосом
- •Вторичное нерасхождение
- •Сцепленное с полом наследование у человека и других видов
- •Определение пола
- •Отношение полов
- •Литература
- •4. Природа генетическогоматериала
- •Бактерии как экспериментальныйобъект
- •Экспериментальные исследованиябактериофагов
- •Нуклеиновые кислоты - наследственный материал вирусов
- •Химический состав и строениенуклеиновых кислот
- •Модель структуры днк Уотсона-Крика
- •Проверка модели Уотсона-Крика
- •Различные формы организациидвухцепочечной днк
- •Организация днк в хромосомах
- •Общие особенности репликации днк
- •Литература
- •5. Геномэукариот
- •Рекомбинация сцепленных генов
- •Генетические карты
- •Трехфакторные скрещивания
- •Генетическая интерференция
- •Когда происходит кроссинговер?
- •Мейоз у грибов
- •Цитологические наблюдениякроссинговера
- •Корреляция между генетическими и цитологическими картами хромосомдрозофилы
- •Внеядерная наследственность
- •Литература
- •6. Тонкая структура гена
- •Бактериофаг как генетическая система
- •СистемаrIi бактериофага т4
- •Природа мутаций в областиrIi
- •Функциональные особенностиrIi-мутаций
- •Цистрон
- •КартированиеrIi-мутаций с помощью делеций
- •Предельная разрешающая способностьрекомбинационного анализа
- •Уточнение генетической терминологии
- •Комплементационный анализу высших эукариот
- •Рекомбинационный анализтонкой структуры генау высших эукариот: дрозофила
- •Литература
- •7. Геномвируса
- •Размножение бактериофагов
- •Мутантные бактериофаги
- •Комплементационный анализусловно летальных мутаций фагаХ174
- •Рекомбинационный анализ мутантовфагаХ174
- •Умеренный бактериофагλ
- •Гены фагаλ
- •Профагλ
- •Сопоставление генетическойи физической карт фага а
- •Организация геномафагов т2 и т4
- •Литература
- •8. Бактериальныйгеном
- •МутантыЕ. Coli
- •Генетические элементыE.Coli
- •Физическое картирование бактериальных генов методомпрерванной конъюгации
- •Кольцевая форма геномаЕ. Coli
- •Подвижные генетические элементы (транспозоны)
- •Генетическое картированиеЕ. Coli
- •Конъюгационное картирование
- •Трансдукционное картирование
- •Обзор результатов генетического анализа
- •Литература
- •9.Методы работы с днк
- •Кинетика ренатурации днк
- •Рестрикция днк и ферменты модификации
- •Рестрикционный анализ молекул днк
- •Определение последовательности нуклеотидов в днк ( секвенирование )
- •Метод рекомбинантных днк
- •Векторы для клонирования днк
- •Библиотеки геномов
- •Обзор методов работы с днк
- •Литература
- •Оглавление
Профагλ
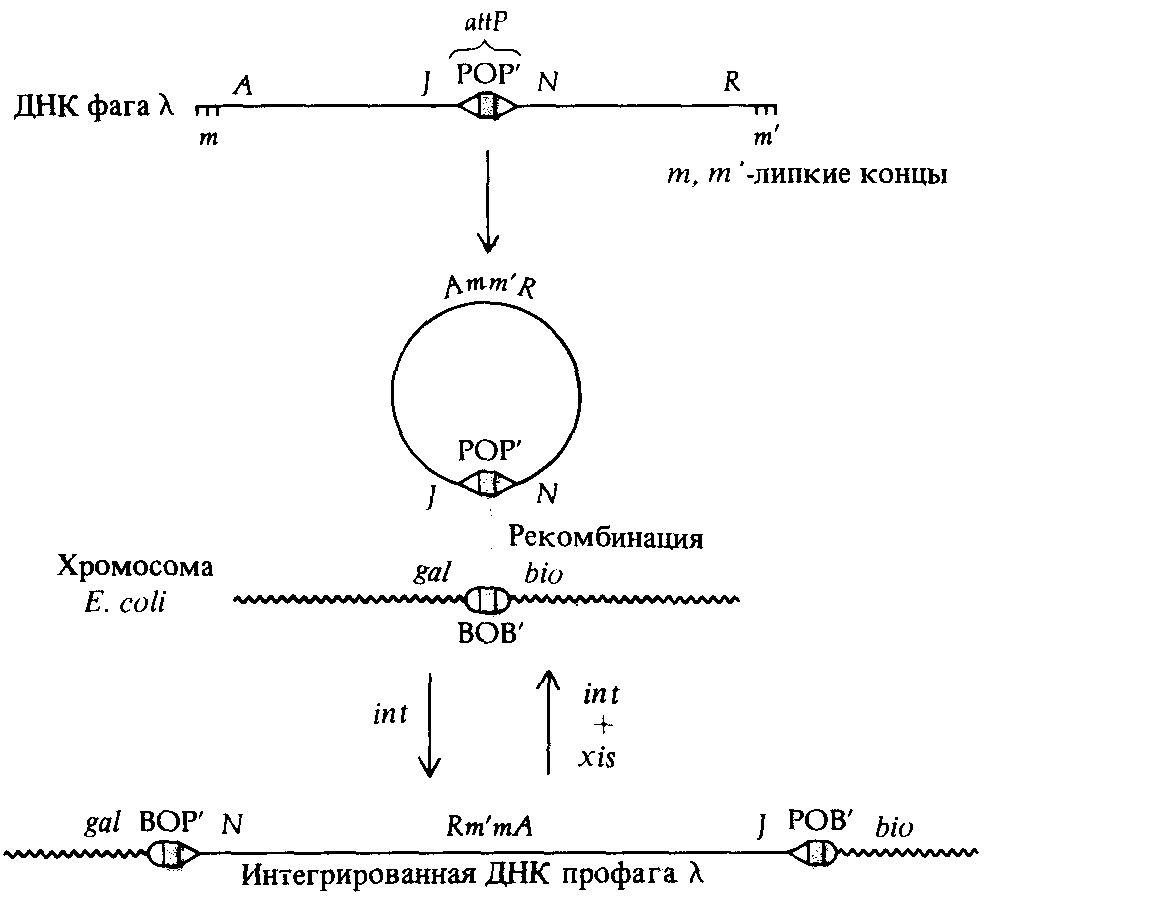
Мутантные гены, содержащиеся в профаге λ и встроенные в бактериальный геном, можно картировать, используя описанные в следующих главах методы генетики бактерий. Такие исследования показали, что профаг λ встраивается в геном Е. coli между генами gal и bio, контролирующими потребление сахара галактозы и синтез витамина биотина соответственно. Последовательность генов на генетической карте профага сравнивали с соответствующей последовательностью на генетической карте фага (рис. 7.8). Они, как ни странно, не тождественны: любая из них получается из другой посредством циклической перестановки. Это различие в последовательности генов возникает из-за механизма, с помощью которого λ-ДНК встраивается в бактериальную хромосому.
Линейная молекула ДНК фага λ имеет комплементарные одноцепочечные концы, состоящие из 12 нуклеотидов. После проникновения в клетку бактерии-хозяина эти «липкие» концы сшиваются ДНК-лигазой и образуется кольцевая молекула. Кольцевая молекула ДНК фага λ может затем встроиться в бактериальную хромосому при участии фагового гена int, кодирующего белок, который катализирует сайт-специфическую рекомбинацию между участком прикрепления ДНК фага к хромосоме бактерии (attP) и соответствующим бактериальным сайтом (attB или attλ). При этом хромосома λ разрывается в attP-сайте, который локализован в середине генетической карты фага, и в результате происходит изменение последовательности генов в профаге, как это показано на рис. 7.8.
После внедрения в бактериальную хромосому все гены λ, кроме двух, перестают работать (инактивируются) и оказываются под контро-
7. Геном вируса209
|
Рис. 7.8. Карты вирулентного фага и профага λ: показаны механизм интеграции кольцевого генома λ в хромосому хозяина. Сайт attP обозначен символом POP', a сайт attB- символом ВОВ'. |
|
лем репрессора - белка, кодируемого геном cI. Наличие репрессора создает у Е. coli (λ) иммунитет к инфицированию другими фагами λ. Προфаг λ реплицируется как часть родительской хромосомы и наследуется дочерними клетками. В популяции лизогенных бактерий примерно 1 из 106 клеток в каждом поколении вследствие спонтанной индукции профага лизируется и освобождает многочисленное потомство фагов λ (рис. 7.6). Такая способность бактериальной культуры с профагом спонтанно продуцировать фаг объясняет происхождение термина лизогения. Причины спонтанной индукции не ясны, однако известно, что нарушение способности клетки-хозяина реплицировать собственную ДНК может вызвать индукцию. Так, например, ультрафиолетовое облучение индуцирует большинство содержащих профаг клеток культуры. Описаны температурочувствительные мутации сI-гена, вызывающие индукцию при повышенной температуре. Эти мутации дают удобный экспериментальный метод изучения последовательных этапов индукции. Первое событие, связанное с индукцией, - выход профага из хромосомы. Механизм этого процесса аналогичен механизму включения профага.Выход из хромосомы контролируется двумя генами фага λ, int и xis; результатом является образование кольцевого генома λ, который начинает реплицироваться посредством θ-механизма и продуцирует множество дочерних геномов. Впоследствии механизм репликации ДНК меняется на σ-тип. Образующиеся при этом линейные геномы фага инкапсулируются в белковую головку (см. гл. 4).
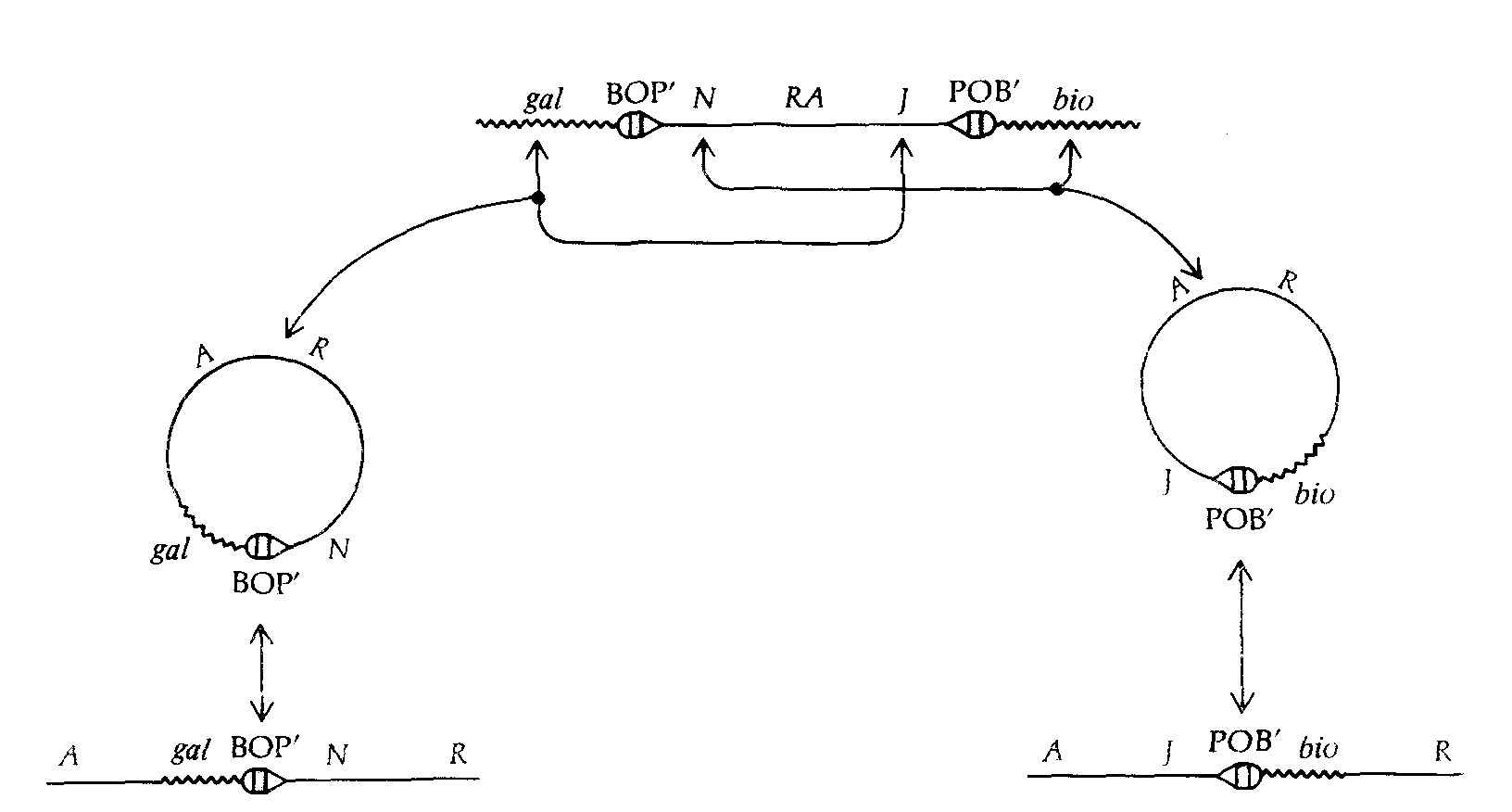
Профаг λ почти всегда вырезается из хромосомы бактерии точно по своим границам, образуя кольцевую форму интактного генома λ. Иногда, однако, вырезание происходит неточно, что приводит к образованию кольцевой молекулы ДНК, в которой один из концевых участковгенома профага утрачен, а вместо него включен участок хромосомы Е. coli, смежный с другим концом генома профага (рис. 7.9). Такие гибридные молекулы могут продуцировать новые жизнеспособные фа-
210Организация и передача генетического материала
|
|
|
Рис. 7.9. Образование трансдуцирующих фагов λgal и λbio в результате неточного вырезания профага из хромосомы бактериальной клетки. |
говые частицы лишь в том случае, если не утрачены какие-либо существенные гены генома λ. Те молекулы, в которые попадает ген bio E, coli (λ bio), жизнеспособны, так как в них обычно отсутствуют лишь несущественные гены между attP и геном N. Напротив, молекулы, в которые попадает ген gal E. coli обычно неполноценны в результате утраты существенных генов, локализованных между attP и левым концом хромосомы. Если какие-либо существенные гены утрачены и фаг неспособен формировать негативные колонии, его называют дефектным и в название такого фага вносится буква d: λdgal. Фаги λdgal или λdbio (в случае, если утрачен существенный ген N) способны размножаться в присутствии нормального фагаλ, компенсирующего функции, нарушенные у этих фагов. Фаги λdgal и λbio легко выявить благодаря их способности трансдуцировать гены gal+ и bio+ в gаl– или bio–бактерии. Эти трансдуцирующие фаги также могут лизогенизировать клетки E. coli (λdgal).
Размер замещенного участка в геноме λ конкретных фаговых штаммов λdgal или λbio можно оценить с помощью комплементационного и рекомбинационного тестов. Например, фагλdgal можно испытывать наспособность либо образовывать рекомбинанты дикого типа в скрещиваниях со множеством различных мутантных линий фага, либо комплементировать с известными мутантами при смешанном инфицировании. В табл. 7.5 представлены данные о наличии или отсутствии рекомбинантов дикого типа при скрещивании нескольких фаговλdgal с носителями определенныхsus-мутаций в различных цистронах. Если в данномштамме λdgal отсутствует соответствующий ген дикого типа, то рекомбинанты дикого типа не образуются. Эти данные позволяют определить положение левого конца, встроенного в геномλ участка генаgal относительно мутаций sus на генетической карте, как это изображено на
7. Геном вируса211
|
Таблица 7.5. Рекомбинация между λdgαl и sus-мутациями в цистронах левого плеча фага λ | |||||
|
|
λ dgal1 |
λdρα12 |
λ dgal3 |
λ dgal4 |
λdgal5 |
|
λ sus A |
— |
+ |
+ |
+ |
+ |
|
λsusB |
— |
— |
+ |
+ |
+ |
|
λsusE |
— |
— |
—- |
+ |
+ |
|
λsusG |
— |
— |
— |
— |
+ |
|
λ susΗ |
— |
— |
— |
— |
+ |
|
λ susΜ |
— |
— |
— |
— |
— |
|
« + » наличие рекомбинантов дикого типа; « — » их отсутствие. По Campbell A. 1959. Virology, 9, 293. | |||||
рис. 7.10. Правый конец этого участка всегда совпадает с сайтом интеграции attP.
После того как получен набор λdgαl фагов с картированными левыми концами, уже легко оказывается определить положение неизвестных точечных мутаций относительно этих концов: требуется лишь узнать, образуются ли рекомбинанты дикого типа между неизвестным мутантом и фагом соответствующей линии λdgαl. Эта методика аналогична методике картирования rII-мутаций с помощью делеций (см. гл. 6).