
- •Редактор Л.М. Тонкошкур
- •УДХТУ, 49005, Дніпропетровськ-5, просп. Гагаріна, 8.
- •Основні характеристики ковалентного зв’язку:
- •Таблиця 1.1
- •Характеристика ковалентних зв'язків
- •Нітроген, пірамідальна будова
- •Оксиген, кутова будова
- •Теорія хімічної будови органічних сполук О.М. Бутлерова
- •Класифікація в залежності від будови вуглецевого ланцюга
- •СПОСОБИ ОДЕРЖАННЯ АЛКАНІВ
- •ХІМІЧНІ ВЛАСТИВОСТІ АЛКАНІВ
- •СПОСОБИ ОДЕРЖАННЯ АЛКЕНІВ
- •ХІМІЧНІ ВЛАСТИВОСТІ АЛКЕНІВ
- •Швидкість приєднання галогеноводнів зменшується в ряду НI > НBr > НCl > НF відповідно із зменшенням міцності зв’язку Н-Hlg.
- •ХІМІЧНІ ВЛАСТИВОСТІ АЛКАДІЄНІВ
- •Природний каучук: цис-1,4-поліізопрен. Гутаперча: транс-1,4-поліізопрен
- •СПОСОБИ ОДЕРЖАННЯ АЛКІНІВ
- •ХІМІЧНІ ВЛАСТИВОСТІ АЛКІНІВ
- •АЛІЦИКЛІЧНІ СПОЛУКИ
- •Циклоалкани. Класифікація, номенклатура та ізомерія
- •Сучасні уявлення про будову циклоалканів
- •СПОСОБИ ОДЕРЖАННЯ ЦИКЛОАЛКАНІВ
- •Спеціальні методи
- •ХІМІЧНІ ВЛАСТИВОСТІ ЦИКЛОАЛКАНІВ
- •АРОМАТИЧНІ ВУГЛЕВОДНІ
- •СПОСОБИ ОДЕРЖАННЯ БЕНЗОЛУ ТА ЙОГО ГОМОЛОГІВ
- •ХІМІЧНІ ВЛАСТИВОСТІ
- •ГЕТЕРОЦИКЛІЧНІ СПОЛУКИ
- •ПЯТИЧЛЕННІ ГЕТЕРОЦИКЛІЧНІ СПОЛУКИ
70
OH |
|
|
OH |
|
OH |
|
+ E + |
E |
|
|
|
Узгоджена: |
|
+ |
|
||
|
NH |
2 |
|
NH |
NH2 |
|
|
|
2 |
E |
|
|
|
|
|
|
|
OH |
|
|
OH |
|
OH |
|
CH3 |
|
|||
Неузгоджена: |
E |
CH3 |
CH3 |
||
|
+ E + |
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
E |
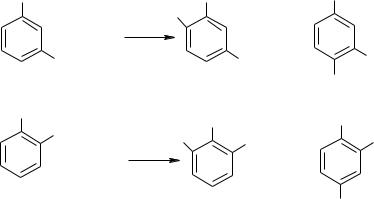
При неузгодженій орієнтації замісників місце входження електрофільного реагенту визначається такими правилами:
1.Вплив замісника, сильноприскорюючого реакції SE завжди переважає вплив інших замісників І-го роду і тим більше замісників ІІ-го роду. Це явище обумовлено утворенням більш стійкого σ-комплексу.
2.Як правило, електрофільний реагент ніколи не входить в положення, яке знаходиться між мета-розташованими замісниками. Це обумовлено просторовими утрудненнями входження нового замісника.
ГЕТЕРОЦИКЛІЧНІ СПОЛУКИ
- циклічні системи в молекулах яких крім атома вуглецю знаходиться гетеро атом (О, N, S). Класифікуються на п’ятичленні цикли, шестичленні цикли. Гетероциклічні сполуки поширені у природі – вони входять до складу хлорофілу і гемоглобіну, багатьох біологічно активних сполук (медикаментів), барвників тощо.
ПЯТИЧЛЕННІ ГЕТЕРОЦИКЛІЧНІ СПОЛУКИ
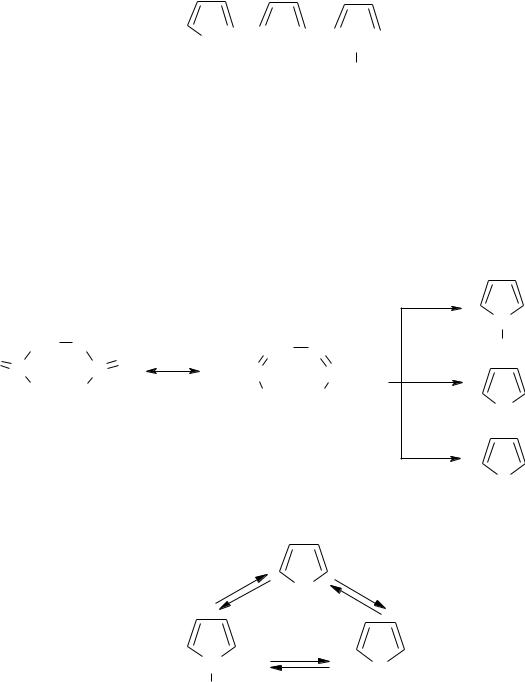
Ароматичність п’ятичленних гетероциклів – фурану, тіофену і піролу зумовлена делокалізацією вільної р-орбіталі гетероатома з утворенням
71
ароматичного секстету електронів. При цьому гетероатом частково лишається нуклеофільних властивостей – здатності до окиснення, утворенню комплексів, алкілуванню.
O
 S
S
 N
N
H фуран тіофен пірол
СПОСОБИ ОДЕРЖАННЯ ПЯТИЧЛЕННИХ ГЕТЕРОЦИКЛІЧНИХ СПОЛУК
1.Всі гетероциклічні сполуки одержують із кам’яновугільної смоли.
2.Із 1,4-дикарбонільних сполук
|
|
|
|
|
|
NH3 |
|
пірол |
|
|
|
|
|
|
|
N |
|
|
CH2 |
CH2 |
|
|
|
|
|
|
O |
O |
CH |
CH |
P2O5 |
H |
|
||
C |
C |
HC |
CH |
|
фуран |
|||
|
H |
H |
|
OH HO |
|
O |
||
бурштиновий альдегід |
бурштиновий альдегід |
|
|
|||||
P2S5 |
|
|
||||||
|
кетона форма |
|
енольна форма |
|
тіофен |
|||
|
|
|
|
|
|
|
S |
|
|
|
|
|
|
|
|
|
|
3. Взаємні перетворення за Юрьєвим (каталізатор – Al2O3, t=5000С)
NH3 |
H2S |
H2O |
O H2O |
N |
H2S |
S |
|
H |
NH3 |
72
ХІМІЧНІ ВЛАСТИВОСТІ ПЯТИЧЛЕННИХ ГЕТЕРОЦИКЛІЧНИХ СПОЛУК
1.Ацидофобність (боязнь кислоти) – руйнування структури під дією мінеральних кислот. Ацидофобніть мають фуран і пірол. Тіофен – не ацидофобний, так як має більш високу ароматичність та значну меншу здатність гетеро атома сірки до протонування:
.. |
+ |
HCl |
+ |
+ |
N |
|
|
N |
|
H |
|
|
H |
H |
.. |
+ |
HCl |
+ |
+ |
O |
|
|
O |
|
|
|
|
H |
|
полімеризація Cl 

Cl полімеризація
2.Кислотно-основні властивості піролу.
Кислотні властивості. Пірол має властивості слабкої кислоти. Він значно
слабше ніж метиловий спирт і більш сильна кислота ніж анілін.
H+ |
+ |
.. аніон пірілію |
N |
|
N |
H |
|
|
Це достатньо стабільний аніон, так як негативний заряд стабілізований мезомерною делокалізацією в циклі.
Як кислота пірол взаємодіє з металевим натрієм або калієм з утворенням солей піролу:
73
|
Na |
|
+ |
H+ |
або |
|
|
N |
|||
|
|
|
|
|
|
N |
|
Na+ |
|
|
|
H |
CH3MgI |
|
|
|
|
|
|
+ H+ |
або |
||
|
- CH4 |
N |
|||
|
+ |
|
|
||
|
|
|
|
||
|
|
MgI |
|
|
|
N |
Na + |
.. |
|
|
+ |
N |
MgI |
|
|
.. |
|
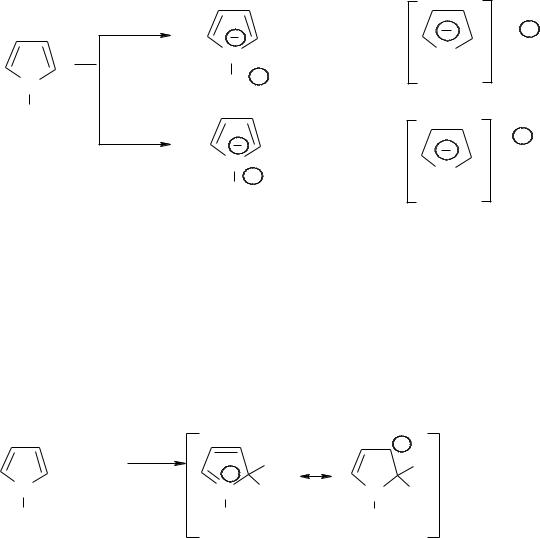
Основні властивості. Пірол має властивості слабкої основи так як пара електронів атому азоту у піролі приймає участь у супряженні, з утворенням π-електронної ароматичної системи. Тому приєднання протону до піролу проходить важко при достатньо високій концентрації Н+ і приводить до порушення ароматичності піролу.
Встановлено, що протонування проходить за α-вуглецевим атомом
+ H+ |
|
H |
+ |
H |
|
.. |
|||
N |
+ |
|
||
N |
H |
N H |
||
H |
H |
|
H |
|
|
граничні структури |
|
||
|
катіон пірілію - не має ароматичного характеру |
|||
так як приєднання протону пройшло за рахунок двох електронів із ароматичної π-електронної системи.
3.Реакції електрофільного заміщення
а.Нітрування. Так як фуран і пірол ацидофобні, то всі реакції електрофільного заміщення проходять при дії спеціальних агентів, які не мають кислотного характеру. Нітрують фуран і пірол сумішшю оцтового ангідриду з нітратною кислотою в піридині (ацетилнітратом).
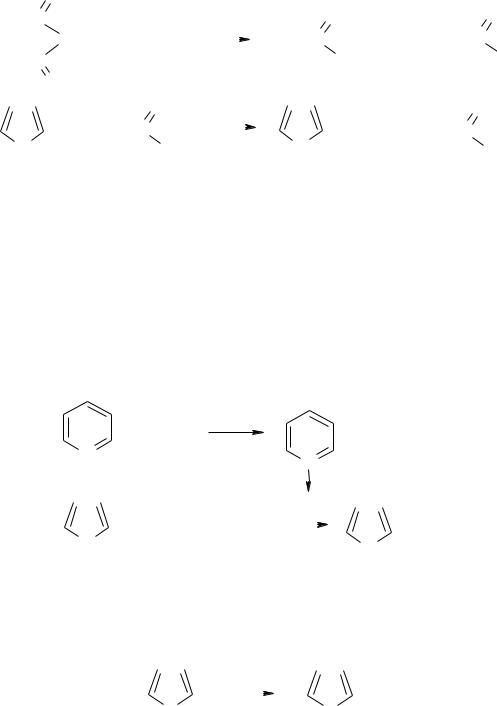
|
|
|
|
|
|
|
|
|
|
|
|
|
|
74 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
H3C |
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
O |
+ HO |
|
NO2 |
|
|
H3C |
|
C |
|
+ H3C |
|
|
C |
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||
H3C |
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
ONO2 |
|
|
|
|
OH |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
α + H3C |
|
C |
піридин |
α |
NO2 + |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
H3C |
|
|
C |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
X |
|
|
ONO2 |
|
|
X |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||||
X = O, NH
Хоча тіофен і не ацидофобний його також нітрують ацетил нітратом, так як нітратна кислота може викликати окиснення і осмолення тіофену.
б. Сульфування. За причиною ацидофобності фурану і піролу, їх сульфують комплексом піридину з сірчаним ангідридом – піридинсульфотриоксид.
N |
+ SO3 |
|
N |
||
|
|
α |
+ C5H5N.SO3 |
SO3 |
|
|
α |
SO H . C H N |
|||
|
||||||||||
|
|
|||||||||
|
|
|
|
|
||||||
|
|
|||||||||
X |
|
|
X |
|||||||
|
|
|
3 |
5 |
5 |
|||||
|
|
|
|
|
|
|
|
|||
X = O, NH
Тіофен не ацидофобний, тому його сульфують концентрованою
сульфатною кислотою при кімнатній температурі: |
|
|
|
||||||
|
|
α |
H2SO4! |
|
|
|
SO3H |
||
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
S |
|
t кімнатна |
S |
|||||
|
|
|
|
||||||
|
|
|
|
|
|||||
α − сульфотіофен Реакція сульфування тіофену при кімнатній температурі застосовують
для виділення тіофену із кам’яновугільної смоли і з бензолу.
в. Ацилювання здійснюється за м’яких умов на каталізаторі ZnCl2 (або StCl2).
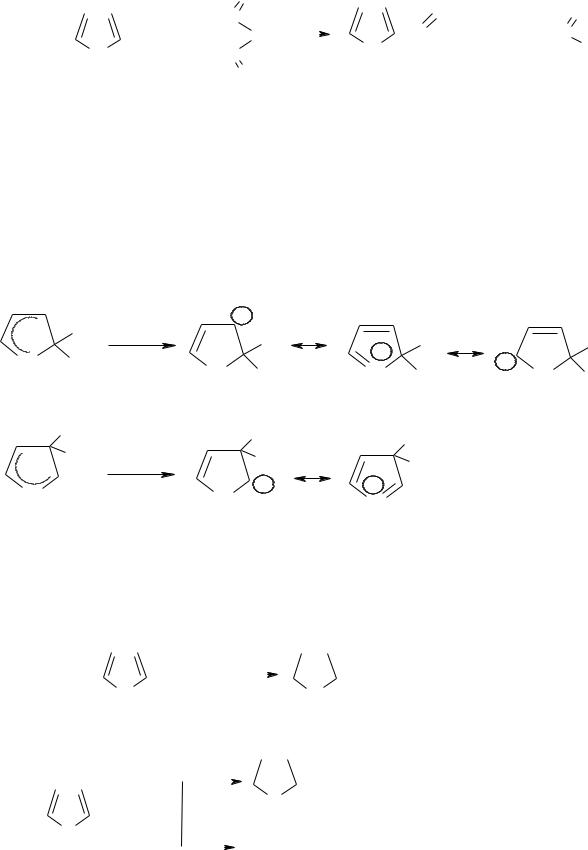
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
O |
|||
|
|
|
H3C |
|
|
|
C ZnCl2 |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
α |
|
|
|
|
|
|
|
|
|
CH3 + H3C |
|
|
|||||
|
X |
+ H3C |
|
|
|
O |
|
|
|
X |
|
C |
|
|
C |
OH |
|||
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
C |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
X = O, S, NH |
|
|
|
O |
α -ацетил ... |
|
|
|
|||||||||||
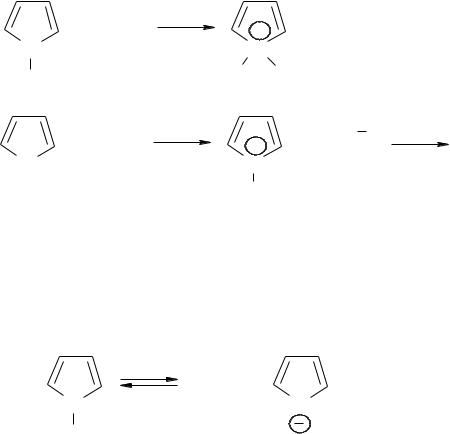
Всі реакції електрофільного заміщення у фурані, тіофені, піролі проходять легше, ніж у бензолі, так як п’ятичленні гетероцикли є більшими донорами електронів ніж бензол.
Механізм SE (електрофільне заміщення) в основному у α-положенні, так як при цьому σ-комплекс має меншу енергію і відповідно більшу стійкість, ніж
σ-комплекс при заміщенні електрофілу у β-положенні. |
|
|
||||||
+ |
H |
|
+ |
|
|
|
|
|
|
H |
+ |
H |
|
H |
|||
X |
E |
X E |
|
+ |
|
|||
X E |
X E |
|||||||
α − σ − комплекс |
|
|||||||
|
|
|
|
|
|
|||
|
H |
|
H |
|
H |
|
|
|
+ |
E |
|
E |
+ |
E |
|
|
|
X |
|
X |
+ |
|
|
|
||
|
|
X |
|
|
|
|||
β − σ − комплекс |
|
|
|
|
|
|
||
3.Реакції приєднання
a. Приєднання водню Для фурану
|
|
|
|
+ |
2 H2 |
|
t, p |
|
|
|
тетрагідрофуран |
||
|
|
|
|
|
|
|
|||||||
|
|
|
O |
|
Ni |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
O |
||||
Для тіофену |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
t, p |
|
|
|
|
|
реакц³я г³друван н ÿ |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
+ 2 H2 |
|
|
Pd |
|
|
|
S |
||||
|
|
|
|
|
|
|
|||||||
|
S |
|
|
t, p |
тетраг³дро т³о ф ен |
||||||||
|
|
|
|||||||||||
|
|
|
|
|
|
C4H10 + S реакц³я ро зкрит т я циклу |
|||||||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
Ni |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Для піролу (єдиний гетеро цикл, який відновлюється воднем в момент виділення)
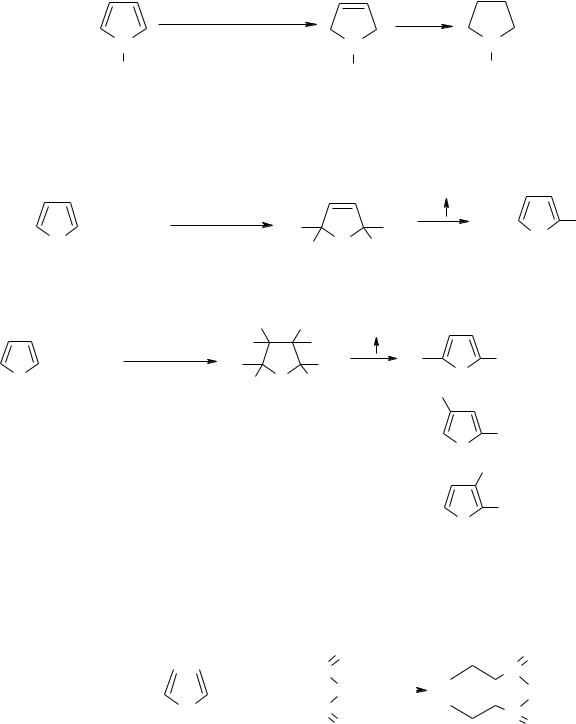
|
76 |
|
|
|
Ni |
|
|
|
CH3COOH + Zn |
H2 |
|
N |
N |
Pt |
N |
H |
H |
|
H |
|
піролін |
|
піролідін |
b. Приєднання галогенів Приєднання брому
|
|
+ |
t кімнатна |
Br |
|
H |
|
t |
|
|
Br |
|
|
O |
Br2 |
|
O |
- HBr |
|
O |
|||||
|
|
|
|
H |
Br |
|
|
|||||
|
|
|
|
|
|
2-бромфуран |
||||||
|
|
|
|
|
|
|
|
|
|
|||
|
Приєднання хлору |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
Cl |
H |
|
|
|
|
|
|
|
|
+ 2 Cl2 |
t кімнатна |
H |
Cl |
|
t |
Cl |
|
Cl |
2,5-дихлортіофен |
||
|
Cl |
H |
|
|
S |
|||||||
S |
|
|
- 2HCl |
|||||||||
|
|
|
H |
S Cl |
|
|
|
|
2% |
|||
|
|
|
|
|
Cl |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
Cl |
2,4-дихлортіофен |
|
|
|
|
|
|
|
|
|
|
Cl |
|
44% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
2,3-дихлортіофен |
|
|
|
|
|
|
|
|
|
|
S |
|
|
54% |
4. Реакції дієнового синтезу (Реакції Дільса-Альдера). Це реакції за якими
можна розрізнити п’ятичленні гетероцикли. |
|
|
|
|
|
||||||||||
a. Легше всього вступає фуран і веде себе як дієн. |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
+ |
HC |
|
C |
|
|
|
|
C |
||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
O |
||||
|
|
|
|
|
|
|
|||||||||
|
|
HC |
|
|
C |
|
|
|
|
C O |
|||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||||||
фуран |
|
|
|
|
|
|
O |
|
|
|
|
||||
малеїновий ангілрид |
|
|
аддукт |
||||||||||||
дієн |
|
|
дієнофіл |
|
|
|
|
|
|||||||
b.Пірол також вступає в реакції дієнового синтезу з малеїновим ангідридом, але за іншим механізмом
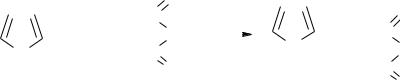
|
|
|
|
|
|
|
|
|
|
|
|
|
77 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HC |
|
C |
O |
|
|
|
|
|
|
|
|
|
|
|
O |
||||
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
C |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
O |
|
|
N |
|||||||||||
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
HC |
|
|
C |
O |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H CH |
|
|
|
C |
|||||||
|
H |
|
|
|
|
|
|
|
|
2 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||
пірол |
малеїновий ангілрид |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
ангідрид 2-пірилбурштинової кислоти |
|||||||||||||||||||||||
дієн |
|
|
дієнофіл |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
c.Тіофен в реакції дієнового синтезу у таких умовах не вступає. Він реагує тільки з дуже реакційно здатними дієнофілами.
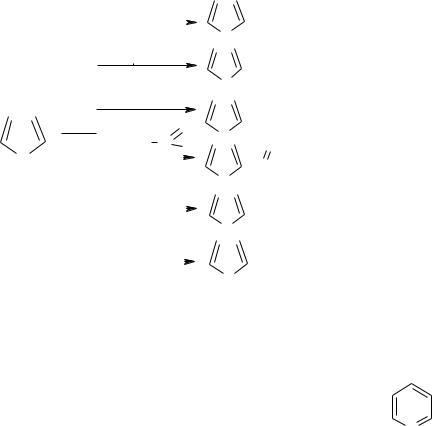
За своїми хімічними властивостями фуран займає проміжне положення між спряженими дієнами і ароматичними сполуками. Він дає реакцію дієнового синтезу з дієнофілами, наприклад малеїновим ангідридом, окиснюється легше, ніж тіофен. При дії мінеральних кислот на молекули фурану і піролу протон кислоти приєднується до гетероатому за рахунок його вільної електронної ари, що приводить до порушення ароматичності молекул, полімеризації та осмоленню дієнів, що утворились. Таке відношення сполук до кислот зветься ацидофобністю. У зв’язку з ацидофобністю піролу і фурану вони не сульфуються і нітруються кислотами.
Звернути увагу на методи одержання фурану, тіофену і піролу, а також на можливість взаємних перетворень цих пятичленних гетероциклів за Юр’євим.
Ароматичні властивості найбільш виражені у тіофені. Він більш стійкий до дії кислот і окиснювачів, і не реагує з дієнофілами. Атом сірки у тіофені більш інертний, алкілується лише в жорстких умовах, не виявляє ацидофобності. Тіофен сульфується на холоду сульфатною кислотою. Ця реакція використовується для очищення бензолу від домішок тіофену, який в цих умовах не сульфується.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
78 |
|
|
|
|
|
|
|
||||
|
|
|
+ Br2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
2-бромтіофен |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
-HBr |
|
|
|
|
|
|
S |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
+ HNO |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
NO2 |
2-нітротіофен |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
- H O |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
2 |
|
|
|
|
|
|
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
+H2SO4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2-тіофенсульфокислота |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
- H2O |
O |
S |
|
|
|
|
|
|
|
SO2OH |
||||||||||||
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
+ CH3 |
C Cl |
|
|
|
|
|
|
|
|
|
|
O |
|
|||||||||
S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2-ацетилтіофен |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
- SnCl (-HCl) |
S |
|
|
|
|
|
|
C CH3 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
+ H2C |
|
CH2 |
|
|
|
|
|
|
|
|
|
C2H5 |
2-етилтіофен |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
AlCl3 |
|
|
|
|
|
|
S |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
+ CH2O , HCl |
|
|
|
|
|
|
|
|
|
|
CH2Cl |
2-хлорметилтіофен |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
хлормети- |
|
S |
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
лювання |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
ШЕСТИЧЛЕННІ ГЕТЕРОЦИКЛІЧНІ СПОЛУКИ
Структура шестичленного гетероциклу – піридину N нагадує бензол. У них близькі довжини зв’язків у циклах (0,140 нм у бензолі, 0,137-0,139 нм в піридині). Валентний кут між зв’язками в обох молекулах 1200С. На
відміну від неполярного бензолу кільце піридину являє собою диполь з великим електричним моментом. Негативний заряд в піридині розташований на атомі нітрогену, а позитивний – на атомі карбону. Вільна р-електронна пара атому нітрогену не приймає участі в утворенні ароматичного секстету, тому нуклеофільні властивості атому нітрогену за рахунок цієї пари електронів зберігаються. Він може приєднувати протон, галогеналкіли, галогени. В цих реакціях піридин веде себе, як основа – третинний амін.
Дефіцит електронної густини на атомах карбону піридинового кільця зумовлює його низьку активність в реакціях електрофільного заміщення (меншу ніж у нітробензолі) і підвищену активність в реакціях нуклеофільного заміщення. Відповідно до розподілу електронної густини має місце β-орієнтація в реакціях електрофільного заміщення і α- , γ- орієнтація в реакціях нуклеофільного заміщення. Електрофільне заміщення потребує жорстких умов
79
і дає невисокі виходи продуктів. Звернути увагу на легкість розкриття кільця піридину на відміну від бензолу.
ОСОБЛИВОСТІ РЕАКЦІЇ ЕЛЕКТРОФІЛЬНОГО ЗАМІЩЕННЯ
Під впливом атому азоту в піридині зменшується електронна густина особливо в α- і γ-положеннях, тому реакції нуклеофільного заміщення проходить в ці положення (2, 4, 6), а реакції електрофільного заміщення в β- положення (3, 5). Таким чином, електрофільне заміщення в піридині проходить трудніше ніж у бензолу. Тому є такі причини:
∙За рахунок електроно-акцепторного впливу атому азоту піридинового кільця менш нуклеофільне ніж бензол;
∙Реакції електрофільного заміщення (нітрування, сульфування) проходять у кислому середовищі, тобто у таких умовах, коли піридин маючи основні властивості утворює солі.
α
β
+ E+
 N
N
γ
|
+ |
|
|
+ |
|
|
H |
+ |
H |
H |
|
N |
|
||||
E |
N |
E |
|
N E |
|
|
|
||||
|
H |
+ |
H |
|
H |
|
E |
|
|
||
|
|
E |
|
E |
|
N |
+ |
|
+ |
||
N |
|
N |
|||
H |
E |
H E |
|
H |
E |
+ |
|
|
+ |
|
|
N |
|
N |
|
+ |
|
|
|
N |
|
Приєднання електрону в α- або γ-положеннях приводить до появлення позитивного заряду на атомі азоту , який є найбільш електронегативним атомом в піролу, що енергетично не вигідно.

80
При заміщенні в β-положенні проміжний σ-комплекс найбільш стабілізований за рахунок де локалізації позитивного заряду між атомами вуглеця.
ПИТАННЯ ДО КОНТРОЛЬНОЇ РОБОТИ №1
1. Дати назви алкану за двома номенклатурами: раціональною та систематичною.
H3C |
|
|
CH3 |
|
|
CH2 |
|
CH3 |
|||||||
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
CH2 |
|
CH |
|
|
CH2 |
|
CH2 |
|||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
CH3 |
||||
2.Синтезувати н-гексан, навести для цього вуглеводню схему і механізм реакції його хлорування.
3.Здійснити поступовий ланцюг перетворень:
3-метил-1-бутен |
НCl |
А |
КОН |
Б |
HBr |
В |
|
спирт. |
H2O2 |
||||
|
|
|
|
|
||
|
|
|
розчин |
|
|
|
Дати назву сполукам. Навести та пояснити механізм одержання сполуки “А”.
4.Навести структурні формули: 1,3-пентадієну та 1,4-пентадієну. Порівняти взаємне розташування π-зв’язків в них. Супряження. Енергія супряження, її визначення.
5.Навести для 1-бутину реакції нуклеофільного приєднання: води, спиру, оцтової кислоти.
6.Дати назви алкану за двома номенклатурами: раціональною та
систематичною.
H3C |
|
|
|
CH |
|
CH2 |
|
CH3 |
|||||||
|
|
|
|
||||||||||||
|
|||||||||||||||
H3C |
|
|
|
C |
|
|
CH2 |
|
|
|
CH2 |
||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
||||||||||
H3C |
|
|
CH2 |
|
|
|
CH3 |
||||||||
|
|
|
|
|
|||||||||||
7.Природа хімічних зв’язків в органічних сполуках: іонні та ковалентні зв’язки, характеристики ковалентного зв’язку. Донорно-акцепторний та семіполярний зв’язки. Навести приклади.

81
8.Синтезувати 2,3-диметилбутан всіма відомими способами, навести для цього вуглеводню схему і механізми реакції його хлорування.
9.Здійснити поступовий ланцюг перетворень:
3-метил-1-бутен |
НCl |
А |
КОН |
Б |
HBr |
В |
|
спирт. |
H2O2 |
||||
|
|
|
|
|
||
|
|
|
розчин |
|
|
|
Дати назву сполукам. Навести та пояснити механізм одержання сполуки “А”.
10.Одержати 2,3-диметил-1,3-пентадієн. Навести для нього реакції бромування та окиснення.
11.Дати назви алкану за двома номенклатурами: раціональною та систематичною.
H3C H3C CH2 CH3 CH C CH CH2
H3C CH3 CH3
12.Гібридизація атома вуглецю. Навести атомно-орбітальну модель молекул етану, етену та ацетилену. Вказати валентні кути.
13.Синтезувати з галогеналканів 2,5-диметилгексан двома способами. Навести та пояснити реакцію та механізм реакцій його нітрування.
14.Пояснити, скільки ізомерних алкенів відповідають емпіричній формулі С4Н8? Навести структурні формули та назви цих ізомерів. Для одного з ізомерів, який містить третинний атом карбону, навести реакції гідрохлорування і гідратації.
15.Для 3-метил-1-бутину навести реакції з HCl, HCN, С2Н5ОН, СН3СОСН3. 16.Дати назви алкану за двома номенклатурами: раціональною та
систематичною.
CH3 CH3
H2C CH CH2
H3C CH CH2 CH3
17.Здійснити перетворення та дати назви продуктам реакцій:

82
|
|
|
|
|
|
|
|
|
|
|
|
|
+NaOHòâ. |
|
SO |
2 |
+ Cl , hν |
? |
|
|
|
|
|
CH3 |
O |
|
|
|
|
|
À |
|
2 |
||||
|
|
|
|
|
|
|
|
|
t0 |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
CH |
|
|
C |
|
|
C |
|
|
|
|
|
|
|
|
|
|||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
H |
O |
|
Na |
+ |
|
електро л³з |
Á |
|
Cl2, hν |
? |
|||||||
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Í 2Î
18.Здійснити поступовий ланцюг перетворень:
HBr А
ізобутилен 
HBr Н2О2  Б
Б
Дайте назву сполукам. Навести та пояснити механізм одержання сполук “А”
19.Хімічні властивості алкадієнів: на прикладі 1,3-пентадієну навести схеми реакцій: а) приєднання хлороводню; б) окиснення в жорстких умовах.
20.Для 2-пентину навести реакції з HCl, HCN, С2Н5ОН, СН3СОСН3
21.Дати назви алкану за двома номенклатурами: раціональною та систематичною.
CH2 CH3
CH3 CH2 CH2 CH3 H3C CH CH CH CH3
22.Здійснити перетворення та дати назви продуктам реакцій:
|
|
|
|
|
|
|
|
|
+NaOHòâ. |
|
|
SO |
2 |
+ Cl , hν |
|
|
|
|
O |
|
À |
|
2 |
||||||
|
|
|
|
t0 |
|
|
|
|||||||
H3C |
|
CH2 |
CH2 |
C |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
O |
|
Na+ |
електро л³з |
|
Á |
|
Cl2, hν |
|||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
Í 2Î |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
?
?
23.Здійснити поступовий ланцюг перетворень:
HBr À
2-м ети л-2-бутен
HBr
Í 2Î 2  Á
Á
Дайте назву сполукам. Навести та пояснити механізм одержання сполук “А”
83
24.Хімічні властивості алкадієнів: на прикладі 2,4-гексадієну навести схеми реакцій: а) приєднання бромоводню; б) окиснення в жорстких умовах.
25.Для 3-метил-1-пентину навести реакції з HCl, HCN, С2Н5ОН, СН3СОСН3 26.Дати назви алкану за двома номенклатурами: раціональною та
систематичною.
|
|
H3C |
|
|
CH2 |
|
|
CH3 |
|||||||
|
|
|
|
|
|
||||||||||
|
|
|
C |
|
|
CH3 |
CH3 |
||||||||
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|||||||||
H2C |
|
CH2 |
|
|
C |
|
CH2 |
|
CH2 |
||||||
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
||||||||||
CH3 |
CH2 |
|
|
CH3 |
|||||||||||
|
|
||||||||||||||
27.Здійснити перетворення та дати назви продуктам реакцій:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+NaOHòâ. |
|
|
SO |
2 |
+ Cl , hν |
? |
|
|
|
|
|
|
|
|
|
CH3 |
O |
|
|
|
|
|
À |
|
2 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
t0 |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
H |
C |
|
CH |
|
|
C |
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
3 |
|
|
|
2 |
H |
O |
|
Na |
+ |
|
електро л³з |
|
Á |
|
Cl2, hν |
? |
. |
||||||
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Í 2Î |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
28.Синтезувати 2,3-диметилпентан всіма відомими способами, навести для цього вуглеводню схему і механізми реакції його хлорування.
29.Здійснити поступовий ланцюг перетворень:
2-м етил-1-бутен |
Í Br |
À |
ÊÎ Í |
Á |
HBr |
 |
|
ñï èðò. |
H2O2 |
||||
|
||||||
|
|
|
|
|
||
|
|
|
ðî ç÷èí |
|
|
|
Дати назву сполукам. Навести та пояснити механізм одержання сполуки “В”.
30.Для 2,3-диметил-1,3-пентадієну навести реакції приєднання бром оводню, озонолізу, дієнового синтезу (дієнофіл – акролеїн).
31.Дати назви алкану за двома номенклатурами: раціональною та систематичною.
H3C CH2 CH3
H3C C CH2
H3C C CH3
H3C CH2
32.Поняття про гомологічний ряд: гомологи та гомологічна різниця. Структурна ізомерія. Поняття про структурні ізомери та конформери.

84
33.Синтезувати з галогеналканів ізопропілізобутилметан двома способами. Навести та пояснити реакцію та механізм реакцій його нітрування.
34.Пояснити, скільки ізомерних алкенів відповідають емпіричній формулі С5Н0? Навести структурні формули та назви цих ізомерів. Для одного з ізомерів, який містить третинний атом карбону, навести реакції гідро
хлорування (механызм) і гідратації.
35.Для 3-метил-1-пентину навести реакції з HCN, С2Н5ОН, СН3СООН. 36.Дати назви алкану за двома номенклатурами: раціональною та
систематичною.
CH3
H3C CH CH2 CH3
H3C CH CH CH2 CH3
37.Одержати диметилізопропілметан із відповідних карбонових кислот: а) електролізом, б) сплавленням з лугом. Навести схему та пояснити механізм реакції сульфохлорування диметилізопропілметану..
38.Хімічні властивості алкенів: гідрогалогенування та гідратація на прикладі 3-метил-1-бутену, механізм реакцій з НBr. Правило Марковнікова.
39.Навести структурні формули алкадієнів складу С6Н10 і вказати тип
гібридизації кожного із атомів карбону. Привести реакції за допомогою яких дані ізомери можливо розрізнити (окиснення, дієновий синтез).
40.Навести для 3-метил-1-бутину реакції нуклеофільного приєднання: води, спиру, оцтової кислоти.
41.Дати назви алкану за двома номенклатурами: раціональною та систематичною.
CH3 CH3
CH CH2 C CH3
CH2 CH2 CH3
CH CH3
CH3

85
42.Одержати 2,3-диметилбутан із відповідних карбонових кислот: а) електролізом, б) сплавленням з лугом. Навести схему та пояснити механізм реакції хлорування 2,3-диметилбутану.
43.Хімічні властивості алкенів: гідрогалогенування та гідратація на прикладі 1-бутену, механізм реакції з HBr. Правило Марковнікова.
44.Навести структурні формули алкадієнів, які мають у своїй структурі 6 атомів карбону і вказати тип гібридизації кожного із атомів карбону. Привести реакції за допомогою яких дані ізомери можливо розрізнити (окиснення дієновий синтез).
45.Навести для 3-метил-1-бутину реакції нуклеофільного приєднання: води, спиру, оцтової кислоти.
46.Дати назви алкану за двома номенклатурами: раціональною та систематичною.
CH3
H3C C CH3 H3C CH CH2
CH2 CH2
H3C CH2
47.За допомогою яких реакцій можна здійснити перехід: 3-метил-1- бутен→2,7-диметилоктан.
48.Навести реакції озонолізу наступних алкенів: а) 2-бутену, б) 2-метил-2- бутену, в) 1-бутену. Для алкену б) навести схему та механізм реакції гідробромування.
49.Для 2,3-диметил-1,3-пентадієну навести реакції приєднання бромоводню, озонолізу.
50.Одержати з ацетилену метилетилацетилен. Навести для нього реакцію з НСl та СН3СООН.
51.Дати назви алкану за двома номенклатурами: раціональною та систематичною.
86 |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
CH3 |
||
|
H3C |
|
|
|
|
|
C |
|
CH3 |
|||
|
|
|
|
|
||||||||
|
|
|
|
|||||||||
H3C |
|
|
CH |
|
|
|
|
|
|
|
||
|
|
|
|
|
CH2 |
|||||||
|
|
|||||||||||
|
|
|
|
|
||||||||
|
|
|
CH |
|
|
|
CH3 |
|||||
|
|
|
2 |
|
|
|||||||
52.Навести реакції озонолізу та вичерпного окиснення наступних алкенів та вказати умови їх проведення: а) 2-бутену, б) 2,3-диметил-2-бутену. Для алкену б) навести схему та механізм реакції гідробромування.
53.Навести структурні формули: 1,3-пентадієну та 1,4-пентадієну. Порівняти взаємне розташування π-зв’язків в них. Супряження, визначення.
54.Одержати з ацетилену пропіл ацетилен і метилетилацетилен та описати їх будову. За допомогою яких реакцій їх можна відрізнити.
55.Пояснити, які із сполук (а-д) виявляють ароматичні властивості: а) б) в)
 N
N
+
Сформулювати критерії ароматичності. Навести π-електроноорбітальну формулу сполуки а).
56.Одержати пропілбензол за реакцією Фріделя-Крафтса. Механізм цієї реакції. Навести структурні формули та дати назву гомологам бензолу загальної формули С10Н14.
57.Порiвняти будову, навести рiвняння реакцiй сульфування бензолу і фурану. Пояснити умови цих реакцiй на основi особливостей структури бензолу і фурану.
58.Пояснити, які із сполук (а-д) виявляють ароматичні властивості: а) б) в)
+
Сформулювати критерії ароматичності.
59.Скласти рівняння реакцій за нижченаведеними схемами:
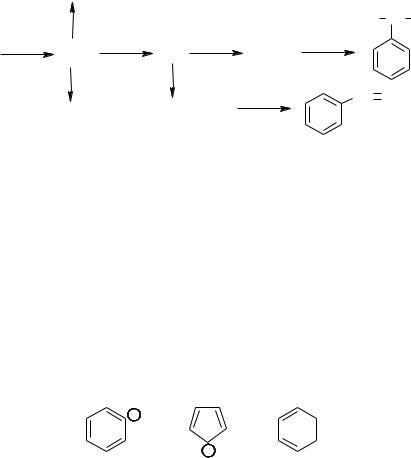
87
C3H4
H3C CH CH3
CaC2 |
? |
C2H2 |
C6H6 |
C6H5Сl |
|
||||
|
|
C2H6 |
C6H5CH2CH3 |
CH CH2 |
|
|
|
60.Зазначити умови перебігу реакцій, дати назву сполукам. Навести механізм одержання сполуки С6Н5Сl.
61.Порiвняти будову бензолу, тiофену i фурану. Навести рiвняння реакцiй
сульфування бензолу, тiофену i фурану. Порiвняти та пояснити умови цих реакцiй на основi будови даних сполук.
62.Пояснити, які із сполук (а-г) відповідають правилу Хюккеля і виявляють
ароматичні властивості: |
|
|
а) |
б) |
в) |
|
− |
|
−
63.Розташувати наведені нижче сполуки за зменшенням їх реакційної здатності в реакціях нітрування: бензол, толуол, сульфобензол. Відповідь обгрунтувати. Навести схеми нітрування кожної сполуки та механізм на прикладі бензолу.
64.На основi сучасних уявлень про будову тiофену та пiролу, порiвняти реакційну здатність цих сполук. Навести схеми вiдповiдних реакцiй.
Пояснити, чому пiрол не можна сульфувати концентрованою сульфатною кислотою.
65.Розташувати наведені нижче сполуки за зменшенням їх реакційної здатності в реакціях нітрування: бензол, пропілбензол, бензойна кислота, бензолсульфокислота. Відповідь обгрунтувати. Навести механізм нітрування на прикладі бензолу.
66.Охарактеризувати будову фурану, тіофену, піролу. Пояснити ароматичний характер цих сполук (правило Хюккеля, розподіл
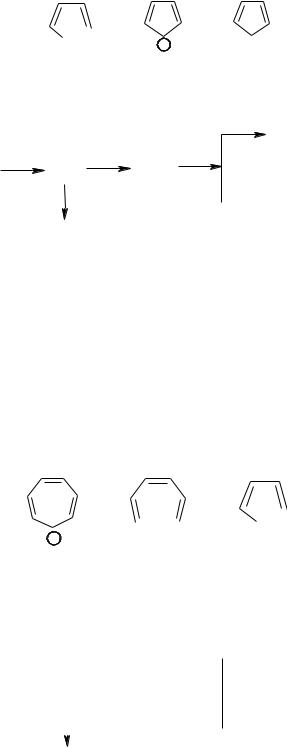
88
електронної густини). Обгрунтуванти реакційну здатність даних гетероциклів.
67. Пояснити , які із сполук (а-г) є ароматичними: а) б) в)
O −
−
Сформулювати критерії ароматичності та правило Хюккеля. 68.Скласти рівняння відповідних реакцій (назвати всі сполуки):
|
|
C6H5Cl |
CH4 |
C2H2 |
C6H6 |
 C6H5SO3H
C6H5SO3H
C3H4
Навести механізм одержання хлорбензолу.
69.Навести схеми реакцій бромування і сульфування фурану, тіофену, піролу. Пояснити умови перебігу реакцій та механізм (для одної з сполук). Обгрунтувати, який з цих гетероциклів вступає в реакцію дієнового синтезу.
70.Пояснити, які із сполук (а-д) відповідають критеріям ароматичності: а) б) в)
+ S
S
Відповідь обгрунтувати. Навести π-електроноорбітальні формули сполук б) та в).
71.Скласти рівняння відповідних реакцій:
 C6H5NO2
C6H5NO2
CH4  C2H2
C2H2 C6H6
C6H6 
 C6H5CH3
C6H5CH3

 C6H5SO3H C2H6
C6H5SO3H C2H6
Назвати всі сполуки. Навести механізм одержання нітробензолу.

89
72.Охарактеризувати специфічні властивості піролу і фурану (кислотність, дієновий синтез). Навести рівняння відповідних реакцій.
73.З огляду на бензол та правила орієнтації в реакціях SE синтезувати наступні сполуки:
à) |
NO2 |
á) |
COOH |
â) |
CH3 |
|
|
Br |
Br |
|
C2H5 |
|
|
|
|
|
Навести механізм утворення нітробензолу.
74.Охарактеризувати будову фурану та піролу. Пояснити, чому ці сполуки не можна сульфувати концентрованою сульфатною кислотою. Навести схему реакції сульфування. Вказати умови перебігу реакції сульфування для цих сполук.
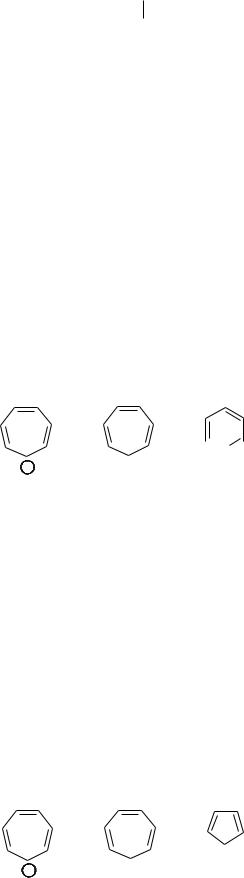
75.Порівняти будову та властивості таких пар сполук: а) циклопропен та катіон циклопропенілію; б) циклогептатриєн та катіон циклогептатриєнілію. Обгрунтувати відповідь на основі критеріїв ароматичності.
76.Написати рівняння реакцій за допомогою яких можна здійснити такі перетворення:
ò î ëóî ë  бен зо йн а кисло т а
бен зо йн а кисло т а
ци кло гексан  áåí çî ë
áåí çî ë  сульф о бен зо л
сульф о бен зо л
гексахло рци кло гексан
Навести механізм одержання нітробензолу.
77.Порiвняти та пояснити ароматичний характер фурану і тiофену виходячи з їх будови. Яка з цих сполук вступає в реакцiю дiєнового синтезу? Навести рiвняння вiдповiдної реакцiї, вiдповiдь обгрунтувати.
78.Написати рівняння реакцій за допомогою яких можна здійснити такі перетворення:
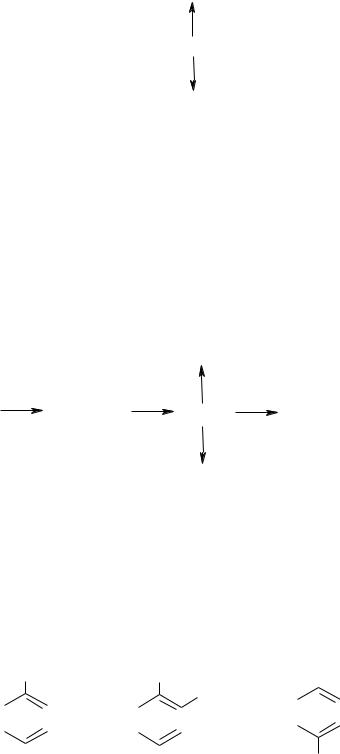
90
бромбензол
метан  ацетилен
ацетилен  бензол
бензол  нітробензол
нітробензол
гексахлорциклогексан
Навести механізм одержання бромбензолу.
79.Охарактеризувати будову фурану, тіофену, піролу. Пояснити ароматичний характер цих сполук (правило Хюккеля, розподіл електронної густини). Обгрунтуванти реакційну здатність даних гетероциклів.
80.Написати рівняння реакцій за допомогою яких можна здійснити такі перетворення:
|
|
ізопропілбензол |
|
метан |
ацетилен |
бензол |
хлорбензол |
гексахлорциклогексан
Навести механізм одержання ізопропілбензолу.
81.Порiвняти будову i властивостi пiролу та бензолу. Порiвняти та пояснити умови нiтрування пiролу та бензолу.
82.З огляду на бензол та правила орієнтації в реакції SE синтезувати наступні сполуки:
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
CH3 |
|
а) H3C C CH3 |
б) |
NO2 |
в) |
|
|
|
||||||||||
|
|
|||||||||||||||
|
|
|
|
|||||||||||||
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
C2H5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NO2
Навести механізм утворення сполук "а".
83.Навести схеми реакцій бромування і сульфування фурану, тіофену, піролу. Пояснити умови перебігу реакцій. Обгрунтувати, який з цих гетероциклів вступає в реакцію дієнового синтезу.
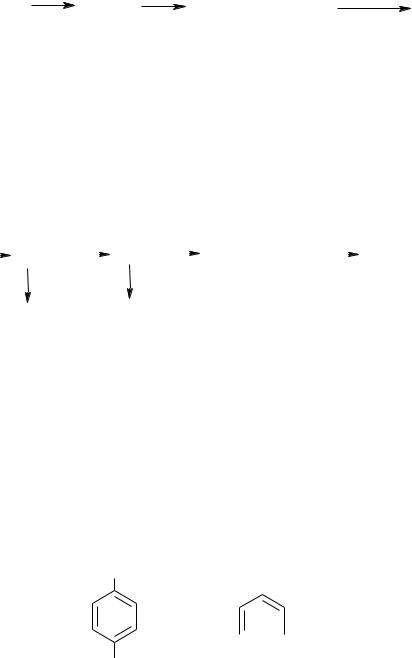
91
84. Бензол має ароматичний характер. Пояснити цей факт, зобразивши його орбітальну будову та використовуючи критерії ароматичності
85.Здійснити поступовий ланцюг перетворень:
бензол |
толуол |
бензойна кислота |
Сl2 |
А |
|
FeCl3 |
|||||
|
|
|
|
Навести механізм реакції одержання толуолу.
86.Охарактеризувати будову фурану та піролу. Пояснити, чому ці сполуки не можна сульфувати концентрованою сульфатною кислотою. Навести схему реакції сульфування. Вказати умови перебігу реакції сульфування для цих сполук.
87.Скласти рівняння реакцій за нижченаведеними схемами:
CH4 |
|
C2H2 |
|
C6H6 |
|
|
бромбензол |
|
³çî ï ðî ï ³ëáåí çî ë |
|
|
|
|
|
|||||
|
|||||||||
|
|
C2H6 |
|
C6H5CH2CH3 |
|
|
|
||
Зазначити умови перебігу реакцій, дати назву сполукам. Навести механізм одержання етилбензолу.
88.Порiвняти та пояснити ароматичний характер фурану і тiофену виходячи з їх будови. Яка з цих сполук вступає в реакцiю дiєнового синтезу? Навести рiвняння вiдповiдної реакцiї, вiдповiдь обгрунтувати.
89.З огляду на бензол та правила орієнтації в реакції SE синтезувати наступні сполуки:
à) |
NO2 |
á) |
CH |
|
|
|
3 |
||
|
|
|
|
|

 SO3H
SO3H
CH3
Навести механізм утворення толуолу.
90.Охарактеризувати будову фурану, тіофену, піролу та піридину. Пояснити ароматичний характер цих сполук (правило Хюккеля, розподіл електронної густини). Обгрунтуванти реакційну здатність даних гетероциклів.

92
ТЕСТОВІ ЗАВДІННЯ ДЛЯ КОНТРОЛЮ ЗНАНЬ СТУДЕНТІВ
1 |
В якій з наведених нижче сполук є атом Карбону в sp2-гібридизованому |
|||||||||||||||||||||
. |
стані? а) CH2 |
CH |
|
CH |
|
CH2 ; б)HC |
|
C |
|
C |
|
CH ; в)CH3 |
C |
|
C |
|
CH3 ; г)CH3 |
CH2 |
CH2 |
CH3 |
||
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|||||||||||||||||||
2 |
Вкажіть кінцевий продукт хлорування метану: |
|||||||||||||||||||||
. |
|
|
|
|
|
CH4 + 4Cl2 |
|
hν |
? + 4HCl |
|||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
а) хлороформ; б) хлоретанол; в) тетрахлорометан; г)хлорметан 3 Яка сполука утвориться при нагріванні брометану з водним розчином
. |
H3C |
|
CH2 |
Br + KOH |
H2O |
? |
калій гідроксиду? |
|
|||||
|
|
|||||
|
|
|
|
|
|
а) CН2=СН2 ; б) CH3–CH3 ; в) CH3CH2OH ; г) CH3COOH
4 Вкажіть види ізомерії, які властиві алканам: а) структурна і оптична;
. б) ендіольна і геометрична; в) ізомерія функціональної групи і
геометрична; г) геометрична і положення 5 Закономірність, яка завбачає напрям реакції алкенів несиметричної
.будови (R-СH=CH2) з галогеноводнями дістала назву правила Марковникова. Воно формулюється таким чином:
а) При взаємодії з галогеноводнями напрям реакції визначається природою галогену б)При взаємодії з галогеноводнями атом водню приєднується за місцем
розриву подвійного зв'язку до менш гідрогенізованого атома вуглецю в) При взаємодії з галогеноводнями атом водню відщеплюється від більш гідрогенізованого атома вуглецю
г) При взаємодії з галогеноводнями атом водню приєднується за місцем
розриву подвійного зв'язку до більш гідрогенізованого атома вуглецю
6 В якій з наведених нижче сполук є атом Карбону в sp-гібридизованому
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
стані? а) CH3 |
CH |
|
CH CH3 ; б) CH3 |
C |
|
C |
|
CH3 в) CH3 |
CH2 |
CH2 CH3 ; г) |
CH2 |
|
CH2 |
|||||||
|
|
|
|
|
||||||||||||||||
|
|
|
|
CH2 |
|
CH2 |
||||||||||||||
|
|
|
|
|||||||||||||||||
7 Дією якого реагенту можна здійснити зазначену реакцію? |
|
|
||||||||||||||||||
. |
|
|
|
|
|
|
|
|
? |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
CH2 |
|
|
|
CH2 |
|
CH2 |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
OH OH |
|
|
||||||
а) K2Cr2O7 + H2SO4; б) KMnO4 (H2O) в) NaOH + I2 ; г) CO + H2O
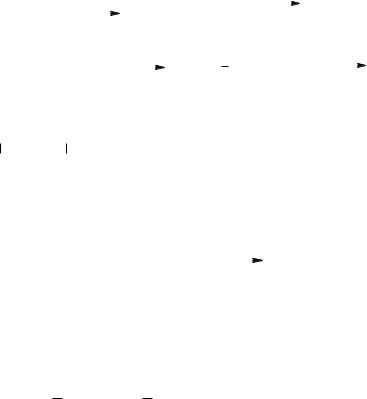
93
8 За будовою карбонового скелету всі органічні сполуки поділяються на:
. а) арени та алкени; б) ароматичні та карбоциклічні; в) гетероциклічні і
оксигеновмісні; г)ациклічні та циклічні
9 Який з реагентів використовують для ідентифікації алкенів? а) HCl;
. б)H2O (H+); в) HBr; г) Br2 (H2O).
1 До проміжних активних частинок відносяться вільні радикали. Вільними
0 радикалами називають: а) незаряджені частинки, що містять неспарений
. електрон; б) частинки, що містять позитивно заряджений атом Карбону; в) частинки, що містять негативно заряджений атом Карбону;
г) незаряджені частинки, що містять неподілену електронну пару 1 Серед названих гетероциклічних сполук вкажіть ароматичну:
1 а) тетрагідрофуран; б) пірол; в) піролідин; г) етиленоксид
.
1 Етиловий спирт утвориться у результаті реакції:
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
Hg2+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
CH |
|
CH + H2O |
|
|
|
|
|
|
|
|
|||||||||||
. а) CH |
|
|
|
CH2 + H2O |
|
|
H2SO4 |
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
2 |
|
|
|
|
|
|
; б) |
|
|
|
|
|
; |
|
|
|
|
|||||||||||||||||||||||||||
|
в) H3C |
|
|
CH |
|
|
CH2 + H2O |
|
H+ |
|
|
CHCl2 + |
H2O |
|
OH- |
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
; г)CH3 |
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
1 |
У наведеній формулі вкажіть третинні атоми Карбону: |
|||||||||||||||||||||||||||||||||||||||||||
3 |
|
6 |
|
|
|
|
|
|
|
|
|
9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
. |
1 |
2 |
CH3 |
3 |
|
|
4 |
CH3 |
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
H3C |
|
|
C |
|
|
CH |
|
|
CH |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
7 |
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
CH3 |
CH3 |
|
|
|
|
|
|
|
|
|
а) 3,4; б) 2,3,4; в) 4; г) 1,5 |
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
1 |
До якого типу належить реакція: |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3-CH3 |
+SO2 + Cl2 |
|
hν |
|
|
CH -CH -SO |
Cl + HCl |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
2 |
2 |
|
|
а) |
електрофільного |
приєднання; |
|
|
б) |
|
радикального заміщення; |
|||||||||||||||||||||||||||||||||||||
|
в) відновлення; г) окиснення |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
1 |
Серед наведених проміжних активних частинок виберіть радикал: |
|||||||||||||||||||||||||||||||||||||||||||
5 |
.. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
- |
|
|
|
|
|
|
. |
|
|
|
|
|
|
|
|
|
||||||
|
а) NH3 ; б) |
|
CH3 |
|
|
CH2 ; в) |
CH3 |
CH2 ; г) CH |
|
CH2 |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
. |
|
|
|
3 |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
Серед названих гетероциклічних сполук вкажіть неароматичну: |
|||||||||||||||||||||||||||||||||||||||||||
6 а) пірол; б) піролідин; в) тіофен; г) бензол
.
1 Вкажіть сполуку, яка утвориться при гідратації ацетилену за реакцією

94
HC CH HgSO4; H2O ?
Кучерова: H2SO4
|
|
CH |
|
C O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
C |
O |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
3 |
|
|
|
|
|
|
|
|
|
|
OH ; в) CH3 |
CH2 |
OH г) |
3 |
|
|
||||||||||||||||
|
а) |
|
OH ; б) CH2 |
CH |
|
H |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
1 |
Яка сполука відноситься до карбоциклічних?: |
|
||||||||||||||||||||||||||||||||
8 |
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
а) |
|
|
|
|
; б) |
|
|
|
|
|
; г) O |
|
|
|
|
|||||||||||||||||||
. |
|
N |
|
|
N |
|
; в) |
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
1 |
Вкажіть вірну назву сполуки за номенклатурою IUPAC: |
|||||||||||||||||||||||||||||||||
9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
CH2 |
C |
|
C |
|
CH2 |
CH3 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 CH3 |
|
|
|
|
|||||||
а) 3,4-Диметилгексен-3; б) 2-Метил-3-етилпентен; в) 2-Етил-3- |
||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||
|
метилпентен-2; г) Диметилдіетилетилен |
|
|
|
|
|||||||||||||||||||||||||||||
2 |
Аліфатичні вуглеводні поділяють на насичені і ненасичені. Яка сполука |
|||||||||||||||||||||||||||||||||
0 |
відноситься до насичених вуглеводнів? |
|
|
|
≡ |
|||||||||||||||||||||||||||||
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
а)CH3–CH=CH2 ; б) CH3–CH2–CH3 ; в) CH2=C=CH2 |
; г) CH3–C CH |
||||||||||||||||||||||||||||||||
2 |
Як впливає карбоксильна група (-СООН) на реакційну здатність |
|||||||||||||||||||||||||||||||||
1 |
бензольного кільця в яке положення направляє наступні замісники в |
|||||||||||||||||||||||||||||||||
.реакціях SE? а) Знижує реакційну здатність; направляє в мета- положення; б) Підвищує реакційну здатність; направляє в мета- положення; в) Знижує реакційну здатність; направляє в орто- і пара- положення; г) Підвищує реакційну здатність; направляє в орто-, пара- положення
2Загальна формула алкінів СnH2n-2. Який клас сполук є ізомерним алкінам?
2а) алкадієни; б) алкени; в) циклоалкани; г) одноядерні арени
. |
|
|
|
|
|
|
2 |
Реакції нітрування для |
ароматичних |
вуглеводнів відбуваються за |
|||
3 |
механізмом: |
|
|
|
|
|
. |
|
|
|
|
NO2 |
NO2 |
|
+ NO2+ |
|
+ |
|
||
|
|
|
H |
|||
|
NO |
+ |
|
|||
|
|
|
2 |
- H |
+ |
|
|
|
|
|
|
||
а) Електрофільного заміщення (SE); б) Вільнорадикального заміщення (SR); в) Нуклеофільного приєднання (AN); г) Нуклеофільного заміщення(SN)

95
2 Основним продуктом наведеної реакції H3C CH2 CH CH2 HBr ? є:
CH2 HBr ? є:
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
CH2 |
|
CH |
|
|
CH2 |
H3C |
|
CH2 |
CH2 |
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
. |
а) |
H3C |
|
CH2 |
CH |
|
CH |
|
Br ; б) |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
Br Br ; в) |
|
|
|
|
Br ; |
||||||||||||||||||
|
|
|||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||
|
г) |
H3C |
|
CH2 |
|
CH |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
Br |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
2 |
До ароматичних відносять вуглеводні, які: а) мають замкнену спряжену |
|||||||||||||||||||||||||||
5 систему та плоску будову молекули; б) мають незамкнену спряжену
. систему подвійних з’вязків; в) мають циклічну будову та неспряжену
систему подвійних з’вязків; г) складаються з Карбону та Гідрогену 2 З якою речовиною пропан вступає в реакцію за наведених умов?
6 а) NaOH, спиртовий розчин; б) Br2, в темноті, 20оС; в) NaOH, водний
. |
розчин; г) Br2, освітлення, 20оС |
|
|
|
|
|
|
|
|
|
|
|||||||||||||
2 |
У |
|
результаті |
реакції алкілування |
бензолу |
|
за Фріделем-Крафтсом |
|||||||||||||||||
7 |
утворюється: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
. |
|
|
|
|
|
|
|
|
|
|
|
+ |
CH3Cl |
|
AlCl3 |
|
|
? |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
CH3 |
CH3 |
CH3 |
|
O |
C |
CH3 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
а) |
|
|
|
; б) |
|
CH3 ; в) H3C |
|
CH3 ; г) |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
2 Вкажіть продукти, які утворюються при дегалогенуванні віцинальних
8 дигалогеналканів при дії металів (цинку або магнію):
. |
R |
|
|
|
CH |
|
|
CH2 |
|
|
|
Zn |
? |
|||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
Br |
Br |
|
|
|
|
|
|
|
||||||
|
а) Алкени; б) Алкани; в) Алкіни; г) Галогеналкани |
|||||||||||||||||
2 |
Яку назву згідно з замісниковою номенклатурою IUPAC має сполука: |
|||||||||||||||||
9 |
CH3 |
|
CH |
|
CH2 |
C |
|
C |
|
CH2 |
CH3 |
|||||||
|
|
|||||||||||||||||
|
|
|
||||||||||||||||
|
|
|
|
|||||||||||||||
. |
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|||||
а) 6-метилгептин-3; б) |
2-метилгептин-4; в) 2-метилгептен-4; |
|||||||||||||||||
|
||||||||||||||||||
|
г) 6-метилгептен-3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
Яка з наведених сполук буде більш активною в реакціях |
|||||||||||||||||
0 |
електрофільного заміщення (SE)? |
|
|
|
|
|
|
|
|
|
|
|||||||

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
96 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
O C H |
|
|
|
|
|
OH |
|
|
|
|
|
NO2 |
|||||||||||||
|
|
|
|
NH2 |
O |
|
|
|
|
|
|
O |
|
|
||||||||||||||||||||
|
|
|
|
|
|
S |
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
а) |
|
|
|
|
|
; б) |
|
|
|
|
; в) |
|
|
|
|
|
|
|
|
|
|
|
; г) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
3 |
Молекула |
якої з |
наведених |
|
сполук містить атом Карбону у стані |
|||||||||||||||||||||||||||||
1 |
sp2-гібридизації ? |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
. |
а) H3C |
|
CH2 |
CH3 ; б) H3C |
|
|
C |
|
|
|
CH ; в) H3C |
|
CH |
|
CH2 ; г) |
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
3 |
Яка із наведених сполук утворюється в результаті повного гідрування |
|||||||||||||||||||||||||||||||||
2 бензолу ?
.
3H2 ? t, p, kat
|
а) |
; б) |
; в) |
; г) |
CH |
3 |
CH |
2 |
CH |
2 |
CH |
2 |
CH |
2 |
CH3 |
|
|
|
|
|
|
|
|||||||||
3 |
Як впливає наявність електроноакцепторних замісників в бензольному |
||||||||||||||
3 |
ядрі на перебіг реакцій електрофільного заміщення (SE): |
||||||||||||||
. |
|
|
|
|
|
|
A |
|
(-I, -M) |
|
|
|
|
||
|
|
|
|
|
δ - |
|
|
|
δ - |
|
|
|
|
|
|
|
а) Сповільнюють реакцію і є мета-орієнтантами; б) Прискорюють |
||||||||||||||
|
реакцію і |
є орто- |
і пара- |
орієнтантами; |
|
в) Не впливають; |
|||||||||
г) Прискорюють і є метаорієнтантами 3 Скільки структурних ізомерів має бутан? а) два; б) три; в) жодного;
4 г) чотири.
.
3 Бензол можна одержати за реакцією:
5 |
а) 3 HC |
|
|
|
CH |
|
|
|
kat |
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
. |
|
|
|
kat |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
б) |
3 H3C |
|
|
|
C |
|
CH |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
в) 4 HC |
|
|
|
|
CH |
|
|
|
kat |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
г) 2 CH3 |
|
CH2 |
CH |
|
Cl + |
2Na |
|
|
||||||||||||
|
|
2 |
|||||||||||||||||||
|
|
|
|||||||||||||||||||
3 |
Назвіть |
|
|
|
кінцевий |
продукт взаємодії металічного натрію і |
|||||||||||||||
6 |
1-хлорпропану: |
|
|
|
|
|
|||||||||||||||
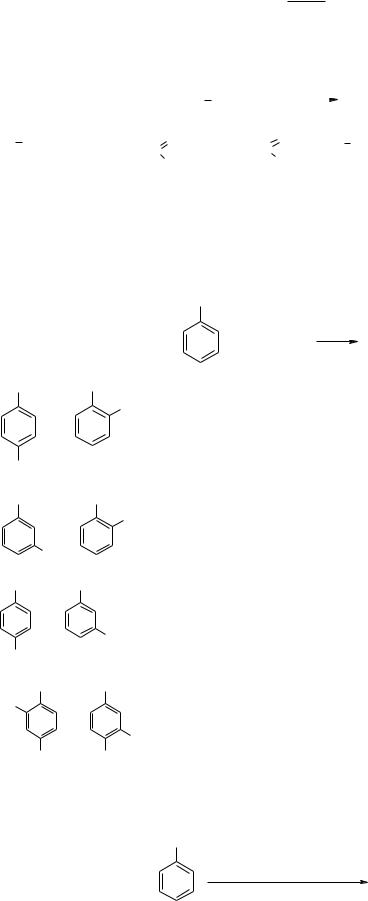
97
2CH3CH2CH2Cl 2Na  ?
?
а) 2-метилпентан; б) пентан; в) гексан; г) циклогексан 3 Вкажіть яка сполука утворюється при гідратації пропіну за Кучеровим:
7 |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
C |
|
|
CH |
|
HgSO4; H2O |
? |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2SO4 |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH3 |
|
CH |
|
CH3 |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O |
CH3 |
|
|
C |
|
CH3 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
CH3 |
|
CH2 |
|
C |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
CH3 CH2 C |
|
|
|
|
|
|||||||||||||||||||||
|
а) |
OH |
; б) |
H ; в) |
|
|
|
|
|
OH ; г) |
|
|
|
O |
||||||||||||||||
3 |
Алкадієнамі називають вуглеводні аліфатичного ряду, які містять два |
|||||||||||||||||||||||||||||
8 подвійні зв'язки. Виберіть загальну формулу гомологічного ряду
. алкадієнів: а) CnH2n-2 ; б) CnH2n+2 ; в) CnH2n ; г) CnH2n+1 3 Оберіть ряд продовження реакції:
9 |
|
|
OH |
|
|
|
|
||
. |
|
|
+ HNO3 розв. |
|
|
OH |
OH |
|
|
|
|
NO2 |
|
|
|
+ |
+H2O |
|
|
а) |
NO2 |
|
|
|
|
|
|
||
|
OH |
OH |
|
|
|
|
NO2 |
|
|
|
+ |
+H2O |
|
|
б) |
NO2 |
|
|
|
|
|
|
||
|
OH |
OH |
|
|
|
+ |
+H2O |
|
|
в) |
|
NO2 |
|
|
NO2 |
|
|
||
|
|
|
||
|
OH |
OH |
|
|
|
O2N |
|
|
|
|
+ |
+H2O |
|
|
г) |
|
NO2 |
. |
|
NO2 |
NO2 |
|||
|
|
4 Вкажіть, який продукт утворюється при нітруванні нітробензену
0 нітруючою сумішшю:
.
NO2
HNO3(конц.) + H2SO4(конц.)
?
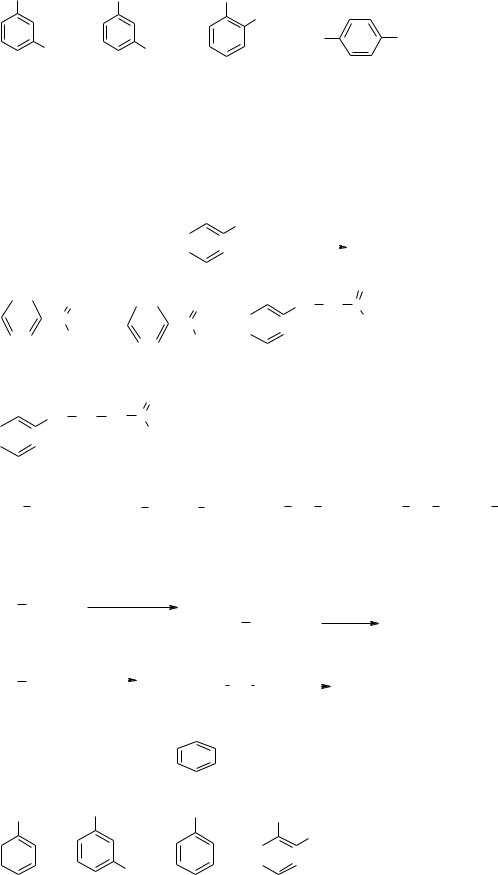
98
NO2 |
|
NO2 |
NO2 |
|
|
|
|
NO2 |
|
а) |
NO2 ; б) |
SO3H ; в) |
г) O2N |
SO3H |
4 За яких з наведених умов відбувається реакція нітрування насичених 1 вуглеводів (алканів)? а) НNO2 + HCl; б) к. HNO3 + к. H2SO4 в) к. НNO3 +
. |
HCl; г) Розв. HNO3 при підв. тиску та підв. температурі |
||||||||||||||||||||||||||||||||
4 |
Кінцевим |
|
продуктом |
окиснення |
алкілбензолів із неразгалуженим |
||||||||||||||||||||||||||||
2 |
алкільним ланцюгом буде: |
|
|
|
|
|
|
||||||||||||||||||||||||||
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C4H9-H |
|
|
[O] |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
CH2 |
CH2 |
C |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
OH |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
а) |
|
|
|
|
|
CH3 ; б) |
|
|
|
|
|
OH ; в) |
|
|
|
|
|
|
|
; |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
CH2 |
CH2 |
CH2 |
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
г) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
4 |
Вкажіть структурну формулу пропену: |
|
|||||||||||||||||||||||||||||||
3 а) CH3 CH CH2 ; б) CH3 CH
CH2 ; б) CH3 CH CH CH3 ; в) CH3 CH2 CH3 ; г) CH3 CH2 CH
CH CH3 ; в) CH3 CH2 CH3 ; г) CH3 CH2 CH CH CH3
CH CH3
.
4 У якій реакції утворюється ацетон?
4 |
|
|
|
|
|
|
|
|
NaOH (âî äí . ð-í ) |
|
|
|
|
|
|
|
|
|
||||
. |
|
CH3 |
|
CH |
|
|
CH3 |
|
|
|
; б) CH3 |
CH |
|
CH2 |
H2O; H+ |
|||||||
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
а) |
|
|
|
|
|
|
|
|
|
|
; |
|||||||||||
|
Cl |
H2O; Hg2+; |
|
|
||||||||||||||||||
|
|
CH3 |
C |
|
|
CH |
|
CH |
|
CH CH OH |
|
[O] |
|
|||||||||
|
в) |
|
H SO |
|
|
; г) |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
2 |
4 |
|
|
3 |
2 |
|
2 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
4 |
З наведених сполук оберіть продукт бромування бензолу: |
|||||||||||||||||||||
5
.
FeBr3
+ Br2  ?
?
Br |
Br |
CH2Br |
OH |
Br
а) |
|
; б) |
Br ; в) |
; г) |
|
|
|
|
|
|
|
||||
4 Які |
|
атоми |
Карбону у |
наведеній сполуці знаходяться у другому |
|||
6
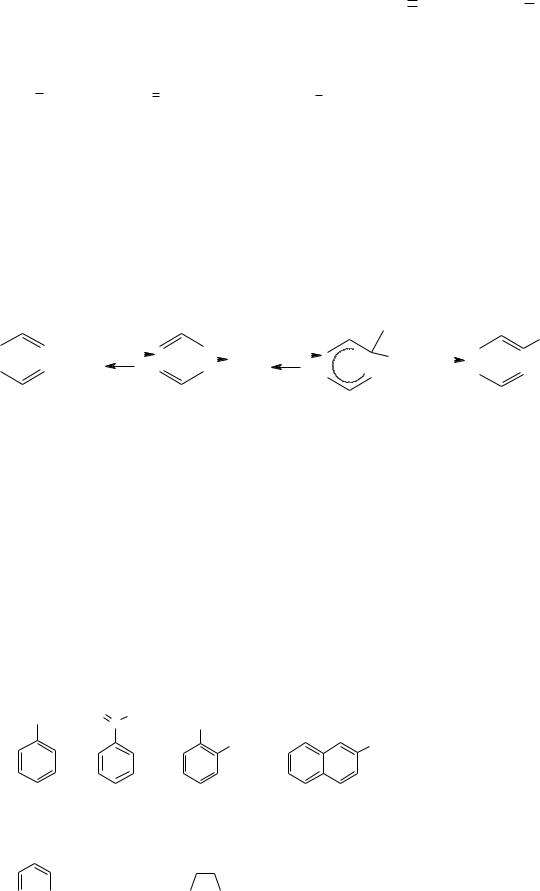
99
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
2 |
|
3 |
4 |
|
5 |
|
6 |
|||||||
|
валентному |
стані |
2 |
-гібридизації)? |
|
CH2 |
|
CH |
|
|
C |
|
C |
|
CH2 |
CH3 |
|||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
(sp |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
а) 2 і 3; б) 1 і 3; в) 1 і 2 ; г)3 і 4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
4 |
Яка із наведених сполук не буде знебарвлювати бромну воду? |
|
|
|
|||||||||||||||||||||||||||||||
7 |
а) CH3 |
CH |
|
CH2 ; б) CH2 |
CH2 ; в) CH |
|
CH ; г) CH3 |
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
За допомогою якого реагенту можна відрізнити бутин-1 (CH3-CH2- |
||||||||||||||||||||||||||||||||||
8 |
C≡CH) від бутину-2 (CH3-C≡C-CH3)? а) [Ag(NH3)2]OH; б) H2O, у |
||||||||||||||||||||||||||||||||||
. |
присутності солей меркурію (ІІ); в) C2H5OH, у присутності C2H5ONa; г) |
||||||||||||||||||||||||||||||||||
|
H2, у присутності катализатора Pt або Ni |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
4 |
Реакції сульфування для ароматичних вуглеводнів відбуваються за |
||||||||||||||||||||||||||||||||||
9 |
механізмом: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
. |
|
|
|
|
+ |
|
|
|
|
|
+ |
|
|
|
|
|
|
|
SO3H |
|
|
|
|
|
|
|
|
|
|
SO H |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
||||
|
|
|
|
+ SO3H |
|
|
|
|
|
SO H |
|
|
|
+ |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
- H |
+ |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
а) Електрофільного заміщення (SE); б) Вільнорадикального заміщення |
||||||||||||||||||||||||||||||||||
|
(SR); |
в) |
|
Нуклеофільного |
|
приєднання |
|
(AN); |
г) |
|
Нуклеофільного |
||||||||||||||||||||||||
заміщення(SN)
5 До проміжних активних частинок відносяться карбкатіони.
0 Карбкатіонами називають: а) проміжні активні частинки, що містять
.атом Карбону з вакантною орбіталлю; б) частинки, що містять позитивно заряджений атом Карбону; в) частинки, що містять негативно заряджений атом Карбону; г) незаряджені частинки, що містять
неподілену електронну пару 5 Вкажіть формулу нітробензолу:
1 |
NO |
|
O |
C |
OH |
|
|
|
2 |
|
CH3 |
|
|
. |
|
|
|
|
NO2 |
NO2 |
|
|
|
|
|
|
|
|
а) |
|
; б) |
|
; в) |
; г) |
5 |
. Вкажіть серед наведених сполук ту, яка буде знебарвлювати бромну |
|||||
2 воду:
.
а)  ; б) СН3-СН3; в)
; б) СН3-СН3; в)  ; г) СН2=СН2 5 До якого типу відноситься реакція:
; г) СН2=СН2 5 До якого типу відноситься реакція:

100
СН2=СН2+Br2  CH2 CH2 Br Br
CH2 CH2 Br Br
а) приєднання; б) заміщення; в) відновлення; г) окислення 5 Який вуглеводень утвориться в реакції:
4
.
CH3-CH2-COONa |
NaOH |
? + Na |
CO |
|
||
|
|
|
3 |
|||
|
сплавл. |
2 |
|
|||
|
|
|
|
|||
а) бутан; б) пропан; в) етан ; г) ізобутан 5 Яка з наведених сполук може існувати у формі цис- і транс-ізомерів:
5 |
а) H3C |
|
|
C |
|
|
C |
|
CH3 ; б) CH3-CH=CH-CH3; в) H3C |
|
CH2 |
C |
|
CH ; г) |
H C |
|
C |
|
CH |
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
3 |
|
H |
|
|
2 |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
Вкажіть реакцію В’юрца: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
6 |
а) 2CH3I + 2Na |
|
|
|
H3C |
|
|
CH3 |
|
+ 2NaI |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
. |
б) |
2 HC |
|
|
|
CH + 2H2 |
to |
|
|
H3C |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
в) |
CH3-CH2-COONa NaOH спл. H3C |
|
|
|
CH3 |
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
г) |
CH3-CH2-Cl + 2HI |
|
|
|
H C |
|
|
CH |
3 |
+ I |
+ HCl |
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
||||||
5 |
Яка з |
|
приведених |
сполук |
(1-4) |
при дегідратації утворює |
2-метил-2- |
||||||||||||||||||||||||||||||||
7 пентен? а) 2,3-диметил-2-бутанол; б) 3-метилпентанол; в) 2-метил-3-
. |
пентанол; г) 3-метил-2-пентанол |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
5 |
Серед наведених нижче сполук, вкажіть ту, в якій є p,π-спряження: |
||||||||||||||||||||||||||||||||||||||||||
8 |
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
. |
а) |
|
|
|
|
|
; б) CH2 |
CH |
|
CH |
|
|
|
CH |
|
|
CH2 ; в) CH |
|
C |
|
CH ; г) |
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
2 |
|
|
|
|
3 |
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
5 |
Яка з наведених нижче сполук містить електроноакцепторний замісник? |
||||||||||||||||||||||||||||||||||||||||||
9 |
|
|
|
|
NO2 |
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
CH3 |
|
|
|
|
|
|
|||||||||
а) |
|
|
|
|
; б) |
|
|
|
|
|
|
|
; в) |
|
|
|
|
|
|
|
|
|
|
; г) |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
6 |
Який з алканів одержано за реакцією: |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
0 |
|
|
|
|
|
|
|
|
H3C |
|
|
CH |
|
CH |
|
|
|
C |
O |
|
+ NaOH (тв.) |
t>3000C |
? |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH ONa |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
а) |
|
2-етил-3-метилбутан; |
|
|
|
|
|
б) |
|
3,4-діетил-2,5-диметилгексан; |
||||||||||||||||||||||||||||||||
|
в) 2-метилпентан; г) 2,3-диметилпентан |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
101
СПИСОК ЛІТЕРАТУРИ
1.Глубіш П.А. Органічна хімія: Навч. посібник. Ч.1. “Аліфатичні та ароматичні вуглеводні”. – К.: НМЦВО, 2002. – 296с.
2.Термодинаміка, кінетика і каталіз в органічній хімії / М.М. Кремльов, Ж.В.Шмельова, Л.Є.Марцинкевич, Н.Д.Бородавко – Київ “УкрВузполіграф”, 1989. – 184с.
3.Петров А.А, Бальян Х.В., Трощенко А.Т. Органическая химия.-М.: Высш. шк, 1981. – 592с.
4.Нейланд О.Я. Органическая химия.-М.: Высш. шк., 1990. – 752 с.
5.Моррисон Р., Бойд Р. Органічна хімія. – М.: Мир, 1974. – 1132 с.
6.Ластухін Ю.О., Воронов С.А. Органічна хімія. – Львів: Центр Європи, 2001. – 864с.
