
Patologija_obmiena-2012
.pdfПричинами, приводящими к недостатку инсулина (ИЗСД), может быть:
нарушение синтеза ДНК и РНК в β-клетках и образования молекул проинсулина и инсулина с нарушенной активностью;
снижение чувствительности β-клеток к стимуляторам синтеза инсулина;
прочная связь инсулина с гранулами β-клеток;
образование антагонистов инсулина.
Развитию сахарного диабета I типа способствуют обширные повреждения поджелудочной железы, образование камней, кальцификация железы, ее кисты, склероз сосудов.
Предрасполагающими факторами развития диабета у взрослых являются диета, богатая углеводами и низкая физическая активность. Длительный прием избыточного количества пищи вызывает гипертрофию β-клеток. Они вырабатывают большое количество инсулина, поступающего в кровь. Гиперинсулинемия способствует ожирению, а также развитию инсулинорезистентности тканей.
При переедании сахарный диабет развивается лишь у людей, генетически к нему предрасположенных, а также у людей с повреждением инкреторного аппарата поджелудочной железы.
Стадии развития ИЗСД
1. Стадия генетической предрасположенности
Белки главного комплекса гистосовместимости вместо аспарагиновой аминокислоты содержат серин, аланин и др. Обмен углеводов нормальный
41
2. Стадия провоцирующих событий
Воздействие инфекционного (чаще вирусного) или химического диабетогена
3. Стадия аутоиммунных реакций
Действие лимфоцитов, макрофагов и антител против β-клеток, на которых появились СД-80 и СД-86 молекулы.
4. Стадия латентного диабета
Снижена выработка инсулина. Уровень глюкозы натощак нормальный.
5. Стадия явного диабета
Гиперкемия натощак. Аутоиммунные реакции сглаживаются. Образуются иммунные комплексы при инсулинотерапии
6. Стадия терминального диабета
Гибель β-клеток. Осложнения (макро- и микрогангиопатии, кетоацидотическая кома и др.)
Причинами ИНСД, как правило, является инсулинорезистентность тканей (аномалии либо блокада инсулиновых рецепторов, пострецепторные блоки в клеткахмишенях), а также разрушение либо инактивация инсулина его антагонистами (инсулиназой, антителами).
Патологическая резистентность к инсулину по механизму возникновения может быть:
I.Пререцепторная:
патологическое изменение гормона
взаимодействие с аутоантителами
выброс проплазмина
II.Рецепторная:
аномалия рецепторов
аутоиммунное поражение рецепторов
42
III.Пострецепторная:
нарушение активности клеточных ферментов
снижение транспорта глюкозы и аминокислот в клетку
снижение синтеза РНК и протеосинтеза
отсутствие снижения активности аденилатциклазы и образованияцАМФ, а также глюкозо-6- фосфатазы в печени
Стадии патогенеза ИНСД
1.Стадия компенсации инсулиновой резинстент-
ности за счет гипертрофии β-клеток и увеличения выработки инсулина
2.Стадия усиления инсулиновой резистентности
обусловлена ожирением вследствие увеличения количества инсулина и действия на жировую ткань. Ожирение, в первую очередь, тормозит транспорт в клетку глюкозы и аминокислот.
3.Стадия снижения инсулиновой секреции (декомпенсация)
выраженный диабет с осложнениями (макро- и микроангиопатии, комы чаще гиперсмолярные в связи с гипергликемией и гипернатриемией) и др.
Для диабета II типа с относительной инсулиновой резистентностью характерно постепенное начало. Как правило, страдают люди пожилого возраста, у пациентов часто наблюдается ожирение, ускоренный атеросклероз, гипертензия.
Инсулинорезистентности способствует ожирение. Инсулин при ИНЗД препятствует липолизу и способствует ожирению. Характерна гиперхолестеролемия.
43
Причиной ИНСД могут быть заболевания печени. При патологических изменениях в печени все эффекты инсулина ослабляются и усиливается действие гормонов с контринсулярными свойствами.
Моделирование сахарного диабета
Моделирование сахарного диабета на животных позволило шаг за шагом приблизиться к пониманию его этиологии и патогенеза. Существуют хирургические и химические методы экспериментального моделирования сахарного диабета. Хирургические модели инсулинзависимого сахарного диабета осуществляют на собаках, крысах путем панкреатэктомии (авторы – И. Меринг и О. Минковский и Ф. Де Доминичи (1889 г). О. Минковский показал, что пересадка кусочка поджелудочной железы под кожу собаки предохраняет панкреатэктомированное животное от СД. Среди химических моделей известны: аллоксановый диабет, дитизоновый диабет (дитизон связывает цинк; у кроликов, островковые β-клетки которых богаты цинком), стрептозотоциновый диабет (антибиотик стрептозоцитн избирательно повреждает β-клетки поджелудочной железы у крысы).
Нарушение обмена веществ при сахарном диабете
У больных сахарным диабетом происходит нарушение всех видов обмена веществ: углеводного, липидного, белкового, нуклеопротеидного, водно-электролитного, нарушение КОС.
44
Нарушения в углеводном обмене проявляются в угнетении цикла Кребса, торможении аэробного гликолиза,активции анаэробного гликолиза, активации глюкогеногенеза, торможении пентозо-фосфатного цикла, снижении гликогенеза и активации гликогенлиза. Как следствие происходит накопление пировиноградной и молочной кислот, повышается уровень глюкозы в крови, уменьшении синтеза пентоз (рибозы и дезоксирибозы), что в последующем является причиной нарушения синтеза нуклеопротеидов, снижении депо гликогена в печени.
Нарушения в липидном обмене проявляются в уменьшении образования нейтральных жиров (при ИЗСД), уменьшении липолиза, повышенном образовании холестерола и кетоновых тел.
Нарушения белкового обмена проявляются в уменьшении анаболических и повышении катаболических процессов, проявляющееся в отрицательном азотистом балансе и гиперазотемии (повышение образования мочевины).
Нарушение водно-электролитного обмена проявляется обезвоживанием и обессоливанием организма. Потеря воды вызвана избыточным выведением осмотически активного вещества – Гл, а также потерей осмотически активных ионов натрия и калия в составе их солей с ацетоуксусной и бетта-оксимасляной кислотами.
Нарушение КОС проявляется в развитие ацидоза вследствие избыточного образования недоокисленных продуктов цикла Кребса, а также кетоновых тел.
45
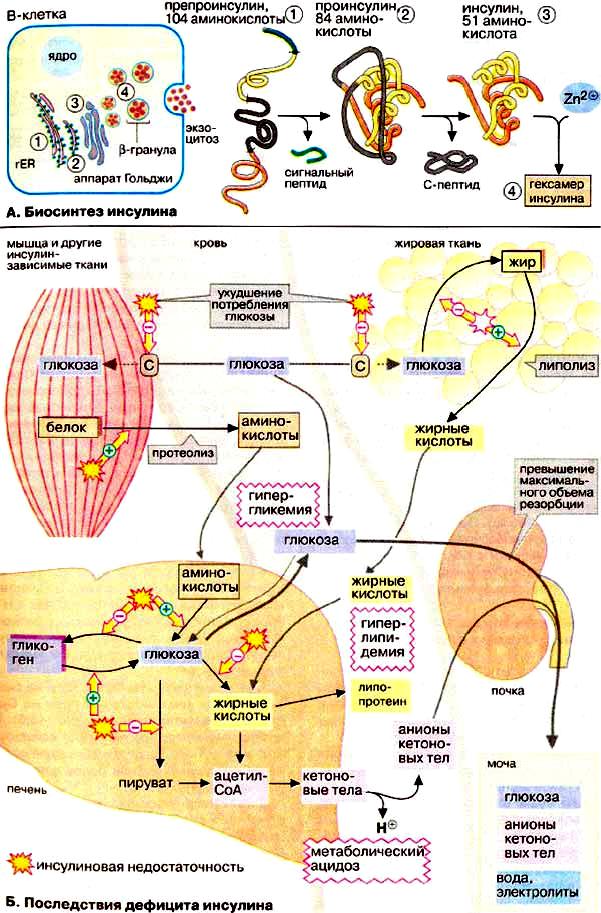
46
Клинические проявления сахарного диабета
Наиболее типичными жалобами для больных диабетом является жажда и сухость во рту, полиурия, слабость и утомляемость, потеря трудоспособности, зуд кожных покровов.
Основным признаком диабета является гипергликемия, обусловленная нарушением утилизации Гл инсулинзависимыми органами, усилением ее образования в печени (глюконеогенез), а также повышенным гликогенолизом.
Первым проявлением инсулиновой недостаточности является пониженная толерантность к Гл. Это выражается в продолжительном повышении уровня Гл в крови при приеме сахара (глюкозы) внутрь натощак в дозе 1,0 (0,5) г/кг. У здорового человека уровень Гл в крови спустя 3060 минут после приема Гл не превышает 7,8 ммоль/л и возвращается к исходной величине через 3 часа. Спустя 2 часа он даже может быть ниже нормального уровня из-за повышенной выработки инсулина. При сахарном диабете через 2 часа после приема Гл уровень Гл в крови выше 11,3 ммоль/л и кривая уровня Гл в крови остается повышенной и через 3 часа.
Сахар крови, как известно, полностью реабсорбируется в почечных канальцах. Однако способность канальцевого эпителия к обратному всасыванию имеет количественный предел: так называемый «почечный порог» для Гл составляет у большинства людей 9-10 ммоль/л. При его превышении появляется глюкозурия. Глюкоза – осмотически активное вещество. Каждый грамм выделяющегося с мочой Гл увлекает за собой 25-40 мл воды, развивается полиурия, что ведет к обезвоживанию организма, сгущению крови, сухости слизистых оболочек и кожи и к полидипсии (повышенному приему воды).
47

Появление Гл в моче может отмечаться при нормальном ее уровне в крови (почечный диабет). Причина глюкозурии в данном случае обусловлена поражением почечных канальцах, в которых происходит реабсорбция Гл в кровь при участии ферментативных систем.
Вследствие недостаточного поступления Гл в ткани развивается слабость, быстрая утомляемость.
В жировой ткани недостаток инсулина приводит к уменьшению синтеза, повышению распада ТГ и исхуданию. В результате в плазме крови повышается уровень свободных жирных кислот. Как отмечено выше, у больных сахарным диабетом II типа наблюдается ожирение.
48

Развившаяся недостаточность инсулина приводит к сдвигу белкового обмена в сторону преобладания катаболических процессов. Повышенный распад белков приводит к увеличению уровня свободных аминокислот, часть которых поступает в печень и превращается в глюкозу путем глюконеогенеза. Катаболизм белка способствует повышению уровня мочевины (до 25 ммоль/л), что является причиной гиперазотемим.
Вследствие нарушения белкового обмена снижена продукция защитных белков, что объясняет плохое заживление ран у больных диабетом и склонность к инфекциям (пиодермия, фурункулы и др.).
При сахарном диабете резко нарушен липидный обмен. Снижен переход углеводов в другие липиды, вследствие чего развивается исхудание.
Недостаток инсулина способствует повышению образования кетоновых тел (ацетон, ацетоуксусная, β- оксимасляная кислоты) – кетоз или кетонемия у больных сахарным диабетом. У здорового человека содержание кетоновых тел в крови составляет 0,08 – 0,46 ммоль/л.
Кетоз обусловлен увеличением содержания в печени ацетил-КоА вследствие усиленного поступления и расщепления жирных кислот. Недостаток инсулина снижает способность мышечной ткани утилизировать кетоновые
49
тела, в то время как кетоновые тела тормозят, в свою очередь, выработку инсулина. Кетонемии также способствует накопление «кетогенных» аминокислот (изолейцина, лейцина, валина) в результате усиленного катаболизма белка.
Ацетоуксусная и β-оксимасляная кислоты наряду с МК и ПК обусловливают ацидоз и потерю натрия и калия в результате их выведения в виде солей этих электролитов.
Для ИНЗД кетоз не характерен.
Для больных сахарным диабетом характерно повышение уровня холестерола (ХС). В норме уровень ХС в плазме крови составляет 3,6-6,2 ммоль/л. Причиной является образование в больших количествах субстратов – ацетоуксусной кислоты и ацетил-КоА вследствие нарушения их ресинтеза в высшие жирные кислоты и окисления в цикле Кребса.
Несмотря на избыток источников энергии (глюкоза, жирные кислоты, аминокислоты), инсулинзависимые органы (печень, жировая, мышечная) из-за отсутствия инсулина не в состоянии утилизировать питательные вещества, в результате чего развивается энергетическое голодание клеток. Это способствует возбуждению пищевых центров, повышению аппетита, вызывает гиперфагию.
Для больных ИЗСД характерно исхудание вследствие обезвоживания организма, усиленной мобилизации жиров, снижения перехода углеводов в жир и превращения белков в углеводы, значительная часть которых выделяется с мочой. Увеличение количества неэстерифицированных жирных кислот в результате липолиза способствует их переходу в жир в печени с развитием жировой дистрофии печени. Как следствие расхода белка на глюконеогенез снижается иммунная реактивность, происходит нарушение продукции антител, замедление заживления ран.
50
