
биотехнология кітап
.pdf3.3 Эмбриональдық діңгек жасушалары
Эмбриональдық діңгек жасушаларын арнайы қоректік ортада өсіру мүмкіндігі болуы себепті, ересек діңгек жасушаларына қарағанда үлкен артықшылыққа ие.
Эмбриональдық діңгек жасушалары дегеніміз – шарананың дамуының ерте кезеңінде оның ағзасынан алынатын жасушалар. Оларды құрамында бластоцит (бластомер) деп аталатын 150-дей жасушасы бар, пішіні жалпақ шеңбер тəрізденіп келген шаранадан, бластулалық даму кезеңдерінде бөліп алынады. Алынған жасушалардың ішінде шарананың бөліктерін құруға қатысатын 30тек-ы ғана эмбриональдық діңгек жасушаларының болашақ желісін қалауға негіз бола алады.
Эмбриондардың |
қалыпты |
дамуы |
барысында |
эмбриональдық |
жасушалары жүктіліктің жетінші күнінен кейін |
жоғалып |
кетіп, олардың барлық |
||
ұлпа түрлеріне айналу мүмкіндіктері сейіледі. |
|
|
||
Эмбриональды діңгек жасушалары ұрықтандырылған аналық жасушаларынан пайда болады. Ересек діңгек жасушалары сияқты, бұлар да диплоидты. Оларда ДНҚ-ның барлық құрамдары түгелдей кездеседі. Ұрықтанған аналық жасушалардан зигота пайда болатыны белгілі. Осы зиготаның даму сатыларының өте ерт кезеңдерінде пайда болатын эмбриональдық діңгек жасушалары, өздерінің ағзаға қажетті түрлі жасушаларға айналу мүмкіндіктерін ұзақ уақыт сақтай алады.
Алғашқы |
діңгек |
жасушаларының жаңа |
ұрықтанған |
аналық жасушасынд |
түзілуі жəне бүтіндей тірі ағзаның бастамасы бола алуы себепті- тотипотентті |
||||
деп аталады. |
|
|
|
|
Дамудың |
ерте |
сатыларынан |
дайындалған |
эмбрионалдық |
жасушаларынан барлық түрдегі жасушалар түзілгенмен, олардан бүтіндей ағза мүшелерін өсіру мүмкін болмайды, немесе ең болмаса қазіргі кездегі технологияның
даму |
дəрежесі |
ондай |
мүмкіндікке |
қол |
. жеткізбейдіСондықтан |
олар |
мультипотентті деп аталады. |
|
|
|
|
||
Ересек адамдарда да діңгек жасушалары кездескенімен, олар өздері шыққан эмбрионалды жасушаларға қарағанда атқаратын қызметтері бойынша көбір дифференцияланған болады. Мысалы, гематопоэтикалық діңгек жасушалары сүйек кеміктерінде кездесетін барлық жасушаларды түзе алады. Бұлардан басқа, олардың бауыр мен бүйрек жасушаларына да айнала алатындары анықталған. Сондықтан бұларды плюрипотентті деп атайды. Плюрипотентті діңгек жасушаларын мидан, бұлшық еттерінен, теріден, ас қорыту жүйесінен, көз айнасының торшасы мен қабықшасынан, бауыр жəне көкбауырдан алу мүмкін болған. Мұндай жасушалар зақымданған ағза мүшелерінің белгілі дəрежеде қалпына келуіне əсер етсе керек деген болжам жасалады.
Теория бойынша, əрбір эмбриональдық діңгек жасушалары көп жасушалы ағзада кездесетін 200 арнайыланған жасушалар түрлеріне айнала алады жəне əлі шынайы түрде дəлелденбесе де, тұтастай ағза мүшелерін түзе алуы мүмкін деген пікір жасауға негіз бере алады. Мұның бір бұлжытпастай дəлелі ретінде, бір аналық жасушасынан пайда болған егіздердің, яғни дамуының өте ерте кезеңінде екіге немесе үшке (үшем) бөлінген ұрықтанған аналық жасушасынан өрбіген сəбилердің туылуын келтіре аламыз.
30
3.4 Эмбриональдық діңгек жасушаларының желісін жасау
Медицинада эмбриональдық діңгек жасушаларын ағзадан тысқары(in vitro) жағдайында аналық жасушасын қолдан ұрықтандыру арқылы алады. Бұл əдіс бойынша жатыр түтікшесінен сорылып алынған аналық ұрық жасушасы, арнайы зертханаларда микроскопты пайдалана отырып, ер адамдардың сперматозоидтармен ұрықтандырылады. Мұнда барлық жағдайлар жасалынып, стерильдіктің қамтамасыз етілуі себепті, ұрықтану нəтижелері де өте жоғары болады. Осындай жолмен ұрықтанған аналық жасушасы– иесінің немесе басқа əйел жатырына(сурогатты шеше) қондырылады. Ең алғашқы қолдан ұрықтандыру арқылы пайда болған бала 1978 жылы Англияда дүниеге келген болатын. Сол уақыттан бастап бұл əдіс медицинада кеңінен қолданыла бастады. Қолдан ұрықтандыру əдісі көптеген балалары жоқ ата-аналардың сəбилі болуын қамтамасыз етті. Бедеулікпен күресуден басқа, қолдан ұрықтандыруды көптеген басқа да мақсаттарда, мысалы мал шаруашылығында жынысы бойынша сұрыптау жұмыстарын жүргізу үшін пайдалануға болады.
Коммерциялық мақсатта қолдан ұрықтандыру жұмыстарын ірі қара мал шаруашылығында пайдалану тиімді екендігін көрсетті. Осындай жолмен алынған зигота, Дьюар құтысындағы сұйық азоттың-960С температурасында қатырылып, ары қарай сақталады. Мұның басты артықшылығы – зигота ұзақ мерзімге шыдайды жəне керек кезінде қажетті жерге оңай тасымалдау мүмкіндігіне ие болады.
Қолдан |
ұрықтандыру жолымен бір сəбидің дүниеге келуі , үшінбіреше |
аналық ұрық |
жасушасын сперматозоидтармен ұрықтау қажет болады. Көпшілік |
жағдайда бір сеанс мерзімінде8-ге дейін аналық жасушасын ұрықтандыруға қол жеткізілгенмен, оның тек 2-уі ғана болашақ ана жатырына бекітіледі. Қалғандары 6-
8 жасушалық |
кезеңдерінде |
сұйық азотта қатырылады. Қазіргі кезде |
АҚШ |
мемлекетінде |
осындай жолмен |
сақталған400 мыңға дейін эмбриондар бар |
деген |
мəліметтер келтіріледі. Соның ішінде 2,8% жуығы ғылыми-зерттеу жұмыстары үшін берілген.
Қатырудың эмбрионға тигізер əсері жөнінде əлі де толық белгісіз, сондықтан көптеген эмбриондар бұл жұмыстардан кейін өліп қалады. Бірақ та қатырылған, соңынан ерітіліп жатырға ендірілген эмбриондардың бір бөлігі өздерінің тіршілікке қабілеттілігін сақтауы себепті, кейіннен олардан аман-сау ұрпақ туылады.
Эмбриональдық діңгек жасушаларының желісін дайындау үшін, зерттеушілер
ерітілген |
зиготаларды |
бластула |
стадиясына дейін өсіп-бөлінуін қадағалай. |
Мұндай |
жұмыстардан |
кейін ол |
эмбрион ретінде ары қарайғы өзіндік маңыз |
жояды. Эмбриональдық діңгек жасушалары болса ары қарай шексіз өсіп-көбейе алады, яғни олар иммортальды қабілетке ие. Жасушалық желіні тоңазытқышта сақталатын ашытқыға ұқсатуға болады. Қажетті орта жағдайы жасалып сақталған оның бір тұтамын алып, жаңа ашытқы жасауға болады емес . пеСол сияқты, адамдардың да кейбір эмбриональдық діңгек жасушалары300-400-ге дейін бөліне алады. Тəжірибе жұмыстарында алынған тышқандардың діңгек жасушалары арнайы орта жағдайында бірнеше онжыл бойы сақталған.
Адамның діңгек жасушасы желісін жасаудың жалпы схемасын келесі7-ші суреттен көруге болады.
31
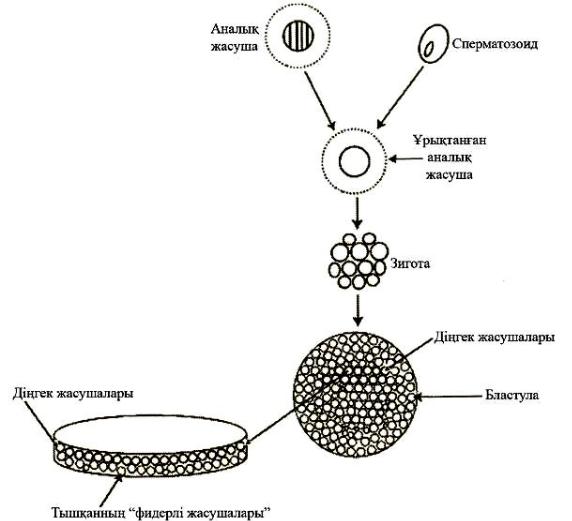
7-сурет. Адамның діңгек жасушасы желісін жасау (Ш. Уолкер. Биотехнология /Путеводитель, 2008.)
Жасуша желілеріне тиісті ерекшеліктерінің бірі– олардың «ойыннан шығу»
қабілеттіліктері болуы |
себепті, ғалымдардың пікірі бойынша оларды ауық-ауық |
|
жаңа жасушалармен |
ауыстырып тұру қажет. Бұл пікір басқа |
да жасушалар |
желілерін, атап айтқанда, адам фибробластарын қоректік ортада көп мерзімде сақтау |
||
барысында жасалынған. |
Мүмкін, ескіріп қалуы себепті көбею |
қабілеттіліктерін |
жоғалта бастаған жасушаларды, жаңа эмбриональды жасушалармен тұрақты түрде ауыстырып тұру қажет болатын шығар. Өйткені, ұзақ уақыт бойына жасанды қоректік ортада өсіріліп келінген басқа жасушаларда мутациялық өзгері жиналып қалуы себепті, оларда көбею қабілеттіліктерінің төмендей бастағаны байқалады.
Адамның діңгек жасушаларының желісі өте əлсіз болып келеді, сондықтан оны құру табандылық пен үлкен тəжірибені талап етеді. Олар мамандандырылған жасушаларға айналуға бейім келеді. Қазіргі кездегі белгілі технология бойынша, тышқанның эмбриональды фибробластары бар, құрамына сиыр қаны сарысуы қосылған, арнайы қоректік ортада адамның діңгек жасушаларының мамандану үдерісі жүрмейтіні анықталған. Құрамында осындай адам ағзасына жат заттары бар
32
қоректік ортада көбейтілген діңгек жасушаларын адамдарға терапиялық мақсатта қолдану, өте үлкен күмəн туғызытын нəрсе. Өйткені мұндай жағдайға жол берілсе, адам жасушасы тышқан немесе сиыр ағзасында болуы мүмкін əртүрлі зиянды заттар немесе вирустармен ластануы мүмкін. 2007 жылы ғалымдар діңгек жасушаларын өсіру үшін қолданылатын қоректік ортадағы хайуандардың компонентт адамдардың сондай элементтерімен алмастыруды ұсынған еді. Алайда, қазіргі кезде, адамдардың жинақталған діңгек жасушалары желісінің, басқа да бөгде заттармен ластану мүмкіндіктері əлі де сақталуда деген қауіп туындайды.
1. Жасушаларды клондау
Жасушаларды клондау жұмыстары – денелік (сомалық) жасушаларының ядросын тасымалдау арқылы жүзеге асырылады. Бұл дегеніміз, құрамында ересек жасушалардан алынған генетикалық материал болғанымен, өздерін эмбриональдық діңгек жасушалары сияқты көрсете алатын жасушалар шығару технологиясына қол жеткізу болып табылады. Осы үдеріс ұрықтанған аналық жасушасы мен ересек ағзадан алынған денелік жасушадан басталады. Мұндағы басты шарт – ұрықтанған аналық жасушасы мен денелік жасуша алынған донорлардың иелері бір тұл болмауы керек. Жұмыстың барысында ұрықтанған аналық жасушасының ядросы алынып тасталып, орнына денелік жасушаның ядросы қондырылады. Денелік жасуша ретінде қандай да болмасын жасушалар, яғни сүйек кемікшесіндегі жасушалардан бастап, тері қабатының жасушаларына дейін алынуы мүмкі. Осындай жолмен құрылған(бөгде генетикалық материал енгізілген) аналық жасушасы зиготаға дейін өсе береді, ал эмбриональдық діңгек жасушаларының желісі болса, басқа да эмбриональдық діңгек жасушаларының дамуы сияқты– бластоциттерден пайда болады. Теория бойынша, құрамында ересек дене жасушасының ядросы бар аналық жасушасын жатырға бекіту арқылы, дəл денелік жасуша иесі сияқты, бүтін ағза өсіріп шығаруға болады деген пікір жасалынған болатын.
Содан бастап ғалымдар денелік жасушалардың ядросын тасым жұмыстарын хайуандармен жүргізе бастады. Сөйтіп, 1996 жылы ересек ағзадан алынған денелік жасуша ядросы аналық жасушасына(яйцеклетка) енгізіліп, одан дамыған алғашқы клонды жануар– доли атты қой дүниеге əкелінді. Осы уақыттан
бастап |
белгілі |
технологияны |
пайдаланып |
мыңдаған |
ірі |
қара, |
тышқандардың жəне басқа да хайуандардың клондары алынды. |
|
|
||||
АҚШ-дағы Гарвард университетінің ғалымдары2005 жылдың тамыз айында денелік жəне эмбриональдық жасушаларды қосу арқылы тұрақты жасуша желілерін алғандары туралы хабарлады. Бірақ, бұлардың алған жасуша желілерінде, денелік жəне эмбриональдық жасуша желілерінің екеуінің де ДНҚ-ы кездеседі. Бұған қарамастан ғалымдар алынған жаңа жасуша желілері ағзада кездесетін барлы ұлпаларды түзуге қатынасатынын анықтаған. Бұл жетістік нəтижесі, біршама уақыттардан кейін, оны адамдар жасушалары желісінде əртүрлі ауруларды емдеу үшін қолдануға болады деген сенімге жетелейді.
Жоғарыда аталған технологияның клондаудан айырмашылығы неде деген сұраққа жауап беретін болсақ, ең негізгісі – аналық жасушаның ядросының
33
алмастырылуы мен модификацияланған жасушаның аналық жатырына ендірілуі себебінен, одан денелік жасуша алынған ағзаның толықтай көшірмесі дам шығатынын айтуға болады.
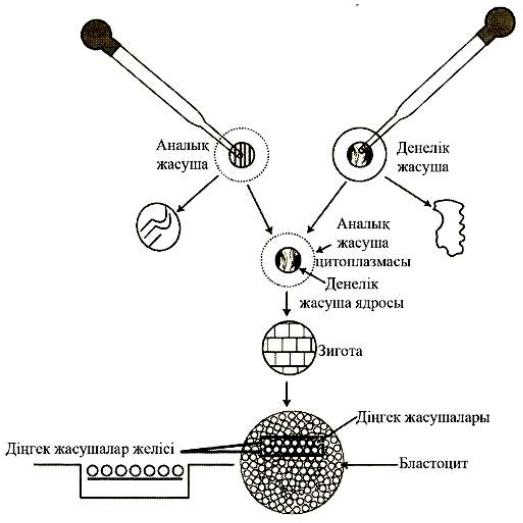
Денелік жасушалардың ядросын тасымалдау жұмыстарының жалпы схемасы келесі 8-ші суретте берілген.
8-сурет. Денелік (сомалық) жасуша ядросын ауыстыру (Ш. Уолкер. Биотехнология /Путеводитель, 2008.)
Терапиялық мақсатта эмбрионалдық діңгек жасушаларын пайд мүмкіндігі өте жоғары. Эмбриональдық діңгек жасушаларының желісін тікелей емделетін ауыру адамның денелік жасушаларын қолдану арқылы да алуға болады. Теория бойынша, осындай жолмен дайындалған эмбриональдық ді жасушаларын, науқас адамның ауру мүшесіне егу арқылы, оның қайта қалпына келуін қамтамасыз етуге болады. Болашақта эмбриональдық жасушаларын пайдалану мүмкіндігі кеңейіп, адам ағзасына қажетті мүшелерді толықтай өсіріп шығару бағытындағы жұмыстар өз жалғасын табады деген болжамдар жасалынуда. Осындай жолмен дайындалған мүшелердің пациенттің денелік жасушаларына дамуы себепті, иммундық жауап реакциясының туындауына ешқандай мүмкіндік туылмайды. Алайда бүтіндей бір мүшені өсіріп шығару деңгейіне жету , үш жасушаның мамандану үдерістері жөнінде түпкілікті зерттеулер жүргіз,
34
толықтай мəліметтер алынуы қажет. Сонымен бірге, егерде науқас адам бір аурудан тұқым қуалаушылық қабілетке ие ,болсаод н дайындалған эмбрионалдық жасушалардың да сол кеселді қайтадан ағзаға апару мүмкіндігі де сейілмейді.
Денелік жасушалар ядросын тасымалдау технологиясын пайдаланудың өзіндік шектеулері мен кемшіліктері де бар. Мысалы, денелік жасушалардың ядросын тасымалдау технологиясын қолдану арқылы жасалынған , кл эмбрионалдық даму кезеңдерінің соңғы мерзімдерінде, түсік тасталу қауіпі немесе əртүрлі кемістердің туылу мүмкіндіктері де жоғары келеді. Сонымен бірге, мұндай технологияны адамдарға қолдану мүмкіндігінің туындауы себепті, қоғамдағы пікірлердің қалыптасуы мен оның моральдық-этикалық тұстары да ескерілуі қажет.
4.1 Адам жəне жануарлар жасушаларын биотехнологияда пайдаланудың маңызы
Биотехнологияда адам жəне жануарлар жасушаларын пайдаланудың кезеңі
1949 жылдан басталады. Ол кезде американдық бір топ ғалымдар Эндерс, Уоллес |
|||||||
жəне Робинс адам ұрығының, бұлшық ет жəне тері жасушаларының дақылдарында |
|||||||
полиомиелит |
ауруының вирусын өсірген. Соңынан вирустарға көбірек адам |
||||||
ұрығының жəне ересек маймылдың бүйрек жасушалары, тауық эмбрионының |
|||||||
амниотикалық |
қабығы |
өзіне |
тез |
қабылдағыш |
болып |
келетіні . аны |
|
Тəжірибелік зерттеу жұмыстарының барысында əрдайым дақылда болатын, егілетін |
|||||||
жасушалар |
желілері (линия) алынды. |
Мысалы, |
олардың қатарында жатыр |
||||
мойнының карцинома жасушалары(НеІа), асыранды атжалмандардың (хомяктар) |
|||||||
эмбриондарының бүйрек |
жасушалары(ВНК-21), |
жасыл |
мешіндердің (зеленые |
||||
мартышки) |
бүйрек жасушаларын (Vero) |
айтуға |
болады. Олар əлемдегі көптеген |
|
|||
зертханаларда вирустарды бөліп алуда жəне |
таза вирустық дəрмектер өндіруде, |
||||||
вирустық инфекцияларды зерттеуде, аурулардың профилактикалық алдын-алу мен |
|
||||||
емдеу шараларына арналған вакцина дайындау үшін пайдаланылады. Егілетін |
|
||||||
жасушалық |
дақылдарды |
алғанға |
дейін |
вирустар |
біріншілік |
ж |
|
дақылдарында өсіріледі. Жаңа əдіс вирустарды таза күйінде бөліп алумен қатар, диагностикалық жəне профилактикалық вакцина дайындау үшін қажетті вирустық материалдарды үлкен масштабта өңдеуге мүмкіндік туғызды.
Адам жəне жануарлардың жасушалық дақылдарын басқа да бағалы заттарды |
|
||
алу мақсатында пайдаланылуы – дифференцияланған жасушарды дақылдау, егілетін |
|
||
жасушалардың |
тұрақсыздығын |
реттеу сияқты мəселелерді шешумен |
т |
байланысты. Сондықтан, қазіргі кезде жасушалық дақылдардың биотехнологияға үлкен жетістікпен енгізілген мысалдарының саны өте аз. Мысал ретінде, адам жəне тышқан жасушаларының суспензиялық дақылдары арқылы антивир гликопротеид-интерферонын, сонымен қатар тəжірибе жүзінде адам, өгіз жəне шошқа ұйқы безінің бета-жасушасының егілетін желілерін пайдалану арқы инсулин гормонын өндіруді айтуға болады.
Жасушаларды дақылға айналдыру үдерісінде жасуша аралық байланыстар бұзылып, механикалық зақымданудың нəтижесінде жасушаның беті өзгеріск
ұшырайды, сондықтан, жасушалық |
дақылдар |
əдісінің |
əрі |
қарай , же |
||
жасушалардың |
организмдегі |
күйін |
ескере |
отырып, дақылдау |
жағдайларын |
|
35
қалыптастыру (оптимизация) жəне |
тұрақтандыру (стабилизация) əдістерін |
||||
қалыптастырумен байланысты болады. |
|
|
|
|
|
Жасушалар |
дақылдарының |
бағалы |
фенотиптік |
белгілерін |
ұзақ |
аралығында сақтап қалуы да шешімді |
талап ететін мəселелердің |
бірі б |
|||
табылады. Осындай |
шешімнің бір |
жолы– |
қалыпты диффенцияланған |
жəне |
|
трансформацияланған жасушаларды |
біріктіру нəтижесінде түзіл, гибридтіен |
||||
жасушаларды алу болып табылады. Мысалы, қалыпты лимфоциттер мен миеломды жасушаларды біріктіруден алынған гибрид, дақылдану үдерісінде шексіз өсуге жəне белгілі антиденелер синтездеуге қабілетті болып келеді. Гибридомды əдісі – бір ғана антигенді детерминантқа қарсы бағытталған жəне жоғары спецификациялық, бір жасушаның ұрпағы түзетін моноклональді антидене алуға мүмкіндік береді. Қазіргі кезде моноклональді антидене өндірісі биотехнологияда маңызды орын алады.
Моноклональді антиденелері – ферменттер мен ақуыздардың полиморфизмін, өсуді реттеу механизмін, денелік (сомалық) жасушалардың пролиферациясын, сəйкессіздіктің антигендерін, дифференцияланған жасушалардың əртүрлі типін сипаттайтын антигендерді зерттеу мақсаттарында пайдаланылады.
Моноклональді антиденелердің тағы бір практикалық маңыздылығы– диагностикалық, емдік жəне профилактикалық заттар ретінде, биологиялық активті заттардың таза дəрмектерін(лейкоциттік интерферон) алуда қолданылуы.
Гибридомдық əдістің қолданылуына байланысты, оның өндірістік маңыздылығы жөнінде американдық қаржылық мекемелерінің деректері бойынша мына фактілерді келтіруге болады: 1987 жылы моноклональді антидене негізіндегі даиагностикалық дəрмектерді өндіруге 500 млн. доллар, ал 1990 жылы тек қатерлі
ісік (рак) ауруларының диагностикумдарын алуға2 млрд. |
доллар қаржы |
|
жұмсалынған. Ғалымдар көптеген қан ауруларына да қарсы |
күрес жүргізуде, осы |
|
мəселені шешудің бір жолы – “қолдан қан жасау” болып есептеледі. |
|
|
Биотехнология жетістіктері мал шаруашылығында |
да |
қолданылады. Бұл |
бағытта аурулардың алдын алу, диагностикалау жəне моноклональды антиденелерді пайдалана отырып емдеу, мал тұқымдарын генетикалық тұрғыдан жақсарту сияқты
жұмыстарды |
айтуға |
болады. Қазіргі |
кезде |
малдарды |
қолдан |
ұрықтандыр |
мəселесінде де биотехнология əдістері кеңінен қолданылуда. |
|
|
||||
4.2 Жасушалық биотехнологияның болашағы жəне даму бағыттары
Биотехнологиясының қарқынды дамып келе жатқан бағыты – биоэлектроника
– биологиялық организмдердің құрылымдары жəне электронды құрылымдарымен
тығыз байланысты. Оларға: |
биологиялық |
сенсорлар (биосенсор), биологиялық |
||||
микрочиптер (биочиптер), биотесттер |
жатады. «Биосенсор» |
деген |
терминді |
|||
айқындайтын |
компоненттің |
болуын |
тікелей |
қоятын |
биологиялық :мате |
|
ферменттер, |
жасушалар, бактериялар, |
ашытқы, |
антигендер, антиденелер, |
|||
липосомалар, органеллалар, рецепторлар, ДНҚ бар сезімді қабат. Бұл компоненттің шоғырлануымен функциональды байланысты, дабылды шығаратын құрылғыны түсіну қажет. Конструкциялық түрде биосенсор – бір-бірімен тығыз байланыстағы екі биохимиялық жəне физикалық түрлендірігіш немесе трансдюсерден тұратын құрамдас құрылғы. Қазіргі уақытта биосенсорлардың бірнеше түрлері бар. Олардың
36
қатарында – хемижəне |
биолюминисценция |
негізіндегі |
ферменттік электродтар, |
|||
ферменттік микрокалориметрлік датчиктер жəне биодатчиктерді айтуға болады. |
||||||
|
Биологиялық микрочиптер – |
əртүрлі |
биохимиялық талдауларды |
жүргізу |
||
үшін |
қолданылатын |
кішкентай |
құрылғылар. Бұл – |
талданатын |
нұсқалар |
|
құрамындағы кез-келген заттармен өзара əрекеттесе алатын, реакцияға қабілетті агенттер түрлері салынған микропластинкалар. Оларда талданатын ерітпелерде бар заттардың молекуларын іріктеп байланыстыратын функциональдық жағдайдағы биологиялық белсенді макромолекулалар химиялық байланған. Биочиптің құрамына келетін болсақ, көптеген көзге əрең көрінетін, əрқайсысының диаметрі 100 микроннан кіші, жартылай сфералық гидрогендік ұяшықтарға салынған, үлкен емес əйнектен жасалған пластинкадан тұрады.
Ғалымдар əртүрлі заттарды жылдам жəне өте нақты айқындауға мүмкіндік беретін биочиптік-тест жүйелерін ойлап шығарды. Кейбір аурулардың бастапқы кезеңдерінде ақуыз қатарында аздаған өзгерістер болып . жатадыОсындай өзгерістерді дер кезінде байқап, алдын-ала профилактикалық шараларды жасау үшін өте қажетті болып табылатын жаңа ғылым саласы– протеомика, ақуыздарды зерттеуге, олардың тірі организмдердегі синтезіне, бір-бірімен өзара əрекеттесуіне жəне күрделі қатынастарға негізделетіні жөнінде оқулық материалдарының келесі тарауларында толықтай беріледі. Ресейлік жəне француз ғылымдары ақуыздардағы өзгерістерді табуға жəне талдауға қабілетті қондырғылар жасауда.
Протеомиканың негізгі бір бағыты– ақуыздың өзара байланысын жəне молекула үсті кешенінде орналасуын анықтау. Бұл бағыт биохимиялық үдерістер
жасушада құрылған жəне олар |
ферменттер, рецепторлар жəне . тб. |
белсенді |
||
байланыстарды таңдау |
арқылы |
жасалды. Ақуыздар арасындағы |
байланысты |
|
анықтау үшін ашытқының екі гибридті жүйесін қолданады. Бұл əдіс ақуыз-ақуыз, |
||||
ақуыз-ДНҚ, ақуыз-РНҚ |
байланыстарын |
анықтайды. Ғалымдар |
протеомика |
|
саласында ақуыздардың өндірілуін жəне олардың денедегі ақуыздардың ауыс
декомпозициясын, сондай-ақ организмде синтезделуінен кейінгі ақуыздардың қалай |
|
||||||||||||||
модификацияланатынын |
зерттеуде. |
Қазіргі |
кезде |
нарықтағы |
фармакологиялық |
||||||||||
заттардың |
95%-ы |
протеиннің |
əсеріне мақсатталған. «Thermo |
Finnigan» |
(АҚШ) |
|
|||||||||
компаниясы жоғары технологиялық талдаушы құралдарды жасайды. Бұл компания |
|
||||||||||||||
хроматография, массалық спектрометрия жəне бағдарламалық өнімдерді шығарумен |
|
||||||||||||||
қатар, |
осы |
бағытта өз |
күштерімен жаңа құралдар |
дайындаумен |
айналысу. |
||||||||||
Мысалы, ақуыздық чиптерді. |
|
|
|
|
|
|
|
|
|
|
|
||||
Ақуыздық микрочиптерді əзірлеу өте күрделі жұмыс болып табылғандықтан, |
|
||||||||||||||
үлкен инвестициялар тартуды қажет етеді. Қазіргі кезде «Сiphergen Inc» компаниясы |
|
||||||||||||||
ең |
танымал |
ақуыздық |
чип |
шығарушы |
|
болып |
. |
таныладыБұлкомпания |
|||||||
хроматографиялық |
ақуыздық |
чиптер |
мен |
. |
массспектрометрлік |
детекторды |
|||||||||
(анықтаушы) байланыстыратын қондырғы жасап шығарды(Protein Chip System). |
|
||||||||||||||
Аталған |
жүйе |
күрделі |
биологиялық |
ортадағы |
|
паталогиялық |
жағ |
||||||||
биомаркерлерді іздейді. Бірінші |
топ – ДНҚ-чиптерінің миниатюралық |
құрылымы |
|
||||||||||||
жасалып, моноклональді |
антиденелер |
немесе |
|
олардың |
|
аналогы |
маркерле |
||||||||
микроөріс құруға қолданылады. Бұл құралдар, |
|
гендер |
мен |
оның |
құрамдас |
||||||||||
бөліктерінің өзара нəзік |
байланыстарының реттелуін зерттеу мақсатынд, |
||||||||||||||
молекулалық биологияның іргелі міндеттерін орындай алады деп есептелінуде. |
|
||||||||||||||
37
Голландиялық «Glaucus Proteomics» фирмасы осы бағыттағы жұмыстарында жетекші орынды алады. Қазіргі күні нарыққа цитокинді, күйзелісті қоздыратын ақуызды анықтайтын арнаулы чиптері шығарылған. Екінші топ – in vitro трансляция арқылы жүзеге асатын ақуыз-ақуыз байланысы жəне фазаға азықты жағуPISA (Protein In Sity Array) трансляцияның жасуша жүйесін жəне ПТР-азықты қолдану арқылы ақуыздарды тасымалдайды. Ақуыздық чипті шығаратын тағы бір компания
«WITA |
Proteomics». |
Жасушалық |
дақылға |
тигізетін |
токсиндік |
||
идентификациялауға |
арналған 2Д-электрофорезі |
сияқты |
ақуыздық |
биочи |
|||
технологиясы өте қарқынды дамып, медициналық диагностикада |
жəне жаңа |
дəрі- |
|||||
дəрмектерді сынауда да кеңінен қолданылуда. |
|
|
|
|
|||
Биоселективтік |
датчиктерін |
ионоселективті |
электродтар |
бетіне |
|||
микроорганизмдер жасушаларын немесе ұлпаларын жұқтыру арқылы жасайды. |
|||||||
Мысалы, |
Neurospora |
europea бактерияларын NH3, ал |
сірке қышқылын |
анықтау |
|||
мақсатында Trichosporon brassiacae пайдаланылады. |
|
|
|
|
|||
Сонымен бірге сенсорлар ретінде өте жоғары сезімталдық қабілетке ие болып табылатын моноклональді антиденелері де пайдаланылады. Биодатчиктер мен биочиптерін жасауда əлемдегі жетекші орындардыHitachi, Sharp сияқты Жапон компаниялары алады.
Қазіргі кезде, өткізгіштік қасиетін ақуыз молекуласы атқаратын, жартылай өткізгіштіктер типтері жасап шығарылуда. Осындай ферменттік негізден тұратын жүйелердің, кремнийден жасалынатын өткізгіштерімен салыстырғанда, жоғары қабілетке ие екендіктері анықталған. Мұндай биочиптер шағын көлемді, сенімді жəне өздігінен ұйымдасуға қабілетті болып келеді. Мəселен, Sony деген Жапон компаниясы, бактериялар өнімі болып табылатын, целлюлозадан жасалынатын жоғары акустикалық қабілетке ие жүйелерін ойлап тапқан. Гель тəрізді целлюлоза арнайы кептіріледі. Осындай өнім құрылысы бойынша көптеген майда ұяшықтардан (сот) тұруы себепті, акустикалық жүйелерге лайықты жалпақ диафрагма ретінде пайдаланылады.
Соңғы жылдары ДНҚ технологияларының жетістіктері– биочиптердің
дамуына байланысты, |
қатты |
жазықтарда |
айқын молекулалардың |
селективтік |
сорбция үдерістерін, детекцияның физикалық əдістерін қолданатын, ДНҚ-сенсорлар |
||||
деп аталатын чиптері |
кеңінен |
пайдаланыла |
бастады. ДНҚ-сенсор жоғары |
сезімді, |
шағын көлемді, кіші |
көлемде өлшеудің байланыссыз əдісін іске асырады жəне |
||||||
қолданылуы |
оңай |
болып |
.келедіҚазіргі |
уақытта |
əртүрлі |
фирмаларды |
|
бағдарламалық |
|
қамтамасыз |
етуімен |
нейлондықмембраналар |
– |
||
микроорганизмдердің, |
өсімдіктердің, сүтқоректілердің жəне адамның гендерімен |
||||||
сүзгіштерге негізделетін ДНҚ-микрочиптердің шығуына қол жеткізілді. |
|
|
|||||
38
ІІтарау бойынша өзін-өзі бақылауға арналған сұрақтар мен тапсырмалар.
1.Жасушалық инженерия ғылымының зерттеу аясы не?
2.Денелік жасушаларын гибридизациялаудың үдерістері қандай кезеңдерден тұрады?
3. |
Денелік жасушаларын |
гибридизациялау |
үдерісін пайдалану адамдарғ |
|
қандай мүмкіндіктер береді? |
|
|
4. |
Хайуандар жасушаларын |
өсірудің негізгі |
бағыттары қандай? Олардың |
|
мəнін түсіндіріңіз. |
|
|
5.Жасанды ортада өсіру үшін қандай жасушаларды таңдап алған дұрыс деп ойлайсыз?
6.«Өлмейтін» қабілетке қандай ұлпаларынан алынған жасушалар ие болады? Денелік жəне ұрықтық жасушаларының басты ерекшеліктері қандай?
7.Эмбриональдық діңгек жасушаларының басты ерекшеліктері артықшылықтары қандай?
8.Гематопоэтикалық жасушалар дегеніміз не жəне олардың қолданы мүмкіндіктері қандай?
9.Плюрипотентті діңгек жасушалары дегеніміз? Олардыңне қолдану мүмкіндігінің болашағы қандай деп ойлайсыз?
10.Ересек діңгек жасушалары қандай ағзадан алынады, олардың басты ерекшеліктері жəне қандай мақсатта қолдануға болады?
11.Ересек діңгек жасушаларының басқа ағзаға қабылданбай қоюының басты себебі неде?
12.Эмбрионалдық діңгек жасушалары қандай ағзалардан алынады?
13. |
Эмбрионалдық |
жасушаларының |
басты |
артықшылықтыры |
|
медицинада қолданылу мүмкіндігінің болашағы қандай? |
|
||
14. |
Медицинада тəжірибелерге қажетті эмбриональдық діңгек жасушалары |
|||
|
қалай алынады? |
|
|
|
15. |
Эмбриональдық |
діңгек жасушаларының желісін |
дайындауда, қандай |
|
сатыға дейін өсіріп қадағалайды?
16.Жасуша желілері не үшін ауық-ауық жаңа жасушалармен ауыстырылып тұру қажет?
17.Жасушаларды клондау жұмыстарының практикалық маңызы қандай?
18.Жасушаларды клондау жұмыстары қалай жүзеге асырылады?
19.Жасушаларды клондау жұмыстарын адамдарға қолдануға бола ма?
20. Биотехнологияда |
адам жəне |
жануарлар |
клеткаларын |
пайдалану қ |
|
|
жылдан басталады? |
|
|
|
|
21. |
Гибридомды əдіс дегеніміз не? Қазіргі кезде моноклональді антительдерді |
||||
|
қандай мақсатта қолданады? |
|
|
|
|
22. |
Моноклональді |
антиденелерді |
қолданудың |
практикалық |
маңыздылығы |
мен болашағы қандай?
23.Биоэлектрониканың болашағы мен мүмкіндіктері қандай деп ойлайсыз?
24.Биосенсорлардың қанша түрлері бар?
25.Биологиялық жəне ақуыздық микрочиптер дегеніміз не жəне оларды қолданылу аймағы мен болашағы қандай?
39
