
- •3. Биологическая роль элементов в зависимости от положения в пс д.И. Менделеева.
- •4. Понятие о биогенных элементах. Макро- и микроэлементы в организме человека. Топография важнейших биогенных элементов в организме человека.
- •5. Общая характеристика s-элементов. Характеристика элементов I a группы. Биогенная роль данных элементов, применение их соединений в медицине. Радионуклид Cs-137.
- •6. Общая характеристика s-элементов II a группы. Их биогенная роль и применение соединений в медицине. Радионуклид Sr-90.
- •7. Общая характеристика p-элементов и их соединений. Характеристика элементов III a группы. Биогенная роль данных элементов, применение их соединений в медицине.
- •19. Характеристика энергетического состояния электрона в атоме системой квантовых чисел. Принцип Паули. Правило Хунда. Принцип минимума энергии.
- •21. Периодичность изменения радиусов атомов и ионов, энергии ионизации, сродства к электрону и электроотрицательности атомов.
- •22. Химическая связь. Природа и типы химической связи. Зависимость потенциальной энергии системы из двух атомов водорода от расстояния между их ядрами. Энергия и длина связи.
- •26. Ионная связь.
- •27. Водородная связь. Межмолекулярная и внутримолекулярная водородная связь. Роль водородной связи в процессе ассоциации молекул.
- •1) Вода
- •28. Комплексные соединения. Координационная теория Вернера. Центральный атом, лиганды. Координационное число центрального атома.
- •31. Комплексообразующая способность s-, p-, d- элементов. Реакции комплексообразования. Реакции разрушения комплексных соединений.
- •39. Метод нейтрализации (кислотно-основное титрование). Ацидиметрия и алкалиметрия. Стандартные растворы. Кислотно-основные индикаторы.
- •48. Энтропия: термодинамическое и статистическое толкование. Уравнение Больцмана. Расчет энтропийного фактора химической реакции по стандартным энтропиям вещества.
- •51. Смещение химического равновесия обратимых реакций при изменении температуры, концентрации и давления. Принцип Ле Шателье.
- •52. Предмет химической кинетики. Химическая кинетика как основа для изучения скорости и механизма биохимических процессов.
- •53. Скорость химической реакции для гомогенных и гетерогенных превращений. Механизм химических реакций; молекулярность реакций.
- •54. Закон действующих масс для скорости химической реакции. Константа скорости. Порядок реакции.
- •57. Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Температурный коэффициент реакции. Энергия активации. Уравнение Аррениуса.
- •58. Теория активного комплекса. Объяснение действия катализатора с позиций данной теории. Катализ и катализаторы. Автокаталитические реакции.
- •59. Кинетика ферментативных реакций. Уравнение Михаэлиса-Ментен. Молекулярная активность (число оборотов) фермента. Факторы, влияющие на активность ферментов.
- •60. Понятие о растворах. Классификация растворов. Роль растворов в жизнедеятельности организмов.
- •61. Способы выражения состава раствора: массовая доля, молярная концентрация, молярная концентрация эквивалента, молярная доля, объемная доля, титр.
- •62. Термодинамика растворения. Теплота растворения.
- •63. Насыщенный раствор. Растворимость. Факторы, влияющие на нее.
- •64. Растворимость газов в жидкостях. Уравнение Генри и Сеченова. Причина возникновения кессонной болезни. Растворимость газов в крови.
- •66. Растворимость жидкости в жидкости. Неограниченно смешивающиеся, несмешивающиеся и частично смешивающиеся жидкости. Закон распределения Нернста-Шилова. Экстракция из растворов.
- •67. Коллигативные свойства растворов. Давление насыщенного пара над раствором. Закон Рауля.
- •68. Криоскопический и эбулиоскопический законы. Криоскопия и эбулиоскопия как методы экспериментального определения молярной массы растворенного вещества.
- •69. Осмос и осмотическое давление. Уравнение Вант-Гоффа. Полупроницаемые мембраны в организме.
- •72. Основные положения теории слабых электролитов Аррениуса. Константа диссоциации, степень диссоциации. Закон разведения Оствальда.
- •74. Роль электролитов в жизнедеятельности человека. Ионный состав внутри- и внеклеточных жидкостей. Ионная сила плазмы крови.
- •77. Буферные системы, классификация, механизм их действия. Расчет рН буферных систем. Уравнение Гендерсона-Гассельбаха. Буферная емкость.
- •81. Метод электронного баланса и метод полуреакций при расстановке коэффициентов в уравнениях ов реакций. Важнейшие окислители и восстановители.
- •82. Устройство и принцип действия гальванических элементов. Ов, диффузные и мембранные потенциалы. Уравнение Нернста. Классификация электродов.
- •83. Потенциометрия. Потенциометрическое определение рН растворов. Хлорсеребряный электрод. Стеклянный электрод с водородной функцией.
- •86. Поверхностные явления и их значение в медицине и биологии. Поверхностная энергия и поверхностное натяжение. Определение поверхностного натяжения сталагмометрическим методом.
- •88. Твердые адсорбенты. Активная поверхность как важнейшая характеристика твердых адсорбентов. Классификация твердых адсорбентов. Биологическая роль пищевого волокна.
- •89. Адсорбция на твердых адсорбентах. Теория мономолекулярной адсорбции Ленгмюра. Уравнение Ленгмюра. Теория полимолекулярной адсорбции Поляни и бэт. Эмпирическое уравнение Фрейндлиха.
- •90. Адсорбция из растворов электролитов: избирательная, ионообменная. Правила Панета-Фаянса. Иониты, их применение в медицине и биологии.
- •91. Адсорбционная терапия. Гемо-, лимфо- и плазмосорбция. Энтеросорбция и энтеросорбенты.
- •92. Дисперсные системы. Их классификация. Методы получения и очистки коллоидных растворов.
- •93. Молекулярно-кинетические и оптические свойства дисперсных систем.
- •94. Электрокинетические явления. Электрофорез, электроосмос. Применение электрофореза в биологических и медицинских исследованиях.
- •95. Строение коллоидной мицеллы лиофобных золей. Двойной электрический слой. Электрокинетический потенциал коллоидной частицы и устойчивость коллоидного раствора.
- •98. Микрогетерогенные системы: эмульсии, аэрозоли, пены.
- •99. Высокомолекулярные соединения и их растворы. Природные и синтетические вмс. Методы получения вмс и их классификация.
- •101. Полиэлектролиты. Изоэлектрическое состояние и изоэлектрическая точка белка. Методы определения иэт.
51. Смещение химического равновесия обратимых реакций при изменении температуры, концентрации и давления. Принцип Ле Шателье.
Состояние химического равновесия является наиболее энергетически выгодным состоянием обратимого процесса, так как характеризуется минимальным запасом внутренней энергии системы(G min)

Принцип Ле Шателье: «Если на систему, находящуюся в состоянии химического равновесия, оказывать внешнее воздействие (изменять темпера-туру, давление, концентрации веществ), то положение равновесия смещается в такую сторону, чтобы ослабить внешнее воздействие». В любом случае равновесие будет смещаться до тех пор, пока не наступит новое положение равновесия, которое соответствует новым условиям. Этот принцип позволяет легко предсказать качественные изменения в равновесной системе при изменении условий


 Изменение
давления не влияет на смещение химического
равновесия, если:
В
реакции не участвуют газы;
Реакция
протекает без изменения количества
газообразных веществ N2
+ O2
↔ 2 NO
Изменение
давления не влияет на смещение химического
равновесия, если:
В
реакции не участвуют газы;
Реакция
протекает без изменения количества
газообразных веществ N2
+ O2
↔ 2 NO



52. Предмет химической кинетики. Химическая кинетика как основа для изучения скорости и механизма биохимических процессов.
Химическая кинетика - это раздел физической химии, изучающий скорость и механизм химических реакций. Кинетический метод исследования, наряду с термодинамическим и квантово-механическим, широко применяется в современном естествознании.

 [A]0_
и
[A]
– исходная и конечная концентрация
вещества, моль/л,
τ
- время реакции, с., мин., (+) – вещество
образуется, (–) – вещество расходуется.
[A]0_
и
[A]
– исходная и конечная концентрация
вещества, моль/л,
τ
- время реакции, с., мин., (+) – вещество
образуется, (–) – вещество расходуется.
 Скорость
гетерогенной реакции равна изменению
количества вещества в единицу времени
на единице площади поверхности раздела
фаз:
Скорость
гетерогенной реакции равна изменению
количества вещества в единицу времени
на единице площади поверхности раздела
фаз:
![]() где
ν0
и
ν – количество вещества в начальный
и конечный момент времени, моль, S –
площадь поверхности раздела фаз, м2.
Большинство биохимических реакций
являются гомогенными. Они протекают с
различной скоростью. Например, химические
реакции, лежащие в основе передачи
нервного импульса, протекают практически
мгновенно. Полное
обновление костной ткани осуществляется
за 4-7 лет. Время обновления белков на
половину составляет около 70 дней. На
скорость химических реакций влияет:
а) природа реагирующих веществ, б) их
агрегатное состояние, в) природа
растворителя (если реакция протекает
в растворе), г) площадь поверхности
реагирующих веществ (для гетерогенных
реак-ций), д) концентрация реагирующих
веществ, е) давление (для газофазных
реакций), ж) температура, з) катализатор.
где
ν0
и
ν – количество вещества в начальный
и конечный момент времени, моль, S –
площадь поверхности раздела фаз, м2.
Большинство биохимических реакций
являются гомогенными. Они протекают с
различной скоростью. Например, химические
реакции, лежащие в основе передачи
нервного импульса, протекают практически
мгновенно. Полное
обновление костной ткани осуществляется
за 4-7 лет. Время обновления белков на
половину составляет около 70 дней. На
скорость химических реакций влияет:
а) природа реагирующих веществ, б) их
агрегатное состояние, в) природа
растворителя (если реакция протекает
в растворе), г) площадь поверхности
реагирующих веществ (для гетерогенных
реак-ций), д) концентрация реагирующих
веществ, е) давление (для газофазных
реакций), ж) температура, з) катализатор.
53. Скорость химической реакции для гомогенных и гетерогенных превращений. Механизм химических реакций; молекулярность реакций.


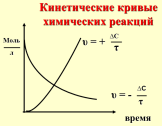
[A]0_ и [A] – исходная и конечная концентрация вещества, моль/л, τ - время реакции, с., мин., (+) – вещество образуется, (–) – вещество расходуется.
 Скорость
гетерогенной реакции равна изменению
количества вещества в единицу времени
на единице площади поверхности раздела
фаз:
Скорость
гетерогенной реакции равна изменению
количества вещества в единицу времени
на единице площади поверхности раздела
фаз:
![]() где
ν0
и
ν – количество вещества в начальный
и конечный момент времени, моль, S –
площадь поверхности раздела фаз, м2.
Большинство биохимических реакций
являются гомогенными. Они протекают с
различной скоростью. Например, химические
реакции, лежащие в основе передачи
нервного импульса, протекают практически
мгновенно. Полное
обновление костной ткани осуществляется
за 4-7 лет. Время обновления белков на
половину составляет около 70 дней. На
скорость химических реакций влияет:
а) природа реагирующих веществ, б) их
агрегатное состояние, в) природа
растворителя (если реакция протекает
в растворе), г) площадь поверхности
реагирующих веществ (для гетерогенных
реакций), д) концентрация реагирующих
веществ, е) давление (для газофазных
реакций), ж) температура, з) катализатор.
Механизм химической реакции – это
число и последовательность элементарных
стадий процесса. Элементарная стадия
– это столкновения молекул реагирующих
веществ, приводящее к образованию
молекулы продукта. Характеристикой
механизма является молекулярность
элементарных стадий. Молекулярность
– это число частиц, участвующих в
элементарном превращении. Различают:
где
ν0
и
ν – количество вещества в начальный
и конечный момент времени, моль, S –
площадь поверхности раздела фаз, м2.
Большинство биохимических реакций
являются гомогенными. Они протекают с
различной скоростью. Например, химические
реакции, лежащие в основе передачи
нервного импульса, протекают практически
мгновенно. Полное
обновление костной ткани осуществляется
за 4-7 лет. Время обновления белков на
половину составляет около 70 дней. На
скорость химических реакций влияет:
а) природа реагирующих веществ, б) их
агрегатное состояние, в) природа
растворителя (если реакция протекает
в растворе), г) площадь поверхности
реагирующих веществ (для гетерогенных
реакций), д) концентрация реагирующих
веществ, е) давление (для газофазных
реакций), ж) температура, з) катализатор.
Механизм химической реакции – это
число и последовательность элементарных
стадий процесса. Элементарная стадия
– это столкновения молекул реагирующих
веществ, приводящее к образованию
молекулы продукта. Характеристикой
механизма является молекулярность
элементарных стадий. Молекулярность
– это число частиц, участвующих в
элементарном превращении. Различают:
а) мономолекулярные превращения: I2 → 2I, б) бимолекулярные превращения: Н2 + I2 → 2HI, в) тримолекулярные превращения: 2NO + O2 → 2NO2. Молекулярность не может быть больше трех, т.к. вероятность столкновения четырех и более частиц ничтожно мала. Химическая реакция является простой, если представляет собой многократное чередование одной элементарной стадии: H2 + I2 → 2HI. Если химическая реакция протекает в несколько стадий, то она является сложной. К наиболее сложным относятся радикальные (цепные) реакции, протекающие с участием радикалов. Радикал – это атом или группа атомов, имеющие неспаренный электрон. Радикалы образуются в результате термолиза, фотолиза, ОВР. H2 + Br2 → 2HBr. Механизм: 1) стадия инициирования (мономолекулярная) Br : Br → 2Br. 2) рост цепи (бимолекулярная стадия): Br + H2 → HBr + H, H + Br2 → HBr + Br, 3) обрыв цепи (бимолекулярная стадия) 2Br → Br2, 2H → H2, H + Br → HBr . Радикальные реакции протекают in vivo под действием радикалов ОН●, НОО●, ROO●, О2 ● и др. Ученые считают, что накопление радикалов во внутриклеточных жидкостях – одна из причин старения. Реакция пероксидного окисления липидов, скорость которой резко возрастает даже под воздействием малых доз радиации, приводит к разрушению клеточных мембран, нарушению обмена веществ в клетке, снижению клеточного иммунитета. Для снижения скорости пероксидного окисления используется антиоксиданты: витамины А, Е, С, соединения селена.
