
- •Глава 5. Термодинамика однокомпонентных систем
- •5.1. Термодинамические потенциалы идеальных газов
- •5.2. Реальные газы. Летучесть
- •5.3. Стандартное состояние
- •5.4. Зависимость летучести от температуры
- •5.5.Фазовые превращения. Уравнение Клаузиуса – Клапейрона.
- •5.6.Диаграммы состояния.
- •5.7. Энантиотропные и монотропные превращения
5.3. Стандартное состояние
Изобарный потенциал реального газа выражается уравнением (5.13), в котором G(T) – постоянная интегрирования, абсолютную величину которойопределить невозможно. Итак, нужно ввести некоторое стандартное состояние как начало отсчетаG. Поскольку прир0 летучесть реального газаfр, то за стандартное состояние можно было бы взять этот нижний уровень. Но такой выбор практически неудобен, так как прир0 изменение потенциала,поуравнению(5.15),G.
Поэтому застандартное состояние индивидуального газа при заданной температуре принимается гипотетическое состояние идеального газа, летучестькоторого равняется единице, аэнтальпия равняетсяэнтальпииреального газа при этой же температуре и нулевом давлении. За единицу давления принимается 1 бар = 1,000.105Па.
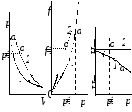
Переход газа из любого состояния в стандартноесхематическиизображен на рис. 5.4. Если реальный газ находится при данной температуре под давлениемр(точкаа), проведем изотермическое расширениедобесконечно малогодавления(р0), а потом сжатиепо изотерме идеального газа кр= 1 (точкао). Это и будет стандартное состояние, в которомfо =р= 1.
Для идеального газа всегда f=риf o= 1 при любой температуре. Для реального газа прир= 1 его состояние мало отличается от стандартного, то есть можно считать, что практически эти состояния совпадают. Итак, уравнения (5.13), с учетом стандартного состояния, можно записать:
G–Go(Т) =RTlnf/f o =RTlna. (5.26)
Рис.
5.4. Переход в стандартное состояние (1
– изотерма реального газа,
2
– изотерма идеального газа)
Для конденсированных фаз (индивидуальной жидкости или твердого тела) в качествестандартноговыбирается реальное состояние вещества прир= 1при заданной температуре. Жидкость или твердое тело находятся в равновесии с насыщенным паром; таким образом, можно определять свойства коденсированнойфазы через свойства насыщенного пара. Влияние давления на летучесть такой фазы описывается уравнением (5.18). Поскольку сжимаемость жидкости или твердого тела очень мала, то практически можно считать, чтоV= const. Тогда
![]() . (5.27)
. (5.27)
5.4. Зависимость летучести от температуры
Продифференцируемуравнение(5.26) по температуре прир= const, принимая во внимание, что летучестьзависит от температуры:
![]() (5.28)
(5.28)
или в соответствии с уравнением (5.26):
![]() . (5.29)
. (5.29)
Поскольку G=H–TS, а (G/T)p= –S(уравн. 4.32), тоG=H+T(G/T)pи
![]() и
и![]() (5.30)
(5.30)
В стандартном состоянии при любой температуре f o=1 и (ln f o/T)p= 0. Подстановка этого значения и уравнения(5.30)вуравнение (5.29) дает:
![]() , (5.31)
, (5.31)
где НоиН– энтальпии газа в стандартном и реальном состояниях, а их различие определяет изменение энтальпии при изотермическом изменении давления от заданного к стандартному.
Если предположить, что это различие не зависит от температуры, то интегрирование уравнения (5.31) дает:
![]() . (5.32)
. (5.32)
Изменение энтальпии можно рассматривать как затраты энергии на преодоление сил взаимодействия при переходе от реального к идеальному состоянию.
