
- •Глава 9. Диаграммы состояния двухкомпонентных систем с конденсированными фазами
- •9.1. Объемная и плоская диаграммы
- •9.2. Двухкомпонентные системы с простой эвтектикой
- •9.3. Термический анализ
- •9.4. Бинарные системы с химическим соединением, плавящимся конгруентно (без разложения)
- •9.5. Системы с химическим соединением, плавящимся инконгруентно (с разложением)
- •9.6. Твердые растворы
- •9.7. Двухкомпонентные системы с ограниченной взаимной растворимостью в твердом состоянии
- •9.8. Физико-химический анализ
9.3. Термический анализ
Диаграммы состояния строятся на основе опытных данных. Наиболее распространенным методом построения диаграмм является термический анализ, который не требует ни разделения сосуществующих равновесных фаз, ни их химического анализа.
В визуальном методе термического анализа производят медленное охлаждение прозрачного раствора известной концентрации и отмечают температуру, при которой появляются первые кристаллы, затем систему медленно нагревают и отмечают температуру исчезновения кристаллов, а затем находят среднее значение. Опыты проводят с серией растворов различной концентрации и таким образом получают данные для построения кривой зависимости температуры начала кристаллизации от состава. Метод применим к ограниченному кругу систем с достаточно низкими температурами кристаллизации.
Наиболее универсальным является метод построения кривых температура – время. В этом методе расплавленный образец (индивидуальное вещество, смесь определенного состава) медленно охлаждается, при этом фиксируется температура (с помощью термометра или градуированной термопары) через определенные промежутки времени (существуют также приборы с непрерывной автоматической записью кривых охлаждения). Основан метод на том, что если в системе не происходит фазовых превращений, то температура при охлаждении падает практически с постоянной скоростью. При любом фазовом изменении (кристаллизации, переходе одной кристаллической модификации в другую) скорость изменения температуры изменяется или наблюдается температурная остановка. Таким образом, любой излом на кривой охлаждения указывает на начало некоторого фазового превращения.
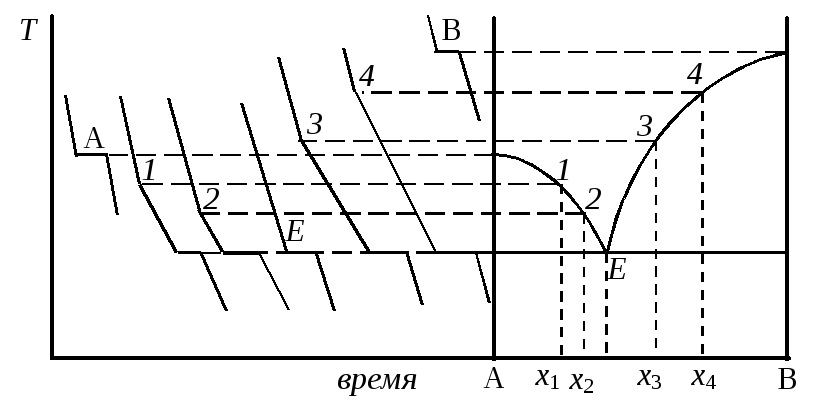 Рис.
9.3. Построение
диаграммы состояния
по кривым охлаждения
Рис.
9.3. Построение
диаграммы состояния
по кривым охлаждения
При охлаждении расплава индивидуального компонента A или B температура падает практически линейно вплоть до температуры кристаллизации, при которой происходит затвердевание компонента и температура остается постоянной до тех пор, пока весь расплав не закристаллизуется, после чего температура вновь продолжает снижаться. При охлаждении бинарного расплава определенного состава х1 (х2, х3,…) температура линейно уменьшается до температуры начала кристаллизации – точка 1 (2, 3 и т.д.).
Вследствие кристаллизации компонента A (или B) выделяется теплота кристаллизации и скорость охлаждения уменьшается – на кривой охлаждения появляется излом. Так как в процессе кристаллизации состав и масса расплава изменяются, то происходит нелинейное изменение температуры до достижения эвтектической точки, при которой вновь наблюдается температурная остановка. Если первоначальный состав расплава в точности соответствует эвтектическому, на кривой охлаждения получается только одна температурная остановка E. Температуры, соответствующие точкам излома или остановкам на кривых охлаждения, переносят на диаграмму состояния (правая часть рисунка) для соответствующих составов и соединяют плавными кривыми. В более сложных случаях, чем рассмотренный, на кривой охлаждения может быть несколько точек излома или температурных остановок.
