
- •VIII. Фізика атомів і молекул §113. Досліди Резерфорда. Ядерна модель атома
- •Шведов федір никифорович
- •§114. Атом водню і його спектр за теорією Бора
- •§115. Формула де Бройля. Дослідне обґрунтування корпускулярно-хвильового дуалізму властивостей речовин
- •Тартаковський петро савич
- •Лашкарьов вадим євгенович
- •Пасічник митрофан васильович
- •§116. Співвідношення невизначеностей як прояв корпускулярно-хвильового дуалізму властивостей матерії. Обмеженість механічного детермінізму
- •§117. Хвильова функція і її статистичний зміст
- •§118. Рівняння Шредінгера. Принцип причинності в квантовій механіці
- •§119. Рух вільної частинки. Частинка в прямокутній потенціальній ямі. Тунельний ефект
- •1. Рух вільної частинки
- •2. Частинка в одномірній прямокутній потенціальній ямі
- •3. Тунельний ефект
- •§120. Атом водню у квантовій механіці
- •1S; 2s2p; 3s3p3d; 4s4p4d4f; ….
- •Храпливий зіновій
- •Кордиш леон йосипович
- •Міліянчук василь степанович
- •§121. Дослід Штерна і Герлаха. Спін електрона
- •§122. Принцип Паулі. Розподіл електронів в атомі за станами
- •§123. Рентгенівські промені
- •Пулюй іван
- •Кордиш леон йосипович
- •Лисиця михайло павлович
- •Давидов олександр сергійович
- •§125. Поглинання, спонтанне і вимушене випромінювання
- •§126. Оптичні квантові генератори
- •Бродин михайло семенович
- •Конділенко іван іванович
- •Лубченко андрій федорович
- •Стасюк ігор васильович
3. Тунельний ефект
Нехай частинка, яка рухається в додатному напрямку осі ОХзустрічає на своєму шляху прямокутний потенціальний бар’єр висотоюU і шириноюl(рис. 297). Отже величинаU вздовж осіОХзмінюється так:


При даних умовах задачі класична
частинка, маючи енергію Е, або пройде
над бар’єром при![]() ,
або відіб’ється від нього при
,
або відіб’ється від нього при![]() і буде рухатися в зворотний бік.
і буде рухатися в зворотний бік.
Для частинки навіть при
![]() є відмінна від нуля ймовірність того,
що
частинка відіб’ється від бар’єра
і буде рухатися у зворотний бік. При
є відмінна від нуля ймовірність того,
що
частинка відіб’ється від бар’єра
і буде рухатися у зворотний бік. При![]() є також відмінна від нуля ймовірність
того, що частинка проникне через бар’єр
і виявиться в області
є також відмінна від нуля ймовірність
того, що частинка проникне через бар’єр
і виявиться в області![]() .
.
Рівняння Шредінгера для кожної з виділених областей має вигляд:
1
і 3: ![]() ;
;![]() ,
,
2: ![]() ;
;![]() .
.
Загальні розв’язки цих диференціальних рівнянь:
![]() ,
,
![]() ,
,
![]() .
.
В області 3є лише хвиля, що пройшла
через бар’єр і поширюється зліва
направо. Тому коефіцієнт![]() .
.
При E<U
в області2q
– уявне число, тобто![]() ,
де
,
де![]() .
.
У результаті
![]() ,
,
![]() ,
,
![]() .
.
Отже, хвильова функція не дорівнює нулю і всередині бар’єра, а в області 3буде мати вигляд хвиль де Бройля з тим самим імпульсом, але меншою амплітудою.
Якісний вигляд функції
![]() ,
,![]() і
і![]() наведений на рис. 298.
наведений на рис. 298.

Таким чином, квантова механіка приводить до принципово нового явища, яке називається тунельним ефектом, в результаті якого частинка може пройти через потенціальний бар’єр.
Знайдемо ймовірність проходження мікрочастинки крізь потенціальний бар’єр, або коефіцієнт пропускання. Цей коефіцієнт також називаютькоефіцієнтом прозорості бар’єра.Він дорівнює відношенню інтенсивності хвилі, що проходить через бар’єр, до інтенсивності хвилі, що падає на межу поділу областей1і2. Оскільки інтенсивність хвилі пропорційна до квадрату амплітуди коливань, то коефіцієнт прозорості бар’єра
![]() .
.
Для того, щоб знайти це відношення,
необхідно використати умови неперервності
функції
![]() у всій області змінхвід
у всій області змінхвід![]() до
до![]() ,
тобто
,
тобто
![]() ,
,
![]() .
.
Для того, щоб функція
![]() була гладкою, повинні виконуватися
умови
була гладкою, повинні виконуватися
умови
![]() ,
, ![]() .
.
Ці
умови дають змогу виразити коефіцієнти
![]() через
через![]() .
В результаті
.
В результаті
![]()
де
 .
.
Для потенціального бар’єра довільної форми:
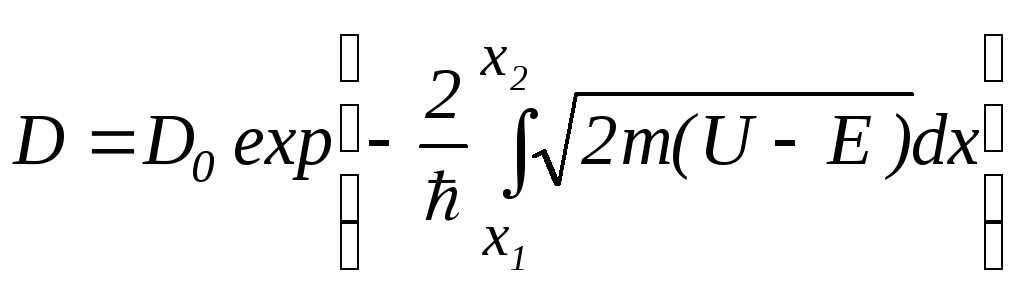 ,
,
де
![]() .
.
Із виразів для Dвидно,
що коефіцієнт прозорості залежить від
маси мікрочастинки, ширини бар’єра
і від різниці![]() .
.
Тунельний ефект є специфічним квантовим
ефектом. Проходження мікрочастинки
крізь область, в яку, згідно із законами
класичної механіки, вона не може
проникнути, можна пояснити співвідношенням
невизначеностей. Невизначеність
імпульсу
![]() на відрізку
на відрізку![]() дорівнює
дорівнює![]() .
Зв’язана з цим розкидом в значеннях
імпульсу кінетична енергія
.
Зв’язана з цим розкидом в значеннях
імпульсу кінетична енергія![]() може виявитися достатньою для того,
щоб повна енергія мікрочастинки
виявилася більшою за потенціальну.
може виявитися достатньою для того,
щоб повна енергія мікрочастинки
виявилася більшою за потенціальну.
Проходження частинок через потенціальний
бар’єр експериментально підтверджено
в явищі холодної емісії електронів
з металу. Тунельний ефект відіграє
основну роль у явищах радіоактивного
![]() - розпаду, перебігу термоядерних реакцій.
- розпаду, перебігу термоядерних реакцій.
§120. Атом водню у квантовій механіці
Розглянемо воднеподібні атоми, які
складаються з нерухомого ядра із зарядом
Zeі електрона, який
рухається навколо нього. ПриZ=1це буде атом водню,Z=2іон гелію![]() ,Z=3двохкратно
іонізований атом літію
,Z=3двохкратно
іонізований атом літію![]() та ін. Заряд ядра можна вважати точковим,
а його електричне поле – сферично-симетричним.
та ін. Заряд ядра можна вважати точковим,
а його електричне поле – сферично-симетричним.
Потенціальна енергія взаємодії електрона з ядром
![]() ,
,
де r– відносна відстань між електроном і ядром.
Графічно функція
![]() зображена на рис. 299.
зображена на рис. 299.
Стан електрона в атомі водню описується
хвильовою функцією
![]() ,
яка є розв’язком стаціонарного
рівняння Шредінгера
,
яка є розв’язком стаціонарного
рівняння Шредінгера

![]() ,
,
де
Е– повна енергія електрона в атомі,
аm– маса електрона.
Оскільки поле, в якому рухається
електрон, є сферично-симетричним,
то для розв’язання рівняння Шредінгера
використовують сферичну систему
координат:![]() .
Підставляючи в рівняння Шредінгера
оператор Лапласа в сферичних
координатах, прийдемо до рівняння:
.
Підставляючи в рівняння Шредінгера
оператор Лапласа в сферичних
координатах, прийдемо до рівняння:
![]()
![]() .
.
Функцію
![]() можна зобразити добутком трьох функцій,
кожна з яких залежить від однієї змінної:
можна зобразити добутком трьох функцій,
кожна з яких залежить від однієї змінної:
![]() .
.
Не вдаючись до математичного розв’язання цієї задачі, обмежимось розглядом важливих результатів, які з нього отримують, пояснивши їх основний зміст.
Для
![]() рівняння Шредінгера має розв’язки, що
задовольняють вимоги однозначності,
скінченності і неперервності хвильової
функції
рівняння Шредінгера має розв’язки, що
задовольняють вимоги однозначності,
скінченності і неперервності хвильової
функції![]() лише при власних значеннях енергії
лише при власних значеннях енергії
![]()
![]() ,
,
де R– стала Рідберга,n – головне квантове число.
Розв’язок рівняння Шредінгера для
атома водню приводить до появи дискретних
енергетичних рівнів. Нижній рівень
![]() ,
що відповідає мінімально можливій
енергії – основний, всі інші
,
що відповідає мінімально можливій
енергії – основний, всі інші![]() збуджені. При
збуджені. При![]() рух електрона є зв’язаним – він
знаходиться всередині гіперболічної
„потенціальної ями”. У міру зростання
головного квантового числаnенергетичні рівні розміщуються тісніше
і при
рух електрона є зв’язаним – він
знаходиться всередині гіперболічної
„потенціальної ями”. У міру зростання
головного квантового числаnенергетичні рівні розміщуються тісніше
і при![]()
![]() .
При
.
При![]() рух електрона є вільний – він може
покинути межі атома.
Енергія іонізації
атома водню дорівнює:
рух електрона є вільний – він може
покинути межі атома.
Енергія іонізації
атома водню дорівнює:
![]() .
.
У квантовій механіці дискретні значення енергій є наслідком самої теорії, вони випливають безпосередньо з розв’язків рівняння Шредінгера.
Рівняння Шредінгера задовольняють
власні функції
![]() ,
що визначаються трьома квантовими
числами: головнимn, орбітальнимlі магнітним
,
що визначаються трьома квантовими
числами: головнимn, орбітальнимlі магнітним![]() .
.
Головне квантове число n визначає енергетичні рівні електрона в атомі
Воно може набувати довільних цілочислових значень, починаючи з одиниці: n=1, 2, 3,...
З розв’язків рівняння Шредінгера
випливає, що момент імпульсу (механічний
орбітальний момент) електрона квантується,
тобто не може бути довільним, а набуває
дискретних значень, які обчислюють за
формулою
розв’язків рівняння Шредінгера
випливає, що момент імпульсу (механічний
орбітальний момент) електрона квантується,
тобто не може бути довільним, а набуває
дискретних значень, які обчислюють за
формулою
![]() ,
,
де l – орбітальне квантове число, що визначає величину модуля вектора моменту імпульсу електрона в атомі
При заданому nнабуває значення![]() ,
тобто разомnзначень.
,
тобто разомnзначень.
З розв’язків рівняння Шредінгера
виходить також, що вектор
![]() моменту імпульсу електрона може мати
лише таку орієнтацію в просторі, при
якій проекція
моменту імпульсу електрона може мати
лише таку орієнтацію в просторі, при
якій проекція![]() на довільний напрямокОZнабуває
квантових значень, кратних
на довільний напрямокОZнабуває
квантових значень, кратних![]() :
:
![]() ,
,
де
![]() -магнітне квантове число, яке
визначає проекцію моменту імпульсу
електрона на заданий напрямок OZ.
-магнітне квантове число, яке
визначає проекцію моменту імпульсу
електрона на заданий напрямок OZ.
Магнітне квантоване число при заданому
l може набувати значення![]() тобто разом
тобто разом![]() значень. Фізичний сенс обмеження
значень. Фізичний сенс обмеження![]() за величиною полягає в тому, що проекція
вектора моменту не може бути більшою
за довжину самого вектора.
за величиною полягає в тому, що проекція
вектора моменту не може бути більшою
за довжину самого вектора.
На рис. 300 наведені можливі орієнтації
векторів
![]() для електронів у випадку
для електронів у випадку![]() і
і![]() .
.

Коли проекція
![]() має деяке значення,то
на основі співвідношення невизначеності
інших проекцій
має деяке значення,то
на основі співвідношення невизначеності
інших проекцій![]() та
та![]() будуть повністю невизначеними. Отже,
вектор моменту імпульсу можна зобразити
у вигляді вектора довжиною
будуть повністю невизначеними. Отже,
вектор моменту імпульсу можна зобразити
у вигляді вектора довжиною![]() ,
який прецесує навколо осіОZі
зберігає свою проекцію на вісьОZ(рис. 301).
,
який прецесує навколо осіОZі
зберігає свою проекцію на вісьОZ(рис. 301).
В магнітному полі рівень з головним
квантовим числом nвнаслідок
наявності квантового числа![]() розщеплюється на
розщеплюється на![]() підрівнів. Відповідно у спектрі атома
повинно спостерігатися розщеплення
спектральних ліній. Розщеплення
енергетичних рівнів в магнітному полі
було виявлено Т. Зееманом
і називаєтьсяефектом Зеемана.
Розщеплення рівнів енергій у зовнішньому
електричному полі називаєтьсяефектом
Штарка.
підрівнів. Відповідно у спектрі атома
повинно спостерігатися розщеплення
спектральних ліній. Розщеплення
енергетичних рівнів в магнітному полі
було виявлено Т. Зееманом
і називаєтьсяефектом Зеемана.
Розщеплення рівнів енергій у зовнішньому
електричному полі називаєтьсяефектом
Штарка.
Хоча енергія електрона і залежить від
головного квантового числа n, але
кожному значенню![]() (при
(при![]() )
відповідає декілька власних функцій
)
відповідає декілька власних функцій![]() ,
що відрізняються значеннямиli
,
що відрізняються значеннямиli![]() .
Отже, атом водню може мати одне і те ж
значення енергії, перебуваючи в декількох
різних станах. Оскільки при даномуnорбітальне квантове числоlможе
змінюватись від0до
.
Отже, атом водню може мати одне і те ж
значення енергії, перебуваючи в декількох
різних станах. Оскільки при даномуnорбітальне квантове числоlможе
змінюватись від0до![]() ,
а кожному значеннюlвідповідає
,
а кожному значеннюlвідповідає![]() різних значень
різних значень![]() ,
то число різних станів, що відповідають
даномуn, дорівнює
,
то число різних станів, що відповідають
даномуn, дорівнює
![]() .
.
Стани з однаковою енергією називаються
виродженими, а кількість станів
з певним значенням енергії називаютькратністю виродження ![]() відповідного енергетичного рівня.
відповідного енергетичного рівня.
Якщо рух електрона має сферичну симетрію,
то його розподіл у просторі залежить
лише від радіальної складової
![]() хвильової функції
хвильової функції![]() .
Ймовірність
.
Ймовірність![]() виявлення електрона в сферичному шарі
товщиноюdrна відстаніrвід ядра дорівнює
об’єму цього шару
виявлення електрона в сферичному шарі
товщиноюdrна відстаніrвід ядра дорівнює
об’єму цього шару![]() на квадрат модуля
на квадрат модуля![]() :
:
![]() .
.
Отже, лінійна густина ймовірності
![]() виявлення електрона на відстаніrвід ядра атома дорівнює
виявлення електрона на відстаніrвід ядра атома дорівнює
![]() .
.
На рис. 302 зображено залежність
![]() від радіусаrдля
перших трьох станів електрона в атомі
водню.
від радіусаrдля
перших трьох станів електрона в атомі
водню.

Густина ймовірності
![]() для основного стану атома
для основного стану атома![]() спочатку дорівнює нулю, а потім
зростає до максимуму і далі експоненціально
зменшується.
спочатку дорівнює нулю, а потім
зростає до максимуму і далі експоненціально
зменшується.
Отже, густина ймовірності виявлення електрона в різних частинах атома різна. Електрон при своєму русі ніби „розмазаний” по всьому об’єму, створюючи електронну хмару, густина якої характеризує ймовірність знаходження електрона в різних точках об’єму атома.
Квантові числа n i l характеризують
розмір і форму електронної хмари, а
квантове число
![]() характеризує орієнтацію електронної
хмари в просторі(рис. 303).
характеризує орієнтацію електронної
хмари в просторі(рис. 303).

Стан електрона, що характеризується
квантовим числом
![]() ,
називаєтьсяs-станом (електрон в
цьому стані називаєтьсяs-електроном),
,
називаєтьсяs-станом (електрон в
цьому стані називаєтьсяs-електроном),![]() –p-станом;
–p-станом;![]() –d-станом;
–d-станом;![]() –f-станом і так далі.
–f-станом і так далі.
Значення головного квантового числа вказується перед умовним позначенням орбітального квантового числа:
