
- •Енергозберігаючі технології
- •4. Основні термодинамічні процеси в ідеальних газах та їх аналіз
- •4.1. Ізохорний процес
- •За рівнянням першого закону термодинаміки
- •4.2. Ізобарний процес
- •4.3. Ізотермічний процес
- •4.4. Адіабатний (ізоентропійний) процес
- •4.5. Політропний процес
- •5. Процеси течіння газів та рідин
- •5.1. Рівняння I-го закону термодинаміки для потоку робочого тіла (відкрита система)
- •Запишемо рівняння (5.8) у вигляді
- •5.2. Витікання газів та пари із сопел, які звужуються.
- •5.2.1. Швидкість руху потоку робочого тіла
- •Рівнянням:
- •5.2.2. Швидкість звуку
- •5.2.3. Перехід через швидкість звуку. Сопло Лаваля
- •5.3. Дроселювання газів і парів. Ефект Джоуля –Томсона
- •6. Процеси стиснення газу в компресорі
- •7. Способи охолодження робочого тіла.
- •7.1. Ізоентальпійне розширення робочого тіла (дроселювання)
- •7.2. Адіабатне розширення робочого тіла з віддачею зовнішньої роботи (детандування)
- •7.3. Аналіз ідеальних процесів розширення робочого тіла в детандерах
- •Література
- •Навчальне видання
- •Енергозберігаючі технології
5.3. Дроселювання газів і парів. Ефект Джоуля –Томсона
Під процесом дроселювання (м’яття) газу чи пари розуміють необоротний процес зміни стану, обумовлений місцевими опорами.
З практики відомо, що якщо в трубопроводі, яким протікає рідина чи газ, поставити заслінку, вентиль, кран чи діафрагму, то це призведе до різкого звуження поперечного перерізу потоку. В процесі проходження такого січення швидкість робочого тіла збільшується, а тиск продовжує падати. За звуженням швидкість зменшується і досягає початкового значення, яке вона мала перед звуженням. Що стосується тиску, то він не досягає значення, яке він мав до звуження. Це обумовлене втратами частини енергії на завихрення і тертя у вузькому січенні (рис. 5.5). Ці втрати перетворюються в теплоту, яка передається робочому тілу (газу чи рідині).
Таким чином, дроселювання - це процес пониження тиску в потоці без здійснення зовнішньої роботи та без підведення і відведення теплоти в процесі проходження потоку через місцевий опір. Цей процес є типовим необоротним, а тому завжди пов’язаний зі збільшенням ентропії.
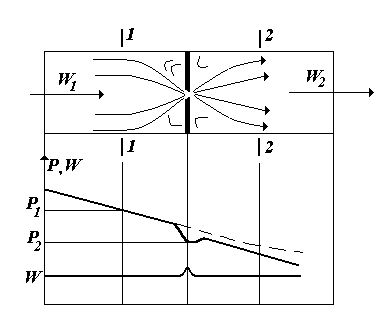
Рис. 4.10. Схема дроселювання та зміни тиску і швидкості вздовж каналу
В процесі протікання газу через діафрагму (перегородку) можна використати рівняння (5.15), яке справедливе як для оборотного, так і для необоротного адіабатного процесу. Тому згідно рівняння (5.15) маємо
![]()
Оскільки перетини I-I і 2-2 однакові, то можна прийняти що W1= W2. Тому масові витрати в перетинах I-I і 2-2 теж будуть однаковими. В зв’язку із сказаним можна прийняти, що процес дроселювання буде здійснюватись за умови незмінної ентальпії.
![]() .
(5.33)
.
(5.33)
На відміну від реального газу, в процесі дроселювання ідеального газу повинна зберігатись рівність
![]() .
(5.34)
.
(5.34)
Тому процес дроселювання ідеального газу буде здійснюватись за умови постійної температури робочого тіла як до діафрагми так і після неї. Що стосується реальних газів, то їх поведінка суттєво відрізняється від поведінки ідеальних газів. В процесі дроселювання реального газу його температура може залишатись незмінною (dT = 0); зменшуватись (dT 0) і збільшуватись (dT 0). Оскільки в процесі дроселювання у всіх випадках dp 0 (дивись рис. 5.5) то в загальному
![]() .
(5.35)
.
(5.35)
В рівнянні (5.35) значення dT залежить від - так званого коефіцієнта адіабатного дроселювання, або диференційного дросель-ефекту. Явище зміни температури в процесі адіабатного дроселювання називають ефектом Джоуля -Томсона.
Для одержання рівняння, яке б визначало умови зміни температури в процесі адіабатного дроселювання, використаємо перший закон термодинаміки. Згідно рівнянь (4.15) і (4.16) перший закон термодинаміки можна записати у вигляді
![]() .
(5.36)
.
(5.36)
Оскільки ентальпія є функцією стану, її можна представити у виді залежності від двох параметрів, наприклад, р і Т:
![]() .
(5.37)
.
(5.37)
Підставимо значення ентальпії (5.36) у (5.37) одержимо:
![]() .
(5.38)
.
(5.38)
Звідки
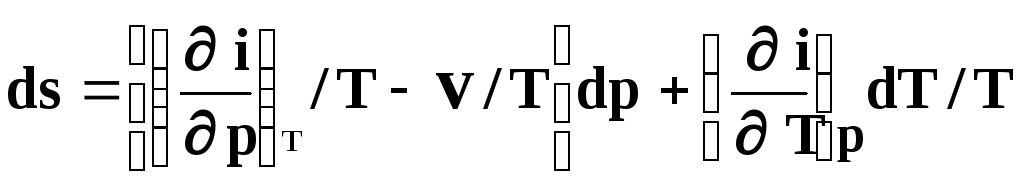 .
(5.39)
.
(5.39)
Оскільки ds як і di є повним диференціалом, то
![]() .
(5.40)
.
(5.40)
Диференціювання рівняння (5.40) дає
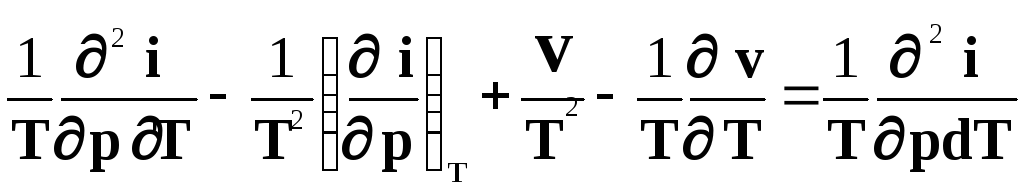 .
.
Після скорочень одержимо:
![]() (5.41)
(5.41)
З
рівняння (4.22) маємо
![]() .
Підставивши цей вираз, а також значення
.
Підставивши цей вираз, а також значення![]() з рівняння (5.41) у рівняння (5.37) одержимо:
з рівняння (5.41) у рівняння (5.37) одержимо:
![]() .
(5.42)
.
(5.42)
Оскільки в процесі дроселювання di = 0, тобто i1 = i2 = const, то
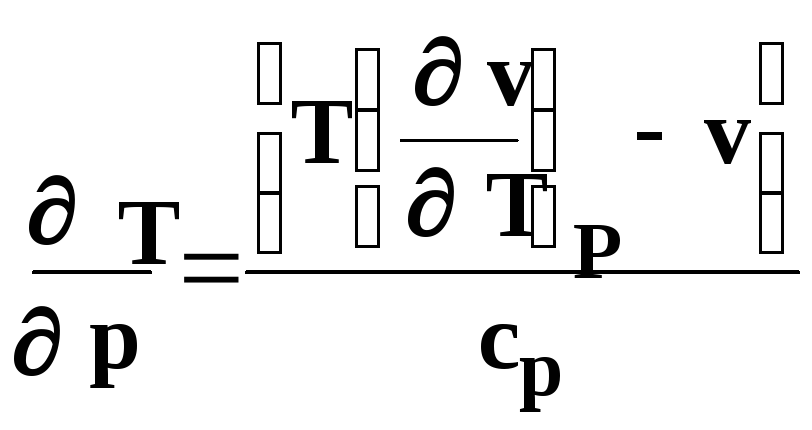 .
(5.43)
.
(5.43)
Одержане рівняння характеризує зміну температури робочого тіла в залежності від зміни тиску в процесі дроселювання. Який же знак має адіабатний дросель-ефект? Для цього проаналізуємо рівняння (5.43). В процесі дроселювання, як було сказано вище, dp 0. Оскільки ср 0, знак коефіцієнта адіабатного дроселювання
![]() (5.44)
(5.44)
визначиться
знаком правої частини чисельника в
рівнянні (5.43), тобто величиною
![]() .
Виходячи з цього виразу випливає, що
якщо
.
Виходячи з цього виразу випливає, що
якщо
![]() ,
(5.45)
,
(5.45)
то
![]()
![]() .
(5.46)
.
(5.46)
і тоді в процесі адіабатного дроселювання температура дросельованого газу підвищується (dT 0).
Якщо ж
![]() ,
(5.47)
,
(5.47)
то
![]() (5.48)
(5.48)
і тоді в процесі адіабатного дроселювання температура газу понижується (dT 0).
І нарешті, якщо
![]() ,
(5.49)
,
(5.49)
то
![]() ,
(5.50)
,
(5.50)
тобто в процесі адіабатного дроселювання температура залишається незмінною.
Оскільки
для ідеального газу
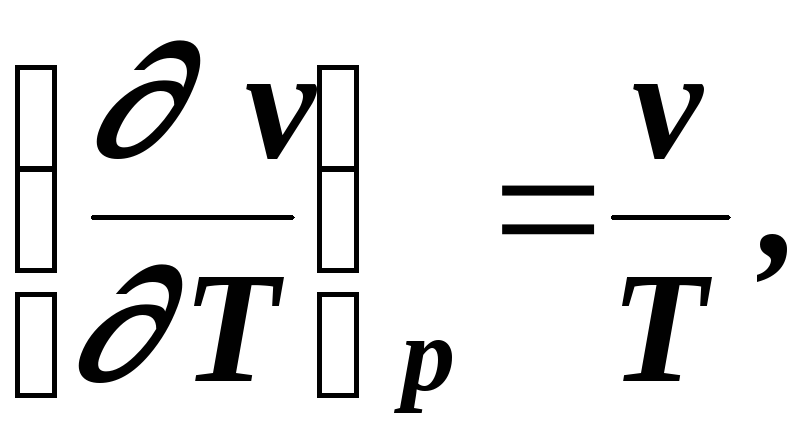 то як було сказано вище (5.34), ідеальний
газ дроселюється за умови незмінної
температури.
то як було сказано вище (5.34), ідеальний
газ дроселюється за умови незмінної
температури.
Таким чином, ефект Джоуля -Томсона має місце тільки для реальних газів і рідин.
Якщо процес адіабатного дроселювання здійснюється за умови значного перепаду тиску на дроселі, то зміну температури називають інтегральним дросель-ефектом, який можна визначити за рівнянням
![]() ,
(5.51)
,
(5.51)
де T1 і T2 - температура газу до і після дроселя.
Зауважимо, що інтегральний дросель-ефект може досягати досить великих значень. Так для водяної пари в процесі дроселювання від тиску р1 = 300 ат і Т1=723 К до тиску р2 = 1 ат, температура пари знизиться до 453 К.
Інтегральний дросельний ефект зручно визначити за допомогою i-T діаграми (рис. 5.6). Якщо відомий стан газу перед дроселем (р1 і Т1) і відомий тиск за дроселем (р2), то за параметрами р1 і Т1 знайдемо на діаграмі i-T точку 1. З точки 1 проведемо ізоентальпу i1 = const до перетину з ізобарою р2 = const знайдемо температуру Т2 за дроселем. Як показали досліди, для однієї і тієї ж речовини знак дросель-ефекта може бути різним в залежності від стану, в якому знаходиться газ в процесі дроселювання. Стан газу, в якому дросель-ефект дорівнює нулю, називають точкою інверсії, а температуру, яка відповідає цьому стану, називають температурою інверсії.
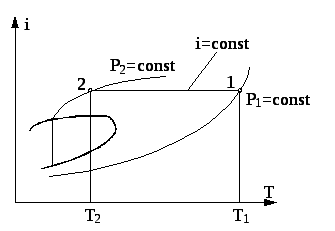
Рис. 5.6. Діаграма і-Т
Геометричне місце точок інверсії на діаграмі стану даної речовини, називають кривою інверсії.
Н
Рис.
5.7. Інверсійна крива для азоту
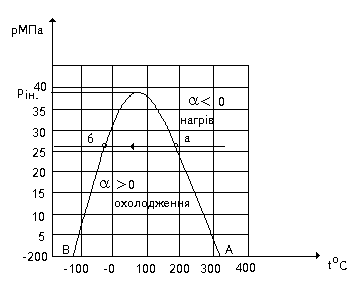
Рис. 5.7. Інверсійна крива для азоту
За цією областю i 0, тобто газ в процесі дроселювання буде нагріватись. Як випливає з рис. 5.7, ізобари р рін двічі перетинають криву інверсії (точка а і б). Переміщаючись по ізобарі в області високих температур ми з області, де i 0 (нагрівання газу в процесі дроселювання), попадаємо в область i 0 (охолодження газу в процесі дроселювання), а потім в області невисоких температур ми знову попадаємо в область, в якій i 0 і в якій газ буде нагріватись в процесі дроселювання.
Для тисків рін р для будь-якої температури газ в процесі дроселювання буде нагріватись (i 0). Точку максимуму на кривій інверсії називають критичною точкою інверсії. Для реального газу параметри критичної точки інверсії мають такі значення
рін = 9ркр; Тін = 3Ткр.; vін = vкр. (5.52)
Процес адіабатного дроселювання знаходить широке застосування як ефективний метод охолодження газів, який буде розглянутий пізніше.
Зауважимо, що процес дроселювання, як було сказано, є необоротним, тому відображення цього процесу на T-s діаграмі чи i-s діаграмі є умовним.
