
Подготовка у универсиаде 2012 / Генетика (Жимулев) / 17ver7
.pdf
Основы онкогенетики |
|
|
|
|
|
|
|
Глава 17 |
||||
Глава 17. Основы |
|
|
|
Рисунок 17.1 |
|
|
|
|
|
|||
онкогенетики |
|
|
|
|
|
|
|
|
|
|||
По статистике в мире ежегодно |
|
|
|
|
|
|
||||||
выявляют более 6 млн. случаев заболеваний |
|
|
|
|
|
|
||||||
раком шести основных органов (легких, |
|
|
|
|
|
|
||||||
желудка, молочной железы, прямой кишки, |
|
|
|
|
|
|
||||||
шейки матки и простаты). Около половины |
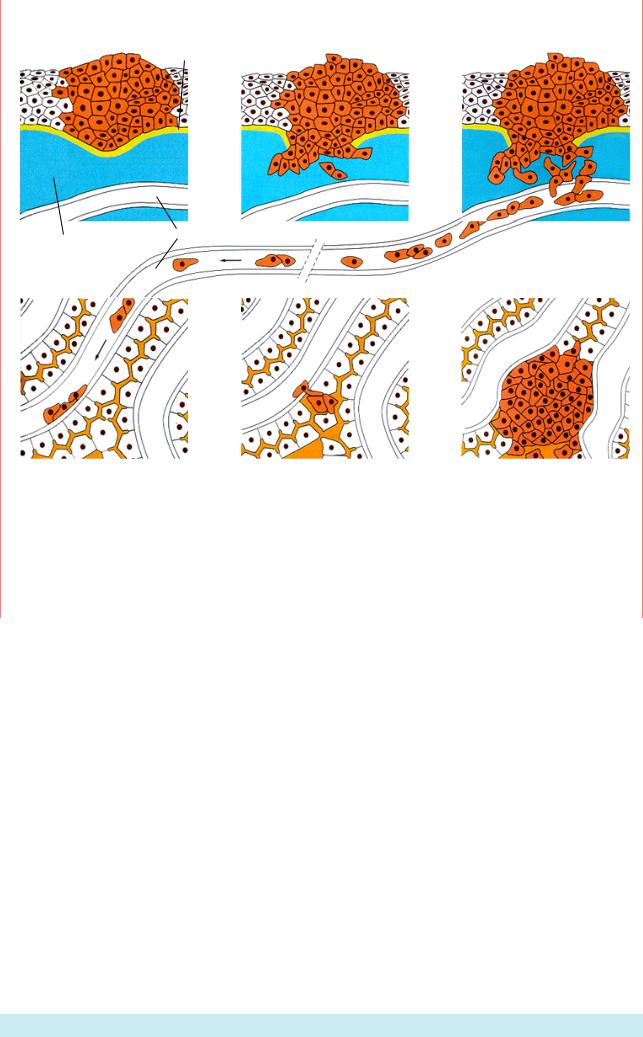
Два опухолевых клона среди клеток |
|||||||||||
заболевших погибает. В конечном счете |
нормального эпителия. Нормальные клетки |
|||||||||||
каждый пятый житель развитых стран |
светлокоричневые. |
Клетки |
клона, |
|||||||||
умирает от онкологических заболеваний (от |
образующего доброкачественную опухоль- |
|||||||||||
“онкос” - греч. - опухоль). Это само по себе |
полип (темно-коричневый цвет), дают |
|||||||||||
избыточный |
прирост |
è |
образуют |
|||||||||
говорит об исключительной важности |
||||||||||||
выпячивание над поверхностью слоя клеток, |
||||||||||||
онкологических исследований даже в чисто |
||||||||||||
но не проникают в соединительную ткань |
||||||||||||
прикладныхцелях.Исследованияизменений |
||||||||||||
под эпителием. Клетки злокачественного |
||||||||||||
в функционировании клеток, возникающих |
||||||||||||
(ракового) клона (показаны красным цветом) |
||||||||||||
при злокачественном перерождении, имеют |
||||||||||||
проникают (инвазия) |
|
под базальную |
||||||||||
|
|
|
|
|
|
|
||||||
фундаментальное теоретическое значение. |
|
мембрану в соединительную ткань (Из: |
||||||||||
17.1. Трансформация клеток |
|
Васильев: 1997б). |
|
|
|
|
||||||
|
Хирургическое |
|
|
удаление |
||||||||
и процесс опухолеобразования |
|
|
||||||||||
доброкачественной опухоли вместе с |
||||||||||||
Числоклетоквкаждойткани,такжекак |
молодыми клетками, пополняющими ее, как |
|||||||||||
и объем ткани, занимаемый ею в теле, более |
правило, прекращает существование этой |
|||||||||||
или менее постоянны. Естественная убыль |
опухоли и она более не возобновляется. |
|||||||||||
клеток пополняется из отделов ткани, |
Главным признаком злокачественной |
|||||||||||
содержащих низкоспециализированные |
опухоли является ее выход за пределы |
|||||||||||
делящиеся клетки (камбий). Темп |
территории, предназначенной для данной |
|||||||||||
восполнения |
утраченных |
клеток |
ткани. Если опухоль врастает в подлежащую |
|||||||||
контролируетсяэкзогеннымииэндогенными |
ткань, происходит инвазия (внедрение) |
|||||||||||
ростовыми и ингибирующими факторами, |
опухолевыхклеток.Инвазия-первыйпризнак |
|||||||||||
выработка которых каким-то образом |
злокачественной опухоли. Если опухолевые |
|||||||||||
определяется потребностями данной ткани в |
клетки отрываются от основного очага, |
|||||||||||
пополнении. Если баланс убыль-пополнение |
разносятсялимфойиликровьюпоорганизму, |
|||||||||||
покаким-либопричинамнарушаетсявпользу |
оседают в других, отдаленных органах (чаще |
|||||||||||
пополнения, возникает избыточная масса |
всего в лимфатических узлах, печени, |
|||||||||||
клеток и в месте нарушения баланса |
легких), и образуют там вторичные очаги |
|||||||||||
образуется гиперплазия (гиперпластическое |
опухолевого |
роста, |
говорят |
î |
||||||||
разрастание) ткани. Она может возникнуть, |
метастазировании, т.е. распространении |
|||||||||||
может длительное время увеличиваться, а |
опухолевого процесса по всему организму |
|||||||||||
может и постепенно исчезнуть. Гиперплазии |
(Ðèñ. 17.2). |
|
|
|
|
|
||||||
могут |
превратиться |
сначала |
â |
Особенно опасны микрометастазы - |
||||||||
доброкачественные, а затем и в |
мельчайшие очажки опухолевого роста, |
|||||||||||
злокачественные |
|
опухоли. |
которые зачастую нельзя ни увидеть, ни |
|||||||||
Доброкачественной опухоль называется, |
удалить хирургически. Когда опухоль |
|||||||||||
если она растет очень медленно и не выходит |
становится |
обнаружимой, |
îíà |
óæå |
||||||||
за пределы своей ткани, т.е. и не внедряется |
достаточно велика и содержит сотни |
|||||||||||
в подлежащие или соседние ткани - не |
миллионов клеток: при числе клеток в |
|||||||||||
инвазирует и не метастазирует (Рис. 17.1). |
|
опухоли 10& она становится видимой в ходе |
||||||||||
387
Глава 17 |
|
Основы онкогенетики |
|
|
|
|
|
|
Рисунок 17.2 |
|
|
|
Базальная |
|
à |
пластина á |
â |
ã
Капилляр
Соединительная
ткань
ä |
å |
æ |
Схема метастазирования опухоли. а - доброкачественная опухоль в эпителии (например, легких). Опухолевые клетки не пересекают базальную пластину (ламину), отделяющую эпителий от соединительной ткани; б - разрыв базальной пластинки и инвазия опухолевых клеток в соединительную ткань; в - попадание опухолевых клеток в кровеносный капилляр; г - миграция клеток по кровеносным сосудам (выживает и образует метастазы менее одной клетки из каждой тысячи опухолевых клеток); д - выжившие клетки прилипают к стенке кровеносного сосуда (например, печени); е,ж - переход опухолевой клетки из сосуда в ткань органа и образование метастаза (Из: Alberts et al., 1994, p. 1269).
рентгеновского обследования, при числе 10' |
соседствующиетканивлияютдругнадругаи |
|
- она пальпируется. Смерть пациента |
взаимноникогданевыходятзаграницысвоих |
|
наступает,когдаопухольсостоитпримерноиз |
территорий. Злокачественные опухоли не |
|
10 клетокионанарушаетжизненноважные |
чувствуют этих влияний. Они инвазируют на |
|
функцииорганов. |
чужиетерриториииспособнырастивчуждом |
|
Клетки практически любой опухоли |
окружении.Способностькметастазированию |
|
можно пересадить другому генетически |
- это не столько способность к отрыву и |
|
сходному(сингенному)животномуиполучить |
распространению,сколькоименно к ростуна |
|
перевиваемую опухоль, которая будет |
чужих территориях и в чуждом |
|
неограниченнорастистолько,сколькоеебудут |
микроокружении. |
|
перевивать. |
Само существование |
Следующим неотъемлемым свойством |
перевиваемых опухолей говорит о том, что |
злокачественной опухоли является |
|
опухоль развиваетсяавтономно, что причина |
бессмертие ее клеток. Нормальные клетки |
|
ее роста в ней самой, так как перенос в |
смертны, их жизненный цикл включает |
|
нормальный организм здорового животного |
запрограмированнуюсмерть-апоптоз.Будучи |
|
не останавливает ее роста. |
высаженными в культуру, они погибают, |
|
Автономность опухоли проявляется |
пройдя определенное число циклов деления. |
|
также в независимости от окружающих |
Клетки опухоли не знают предела для |
|
тканей. В |
нормальном развитии |
размножения ни в организме, ни вне его. |
388

Основы онкогенетики |
Глава 17 |
|
|
Очень важным и обязательным признаком злокачественной опухоли является ее моноклональность. Злокачественная опухоль развивается из одной генетически измененной клетки. В этом смысле она представляет собой клон, т.е. потомство генетически однородных клеток, возникших из одной клетки. Одно из доказательств моноклональности получено в результате анализа ДНК. Почти у всех пациентов, страдающих от хронической миелогенной лейкемии, лейкемические белые кровяные клетки отличаются от нормальных клеток специфической хромосомной перестройкой, так называемой Филадельфийской хромосомой - транслокацией между длинными плечами хромосом 9 и 22 (см. Рис. 17.6). Когда была клонирована и секвенирована ДНК в участке транслокации, обнаружили, что участок разрыва и объединения транслоцированных фрагментов идентичен во всех лейкемических клетках каждого больного индивидуума, но больные между собой несколько отличаются в том смысле, что точки разрыва-воссоединения ДНК хромосом могут различаться на несколько сот или тысяч пар нуклеотидов.
Âдальнейшем, в череде генераций в опухоли возникают мутации, которые порождают новые, вторичные клоны, создающие генетическую разнородность внутри опухоли, но это уже вторичная разнородность (см. ниже).
Âпроцессе прогрессии опухоли и селекции клеток, у последних постепенно исчезают признаки исходной ткани, т.к. они зачастую являются мишенью для контроля опухоли со стороны организма или соседних тканей. Однако признаки ткани, из которой развилась опухоль, до конца все же никогда не исчезают полностью. Это важная особенность опухоли, позволяющая точно определить, в каком органе и из каких клеток она возникла и к какому лечению вероятнее
всего будет чувствительна.
17.2. Причины возникновения опухолей
Хорошо известны несколько типов воздействий, с помощью которых можно индуцировать опухоли. Это канцерогенные вещества, опухолеродные вирусы, рентгеновское и ультрафиолетовое облучение. Однако, значительная, если не основная часть опухолей возникает спонтанно, т.е. без видимой связи с индуцирующимиагентами.
1.Канцерогенные вещества весьма разнообразны - от таких простых, как
четыреххлористый углерод (CCl") до весьма сложных, таких как метихолантрен или бензантрацен. Чаще всего они дают сходные биологические эффекты - вызывают мутации, стимулирующие размножение клеток-предшественниц опухоли.
К канцерогенным веществам примыкают вещества, способствующие росту и делению возникших одиночных опухолевых клеток - это так называемые промоторы канцерогенеза. Эти вещества являются чрезвычайно важным компонентом химического канцерогенеза, т.к. одиночные опухолевые клетки, находясь
âокружениинормальнойткани,какправило, не в состоянии преодолеть ее сдерживающего влияния и годами способны сохраняться в латентном состоянии, не проявляясь в виде опухоли. Промоторы снимают это влияние, что внешне выглядит как сильный канцерогенный эффект.
Канцерогенные вещества (включая промоторы) являются причиной многих опухолей человека, например, каменноугольный деготь и содержащийся в нем форболовый эфир (промотор канцерогенеза) вызывает так называемый “рак трубочистов”, анилин вызывает у работников красильного производства рак мочевого пузыря, курение - рак легких.
2.Опухолеродные вирусы. Это могут быть ДНК-содержащие вирусы или РНКсодержащие ретровирусы. Все они обладают уникальной способностью к интеграции с геномом клетки-хозяина. Эта удивительная
389

Глава 17 Основы онкогенетики
особенность опухолевых вирусов была |
|
Дополнение 17.1 |
|
|
|
предсказана российским вирусологом Л.А. |
|
Пейтон Раус (Peyton Rous) получил |
|||
Зильбером. |
|
Нобелевскую премию 1966 года за открытие |
|||
Первый опухолеродный вирус был |
|
онкогенных вирусов. |
|
|
|
открытв1910годуП.Раусомукур.Инъекции |
специфическиххромосомныхтранслокацийв |
||||
бесклеточного фильтрата из саркомы |
клеткахопухоли. |
|
|
||
вызывали новые опухоли. Инфицирующим |
|
2. Стабильность злокачественных |
|||
агентом (вирус саркомы Рауса) является |
свойств в трансформированных клетках и их |
||||
РНК-содержащий ретровирус, т.е. вирус, на |
передача из одного клеточного поколения в |
||||
наследственной молекуле РНК которого с |
другое также свидетельствуют в пользу |
||||
помощью обратной транскриптазы |
генетической природы злокачественности. |
||||
синтезируется ДНК, которая встраивается в |
Наиболее |
прямые |
доказательства |
||
геном клетки-хозяина. |
генетического контроля образования |
||||
3. Лучевой канцерогенез. Это одна из |
злокачественныхопухолейбылиполученыпри |
||||
форм канцерогенеза, сопровождавшего |
изучениитемпературочувствительныхмутаций |
||||
первых радиологов, работавших с радием и |
у вирусов. В начале 1970-х годов были |
||||
лучами Рентгена без какой-либо защиты от |
получены температурочувствительные |
||||
облучения. Обычно это были раки кожи. |
мутанты |
вируса |
саркомы, которые |
||
Наиболее частыми при общем облучении |
трансформировали нормальные клетки в |
||||
организма являются лейкозы, т.е. различные |
раковые |
только |
ïðè |
определенной, |
|
формы опухолей кроветворной системы. |
пермиссивнойтемпературе.Этозначит,чтопри |
||||
4.Роль генотипа. В основе этойтемпературеэкспрессируетсямутантная
возникновения большинства опухолей лежат генетические причины: реорганизация генома и различные мутации в широком смысле этого слова. В одних случаях это результатотбора.Так,умышейпутемотбора получены чистые линии со 100% вероятностью возникновения определенных форм опухолей - лейкозов, рака молочных желез и рака легких. В первых двух случаях имеет место сочетание генотипа животных и вируса, а в случае наследственного рака легкихречьидетосочетанииканцерогенного воздействия и генома животного. Во множестве других случаев причиной возникновения опухолей являются мутации генов, контролирующих нормальное протекание клеточного деления. Под генетическим контролем, по-видимому, находится и процесс метастазирования.
17.3.Онкогены
Âпользу генетической природы злокачественности свидетельствуют два факта:
1. Корреляции между существованием наследуемых опухолей и наличием
форматолькоодногогена,и этогодостаточно для того, чтобы вызвать опухолевую трансформацию и поддерживать ее. Инактивация этой мутации при другой, не пермиссивнойтемпературевозвращалаклетку в нормальное состояние. Таким образом, сделали вывод, что в вирусе саркомы содержится один ген, вызывающий и поддерживающийзлокачественность.Онбыл назван онкогеном. В конце 1970-х годов был выделен первый онкоген из вируса саркомы курицы - src (Рис. 17.3).
Вирус саркомы Payca несколько необычен среди ретровирусов, несущих онкогены, поскольку в нем сохраняются все тригена,необходимые дляжизненногоцикла вирусов: gag, pol и env. У других онкогенных вирусов один или два этих гена частичноили полностьюпотерянывобменнаприобретение трансформирующего онкогена. Поэтому частицы трансформирующего вируса могут формироваться только в клетке, которая одновременно инфицирована нормальным (недефективным) нетрансформирующим вирусом-помощником,которыйкомпенсирует отсутствующиефункции.
390
Основы онкогенетики |
|
|
|
Глава 17 |
|
Рисунок 17.3 |
|
|
|
|
|
à |
|
Концевые повторы |
|
|
|
|
|
|
|
|
|
Êýï |
|
|
|
|
|
5’ |
|
|
3’ |
|
|
|
gag |
pol |
|
|
|
|
|
|
env |
|
|
á |
|
|
|
|
|
Êýï |
|
|
|
|
|
5’ |
|
|
|
3’ |
|
|
gag |
|
env |
|
|
|
|
pol |
src |
|
|
â |
|
|
районы, кодирующие |
|
|
ÄÍÊ |
|
|
|
|
|
экзон |
интрон |
киназный домен |
|
|
|
хозяина |
|
|
|||
|
|
|
|
|
|
5’ |
|
протоонкоген c-src цыпленка |
3’ |
|
|
|
|
src |
|
|
|
|
|
онкоген |
|
|
|
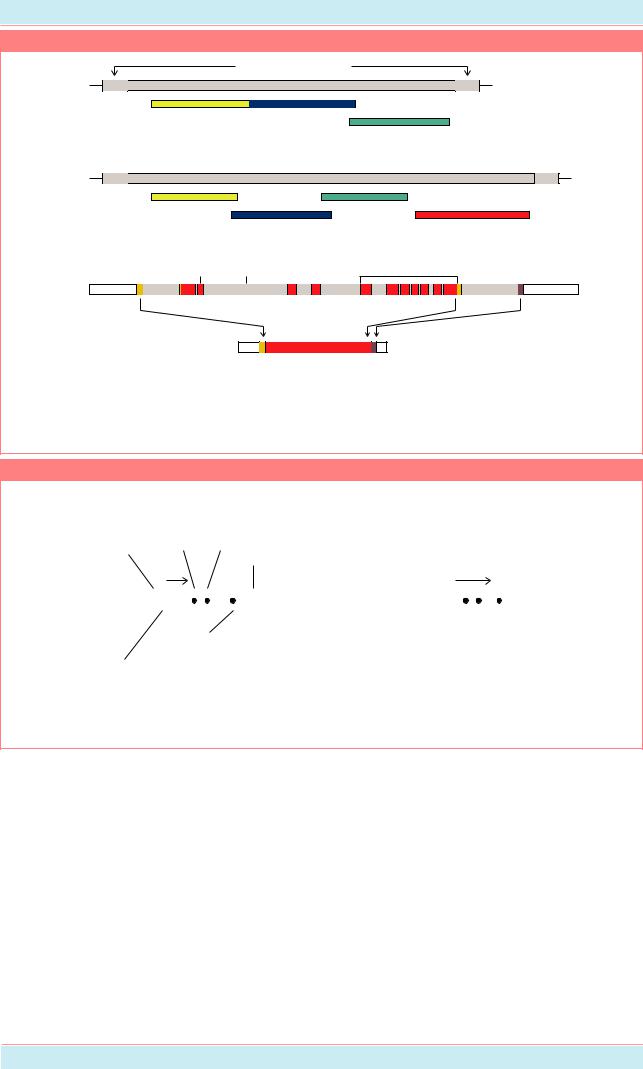
Структура вирусов лейкемии мыши (а), и саркомы Рауса (б), а также |
онкогена src |
è |
|||
протоонкогена c-src (в); gag - ген, кодирующий белок капсиды вируса; pol - ген обратной |
|||||
транскриптазы; env - ген, кодирующий гликопротеиновую оболочку вируса; src - онкоген (Из: |
|||||
Alberts et al., 1994, p. 1276). |
|
|
|
|
|
Рисунок 17.4 |
|
|
|
|
|
4-6 пн прямой |
Сигналы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
начала |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
повтор, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
транскрипции |
|
|
|
|
|
Сигнал |
|
|
|||||||||||
ограничивающий |
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
Полипуриновый |
|
|
|
|
|
|
|
|
||||
сайт встраивания CCAAT |
|
TAATA |
|
полиаденилирования |
|||||||||||||||||
провируса |
|
|
|
|
|
|
IRS |
|
тракт |
AATAA |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
gag |
pol |
env |
|
|
|
|
|
|
|
|
|
|
|
|
|
U3 |
|
R U5 |
|
|
U3 |
R U5 |
|
|
|||||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
ñàéò |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Короткий |
|
|
|
|
|
кэпирования |
|
|
LTR |
|
|
|
|
|
|
|
|
||||
инвертированый |
|
|
|
|
ìÐÍÊ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
повтор (IRS), |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
ограничивающий LTR |
|
|
LTR |
|
|
|
|
|
|
|
|
|
|
|
|||||||
Особенности организации длинных концевых повторов (LTR) в ДНК у ретровирусов. U!, R è U# - элементы вирусных геномов (Из: Russell, 1998, p. 593).
LTR вирусов содержат многие из регуляторныхсигналовтранскрипции:сайты инициациитранскрипции,полиаденилирования и др. (Рис. 17.4).
Вскоре было показано, что искусственное введение гена src в генетический аппарат клетки трансформирует ее и без вируса.
После этого были открыты и другие вирусные онкогены: myc, ras, abl и многие другие. Стало ясно, что опухолевые вирусы вызывают опухоли не сами по себе, а потому, что вносят онкоген в генетический аппарат клетки и закрепляют его там. Если удалить
онкоген из генетическогоаппарата вируса, то последний, не лишаясь способности размножаться и интегрироваться в геном клетки, утратит возможность вызывать формирование злокачественных опухолей.
Геномы нормальных клеток позвоночных содержат последовательности, которыепохожи,нонеполностьюидентичны гену src, входящему в состав вируса саркомы Рауса, поэтому их называют несколько по разному: v-src вирусный (онкоген), c-src - клеточный (протоонкоген). На Рис. 17.3 показана схема организации онкогена src и протоонкогена c-src. Интроны, которые
391

Глава 17 |
Основы онкогенетики |
|
|
Таблица 17.1
Характеристики некоторых онкогенов и протоонкогенов (Из: Alberts et al., 1994, p. 1276).
Онкоген |
Функции |
Источник |
Опухоль, индуцируемая |
|
протоонкогена |
вируса |
данным вирусом |
||
|
||||
|
|
|
|
|
abl |
протеинкиназа (тирозин) |
мышь, кошка |
лейкемия, саркома |
|
|
|
|
|
|
|
протеинкиназа (тирозин): рецептор |
|
|
|
|
эпидермального фактора роста (EGF). |
|
эритролейкемия, |
|
erb-B |
Мутантный рецептор фактора роста |
курица |
||
фибросаркома |
||||
|
непрерывно пересылает сигналы к |
|
||
|
|
|
||
|
пролиферации |
|
|
|
|
|
|
|
|
fes |
протеинкиназа (тирозин) |
кошка, курица |
саркома |
|
|
|
|
|
|
|
протеинкиназа (тирозин): рецептор |
|
|
|
fms |
фактора, стимулирующего колонии |
кошка |
саркома |
|
|
(M-CSF) |
|
|
|
|
|
|
|
|
fos, |
ассоциирующиеся продукты, |
|
остеосаркома, |
|
образующие ген, регулирующий белок |
мышь, курица |
|||
jun |
фибросаркома |
|||
AP1 |
|
|||
|
|
|
||
|
|
|
|
|
kit |
протеинкиназа (тирозин) |
кошка |
саркома |
|
|
|
|
|
|
raf |
протеинкиназа (серин/ треонин), |
курица/мышь |
саркома |
|
активируемая белком RAS |
||||
|
|
|
||
|
|
|
|
|
|
ген, регулирующий белок из |
|
саркома, миелоцитома, |
|
myc |
семейства HLH. Ядерный фактор, |
курица |
карцинома, лейкоз птиц |
|
активность которого ведет к |
и многие опухоли |
|||
|
|
|||
|
непрерывному делению клеток |
|
человека и животных |
|
|
|
|
|
|
|
GTP-связывающий белок, |
|
|
|
H-ras |
цитоплазматический активированный |
крыса |
саркома, эритролейкемия |
|
|
передатчик сигналов в клетку, |
|
|
|
|
ведущий к ее пролиферации |
|
|
|
|
|
|
|
|
K-ras |
-"- |
-"- |
-"- |
|
|
|
|
|
|
rel |
ген, регулирующий белок, |
индейка |
ретикулоэндомиелоз |
|
связанный с NFкB |
||||
|
|
|
||
|
|
|
|
|
sis |
ростовой фактор тромбоцитов - PDGF |
мартышка |
саркома |
|
|
|
|
|
|
|
протеинкиназа (тирозин), |
|
саркома птиц и |
|
src |
активированный передатчик сигналов |
курица |
||
млекопитающих |
||||
|
в клетку, ведущий к ее пролиферации |
|
||
|
|
|
||
|
|
|
|
присутствовали в c-src, сплайсированы в v- src.
Позднее было установлено, что во всех нормальныхклеткахестьгены,оченьблизкие по структуре к известным вирусным онкогенам. Их известно уже около 100. Характеристики некоторых вирусных онкогенов и соответствующих им протоонкогенов представлены в Табл. 17.1.
Эти гены регулируют нормальное поведение клетки - ее ответы на ростовые
факторы, на гормоны, нормальный темп и “расписание”ееделений.Чтобыклетканачала расти и размножаться, нужны специальные сигналы, вырабатываемые чаще всего другими клетками, а иногда и самой клеткой. Этообычнобелковыемолекулы,называемые факторамироста(Рис.17.5).Ихсинтезстрого регулируется,ноеслипроисходитнарушение регуляции,тофакторымогутнакапливатьсяв больших количествах. Они начинают сигнализировать клетке о необходимости
392

Основы онкогенетики |
Глава 17 |
|
|
Рисунок 17.5
рецептор PDGF рецептор EGF [erbB] рецептор M-CSF [fms]
белки Ras [H-ras] [N-ras] [K-ras]
|
PDGF [sis] |
|
|
EGF |
|
|
M-CSF |
|
Src протеин киназа |
ростовые факторы |
|
[src] |
||
|
рецепторы ростовых |
GTP-связывающий |
мембранно/цитоскелет- |
факторов действующие |
белок |
связанная тирозин- |
через тирозин- |
|
специфическая протеин |
специфическую протеин |
|
киназа |
киназу |
|
|
[fes] |
рецептор тиреоидного |
[raf] |
|
гормона [erbA] |
|
|
|
ядерные белки |
цитоплазматическая |
рецептор ростового |
серин/треонин |
тирозин-специфическая |
фактора стероидного |
специфическая |
протеинкиназа |
òèïà |
протеинкиназа |
Основные этапы передачи сигнала для роста и деления клеток от клеточной оболочки до клеточного ядра (Из: Alberts et.al. 1994, p. 1278).
растииделиться.Поэтомугены,кодирующие факторы роста, могут выступать в роли онкогенов. Чтобы фактор подействовал, необходим рецептор для данного фактора, расположенный на поверхности клеткимишени. Когда фактор присоединяется к рецептору,последнийактивируется,чтоможет в ряде случаев выразиться в ферментативной реакции, например фосфорилировании определенныхбелков.Врезультатенекоторых поврежденийрецепторовфакторовростаони обретают свойства активироваться даже при отсутствии своего фактора роста. Такой рецепторбудетнепрерывнопередаватьсигнал о необходимости начинать рост, хотя фактор роста и отсутствует. В случае повреждения этот ген становится онкогеном. Передача сигнала на рост клетки не ограничивается факторамиростаиихрецепторами.Впередаче такого сигнала участвует много других белков и сам процесс часто идет путем фосфорилирования одним белком второго, вторым - третьего и т.д. Гены, кодирующие участниковэтихцепей,могутвыступатьвроли онкогенов.
Цепипередачисигналовзаканчиваются
âклеточном ядре. Там происходит активация факторов транскрипции, то есть белков, связывающихся с регуляторными участками определенных генов и активирующих транскрипцию данных генов. Под действием факторовтранскрипциинасоответствующих генахпроисходитсинтезматричныхРНК,ана матрице последних – белков. Это те белки, которые нужны для роста и размножения клеток. И среди генов, кодирующих факторы транскрипции,оказываютсяонкогены(см.рис. 17.5). Таким образом, многие гены, кодирующие белки передачи сигнала для роста и размножения клеток, являются потенциальными онкогенами и при поврежденииилинерегулируемойактивации этих генов клетки превращаются в раковые.
Можно таким образомзаключить, что у вирусов в процессе цикла их развития происходит захват генов хозяина (например, мышииличеловека),ипоследниевыступают
âроли онкогенов.
Известны различные пути активирования протоонкогенов, в результате
393

Глава 17 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Основы онкогенетики |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Рисунок 17.6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Îíê |
|
|
|
|
|
Происхождение и активация онкогенов. |
|
|||||||||
I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
I - вирусный онкоген: часть вирусного генома, |
|||||||
Õð |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
интегрированного в хромосому хозяина |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
провирус |
|
|
|
|
|
|
|
|
|
(провирус). Онк - онкогены ретровирусов: src, |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Îíê |
|
|
|||||||||||
II |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
myc, ras, erb, Хр -хромосома хозяина. |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
II - активация клеточного онкогена встроенным |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Õð |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
провирусом (онкоген Int-1 при раке молочных |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
провирус |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
желез мышей). |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
À |
|
Îíê |
|
|
|
|
|
|
|
|
|
|
III - Хромосомные транслокации - разрыв и |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
III |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
воссоединение фрагментов разных хромосом в |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Õð À |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Õð Â |
|
единую новую хромосому могут привести к |
||||||||||||||||||
|
|
|
|
|
|
|
|
À |
 |
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
активации онкогена или образованию нового. |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
В первом случае молчащий ген попадает под |
|||||||
Õð À |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Õð Â |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
контроль работающего |
промотора |
èëè |
|||||||||||||||||
|
|
|
|
|
|
|
|
Химерный белок |
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
энхансера клеточного гена и активируется (ген |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
myc |
myc |
|
myc |
myc |
myc myc |
myc при лимфоме Бэркитта). Во втором случае |
|||||||||||||||||||||||||||
IV |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
в месте разрыва-воссоединения образуется |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
новый химерный ген, кодирующий химерный |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
белок (белок химерного гена bcr-abl при |
|||||||
|
|
|
|
|
|
|
|
Îíê* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
хроническом миелолейкозе). |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
IV - амплификация (увеличение числа копий) |
|||||||||||||
V |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
протоонкогена, |
ведущая к |
опухолевой |
||||||
Õð |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
трансформации (амплификация гена myc при |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
Ген-супрессор* |
|
|
|
|
|
|
|
|
|
|
опухолях нервной системы). |
|
|
||||||||||||||||
VI |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V - мутация протоонкогена - синтез мутантного |
|||||||||
|
Õð n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
онкобелка (c-ras, при спонтанных и |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Îíê |
|
|
|
|
|
|
|
|
|
канцерогенных опухолях). |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
VI - инактивация или утрата гена - супрессора |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
Õð m |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
опухолевого роста, ведущая к активации |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
протоонкогена |
(ãåí |
RB |
в клетках |
||||
* - мутантный ген |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ретинобластомы человека; ген p53 в клетках |
||||||||||||||||||||
|
|
|
|
- активация экспрессии гена |
|||||||||||||||||||||||||||||||
|
|
|
|
разных опухолей человека) (Из: Абелев, 1997) |
|||||||||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||
чего они становятся автономными (Рис. |
|
Дополнение 17.2 |
|
|
|
||||||||||||||||||||||||||||||
17.6). Как правило, опухолеродное действие |
|
Нобелевская премия |
1975 |
ãîäà |
|||||||||||||||||||||||||||||||
различных канцерогенных факторов |
|
присуждена Дэвиду Балтимору (D. Baltimore), |
|||||||||||||||||||||||||||||||||
приводит к |
постоянной |
активности |
|
Ренато Дульбекко (R. Dulbecco) и Ховарду |
|||||||||||||||||||||||||||||||
протоонкогена. |
Òàê, |
хромосомные |
|
Темину (H. Temin) за установление связи |
|||||||||||||||||||||||||||||||
|
между |
опухолеродными |
вирусами и |
||||||||||||||||||||||||||||||||
транслокациимогутперенестипротоонкоген |
|
||||||||||||||||||||||||||||||||||
|
генетическим материалом клетки. Дж.M. |
||||||||||||||||||||||||||||||||||
в новое положение - под контроль постоянно |
|
||||||||||||||||||||||||||||||||||
|
Бишоп |
(J.M. Bishop) и Х.Е. Вармус (H.E. |
|||||||||||||||||||||||||||||||||
активного промотора |
(Ðèñ. 17.7). Â |
|
|||||||||||||||||||||||||||||||||
|
Varmus) в 1989 году получили Нобелевскую |
||||||||||||||||||||||||||||||||||
результате этого переноса протоонкоген |
|
||||||||||||||||||||||||||||||||||
|
премию по медицине за открытие клеточной |
||||||||||||||||||||||||||||||||||
начинает работать непрерывно, не давая |
|
||||||||||||||||||||||||||||||||||
|
природы ретровирусных онкогенов. |
|
|||||||||||||||||||||||||||||||||
клетке выйти из цикла делений (myc), или |
|
|
|||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||
экспрессию (“вставочный” канцерогенез) |
|||||||||||||||||||||||||||||||||||
посылая непрерывные сигналы с мембраны |
(Ðèñ. 17.8). |
|
|
|
|
||||||||||||||||||||||||||||||
в ядро (ras), или приводя к синтезу ростовых |
Канцерогенные вещества и облучение |
||||||||||||||||||||||||||||||||||
факторов. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
обладают высокой мутагенной активностью, |
||||||||||
Некоторые опухолевые вирусы сами по |
|||||||||||||||||||||||||||||||||||
вызывая мутации в различных генах, в том |
|||||||||||||||||||||||||||||||||||
себе не содержат онкогена, но, встраиваясь |
числеивпротоонкогенах.Этимутациимогут |
||||||||||||||||||||||||||||||||||
в хромосому рядом с протоонкогеном, |
вести либо к нарушению регуляции |
||||||||||||||||||||||||||||||||||
активируют его, вызывая непрерывную |
протоонкогена, и тогда он выходит из-под |
||||||||||||||||||||||||||||||||||
394
Основы онкогенетики |
|
|
Глава 17 |
Рисунок 17.7 |
|
|
|
Ãåí bcr в хромосоме 22 |
Ãåí abl в хромосоме 9 |
||
5’ |
3’ |
5’ |
3’ |
Точка |
|
Точка |
|
разрыва |
|
разрыва |
|
|
Филадельфийская |
|
|
|
транслокация |
|
|
5’ |
|
3’ |
ãåí bcr/abl |
|
|
|
|
|
|
Транскрипция |
|
5’ |
|
3’ |
ïîëè-A ìÐÍÊ bcr/abl |
|
|
|
|
|
|
Трансляция |
|
|
|
|
белок Bcr/Abl |
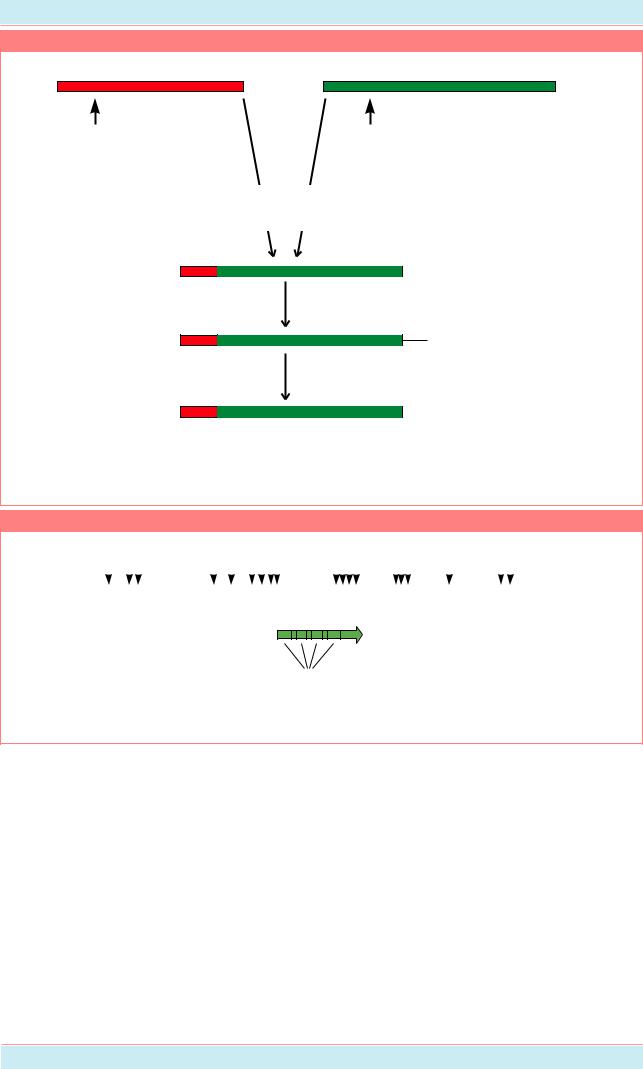
Превращение протоонкогена abl в онкоген у пациентов с хронической миелогенной лейкемией. |
|||
В результате транслокации 22 и 9 хромосомы (Филадельфийская хромосома) ген bcr |
|||
соединяется с геном abl тирозиновой протеинкиназы, в результате чего этот ген функционирует |
|||
не по своему расписанию (Из: Alberts et al., 1994, p. 1278) |
|
||
Рисунок 17.8 |
|
|
|
Ãåí Wnt-1
5’ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3’ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5000 ï.í. |
ÐÍÊ |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Экзоны
Локализация инсерций (показаны стрелками) вируса рака молочных желез мыши (MMTV), активирующих транскрипцию гена Wnt-1. Инсерция влияет на экспрессию гена, даже если она на расстоянии до 10 т.п.н. (Из: Alberts et al., 1994, p. 1277)
контроля, либо к изменению свойств белка, кодируемого этим онкогеном.
17.4. Антионкогены или генысупрессоры опухолей
Вскоре после открытия первых онкогенов появились сообщения о существованиигенов,утратаилиподавление активности которых также приводит к развитию опухолей. Иными словами, белковые продукты этих генов необходимы для того, чтобы не дать клетке превратиться в раковую. Эти гены были названы антионкогенами или генами-супрессорами
опухолей (ГСО). ЧислоизвестныхГСОтоже быстро растет, хотя и уступает числу открытых онкогенов.
Примерноодинизкаждых20тыс.детей имеет предрасположенность к ретинобластоме - опухоли, возникающей в детстве из предшественников клеток сетчатки глаза. Известны две формы заболевания - наследственная и ненаследственная. В случае наследственной формы множественные опухоли обычно возникают независимо в обоих глазах. При ненаследственной форме возникает только одна опухоль и только в одномглазу.
395
Глава 17 |
Основы онкогенетики |
|
|
Рисунок 17.9
а) Нормальный здоровый индивид
В одной из клеток спонтанно инактивируется один из нормальных аллелей гена Rb
б) Наследственная ретинобластома в) Ненаследственная ретинобластома
наследуется мутантный ген Rb
В клетке, гетерозиготной по аллелям Rb, происходит еще
одна мутация Rb 
 Ускоренная клеточная
Ускоренная клеточная
пролиферация приводит к образованию ретинобластомы
В одной из клеток происходит мутация гена Rb
В потомстве этой клетки иногда мутирует второй ген Rb
Ускоренная клеточная пролиферация приводит к образованию ретинобластомы
Результат: опухоль не образуется |
Результат: у большинства |
Результат: только у одного |
|
индивидуумов с наследуемой |
индивидуума из 3000 нормальных |
|
мутацией образуется опухоль |
людей формируется опухоль |
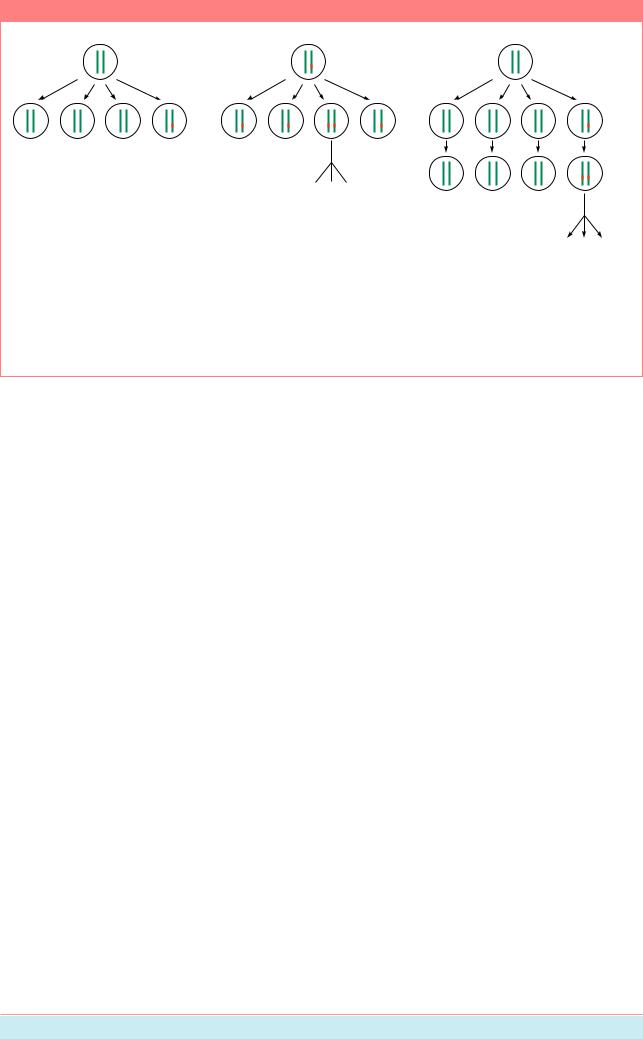
Схема мутирования гена Rb и образования наследственной и ненаследственной форм ретинобластомы у человека (Из: Alberts et al., 1994, p. 1282).
На Рис. 17.9 показаны схемы наследования мутантной формы гена, индуцирующегоретинобластому.
Предположили, что у особей с наследственнойформойутраченаактивность гена-супрессораопухолеобразованияводной из хромосом. Поэтому гетерозиготы по мутации данного гена являются генетически предрасположенными к раку. Первая же соматическая мутация этого локуса, делает данную клетку гомозиготой по мутации, из которойиначинаетразвиватьсяопухоль.Таким образом, ретинобластома возникает по двухударному механизму: одна мутация происходитвгенеративныхклетках,другая-в соматических.Этотген,отсутствиеактивности которого у человека является критическим обстоятельствомвразвитииретинобластомы, называется Rb. У детей-гомозигот по нормальному аллелю гена Rb опухоль возникает очень редко, только вследствие случайноговозникновениямутацийгена Rbв обеиххромосомаходнойклетки.
В более поздних исследованиях было установлено, что потеря активности гена Rb вызываетразнообразныеформыопухолей,не толькоретинобластому.
Ген Rb был клонирован в 1986 году, он занимаетв геноме 180т.п.н.икодируетбелок с молекулярной массой 110 кДа. Ген активно
функционирует в большинстве нормальных клетоктела,и егопродуктдействуеткакодин изглавных“тормозов”вклеточныхделениях. Функционированиегена Rb непосредственно связано с контролем продвижения клетки в митотическом цикле.
Как указывали выше (Раздел 6.3.), размножаясь, клетки проходят через несколькофазклеточногоцикла.Важнейшие фазы – это деление клеток или митоз (M); фаза, предшествующая синтезу ДНК (G ); фаза репликации ДНК (S); следующая за ней фаза подготовки к делению (G ) и снова митоз (M). Кроме того, клетки могут переходить из G не в S, а в фазу G или в фазу покоя (см. детали в Разделе 6.3.2). Переход из одной фазы клеточного цикла в другую – это строго регулируемый процесс. На определенных этапах клеточного цикла существуют так называемые “точки проверки” (check points), в которых специальные белки определяют, все ли в клетке в порядке и готова ли она к переходу в следующую фазу цикла. Например, если в клетке повреждена ДНК, сигнал об этом блокирует переход в следующую фазу. Такая система проверок требует большого числа специальных белков. Ключевая роль в разрешении на продвижение по циклу принадлежит белкам из семейства циклинов.
396
