
Подготовка у универсиаде 2012 / Генетика (Жимулев) / 16ver7
.pdf
Глава 16 |
Основы иммуногенетики |
|
|
Глава 16. Основы иммуногенетики
16.1. Понятие об иммунитете
Наша иммунная система спасает нас от неминуемой гибели вследствие инфекций. Любое позвоночное животное, родившееся с сильнымиповреждениямииммуннойсистемы, вскоре погибнет, если его полностью не изолировать от каких бы то ни было инфицирующихагентов.
Иммунность – (immunitas = ëàò. – свободный от чего либо) означает нечувствительность к данному виду возбудителей болезней, а иммунитет – способность организма защищать собственнуюцелостность.Областьгенетики, в которой изучают генетические механизмы иммунного ответа, называют иммуногенетикой.
Иммунитет – защита организма от инфекции или, в более широком смысле, - реакция организма на чужеродные макромолекулы, микроорганизмы и клетки. Защита осуществляется с помощью двух систем – неспецифического (врожденного, естественного)испецифического иммунитета. Этидвесистемымогутрассматриватьсяикак две стадии единого процесса защиты организма. Неспецифический иммунитет выступаеткакперваялиниязащиты.Система врожденногоиммунитетадействуетнаоснове реакции воспаления и фагоцитоза. Она реагирует только на корпускулярные агенты (микроорганизмы, занозы) и на токсические вещества,разрушающиеклеткииткани,вернее, на корпускулярные продукты этого разрушения.
Вторая и наиболее сложная система – приобретенного иммунитета - основана на специфическихфункцияхлимфоцитов,клеток крови, распознающих чужеродные макромолекулы(антигены)иреагирующихна них либо непосредственно, либо выработкой защитныхбелковыхмолекул–антител.
Антигеном(антиген– тоесть ãåíератор àíòèтел)можетбытьневсякоевещество.Оно
должно быть чужеродным, макромолекулярным (с мол. весом более 10000-12000) и иметь устойчивую химическуюструктуру.Ктипичнымантигенам относятсябелкииполисахариды.
Приобретенный иммунитет характеризуется четырьмясвойствами:
1.Организм отличает свои антигены от чужих.
2.Способностьотличатьзапоминается.Эта такназываемаяиммунологическая“память”.
3.“Память” специфична, запоминается контакт лишь с определенным антигеном. Специфичность этого запоминания очень высока.
4.Иммунный ответ на чужеродную макромолекулуможноизбирательноподавить, если ввести ее в развивающийся организм внутриутробно или в первые часы после рождения.Такоеподавлениереакциинабелок называется толерантностью (терпимостью). Указанные четыре признака неразделимы и всегда проявляются вместе.
Система приобретенного иммунитета имеется в организме человека и других животных (рыбы, земноводные, пресмыкающиеся, птицы, млекопитающие). Способность приобретенного иммунитета широкоиспользуетсядлявакцинации,тоесть введения ослабленных или убитых микроорганизмов, или выделенных из них макромолекул, вызывающих иммунологическую реакцию на эти микроорганизмы. Вакцинация является основным способом предупреждения таких страшных заболеваний как оспа, туберкулез, полиомиелит,сибирскаяязваимногихдругих. Приобретенный иммунитет составляет основноепрепятствиедляпересадокорганов (сердце, почки, печень) и тканей (кожа) от одного человека другому. Для преодоления этого барьера несовместимости пользуются препаратами, подавляющими иммунную систему.
Каким образом осуществляется приобретение иммунитета? У человека существуюттриллионылимфоцитов–белых кровяных клеток. Они находятся в
376

Основы иммуногенетики |
|
|
|
Глава 16 |
Рисунок 16.1 |
|
|
|
|
à |
á |
|
â |
|
|
TCR |
CD4 |
TCR |
CD8 |
антиген- |
|
|
|
связывающий |
|
|
|
рецептор |
B-клетка |
TH-клетка |
TC-клетка |
(антитело) |
|
|
|
Типы лимфоцитов (Из: Kuby, 1994, p. 11). a – B-клетка имеет примерно 105 молекул антител, расположенных на мембране. Все молекулы антител на поверхности клетки имеют ту же самую антигенную специфичность и могут непосредственно связываться с антигеном. б - Т-клетки, несущие СD4, распознают только антигены, связанные с молекулами МНС класса II. в – Т- клетки, несущие CD8, распознают антиген, связанный с молекулами МНС класса I. Клетки CD4+T функционируют в качестве хелперов (TH), а клетки CD8+ функционируют в качестве цитотоксических клеток (TÑ). Оба типа Т-клеток содержат около 105 идентичных молекул антиген-связывающих рецепторов (TCR) на одну клетку.
кровеносном русле, в лимфоидных органах (тимус, лимфоузлы, селезенка и аппендикс) и в лимфе (бесцветная жидкость в лимфатических сосудах, соединяющих лимфоузлы).
Существуют две составляющие иммунной системы, каждая из которых ассоциирована с лимфоцитами определенного типа. Лимфоциты, созревающие в тимусе (вилочковой железе), называются Т-лимфоцитами, в отличие от В- лимфоцитов, развивающихся в костном мозге (Рис. 16.1). Клеточный иммунитет обеспечивается Т-клетками, а гуморальный
– как В -, так и Т – лимфоцитами. Клеточный иммунитет опосредуется преимущественно специфическими Т-клетками – цитотоксичными Т-лимфоцитами или “киллерами” (CTL), и направлен против клеток, несущих на своей поверхности чужеродные антигены.
Активирование как гуморальной, так и клеточной ветвей иммунной системы требует цитокинов, продуцируемых TH- клетками, которые в свою очередь активируются только в том случае, если антиген появляется в комплексе с
молекулами МНС на поверхности специализированных клеток, называемых антиген-представляющих клеток (APS). Эти клетки (макрофаги, B-лимфоциты, дендритные клетки) поглощают антигены и затем выделяют часть антигена в комплексе
ñмолекулой МНС на своей мембране. Затем
TH-клетки опознают антиген, связанный с молекулой МНС на поверхности антигенпредставляющих клеток.
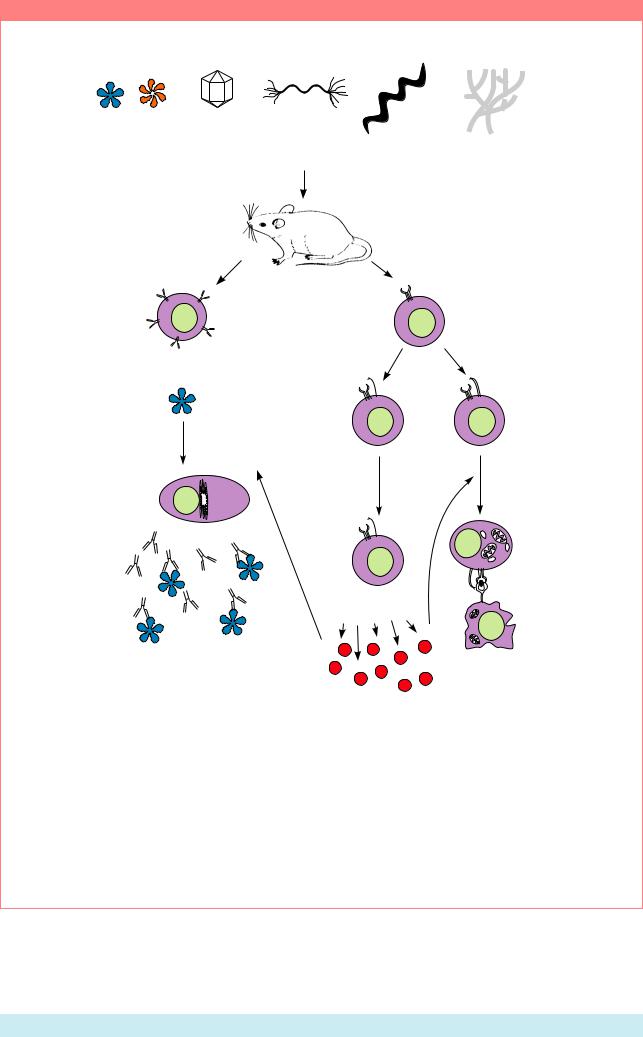
Гуморальная ветвь иммунной системы включает в себя взаимодействие B-клеток с антигеном, последующую пролиферацию последнихиихдифференцировкувантитела - секретирующие плазматические клетки (Рис. 16.2). Когда антигены связываются с антителами, эти комплексы тем или иным способом удаляются из организма.
Несмотря на то, что антигены обычно имеют большие размеры, они опознаются В
– или Т – лимфоцитами, поскольку антитела, расположенныенаэтихклетках,связываются
ñнебольшими участками антигена, называемыми антигеннымидетерминантами илиэпитопами.В-клеткираспознаютэпитопы самостоятельно, в то время как Т-клетки распознают эпитоп только если он
377
Глава 16 |
Основы иммуногенетики |
|
|
Рисунок 16.2
Антигены
Чужеродные |
Вирусы Бактерии Паразиты |
|
Грибы |
белки |
|
|
|
Гуморальный |
|
Клеточный |
|
иммунитет |
|
иммунитет |
|
|
Тело позвоночного |
|
|
B-клетка |
|
|
T-клетка |
|
|
|
|
+ |
TH-клетка |
|
TC-клетка |
Антиген |
|
|
|
|
+ цитокины |
|
|
|
TH-клеток |
|
Молекула |
Антитела- |
Молекула |
|
|
антиген-класс II |
|
антиген-класс I |
|
секретирующая |
|
||
MHC |
|
MHC |
|
плазматическая |
|
|
|
клетка |
|
|
CTL |
|
|
|
|
Элиминация |
|
|
Уничтожение |
Активированная |
измененной |
||
антигенов |
клетка |
|
клетки |
Измененная
клетка
Секреция
цитокинов
Две составляющие иммунной системы (Из: Kuby, 1994, p. 13). В ходе осуществления гуморального иммунитета происходит взаимодействие B-клеток с антигеном и последующая дифференцировка B-клеток в антитела-синтезирующие плазматические клетки. Секретируемые антитела связывают антигены и облегчают их удаление из организма. Клеточный иммунитет включает в себя различные субпопуляции T-клеток, которые опознают антиген, связанный с белком МНС I класса. TH-клетки отвечают на появление антигена продукцией цитокинов. TC-клетки отвечают на антиген дифференцировкой в цитотоксические T-лимфоциты (CTL), которые обеспечивают убийство измененной антигеном клетки (например, клетки, инфицированной вирусами).
расположен на поверхности |
антиген- |
Как устроены антитела и рецепторы |
представляющей клетки в комплексе с |
лимфоцитов? Очевидно, что их структура |
|
молекулой МНС. Часть |
антигена, |
должна быть необычной, так как они строго |
взаимодействующая с белками МНС, |
специфически распознают громадное |
|
называется агритопом (Рис. 16.3). |
множество различных антигенов – любой |
|
|
|
|
378
Основы иммуногенетики |
|
|
|
Глава 16 |
|||
|
|
|
|
|
|||
|
|
|
|
(Light – легких) – примерно 25000 Да. Цепи |
|||
Рисунок 16.3 |
|
|
|
||||
Антиген-представляющая клетка |
|
соединены друг с другом ковалентными |
|||||
|
|
|
|
(дисульфидными) связями (Рис. 16.4). |
|||
|
|
|
|
Рецептор лимфоцитов, в отличие от антител, |
|||
|
|
|
|
-гетеродимер,состоящийизпарыразличных |
|||
|
|
|
|
цепей - α è β |
с молекулярным весом около |
||
|
|
|
|
50000 Да, соединенных между собой одной |
|||
класс II MHC |
|
дисульфидной связью. В основе структуры |
|||||
Агритоп |
|
||||||
|
иммуноглобулинов лежит |
сходное |
|||||
|
|
|
|
||||
|
|
|
|
повторяющееся звено (домен), состоящее |
|||
|
|
|
|
примерно из 110 аминокислот, свернутых в |
|||
Эпитоп |
|
глобулы,напоминающиедругдруга (см. Рис. |
|||||
|
16.4, где эти звенья обозначены как |
||||||
TCR |
|
|
|
||||
|
|
|
прямоугольники). Каждый домен в молекуле |
||||
|
|
|
|
||||
|
|
|
|
антитела или РТК выполняет свою |
|||
|
|
|
|
биологическуюфункцию,анаиболееважную |
|||
|
|
|
|
èç íèõ – распознавание и связывание с |
|||
|
|
|
|
антигеном– осуществляютконцевыедомены |
|||
TH-клетка |
|
(см. Рис.16.4).Параконцевыхдоменов(один |
|||||
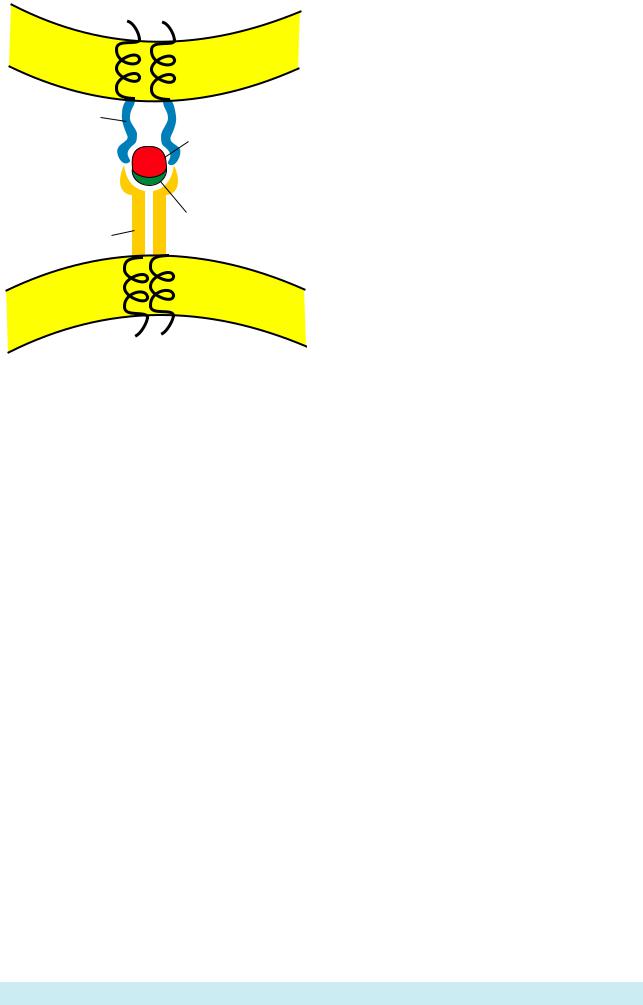
Схематическое изображение комплекса из |
|
èçH-цепи,другойизL-цепи,авРТК -одиниз |
|||||
антигена, рецептора T-клетки (TCR) и |
|
β -цепи,другойизα -цепи)образуютактивный |
|||||
молекулы MHC (Из: Kuby, 1994, p. 97). |
|
центр, уникальную по структуре полость, |
|||||
Антигены, которые опознаются T-клетками, |
|
распознающую в молекуле |
антигена |
||||
имеют два участка контактов: агритоп, |
|
небольшиедискретныеучастки,состоящиеиз |
|||||
взаимодействующий с молекулами MHC |
|
4-8 аминокислот (Рис. 16.5). |
|
|
|||
класса I или II и эпитоп, взаимодействующий |
|
|
|
||||
|
Эти участки антигена подходят к |
||||||
с рецептором T-клеток. |
|
||||||
|
структуре активного центра, “как ключ к |
||||||
|
|
|
|
||||
чужеродный белок, полисахарид или |
|
||||||
|
замку”, образуя прочные нековалентные |
||||||
синтетическую молекулу, вообще в природе |
связи антигена с антителом. Разные антитела |
||||||
не встречающуюся. Антитела являются |
(и РТК также) отличаются друг от друга |
||||||
иммуноглобулинами. |
|
|
структурой |
активных центров. |
Íà |
||
|
|
|
|
||||
У млекопитающих, включая человека, |
молекулярном уровне отличия активных |
||||||
известны пять классов иммуноглобулинов: |
центровопределяетсяпервичнойструктурой |
||||||
IgM, IgG, IgA, IgD и IgE. Каждый класс |
концевых доменов H - è L - , α è β -цепей, то |
||||||
обладает своими структурными и |
|
есть последовательностью аминокислот в |
|||||
биологическими свойствами (Табл. 16.1). |
|
них. Участки H è L цепей (равно как α |
è β ), |
||||
Иммуноглобулины всех классов |
образующие “стенки” активного центра, |
||||||
построены по общему |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 16.1 |
|
|
|
|
|
|
|
|
|
|
|
|
||
плану. Это можно |
Некоторые биологические характеристики иммуноглобулинов |
|
||||||||||||
проиллюстрировать на |
человека (Из: Галактионов, 1997). |
|
|
|
|
|
|
|
|
|||||
примере молекулярной |
Свойство |
|
IgM |
|
IgG |
|
IgA |
|
IgD |
|
IgE |
|||
|
|
|
|
|
||||||||||
организации IgG (Ðèñ. |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
16.4). |
Обозначение |
H-öåïè |
|
µ |
|
γ |
|
α |
|
δ |
|
ε |
||
Антитело состоит |
|
|
|
|
|
|
|
|
|
|
|
|
||
L-öåïè |
|
κ èëè λ |
κ |
èëè λ |
|
κ èëè λ |
|
κ èëè λ |
|
κ èëè λ |
||||
из двух идентичных пар |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Молекулярная формула |
|
(µ 2 κ 2 )5 |
|
(γ 2 κ 2 ) |
|
(α 2 κ 2 )n |
|
(δ 2 κ 2 ) |
|
(ε 2 κ 2 ) |
|||
полипептидныхцепей:H |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|||||||
(Heavy –тяжелых) с |
|
Число доменов H-цепи |
|
5 |
|
4 |
|
4 |
|
4 |
|
5 |
|
|
молекулярным весом |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Молекулярная масса (кД) |
|
900 |
|
160 |
|
170 |
|
185 |
|
185 |
|
||
примерно 50000 Да и L |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
379
Глава 16 |
Основы иммуногенетики |
|
|
Рисунок 16.4
Àêò. ö. |
VH |
|
|
|
|
VH |
Àêò. ö. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
VL |
C |
|
1 C 1 |
|
VL |
Àêò. ö. |
|
|
|||||
H |
|
|
|
|
|
|
|||||||
|
|
|
H |
|
|
|
|
|
|
|
|
||
CL |
-S-S- |
-S-S- -S-S- |
CL |
|
|
|
|
|
|||||
|
|
-S-S- |
|
V |
|
|
|
|
V |
||||
|
L |
|
|
|
|
L |
|
|
|
|
|||
|
CH2 |
|
|
|
|
CH2 |
èëè |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
H |
|
H |
|
|
|
-S-S- |
|
||||
|
Антитело |
|
|
|
|
|
M |
||||||
|
|
|
|
|
|
|
|
||||||
ÐÒÊ
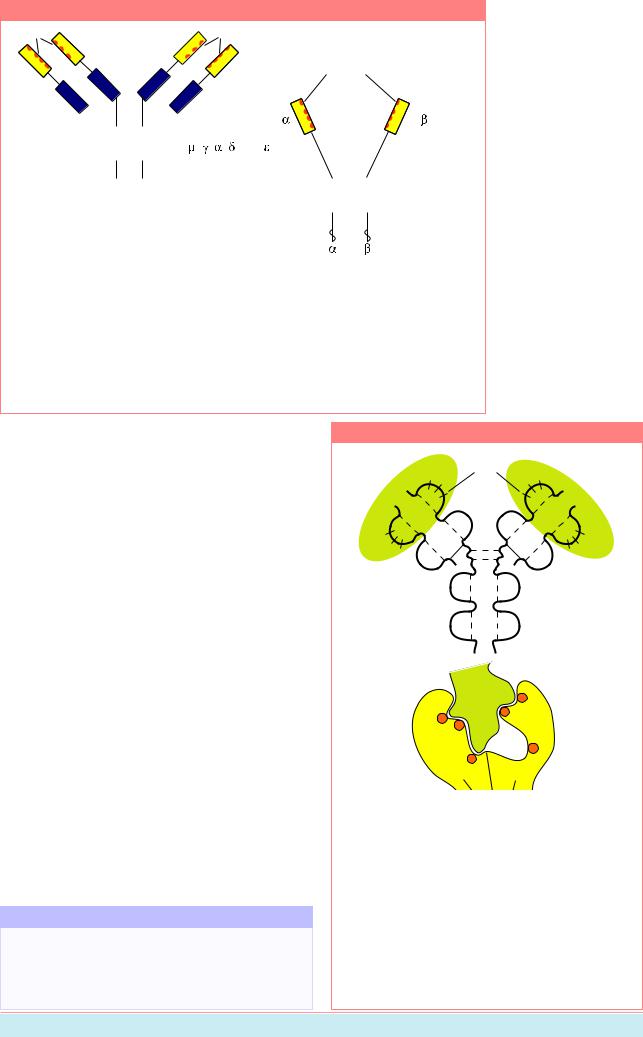
Принципиальная схема строения антител и рецепторов T-клеток (РТК). H è L – тяжелая и легкая цепи антител соответственно, VL è VH – вариабельные районы соответственно легких и тяжелых цепей; Vα è Vβ – вариабельные районы α - и β -цепей; Акт. ц. – активные центры антител и РТК. Прямоугольники – повторяющиеся сходные звенья (домены) в структуре полипептидных цепей; М – клеточная мембрана (Из: Абелев, 1996 и Kuby, 1994, p. 113).
у н и к а л ь н о м у г е н е т и ч е с к о м у механизму – н е з а в и с и м о м у г е н е т и ч е с к о м у контролю V- è C- р а й о н о в , составляющих одну полипептидную цепь, и сборке гена, контролирующего вариабельный район, из фрагментов в процессе созревания лимфоцита.
З а г а д к а сосуществования константных и в а р и а б е л ь н ы х участковводнойитой
носят название вариабельных (или V) районов.Остальнаячастьмолекулпостоянна и носит название константного (C) района. Вариабельных районов среди молекул антител тысячи, константных – единицы. Главная функция вариабельных районов – образованиеактивныхцентровантителиРТК. Разнообразие активных центров очень велико, не менее 107-108, что вполне достаточно для более или менее специфического распознавания любого произвольно взятого антигена. Таким образом, структура антител, а точнее их активных центров, обеспечивает узнавание любого чужеродного белка или полисахарида, попавшего в организм.
Как же осуществляется контроль синтеза полипептидных цепей, один из районов которых постоянно варьирует при переходе от одного антитела (или РТК) к другому (вариабельный, V-район), а остальные строго постоянны (константные, С-районы). Эта задача решается благодаря
Дополнение 16.1
В 1972 году Дж.М. Эдельман и Р.Р. Портер (G.M. Edelman, R.R. Porter) получили Нобелевскую премию за исследование химической структуры антител.
Рисунок 16.5
à |
|
|
|
|
|
|
|
|
|
ñ |
|
ò |
|
|
|
|
|
|
|
|
|
|
|
|
é |
|
|
|
|
|
|
|
|
|
|
|
|
à |
|
|
|
|
|
|
|
|
|
|
|
|
é |
|
|
|
|
|
|
|
|
|
|
|
|
|
è |
|
|
VH |
|
|
|
|
|
|
|
|
|
|
ù |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
þ |
|
|
|
|
|
|
|
|
|
|
|
|
à |
|
|
|
|
|
|
|
|
|
|
|
ç |
û |
â |
|
|
|
|
|
|
|
|
|
|
ÿ |
|
|
S |
|
|
|
||
|
|
|
|
â |
|
|
|
|
|
CH1 |
|||
|
|
|
ñ |
|
|
|
|
|
|
|
|||
|
|
í |
|
|
|
|
|
S |
|
||||
|
å |
|
|
|
|
|
|
|
|
|
|
||
ã |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
S |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
è |
|
|
|
|
|
|
|
|
|
|
|
|
S |
ò |
|
|
|
|
|
|
|
|
S |
|
|
|
|
í |
|
|
|
|
|
|
|
|
|
|
|
|
S |
À |
|
|
|
VL |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
|
|
CL
CDR
CH1
S
S S
S S
À |
|
|
|
|
íòèã |
|
|
|
|
|
å |
|
|
|
VH |
|
í |
|
|
|
ñ |
|
||
|
|
|
â |
|
|
|
|
ÿ |
|
|
|
|
ç |
|
|
|
|
û |
|
|
|
|
â |
|
|
|
|
|
à |
|
S |
|
|
þ |
S |
|
|
ù |
|
|
|
|
é |
|
|
|
|
|
è |
|
|
|
S |
à |
|
|
|
|
ñ |
S |
|
S |
|
é |
|
|
|
ò |
|
|
|
|
|
|
|
|
|
|
VL |
S |
|
|
|
|
S |
|
|
|
|
CL
CH2 |
S |
S |
CH2 |
|
S |
S |
|||
|
|
|||
CH3 |
S |
S |
CH3 |
|
S |
S |
|||
|
|
á
Антиген
Антигенсвязывающий
ñàéò
Легкая Тяжелая цепь цепь
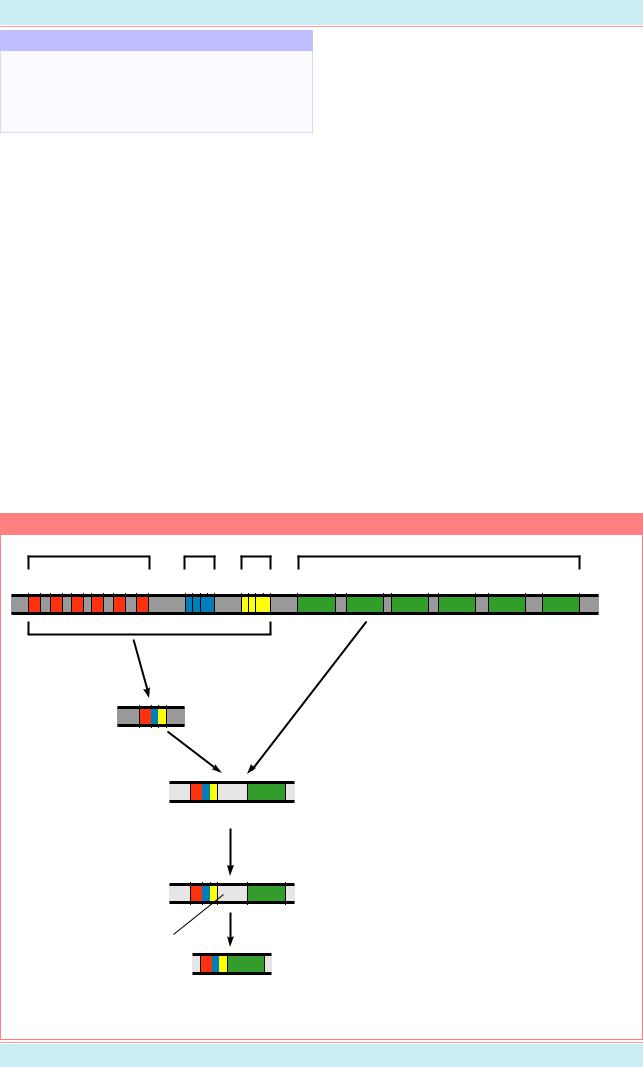
Структура антиген-связывающего участка в молекуле антитела. а. Комплекс антигена и антитела. Указаны вариабельная и константная области легкой (VLCL) и тяжелой (VHCH) цепей, а также отдельные домены константных областей тяжелой цепи (CH1, CH2, CH3) и антигенсвязывающие сайты в вариабельных областях и CDR. б. Структура активного центра в молекуле антитела (Из: Сингер, Берг, 1998, стр. 284, 286).
380
Основы иммуногенетики |
|
|
|
|
|
|
|
|
|
Глава 16 |
|
Дополнение 16.2 |
|
|
|
недифференцированныхлимфоцитовмного– |
|||||||
Нобелевскую премию в 1987 году |
|
от 50 до 1000 для разных цепей и все они |
|||||||||
получил Сузуму Тонегава (Susumu Tonegava) |
|
отличаютсядруготдругапосвоейструктуре. |
|||||||||
за открытие генетических |
принципов |
|
D-гены представленынесколькимидесятками |
||||||||
формирования разнообразия антител. |
|
копий, а J – единичными, причем каждая из |
|||||||||
же полипептидной цепи была разрешена в |
|
копий имеет уникальную структуру. В |
|||||||||
конце 1970х годов С. Тонегавой. Он показал, |
|
процессе созревания лимфоцита фрагменты |
|||||||||
что фрагменты ДНК, кодирующие V- è C- |
|
V-гена объединяются на случайной основе в |
|||||||||
участки,расположенныеввиденепрерывных |
|
V’DJ-ген (Рис. 16.6), причем число |
|||||||||
последовательностей в геноме миеломы |
|
возможных сочетаний равно произведению |
|||||||||
мыши, пространственно разобщены у |
|
числа V’-, D- è J-генов. Для различных цепей |
|||||||||
эмбрионовили в сперматозоидахмыши. |
|
антител или РТК число таких сочетаний |
|||||||||
Ãåíû, контролирующиеструктуруодной |
|
варьирует от тысячи до десятков тысяч. |
|||||||||
полипептидной цепи антитела или РТК, |
|
Кроме того, в процессе сборки возможны |
|||||||||
объединены в семейства, расположенные в |
|
ошибки и изменения в последовательности |
|||||||||
одном участке хромосомы. При этом гены, |
|
нуклеотидов объединяющихся фрагментов, |
|||||||||
соответствующиеV-районам,“разорваны”на |
|
что резко увеличивает число возможных |
|||||||||
2 или 3 фрагмента – основной V’ è îäèí èëè |
|
комбинаций. Дальнейшее разнообразие |
|||||||||
два дополнительных – D è J (D – îò diversity |
|
активных центров возникает за счет |
|||||||||
(разнообразие), J – îòJoining (соединяющий). |
|
объединения вариабельных районов в пары |
|||||||||
V’ – фрагмент гена контролирует первые 95 |
|
цепей, составляющих этот центр. Таким |
|||||||||
аминокислот в V-доменах, D – îò 2 äî 10 è J |
|
образом, благодаря сборке V-ãåíà èç |
|||||||||
– îò 5 äî 15). V’-фрагментов в геноме |
|
фрагментовиобразованияактивныхцентров |
|||||||||
Рисунок 16.6 |
|
|
|
|
|
|
|
|
|
|
|
V ãåíû |
D ãåíû J ãåíû |
|
|
C ãåíû |
|
|
|
|
|||
1 2 3 4 5 n |
|
|
1 |
2 |
3 |
4 |
5 |
|
|
n |
|
|
Объединение |
|
|
|
|
|
|
|
|
|
|
|
отдельных |
|
|
|
|
|
|
|
|
|
|
|
V, D и J генов |
Один из C генов |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|||
Полный V ген, |
|
|
|
|
|
|
|
|
|
|
|
готовый для |
|
|
|
|
|
|
|
|
|
|
|
соединения с |
|
|
|
|
|
|
|
|
|
|
|
C геном |
|
|
|
|
Схема |
|
объединения |
генов, |
|||
|
|
|
|
|
|
||||||
|
V ãåí |
C ãåí |
|
|
кодирующих тяжелую цепь антител. |
||||||
|
|
Транскрипция |
Отобранные D-, и J- сегменты |
||||||||
|
|
перемещаются |
èç |
|
различных |
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
районов хромосомы и формируют |
||||||
|
|
|
|
|
вариабельный |
ãåí, |
|
который |
|||
|
|
Процессинг мРНК |
соединяется с одним из константных |
||||||||
Интрон |
С–генов. |
Интрон |
|
между |
|||||||
|
|
|
|
|
вариабельной |
è |
константной |
||||
|
|
|
|
|
последовательностями удаляется из |
||||||
|
Зрелая мРНК |
|
|
РНК-транскрипта, в результате чего |
|||||||
|
тяжелой цепи |
|
|
образуется молекула мРНК. |
|||||||
|
|
|
|
|
|
|
|
|
|
|
381 |

Глава 16 |
Основы иммуногенетики |
|
|
из разных цепей, создается 107-108 уникальных по своей структуре участков молекулы антител, среди которых всегда найдутся способные взаимодействовать с любым произвольно взятым антигеном. Все это разнообразие и составляет репертуар антител. Следует подчеркнуть, что этот репертуар возникает до встречи с антигеном и независимо от антигена и что большая часть набора антител не потребуется в течение всей жизни особи.
Эти антитела присутствуют на поверхности лимфоцитов, образуя там антиген-распознающие рецепторы. Чрезвычайно важно, что на поверхности однойклеткинаходятсяантителаоднойитой же специфичности. Один лимфоцит может синтезировать антитела только одной специфичности, не отличающиеся друг от друга по структуре активного центра. Это формулируетсякакпринцип“одинлимфоцит
– одно антитело”.
Каким же образом антиген, попадая в организм,вызываетусиленныйсинтезименно тех антител, которые специфично реагируют только с ним? Ответ на этот вопрос дала теория селекции клонов австралийского исследователя Ф.М. Бернета. Согласно этой теории, высказанной в 1957 году и полностьюподтвержденной последующими экспериментами, одна клетка синтезирует лишь один тип антител, которые локализуются на ее поверхности. Роль антигена заключается лишь в том, чтобы найти клетку, несущую на своей мембране антитело, реагирующее именно с ним, и активировать эту клетку. Активированный лимфоцит вступает в деление и дифференцировку. В результате из одной клетки возникает 500-1000 генетически идентичных клеток (клон), синтезирующих один и тот же тип антител, способных специфически распознавать антиген и
Дополнение 16.3
Нобелевскаяпремия1960годабылаприсуждена Ф.М. Бернету и П.Б. Медавару (F.M. Bernet, P.B. Medawar) за открытие приобретенной иммунологической толерантности.
соединяться с ним. В результате дальнейшей дифференцировкилимфоцитпревращаетсяв клетку, не только синтезирующую данное антитело, но и секретирующую его в окружающуюсреду.Такимобразом,функции антигена - найти соответствующий ему лимфоцит, вызвать его деление и дифференцировку в клетку, секретирующую антитела.Вэтомизаключаетсясутьимунного ответа: в селекции нужных клонов и их стимуляциикделению.Динамикапервичного и повторного ответов, согласно теории Бернета, - это отражение динамики размноженияклоновклеток,продуцирующих антителакданномуантигену.Толерантность– утратаклонаклетоквследствиеихконтактас антигеномвпроцессесозреваниялимфоцита.
Для того, чтобы чужеродный белковый антиген опознавался Т-клетками, он должен деградировать на небольшие пептиды, формирующие физические комплексы с молекуламибелковклассаI èëèII,кодируемых генамиМНС(локусгистосовместимости).Это превращение белков в МНС-связанные пептидные фрагменты называется процессингом антигена(Рис.16.7).
В результате процессинга пептиды в комплексе с белками МНС появляются на мембранет.н.антиген-представляющихклеток (макрофаги, B-лимфоциты, дендритные клетки). Затем Т-клетки опознают этот комплексантигенаиМНСбелков,причемCD4 TC-клетки связываются с клетками, содержащими на мембране белки класса II MHC, àCD8 TC-клетки-классаI ÌÍÑ.
У человека белки классов I è II локуса МНСкодируютсягенами,расположеннымив кластере HLA хромосомы 6, ó ìûøè – â H-2 комплексе хромосомы 17 (Рис. 16.8).
Дополнение 16.4
Б. Бенасерраф, Ж. Доссе и Дж. Снелл (B. Benacerraf, J. Dausset, G. Snell) получили Нобелевскую премию 1980 года за открытие генетически детерминированных структур на поверхности клеток, которые регулируют иммунологические реакции.
382

Основы иммуногенетики |
|
|
|
|
|
|
|
|
Глава 16 |
|||||
Рисунок 16.7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
à |
|
Комплекс пептида и белка |
á |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
класса II MHC |
|
Комплекс пептида |
|
Вирусный пептид и |
|
|
|
|||||
|
|
|
|
|
|
|
белок класса I MHC |
|
|
|
||||
|
|
|
|
|
|
и белка класса I MHC |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
||||
Антиген, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
захватываемый |
|
|
|
|
|
|
|
Везикула |
|
|
|
|||
клеткой |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
Комплекс Гольджи |
|
|
|
|
|
|
|
|
Пептиды |
|
|
|
|
|
Полисома |
|
|
|
|
|
|
|
|
антигена |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Класс II MHC |
Вирусные |
|
|
Шероховатый |
|
|
||||
|
|
|
|
|
|
пептиды |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
эндоплазматический |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
Вирусная мРНК |
ретикулюм |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
ßäðî |
|
|
|
|
|
|
|
ßäðî |
|
|
|
|
|
|
Вирусная ДНК |
|
|
|
|
|
|
|
|
|
|
|
|
Вирус |
|
|
|
|
|
|
Процессинг экзогенных (а) и эндогенных (б) антигенов (Из: Kuby, 1994, p. 16). |
|
|
||||||||||||
Рисунок 16.8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
комплекс у мыши |
|
|
|
|
|
|
|
|
|
|
|
|
||
комплекс |
|
|
|
|
|
|
H-2 |
|
|
|
|
Tla |
||
класс |
I |
|
|
II |
|
|
|
III |
|
|
I |
|
I |
I |
MHC |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
район |
K |
|
IA |
IE |
|
|
|
S |
|
|
D |
|
Qa |
Tla |
|
|
|
|
|
|
|
|
|
фактор |
|
|
|
|
|
продукты |
|
|
IA |
IE |
белки |
|
опухолевого |
|
|
|
Tla, |
|||
H-2K |
|
|
некроза |
H-2D |
H-2L |
Qa |
||||||||
генов |
αββ |
αββ * |
комплемента |
|
Qa |
|||||||||
|
|
|
|
|
|
|
|
TNF-α TNF−ββ |
|
|
|
|
||
комплекс у человека |
|
|
|
|
|
|
|
|
|
|
|
|||
комплекс |
|
|
|
|
|
|
|
HLA |
|
|
|
|
|
|
класс |
|
|
II |
|
|
|
III |
|
|
|
I |
|
|
|
MHC |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
район |
DP |
DQ |
DR |
|
C4, C2, BF |
|
|
B |
C |
|
A |
|||
|
|
|
|
|
|
|
|
фактор |
|
|
|
|
||
продукты |
DP |
DQ |
DR |
белки |
|
|
опухолевого |
|
|
|
|
|||
|
|
некроза |
HLA-B |
HLA-C |
HLA-A |
|||||||||
генов |
αββ |
|
αββ |
αββ |
комплемента |
|
||||||||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
TNF-α TNF−ββ |
|
|
|
|
||
Схематичное изображение главных локусов гистосовместимости у мыши и человека (Из: Kuby, |
||||||||||||||
1994, p. 210). Желтым цветом показаны гены класса I, зеленым – класса II, фиолетовым - класа III. |
||||||||||||||
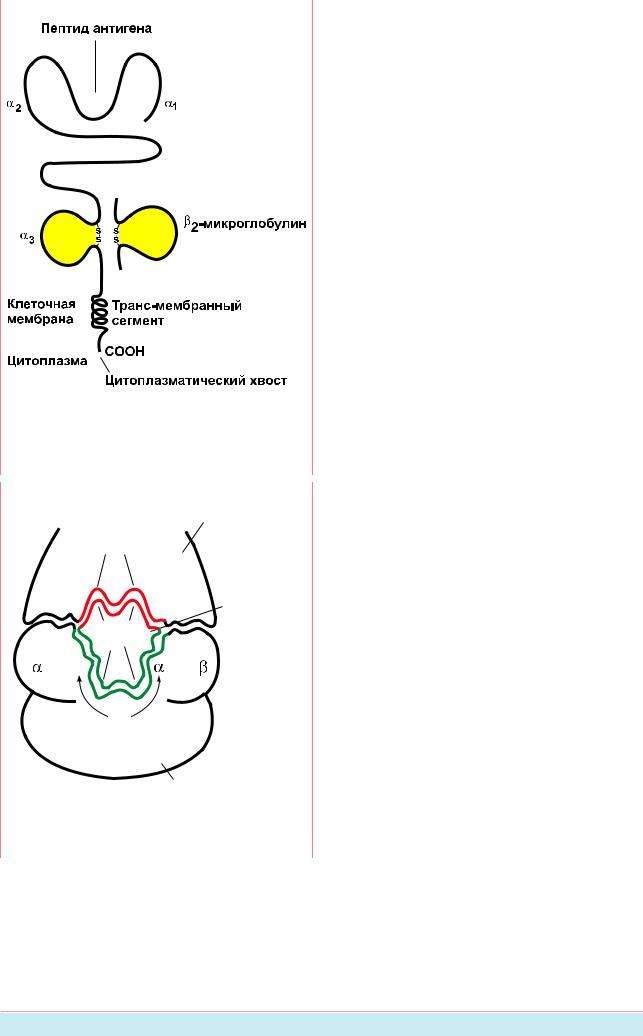
Молекулы MHC класса I состоят из |
|
èK, D/I локусаH2 ó ìûøè). β 2-микроглобулин |
||||||||||||
тяжелой α цепи, соединенной нековалентно с |
|
является инвариантным белком размером 12 |
||||||||||||
легкойцепью–β 2 – микроглобулина(Рис.16.9). |
|
êDa икодируетсяневлокусеМНС,авдругой |
||||||||||||
α -цепь – это транс-мембранный белок |
|
хромосоме. Взаимодействие антигена, Т- |
||||||||||||
размером 45кDa, кодируемый локусом МНС |
|
рецепторовимолекулыМНСпоказанонаРис. |
||||||||||||
классаI(геныA, B èC локусаHLA у человека |
|
16.10. |
|
|
|
|
|
|||||||
383
Глава 16 |
Основы иммуногенетики |
|
|
|
ассоциации с молекулами МНС класса II è |
Рисунок 16.9 |
|
|
функционируют, главным образом, как |
|
хелперы, в то время как CD8+T-клетки |
|
распознаютантигенвассоциациисмолекулами |
|
МНС класса I и функционируют, главным |
|
образом, как цитотоксические клетки CD4 – |
|
это гликопротеин, содержащий четыре |
|
иммуноглобулин-подобных домена, CD8 – |
|
представлен чаще всего гетеродимером αβ , |
|
связаннымдисульфиднымисвязями. |
|
|
|
|
|
|
Литература к разделу 16.1. |
|
|
|
|
|
|
|
Абелев Г.И. Основы иммунитета. Соросовский |
|
|
|
|
|
|
|
образовательный журнал 5: 4-10, 1996. |
|
|
|
|
|
|
|
Галактионов В.Г. Как работает иммунная |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
система. Соросовский образовательный |
|
|
|
|
|
|
|
журнал 12: 2-9, 1997. |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
Инге-Вечтомов С.Г. Генетика с основами |
|
|
|
|
|
|
|
селекции. Москва, Высшая школа, 433- |
|
Схема молекул МНС класса I (Èç: Kuby, 1994, |
435, 1989. |
||||||
Попова Н.А. Иммунология. Новосибирск, |
|||||||
p. 215). Домены α 3 è β 2 – микроглобулинов |
|||||||
Новосибирский государственный |
|||||||
имеют характерную для иммуноглобулинов |
университет, 1-96, 1999. |
||||||
структуру (желтый цвет). |
|
|
|||||
|
|
Ройт А. Основы иммунологии. Москва, Мир, |
|||||
|
|
|
|
|
|
||
|
|
|
|
|
|
1-327, 1991. |
|
Рисунок 16.10 |
|
|
|
||||
|
|
|
Сингер М., Берг П. Гены и геномы. Т. 2, 283- |
||||
|
|
рецептор T-клеток |
|||||
|
|
302, 1998. |
|||||
|
|
|
|
|
|
||
|
|
CDR3 |
|
|
|
Щелкунов С.Н. Эпидемия СПИДа. |
|
|
|
|
|
|
Соросовский образовательный журнал |
||
|
|
|
|
|
|
||
|
|
|
|
|
|
11: 22-28, 1999. |
|
|
CDR1/2 |
|
CDR1/2 |
пептид |
Alberts B., Bray D., Lewis J., Raff M., Roberts K., |
||
|
|
эпитоп |
|
антигена |
Watson J.D. Molecular biology of the cell |
||
|
|
|
|
|
(Third edition). Garland Publishing, Inc. New |
||
|
MHC |
агритоп |
MHC |
||||
|
|
York, London, 1195-1254, 1994. |
|||||
1 |
|
2 èëè |
1 |
|
Kuby J. Immunology, second edition New York, |
||
|
|
|
|
|
|
W.H. Freeman, 1-660, 1994. |
|
|
|
16.2. Некоторые отклонения |
|
|
в работе иммунной системы |
молекула MHC |
16.2.1. Синдром |
|
Взаимодействие сайтов пептида антигена с |
|
|
|
приобретенного |
|
рецептором T-клеток и МНС-молекулой (Из: |
||
Kuby, 1994, p. 268). |
иммунодефицита – СПИД |
|
|
|
|
МолекулыМНСклассаII такжесодержат |
Болезнью иммунной системы является |
|
двецепи–α иβ . Обецепикодируютсягенами |
СПИД (синдром приобретенного |
|
района D комплекса HLA (у человека) или |
иммунодефицита). Возбудителем является |
|
района I комплексаH-2 (ó ìûøè). |
ретровирус, получивший название Вируса |
|
Важными ко-рецепторами являются |
иммунодефицита человека – ВИЧ. На |
|
трансмембранные молекулы CD4 è CD8. |
вирусной молекуле РНК с помощью |
|
CD4+T-клетки распознают антиген в |
обратнойтранскриптазысинтезируетсяДНК, |
|
384

Основы иммуногенетики |
Глава 16 |
|
|
встраивающаяся в геном. В результате транскрипции провирусной ДНК и сборки вирусных частиц клетка-хозяин гибнет. Эта болезнь сопровождается развитием у больных глубокой иммунной недостаточности, проявляющейся в том, что безопасные для здорового человека микроорганизмы приобретают способность вызывать тяжелые инфекционные заболевания. Отличительным свойством ВИЧ является то, что он адсорбируется на поверхности только тех клеток, которые содержат мембранный белок, называемый антигеном СD4. Такой поверхностный антиген в основном содержат Т - лимфоциты, играющие важнейшую роль0в координацииработывсейиммуннойсистемы человека. Уничтожение вирусом лимфоцитов этого типа и обуславливает иммуносупрессорное действие ВИЧ (см. Дополнение 16.5).
Дополнение 16.5
Первые случаи СПИДа были зарегистрированы у гомосексуалистов в США в 1981 году. Причины и пути передачи СПИДа сначала были неясны. Однако уже в 1983 году усилиями двух лабораторий в США и Франции удалось открыть возбудитель СПИДа. Им оказался ретровирус, получивший название “вирус иммунодефицита человека” (ВИЧ).
Источником ВИЧ–инфекции является человек, больной СПИДом или вирусоноситель. ВИЧ обнаружен в крови, сперме, грудном молоке, секрете шейки матки, слюне, слезной жидкости, моче. Однако реально инфекционными являются лишь кровь, сперма, секрет шейки матки и грудное молоко. ВИЧ-инфекция не передается от больного к здоровому при обычном общении. Не выявлено ни одного случая передачи ВИЧ через укусы кровососущих насекомых, таких, как комары, вши или постельные клопы. Обычным путем распространения вируса являются половые контакты (вероятность заражения 10-70%). Другой путь передачи вируса – через зараженную донорскую кровь или ее компоненты (вероятность заражения близка к 100%), донорские органы и сперму. Чрезвычайно быстро ВИЧ распространяется
16.2.2. Моноклональные антитела
При введении даже одного антигена в организме в ответ возникает большое семейство антител. Связано это с тем, что каждоеантителовырабатываетсяненабелок или полисахарид, а на их детерминантные группы. В белках детерминантная группа состоит из 6-8 аминокислот, формирующих пространственную структуру данной молекулы. В одной молекуле белка может быть около десятка разных детерминант. В полисахаридах детерминантные группы формируются 3-6 остатками моносахаридов. И даже к одной детерминанте образуется несколько антител, несколько различающихся по свойствам.
Длянекоторыхцелей,впервуюочередь экспериментальных, требуются не многокомпонентные смеси антител, а отдельные антитела, направленные лишь к одной детерминанте антигена –
между наркоманами, использующими общие иглы для внутривенного введения наркотиков. От инфицированной матери к ребенку ВИЧ передается до или во время родов с вероятностью 25-50%. Кроме того, ребенок может быть заражен ВИЧ во время кормления грудью.
Точное время и место начала развития ВИЧ/СПИД неизвестны. Однако полагают, что ВИЧ существовал в небольших изолированных поселениях где-нибудь в Центральной Африке, поскольку антитела к ВИЧ были обнаружены в донорской крови, полученной в Заире еще в 1959 году.
К настоящему времени эпидемия СПИДа достигла внушительных размеров: к концу 1996 года в мире было выявлено более 8,4 млн. случаев СПИДа, 74% этих случаев приходилось на Африку, 8 % – на Северную Америку, 7% - на Латинскую Америку, 6% - на Азию, 4% - Европу, и 1% - на Австралию и Новую Зеландию. При этом ВИЧ - инфицированных на тот момент превысило 24 млн. человек (из них 16 млн. приходилось на Африку и лишь 29 тыс. – на Восточную Европу и Центральную Азию (Из: Щелкунов, 1999).
385
