
- •Московский государственный машиностроительный университет (мами)
- •Газовая динамика
- •Москва - 2015
- •Глава 1. Основные понятия газовой динамики и физические свойства жидкостей и газов …………………………………………………….
- •Глава 3. Уравнения газовой динамики элементарной струйки
- •3.1. Уравнение неразрывности
- •3.2. Уравнение количества движения (первое уравнение Эйлера)
- •3.3. Уравнение моментов количества движения (второе уравнение Эйлера)
- •3.4. Уравнение энергии
- •Механическая форма уравнения энергии
- •3.5. Параметры торможения
- •3.6. Примеры расчётов параметров движущегося газа
- •Глава 4. Одномерное движение газа
- •4.1. Уравнение обращения воздействий
- •4.2. Газодинамическая форма уравнения расхода
- •4.3. Уравнения количества движения в полных импульсах
- •4.4. Примеры расчёта газовых течений с помощью уравнений расхода и количества движения
- •Глава 5. Скачки уплотнения и ускорение газового потока
- •5.1. Плоская ударная волна и прямой скачок уплотнения
- •5.2. Основное кинематическое и основное динамическое соотношения для прямого скачка уплотнения
- •5.3. Косые скачки уплотнения
- •5.4. Обтекание внешнего тупого угла сверхзвуковым потоком (течение Прандтля - Майера)
3.4. Уравнение энергии
Согласно первому закону термодинамики, который выражает закон сохранения энергии, тепло, подведённое к элементу жидкости (газа), идёт на совершение технической работы, работы сил трения и на изменение его внутренней, потенциальной и кинетической энергии. В дифференциальной форме уравнение энергии для единицы массы газа имеет следующий вид:
dq
= dqн +
dqтр =
dLтех +
dLтр + dU
+ gdz d d
d ,
(3.13)
,
(3.13)
где
qн
– внешнее (наружное) тепло, подведённое
к газу, qтр
- внутреннее
тепло, подведённое к газу при действии
сил трения; Lтех–
техническая
работа (компрессор, турбина и др.),
Lтр
– работа
сил трения, U
– внутренняя
энергия единицы массы газа,
gz
– потенциальная
энергия уровня,
 - потенциальная
энергия давления единицы массы газа,
- потенциальная
энергия давления единицы массы газа,
 -
кинетическая энергия единицы массы
газа.
-
кинетическая энергия единицы массы
газа.
Все
указанные величины измеряются в
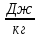 .
.
После интегрирования (3.13) вдоль струйки тока получаем (qтр и Lтр равны и, соответственно, сокращаются) :
Qн
– Lтех
= g(z2
– z1) +
U2 – U1
+
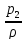 -
- +
+ (3.14)
(3.14)
Введём в рассмотрение энтальпию газаi = cpT, гдеcp–теплоёмкость при постоянном давлении. Из курса термодинамики известно уравнение Майера:
cp – cv = R, (3.15)
где cv – теплоёмкость при постоянном объёме. Далее имеем
cv = сp – R
U = cvT = cpT – RT (3.16)
Используя уравнение состояния (1.1) , запишем уравнение (3.16) в следующем виде:
U
= cpT
-
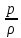 =i -
=i -
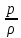 (3.17)
(3.17)
Подставляя (3.17) в уравнение энергии (3.14), получаем уравнение энергии в форме энтальпии:
Qн
– Lтех =
g(z2
– z1)
+ i2
– i1
+
 (3.18)
(3.18)
Обычно при исследовании процессов в тепловых двигателях изменением потенциальной энергии уровня можно пренебречь. Тогда уравнение энтальпии принимает следующий вид:
Qн
– Lтех
= i2 – i1
+
 (3.19)
(3.19)
При отсутствии теплообмена с окружающей средой и технической работы, то есть в случае теплоизолированного течения газа, получаем уравнение энтальпии в следующем виде:
i2
+
 = i +
= i + (3.20)
(3.20)
откуда следует, что в случае полного торможения потока газа энтальпия достигает максимального значения и обозначается как энтальпия торможения i*, или полная энтальпия:
i*
=
i
+
 (3.21)
(3.21)
Поскольку i* = cpT*, то температура T* называется температурой торможения.
Механическая форма уравнения энергии
Запишем уравнение энергии в дифференциальной форме и вычтем из него уравнение первого закона термодинамики:
dQ
–dLтех
= dU
+ gdz
+ d(pv)
+ d + dLтр
+ dLтр
-
dQ = dU – pdv
-dLтех
=
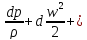 gdz
+ dLтр
(3.22)
gdz
+ dLтр
(3.22)
[d(pv)
– pdv
= pdv
+ vdp
– pdv
= vdp
=
 ]
]
Мы получили уравнение энергии в механической форме для элементарной струйки тока. Интегрируя вдоль элементарной струйки, получим уравнение в интегральном виде, которое носит название уравнения Бернулли:
-Lтех
=
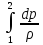 +
+ +g(z2
– z1)
+ Lтр
(3.23)
+g(z2
– z1)
+ Lтр
(3.23)
В Главе второй интеграл Бернулли был нами получен из рассмотрения уравнений Эйлера. В гидравлике и газовой динамике применяется более простая форма уравнения Бернулли, когда техническая работа и работа сил трения равны нулю (Lтех = Lтр = 0). Если рассматривать горизонтальное течение жидкости без потерь, то уравнение (3.23) принимает вид:
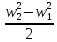 +
+
 = 0(3.24)
= 0(3.24)
Если на участке 1 – 2 элементарной струйки плотность жидкости остаётся постоянной, то интеграл в уравнении (3.24) будет равен:
 =
=
 .
.
В результате уравнение (3.24) приобретает вид уравнения для идеальной несжимаемой жидкости, полученное Бернулли в 1738 году:
gz1
+
 = gz2
+
= gz2
+
 = const,
(3.25)
= const,
(3.25)
где
gz
– напор высоты уровня,
 – потенциальная энергия уровня
(пьезометрический напор),
– потенциальная энергия уровня
(пьезометрический напор), - скоростной
напор. Размерность всех членов уравнения
(3.25) –
- скоростной
напор. Размерность всех членов уравнения
(3.25) –

Применение
уравнения Бернулли для сжимаемой
жидкости связано с вычислением интеграла
 ,
которое зависит от вида термодинамического
процесса. Предоставляя студенту
самостоятельно взять интегралы для
изохорического, изобарического и
изотермического процессов (что
рассматривалось в курсе термодинамики),
проведём его вычисление для адиабатического
процесса, который имеет наибольшее
значение в газовой динамике двигателей.
Адиабатический процесс предполагает
отсутствие теплообмена с внешней средой.При
этом, если имеет место выделение тепла
от работы сил трения, то энтропия процесса
увеличивается, но сам процесс остаётся
адиабатическим.
Итак, считаем, что состояние газа
изменяется по идеальной адиабате:
,
которое зависит от вида термодинамического
процесса. Предоставляя студенту
самостоятельно взять интегралы для
изохорического, изобарического и
изотермического процессов (что
рассматривалось в курсе термодинамики),
проведём его вычисление для адиабатического
процесса, который имеет наибольшее
значение в газовой динамике двигателей.
Адиабатический процесс предполагает
отсутствие теплообмена с внешней средой.При
этом, если имеет место выделение тепла
от работы сил трения, то энтропия процесса
увеличивается, но сам процесс остаётся
адиабатическим.
Итак, считаем, что состояние газа
изменяется по идеальной адиабате:
 =
const
=
const
Тогда
ρ
= ρ1( )1/k
)1/k
 =
=
 =
= k-1|k-1]
(3.26)
k-1|k-1]
(3.26)
Подставляя (3.26) в (3.24), получаем:
 –1]
+
–1]
+ = 0
(3.27)
= 0
(3.27)
