- •34. Несжимаемая жидкость. Уравнение непрерывности для несжимаемой жидкости.
- •35.Уравнение Бернулли. Какой из законов сохранения выражает уравнение Бернулли?
- •36. Макроскопическая система. Что называется молем вещества? Молярная масса, число Авогадро, его величина и размерность.
- •37. Тепловое равновесие.
- •38. Идеальный газ. Основное уравнение молекулярно-кинетической теории идеального газа.
- •39. Связь средней кинетической энергии молекул газа с его температурой.
- •40. Постоянная Больцмана, ее величина, размерность, физический смысл.
- •41. Уравнение Клапейрона - Менделеева. Физический смысл универсальной газовой постоянной.
- •42. Давление и температура с точки зрения молекулярно кинетической теории.
- •43.Среднеквадратичная скорость молекул газа.
- •44.Уравнение изобарного процесса. Его график в координатах pv, pt, vt.
- •45.Уравнение изохорного процесса. Его график в координатах pv, pt, vt.
- •46.Уравнение изотермического процесса. Его график в координатах pv, pt, vt.
- •48.Внутренняя энергия.
- •49. Формула работы для элементарного квазистационарного процесса. Геометрическое изображение работы в координатах pv.
- •50. Адиабатический процесс. Уравнение Пуассона.
- •51.Первое начало термодинамики. Теплоемкость тела, её единицы измерения. Молярная и удельная теплоемкости.
- •52.Первый закон термодинамики для изохорного процесса. Внутренняя энергия идеального газа.
- •53. Первый закон термодинамики для изобарного процесса.
- •54. Формула Майера для теплоемкостей.
- •55.Первый закон термодинамики для изотермического и для адиабатического процессов.
- •56.Второе начало термодинамики.
- •57. Энтропия. Обратимые и необратимые процессы. Изменение энтропии замкнутой системы при необратимом процессе.
- •Обратимый цикл Карно
- •Необратимый цикл Карно
- •58. Циклические процессы.
- •59.Функция распределения физической величины. Распределение Максвелла для скоростей молекул газа.
- •60. Изменение распределения Максвелла при изменении температуры газа. Вид распределения Максвелла в зависимости от молекулярной массы газа.
- •61. Среднеквадратичная скорость. Наиболее вероятная скорость молекул.
- •62. Распределение Больцмана
- •63. Барометрическая формула
- •64. Закон сохранения электрического заряда. Элементарный электрический заряд.
- •65. Закон Кулона (в системе си).
- •66. Напряженность электрического поля, единицы измерения. Напряженность поля точечного заряда.
- •67. Силовые линии (линии напряженности) электрического поля. Однородное поле
56.Второе начало термодинамики.
В 1824 г. Карно доказал, что для работы теплового двигателя необходимо не менее двух источников теплоты с различными температурами. Невозможность создания вечного двигателя второго рода подтверждается вторым началом термодинамики.
Приведем некоторые формулировки второго начала термодинамики:
Невозможен процесс, единственным результатом которого является превращение всей теплоты, полученной от нагревателя в эквивалентную ей работу (формулировка Кельвина).
Невозможен вечный двигатель второго рода (формулировка Томпсона – Планка).
Невозможен процесс, единственным результатом которого является передача энергии в форме теплоты от холодного тела к горячему (формулировка Клаузиуса).
Энтропия замкнутой системы при любых происходивших в ней процессах не может убывать (или увеличивается, или остается неизменной).
57. Энтропия. Обратимые и необратимые процессы. Изменение энтропии замкнутой системы при необратимом процессе.
Итак, энтропия – отношение полученной или отданной системой теплоты в обратимом процессе к температуре, при которой происходит эта передача.
|
|
|
|
|
Энтропия
– величина аддитивная,
т.е. она равна сумме энтропий всех тел,
входящих в систему: ![]() .
.
Обратимый цикл Карно
Из п. 5.2 мы знаем, что в тепловой машине, работающей по принципу Карно, имеются три тела: холодильник, нагреватель, рабочее тело (газ).
Изменение
энтропии газа в тепловой машине ![]() так
как газ возвращается в исходное состояние.
так
как газ возвращается в исходное состояние.
Изменение
энтропии нагревателя:
![]()
Для
холодильника:
![]()
т.е. S – константа. Таким образом, мы пришли к выражению, полученному в п. 6.1, называемому равенство Клаузиуса.
Необратимый цикл Карно
Мы
знаем, что ![]() т.е.
т.е.
Отсюда 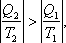 тогда
тогда![]() .
.
Таким образом, это выражение называют неравенством Клаузиуса: при любом необратимом процессе в замкнутой системе энтропия возрастает (dS > 0).
58. Циклические процессы.
Как правило, любая тепловая машина (двигатель) использует циклический процесс. Ее рабочее тело, т.е. термодинамическая система, преобразующая часть полученного тепла в работу, периодически через цикл приходит в начальное состояние.
Так как в результате
циклического процесса внутренняя
энергия не изменяется, т.е. ![]() ,
то из первого начала термодинамики
следует, что совершенная за цикл работа
равна площади петли цикла на диаграмме
p-V и она же равна разности полученной и
отданной за цикл теплоты: A=Q1-Q2.К.п.д.
тепловой машины (цикла) равен отношению
произведенной за цикл работы к полученному
от нагревателя теплу:
,
то из первого начала термодинамики
следует, что совершенная за цикл работа
равна площади петли цикла на диаграмме
p-V и она же равна разности полученной и
отданной за цикл теплоты: A=Q1-Q2.К.п.д.
тепловой машины (цикла) равен отношению
произведенной за цикл работы к полученному
от нагревателя теплу:![]() Заметим,
что тепло распространяется от нагретого
тела к холодному, но не наоборот:
Заметим,
что тепло распространяется от нагретого
тела к холодному, но не наоборот:![]() .Это
утверждает формулировка Клаузиуса второго
начала термодинамики: невозможны такие
процессы,единственным результатом
которых был бы переход тепла от холодного
тела к нагретому.
.Это
утверждает формулировка Клаузиуса второго
начала термодинамики: невозможны такие
процессы,единственным результатом
которых был бы переход тепла от холодного
тела к нагретому.
59.Функция распределения физической величины. Распределение Максвелла для скоростей молекул газа.
ФУНКЦИЯ РАСПРЕДЕЛЕНИЯ – плотность вероятности распределения частиц макроскопической системы по координатам, импульсам или квантовым состояниям. Функция распределения является основной характеристикой самых разнообразных (не только физических) систем, которым свойственно случайное поведение, т.е. случайное изменение состояния системы и, соответственно, ее параметров. Даже в стационарных внешних условиях само состояние системы может быть таким, что результат измерения некоторого его параметра является случайной величиной. Функция распределения в подавляющем большинстве случаев содержит в себе всю возможную и потому исчерпывающую информацию о свойствах таких систем.
Основываясь
на опыте Штерна, можно ожидать, что
наибольшее число молекул будут иметь
какую-то среднюю скорость, а доля быстрых
и медленных молекул не очень велика.
Необходимые измерения показали, что
доля молекул ![]() ,
отнесенная к интервалу скорости Δv,
т.е.
,
отнесенная к интервалу скорости Δv,
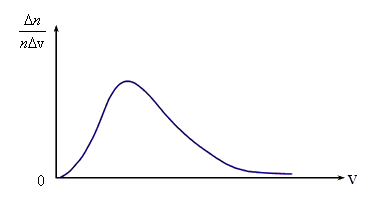
т.е. ![]() ,
имеет вид, показанный на рисунке. Максвелл
в 1859 г. теоретически на основании теории
вероятности определил эту функцию. С
тех пор она называется функцией
распределения молекул по скоростям или
законом Максвелла.
,
имеет вид, показанный на рисунке. Максвелл
в 1859 г. теоретически на основании теории
вероятности определил эту функцию. С
тех пор она называется функцией
распределения молекул по скоростям или
законом Максвелла.
 Аналитически
она выражается формулой
Аналитически
она выражается формулой
где m – масса молекулы, k – постоянная Больцмана.
Установление этой зависимости позволило определить кроме уже известной среднеквадратичной скорости еще две характерные скорости – среднюю и наиболее вероятную. Средняя скорость – это сумма скоростей всех молекул, деленная на общее число всех молекул в единице объема.
Средняя
скорость, подсчитанная на основании
закона Максвелла, выражается формулой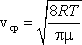
![]()
Наиболее вероятная скорость – это скорость, вблизи которой на единичный интервал скоростей приходится наибольшее число молекул. Она рассчитывается по формуле: