
- •34. Несжимаемая жидкость. Уравнение непрерывности для несжимаемой жидкости.
- •35.Уравнение Бернулли. Какой из законов сохранения выражает уравнение Бернулли?
- •36. Макроскопическая система. Что называется молем вещества? Молярная масса, число Авогадро, его величина и размерность.
- •37. Тепловое равновесие.
- •38. Идеальный газ. Основное уравнение молекулярно-кинетической теории идеального газа.
- •39. Связь средней кинетической энергии молекул газа с его температурой.
- •40. Постоянная Больцмана, ее величина, размерность, физический смысл.
- •41. Уравнение Клапейрона - Менделеева. Физический смысл универсальной газовой постоянной.
- •42. Давление и температура с точки зрения молекулярно кинетической теории.
- •43.Среднеквадратичная скорость молекул газа.
- •44.Уравнение изобарного процесса. Его график в координатах pv, pt, vt.
- •45.Уравнение изохорного процесса. Его график в координатах pv, pt, vt.
- •46.Уравнение изотермического процесса. Его график в координатах pv, pt, vt.
- •48.Внутренняя энергия.
- •49. Формула работы для элементарного квазистационарного процесса. Геометрическое изображение работы в координатах pv.
- •50. Адиабатический процесс. Уравнение Пуассона.
- •51.Первое начало термодинамики. Теплоемкость тела, её единицы измерения. Молярная и удельная теплоемкости.
- •52.Первый закон термодинамики для изохорного процесса. Внутренняя энергия идеального газа.
- •53. Первый закон термодинамики для изобарного процесса.
- •54. Формула Майера для теплоемкостей.
- •55.Первый закон термодинамики для изотермического и для адиабатического процессов.
- •56.Второе начало термодинамики.
- •57. Энтропия. Обратимые и необратимые процессы. Изменение энтропии замкнутой системы при необратимом процессе.
- •Обратимый цикл Карно
- •Необратимый цикл Карно
- •58. Циклические процессы.
- •59.Функция распределения физической величины. Распределение Максвелла для скоростей молекул газа.
- •60. Изменение распределения Максвелла при изменении температуры газа. Вид распределения Максвелла в зависимости от молекулярной массы газа.
- •61. Среднеквадратичная скорость. Наиболее вероятная скорость молекул.
- •62. Распределение Больцмана
- •63. Барометрическая формула
- •64. Закон сохранения электрического заряда. Элементарный электрический заряд.
- •65. Закон Кулона (в системе си).
- •66. Напряженность электрического поля, единицы измерения. Напряженность поля точечного заряда.
- •67. Силовые линии (линии напряженности) электрического поля. Однородное поле
38. Идеальный газ. Основное уравнение молекулярно-кинетической теории идеального газа.
Идеальный газ - это физическая модель газа, взаимодействие между молекулами которого пренебрежительно мало. - вводится для математического описания поведения газов. Реальные разреженные газы ведут себя как идеальный газ! Свойства идеального газа: - взаимодействие между молекулами пренебрежительно мало - расстояние между молекулами много больше размеров молекул - молекулы - это упругие шары - отталкивание молекул возможно только при соударении - движение молекул - по законам Ньютона - давление газа на стенки сосуда - за счет ударов молекул газа
Основное уравнение
МКТ связывает микропараметры частиц (
массу молекулы, среднюю кинетическую
энергию молекул, средний квадрат скорости
молекул) с макропараметрами газа (р -
давление, V - объем, Т - температура).
Давление
газа на стенки сосуда пропорционально
произведению концентрации молекул на
среднюю кинетическую энергию
поступательного движения молекулы.
Основное
уравнение МКТ:![]()
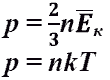
39. Связь средней кинетической энергии молекул газа с его температурой.
Температура — мера средней кинетической энергии молекул.
![]() Средняя
кинетическая энергия поступательного
движения молекулы не зависит от её
природы и пропорциональна абсолютной
температуре газа T. Отсюда следует, что
абсолютная температура является мерой
средней кинетической энергии
молекул.Сравнивая
уравнение состояния идеального газа и
основное уравнение кинетической теории
газов, записанные для одного моля (для
этого число молекул N возьмём
равным числу Авогадро NА),
найдём среднюю кинетическую энергию
одной молекулы:
Средняя
кинетическая энергия поступательного
движения молекулы не зависит от её
природы и пропорциональна абсолютной
температуре газа T. Отсюда следует, что
абсолютная температура является мерой
средней кинетической энергии
молекул.Сравнивая
уравнение состояния идеального газа и
основное уравнение кинетической теории
газов, записанные для одного моля (для
этого число молекул N возьмём
равным числу Авогадро NА),
найдём среднюю кинетическую энергию
одной молекулы:
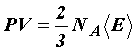 и
и ![]() .Откуда
.Откуда .
.
40. Постоянная Больцмана, ее величина, размерность, физический смысл.
Постоя́нная
Бо́льцмана (![]() или
или ![]() ) — физическая
постоянная,
определяющая связь междутемпературой и энергией.
Названа в честь австрийского физика Людвига
Больцмана,
сделавшего большой вклад в статистическую
физику,
в которой эта постоянная играет ключевую
роль. Её экспериментальное значение
в Международной
системе единиц (СИ) равно:
) — физическая
постоянная,
определяющая связь междутемпературой и энергией.
Названа в честь австрийского физика Людвига
Больцмана,
сделавшего большой вклад в статистическую
физику,
в которой эта постоянная играет ключевую
роль. Её экспериментальное значение
в Международной
системе единиц (СИ) равно:
![]() Дж/К[1].
Дж/К[1].
Постоянная Больцмана дает возможность напрямую связать характеристики микромира с характеристиками макромира — в частности, с показаниями термометра. Вот ключевая формула, устанавливающая это соотношение:
1/2 mv2 = kT
где m и v — соответственно масса и средняя скорость движения молекул газа,Т — температура газа (по абсолютной шкале Кельвина), а k — постоянная Больцмана. Это уравнение прокладывает мостик между двумя мирами, связывая характеристики атомного уровня (в левой части) с объемными свойствами (в правой части), которые можно измерить при помощи человеческих приборов, в данном случае термометров. Эту связь обеспечивает постоянная Больцмана k, равная 1,38 x 10–23 Дж/К.
41. Уравнение Клапейрона - Менделеева. Физический смысл универсальной газовой постоянной.
Для произвольной массы газа состояние газа описывается уравнением Менделеева—Клапейрона: pV = mRT/M, где р — давление, V — объем, m — масса, М — молярная масса, R — универсальная газовая постоянная. Физический смысл универсальной газовой постоянной в том, что она показывает, какую работу совершает один моль идеального газа при изобарном расширении при нагревании на 1 К (R = 8,31 ДжДмоль • К)). Уравнение Менделеева—Клапейрона показывает, что возможно одновременное изменение трех параметров, характеризующих состояние идеального газа. Однако многие процессы в газах, происходящие в природе и осуществляемые в технике, можно рассматривать приближенно как процессы, в которых изменяются лишь два параметра. Особую роль в физике и технике играют три процесса: изотермический, изохорный и изобарный.
