
Методички / Н.Н. Демидова Физика. Методические указания по выполнению контрольных работ для студентов заочной формы обучения (сокращенные сроки обучения на базе среднего проф. образования)
.pdf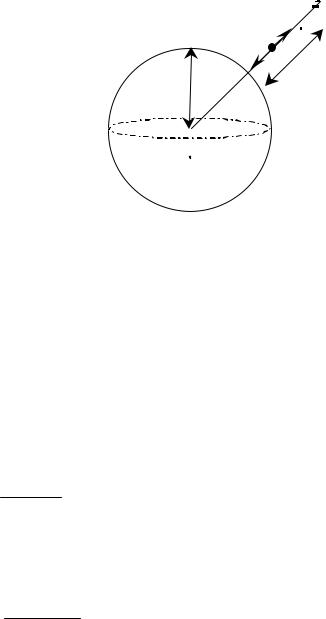
20
равную радиусу RЗ Земли? Считать известным ускорение g свободного падения на поверхности Земли.
|
Дано: |
|
|
|
|
|
РЕШЕНИЕ. |
|
|
|
|
|
|
|
||
|
H = RЗ |
На ракету массой m действует переменная гравитационная сила |
||||||||||||||
|
m |
F (r)= |
G |
m MЗ |
, где МЗ - масса Земли, r = RЗ +h - расстояние |
|||||||||||
|
g |
|
||||||||||||||
|
гр |
|
r |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Aдв - ? |
от центра Земли до ракеты. |
|
|
|
|
|
|
|
|
|
|
||||
|
Работа |
гравитационной силы |
|
|
|
r 2 |
|
|
|
|
|
|
||||
|
|
r2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Aгр = ∫Fгр(r) cosα d r . |
|
|
|
r ∆r |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
F |
|||||||||||
|
|
r1 |
|
|
|
|
1 |
|
H |
|||||||
r |
Угол α между вектором силы |
RЗ |
|
|
|
|
|
|
|
|||||||
Fгри вектором перемещения d rr |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|||||||
равен π (cosα = -1), тогда
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 1.16 |
|
|
|
|
|
|
|
|
||
R З +H |
|
|
m M |
|
|
|
|
|
|
R З +H |
d r |
|
|
|
|
|
|
1 |
|
|
R |
+H |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
Aгр = − ∫ |
|
|
З |
|
|
|
|
|
∫ |
|
|
|
|
|
|
|
З |
|
||||||||||||
G |
|
|
|
d r = −G m MЗ |
|
|
|
|
|
= −G m MЗ |
− |
|
|
|
|
|
|
|
||||||||||||
|
r |
2 |
|
|
|
r |
2 |
|
|
r |
|
|
|
|||||||||||||||||
R З |
|
|
|
|
|
|
|
|
|
|
R З |
|
|
|
|
|
|
|
|
|
|
|
|
R З |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
1 |
|
|
|
1 |
|
|
|
|
|
1 |
|
1 |
|
G m MЗ |
||||||||||||
= −G m M |
|
− |
|
|
|
+ |
|
|
= −G m M |
|
− |
|
|
+ |
|
|
= − |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
З |
|
|
|
|
|
|
|
|
|
|
|
З |
|
|
2 RЗ |
|
|
|
|
|
|
2 RЗ |
||||||||
|
|
|
|
RЗ+ H RЗ |
|
|
|
|
|
|
RЗ |
|
|
|
||||||||||||||||
Учтём, что гравитационная сила на поверхности Земли равна силе тяжести:
Fгр(RЗ )= G mRM2 З = m g ,
З
тогда |
G MЗ = g RЗ2 , |
подставляя, получим работу гравитационной силы:
Aгр = − m g2 RЗ
(которая является работой внешней силы для ракеты). Для подъёма ракеты на высоту H = RЗ двигателям необходимо совершить работу
=
.
Aдв = −Aгр = |
|
. |
|
2 |
|||
|
|

21
ПРИМЕЧАНИЯ 1.7: |
|
|
|
1. При определении ускорения gh свободного падения (задачи |
|||
1.62, 1.65, 1.68) учтите, что m gh = G |
m M |
, где R - радиус плане- |
|
(R+ h)2 |
|||
|
|
||
ты; h – расстояние до поверхности планеты.
2. Закон Гука для деформации сдвига в случае малых углов сдви-
га (задача 1.64) можно записать в виде tg γ γ = ∆hx .
3.При решении задач 1.67, 1.68 будьте внимательны при выборе пределов интегрирования: нижний предел равен бесконечности (∞) (задача 1.67) или h (задача 1.69) верхний предел – радиус RЗ Земли.
4.Определяя работу упругих сил (задачи 1.69, 1.70), дополнительно сжимающих пружину, учтите, что сила упругости Fупр – пере-
∆l2
∫k x d x ,
∆l1
где ∆l1 –первичная деформация, ∆l2 = ∆l1 + ∆l - конечная деформация.
8. Задачи 1.71-1.80 на тему «Элементы теории относительности»
[1, гл. 7]; [2, гл. 7]; [3, §5].
В задачах данной темы рассматриваются релятивистские частицы, движущиеся со скоростью V ~ c (c = 3 108 м/с – скорость света в вакууме). Законы, которыми описывается поведение этих частиц, отличны от законов классической механики.
•Энергия покоящейся частицы массой m0
E0 = m0 c2
•Кинетическая энергия релятивистской частицы
|
|
1 |
|
|
|
2 |
|
|
1 |
|
|
|
V |
|
|
|
|
|
|
|
|
|
|
, (β = |
|
||||
T = E0 |
|
|
|
−1 |
= m0 c |
|
|
|
|
|
−1 |
|
). |
|
1−β |
2 |
|
1−β |
2 |
c |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
Сравните: кинетическая энергия классической частицы (задачи 1.71, 1.72) T = m02V2 и её масса m0 не зависит от скорости V движения час-
тицы, которая много меньше скорости света в вакууме (V << c). Значения массы m0 покоящихся частиц и их энергий Е0 приводятся в прило-

22
жении табл. 5. Для электрона (задачи 1.73, 1.77, 1.78, 1.80), для протона
(задачи 1.76, 1.79).
•Полная энергия Е релятивистской частицы (задача 1.74) равна
E = m c2 = E0 + T = m0 c2 + T .
•Масса m движущейся релятивистской частицы (задачи 1.73, 1.74) отличается от массы m0 покоящейся частицы:
m = m0 |
= |
m0 |
. |
||
1 |
− |
V2 |
|
1−β2 |
|
c2 |
|
|
|
||
|
|
|
|
|
|
•Продольные размеры l тел в инерциальных системах отсчёта, движущихся со скоростью V ~ c относительно неподвижной системы (задача 1.79), определяются из уравнения
l = l0 1− |
V2 |
=l0 |
1−β2 , |
|
c2 |
|
|
где l0 – продольные размеры тел в неподвижной системе отсчёта.
ПРИМЕЧАНИЯ 1.8:
1.Большинство задач данной темы (задачи 1.71 – 1.73, 1.79) решаются с применением формулы кинетической энергии релятивистской частицы.
2.Работа, необходимая для увеличения скорости частицы (задача 1.72), определяет изменение её кинетической энергии:
A= ∆T = T2 −T1.
3.Приставка Г (гига), записанная перед единицей измерения, уве-
личивает её в 109 раз (задача 1.76).
4. Работа совершается за счёт энергии электрического поля, поскольку заряженная частица проходит ускоряющую разность потенциа-
лов ∆ϕ (задачи 1.78-1.79)
A = Q ∆ϕ ,
где Q – заряд частицы. Заряды протона и электрона противоположны по знаку, но одинаковы по величине и равны элементарному заряду:
e= 1,6 10-19 Кл.
5.При решении задач 1.71, 1.80 используйте связь импульса Р, кинетической энергии Т и энергии Е0 покоящейся частицы:
P = 1c T(T+ 2 E0 ),
где с – скорость света в вакууме.

23
МЕТОДИЧЕСКИЕ УКАЗАНИЯ ПО ВЫПОЛНЕНИЮ КОНТРОЛЬНОЙ РАБОТЫ №2
В контрольную работу №2 включены задачи по молекулярной физике и электростатике. По каждому разделу изучаемых тем даются ссылки на учебники. Не приступайте к решению задач, не проработав теоретический материал соответствующего раздела.
1. Задачи 2.1-2.10 на тему «Энергия теплового движения»
[1, §50]; [2, §10.11]; [3, §9].
Энергия теплового движения складывается из энергии молекул, участвующих во всех видах движения. Если молекула жёсткая, то обладает только энергией поступательного и вращательного движений.
•Число степеней свободы молекул. Под числом степеней свободы i
понимают число независимых перемещений, в которых может участвовать молекула.
Для поступательного движения число степеней свободы i =3 (задачи 2.4, 2.5, 2.7).
Для вращательного движения число степеней свободы iвр зависит
от числа атомов в молекуле: |
iвр =0; |
для одноатомной молекулы |
|
двухатомной |
iвр =2 (задача 2.1); |
трёх- и многоатомных |
iвр =3 (задачи 2.2). |
•Закон равномерного распределения энергии по степеням свободы теплового движения, согласно которому на каждую степень свободы в среднем приходится одинаковая энергия:
< ε >= 12 k T ,
где k – постоянная Больцмана; Т - термодинамическая температура.
•Энергия теплового движения Е, определяющая внутреннюю энергию U молекул идеального газа:
E = U = N 2i k T = Mm NA 2i k T = ν 2i R T ,
где N = Mm NA = νNA - число молекул в данной массе газа;
ν = Mm - число молей газа; NA – число Авогадро; M – молярная масса;

24
R = k NA - молярная газовая постоянная.
ПРИМЕР 2.1. Определить среднюю кинетическую энергию молекулы кислорода при температуре 17°С. Во сколько раз она больше средней энергии молекулы гелия при той же температуре? Найти кинетическую энергию вращательного движения всех молекул, содержащихся в 4 г кислорода.
|
Дано: |
|
РЕШЕНИЕ. |
|||||||||||
|
Средняя кинетическая энергия молекулы равна |
|||||||||||||
|
|
|
||||||||||||
t = 17°C, T = 290 K |
|
|
|
|
|
< ε >= |
i |
|||||||
Mк= 32 10-3кг/моль |
|
|
|
|
|
|
|
k T , |
||||||
где i – число |
2 |
|||||||||||||
iк = 5, |
iвр = 2 |
|
степеней свободы; k – постоянная |
|||||||||||
iHe = 3 |
|
Больцмана; Т – температура газа по шкале Кельвина. |
||||||||||||
mк = 4 10-3 кг |
Для двухатомной молекулы кислорода iк = 5, поэтому |
|||||||||||||
|
< ε >к |
|
средняя кинетическая энергия молекулы кислорода |
|||||||||||
|
- ? Евр - ? |
|
|
|
5 |
|
||||||||
|
|
|
|
|
|
|
< ε >к= |
|
k T. |
|||||
|
< ε >He |
|
|
|
||||||||||
|
|
|
|
2 |
||||||||||
|
Для молекулы гелия iHe = 3 и |
< ε >He = |
3 |
k T . |
||||||||||
|
|
|||||||||||||
|
|
|
|
|
|
2 |
|
|
|
|
|
|||
|
Найдём отношение средних кинетических энергий молекулы ки- |
|||||||||||||
слорода и молекулы гелия: |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
< ε >к |
= |
|
5 |
=1,67. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
< ε >He |
3 |
|
|
|
|
|
|
|||
Средняя кинетическая энергия вращательного движения молекулы кислорода
< εвр >к = iвр2 k T .
Число молекул, содержащихся в 4 г кислорода:
N = mк NA . Mк
Средняя кинетическая энергия вращательного движения всех мо-
лекул кислорода: |
Eвр = N < εвр >к= |
m |
к |
NA |
iвр |
k T = |
iвр |
|
m |
к |
R T . |
Mк |
2 |
2 |
|
|
|||||||
|
|
|
|
|
Mк |
||||||

|
|
25 |
|
|
Вычисляем |
Eвр = |
2 4 10−3 кг 8,31Дж/(К моль) 290К |
= 300 Дж. |
|
2 32 10−3 кг/моль |
||||
|
|
|
ПРИМЕЧАНИЯ 2.1:
4.При решении задач 2.4, 2.7-2.10 необходимо дополнительно воспользоваться уравнением Менделеева-Клапейрона.
5.В задаче 2.6 требуется определить молярную внутреннюю энергию идеального газа (энергию одного моля газа).
6.В задачах 2.8-2.10 помимо уравнения Менделеева-Клапейрона, используйте выражение для средней квадратичной скорости
Vкв = 3R T .
M
2. Задачи 2.11-2.20 на тему «Длина свободного пробега молекул. Явле-
ния переноса» [1, §46, 48]; [2, §10.6, 10.8]; [3, §9].
При защите задач данной темы необходимы знания сущности протекающих явлений, изложенных ниже.
Молекулы газа, находясь в хаотическом тепловом движении, сталкиваются друг с другом.
•Среднее число столкновений <Z> определяется по формуле
< Z >=  2 πd2 n < V >< l >,
2 πd2 n < V >< l >,
где d - эффективный диаметр молекулы; n - число молекул в единице объёма (концентрация молекул).
•Средняя арифметическая скорость <V> молекул равна:
< V >=  8πRMT ,
8πRMT ,
где R – универсальная газовая постоянная; T – абсолютная температура;
M – молярная масса газа.
•Средняя длина свободного пробега <l> молекул между двумя последовательными столкновениями:
< l >= |
< V > |
= |
1 |
. |
|
< Z > |
|
2 πd2 n |
|
•Явления переноса связаны с переходом вещества из неравновесного состояния в равновесное. К ним относятся диффузия, внутреннее трение и теплопроводность.

26
•При диффузии переносится масса ∆m вещества через площадку ∆S за время ∆t в направлении, допустим, оси Х:
∆m = −D |
∆ρ |
∆S ∆t , |
D = |
1 |
|
< V > < l >, |
||
∆x |
|
|
|
|||||
|
3 |
|||||||
|
|
|
|
|||||
где D – коэффициент диффузии, зависящий от средней арифметической скорости <V> и средней длины <l> свободного пробега молекул; ∆∆xρ -
градиент плотности.
•Явление внутреннего трения в газах обусловлено переносом импульса молекул из одного слоя в другой. При этом возникает сила F внутреннего трения, действующая между слоями площадью ∆S, движущимися горизонтально:
F = η ∆∆VZ ∆S,
где η - коэффициент внутреннего трения, определяемый через характеристики молекул <V> и <l>, а также плотность вещества ρ:
η = 13 < V > < l > ρ.
•Теплопроводность связана с переносом энергии молекул. Количество теплоты ∆Q, переносимое через площадку ∆S за время ∆t , определяется по формуле
∆Q = −λ ∆∆Tx ∆S ∆t ,
где λ = 13 ρ < V > < l > CV - коэффициент теплопроводности, зави-
сящий от удельной теплоёмкости СV газа при постоянном объёме; ∆∆Tx
- градиент температуры в направлении переноса энергии молекул.
•Удельная теплоёмкость при постоянном объёме
СV = 2i MR ,
где i – число степеней свободы.
ПРИМЕЧАНИЯ 2.2:
1. Нормальные условия (задачи 2.11, 2.13, 2.14, 2.19): Tн.у = 273 К, pн.у = 105 Па.
27
2.Плотность азота при нормальных условиях ρ = 1,25 кг/м3
(задача 2.14).
3.При решении задач 2.17, 2.19, 2.20 дополнительно воспользуйтесь формулой
p = n k T ,
где р – давление газа; k – постоянная Больцмана; n - концентрация молекул.
4.К задаче 2.17 1мм.рт.ст. ≈ 133,3 Па .
3.Задачи 2.21-2.30 на тему «Первое начало термодинамики»
[1, §51,52,54]; [2, гл.9]; [3, §11].
•Первое начало термодинамики. Переданное системе количество теплоты δQ расходуется на увеличение внутренней энергии dU системы
и на совершение системой работы δA над внешними силами:
δQ = dU+ δA .
В применении к тепловым процессам первое начало термодинамики запишется:
•Изотермический процесс протекает при постоянной (T = const) температуре, поэтому внутренняя энергия системы не изменяется dU = 0 и подводимое к системе тепло идёт полностью на совершение системой работы (задачи 2.25, 2.26, 2.28):
δQ = δA .
•Изохорный процесс протекает при постоянном (V = const) объёме, следовательно, δA = 0 и переданное системе тепло идёт только на увеличение внутренней энергии (задача 2.21):
δQ = dU .
•Изобарный процесс протекает при постоянном (р = const) давлении, переданное при этом условии системе тепло расходуется и на увеличение внутренней энергии системы, и на совершение ею работы над внешними телами (задача 2.22-2.24, 2.27).
•Адиабатный процесс протекает без теплообмена с окружающей средой (δQ = 0, энтропия системы постоянна dS = 0), следовательно, при совершении системой работы её внутренняя энергия уменьшается
(задачи 2.29, 2.30):
δA = −dU.
Поскольку внутренняя энергия U является функцией состояния, то её изменение определяется для любого процесса по формуле

28
|
dU = |
i |
|
m |
R dT , |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
2 M |
|
|
|
|
|
|
|
|
|
|
|
||||
в то время как работа А (следовательно, |
|
|
|
|
|
|
|
||||||||||
и количество теплоты Q) зависит от типа Р |
|
|
|
|
|
||||||||||||
|
|
|
1 |
|
|
||||||||||||
процесса и определяется в каждом кон- |
|
|
|
|
|
|
|||||||||||
Р1 |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
||||||||||||
кретном случае. |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|||
Работа при изобарном расширении от V1 |
|
|
|
|
|
|
|
||||||||||
до V2 (рис.2.1, график 1) |
|
|
|
|
|
|
|
|
3 |
|
|
||||||
V |
V |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
A = ∫2 p dV = p ∫2dV = p (V2 − V1 )= p ∆V . |
|
|
|
|
|
|
|||||||||||
0 V1 |
V2 V |
||||||||||||||||
V1 |
V1 |
|
|
|
|
|
|
|
|
|
|
|
Рис. 2.1 |
||||
•Работа при изотермическом расширении от V1 |
|
|
|
||||||||||||||
до V2 (рис.2.1, график 2) |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
V2 |
|
|
m |
V2 dV m |
|
|
|
V |
|
|
|
||||
|
A = ∫p dV = |
|
R T ∫ |
|
|
|
2 |
|
|
|
|||||||
|
|
|
= |
|
R T ln |
|
, |
|
|
||||||||
|
M |
V |
M |
V |
|||||||||||||
|
|
V1 |
|
|
|
V1 |
1 |
|
|
|
|||||||
так как из уравнения Менделеева – Клапейрона: p = Mm RVT .
•Работа при адиабатном расширении от V1 до V2 (рис.2.1,
график 3)
|
i |
|
m |
|
R T1 |
|
m |
|
|
V1 |
|
γ−1 |
|
|
|
|
|
|
|
|
|
|
|||||||
A = −∆U = − |
|
R ∆T = |
|
|
|
|
|
|
, |
|||||
|
|
|
|
|
|
|||||||||
2 |
M |
γ−1 |
1 |
− |
|
|
|
|
||||||
|
|
|
|
M |
V2 |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
где γ = i +i 2 - показатель адиабаты (коэффициент Пуассона).
ПРИМЕР 2.2. Кислород массой 160 г был нагрет при постоянном давлении от t1 = 47°C до t2 = 67°C. Определить количество теплоты Q, поглощённое газом, изменение внутренней энергии ∆U и работу A расширения газа.
Дано:
t1= 47°C, T1= 320K t2= 67°C, T2= 340K M = 32 10-3кг/моль
m = 0,16 кг
Q - ? A - ? ∆U - ?
РЕШЕНИЕ.
Изменение внутренней энергии газа
∆U = 2i Mm R ∆T ,
где m – масса газа; M – молярная масса; i – число степеней свободы газа (для кислорода – двухатомного газа i = 5); R – газовая постоянная; ∆Т – изменение

29
температуры газа.
Количество теплоты, необходимое для нагревания газа при постоянном давлении:
Qp = m Cmp ∆T = Mm CMp ∆T.
Здесь Сmp и CMp – удельная и молярная теплоёмкости газа при постоянном давлении. Молярная теплоёмкость идеального газа при постоянном
давлении равна CMp = 2i R+ R = i +22 R
Работа, совершаемая газом при постоянном давлении:
A = p ∆V = p (V2 −V1 ),
где ∆V – изменение объёма газа. Для определения ∆V воспользуемся уравнением Менделеева – Клапейрона:
|
|
p V = |
m |
|
R T , |
p V |
= |
m |
R T , |
||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
1 |
|
|
|
M |
1 |
|
|
2 |
|
M |
2 |
||||||||
|
|
|
|
|
|
|
|
|
m |
|
|
|
|
|
|
||||||
откуда |
A = p (V |
− V )= |
|
R (T |
−T ) . |
|
|||||||||||||||
|
|
|
|||||||||||||||||||
|
|
2 |
1 |
|
|
M |
2 |
1 |
|
|
|||||||||||
|
|
|
0,16кг |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
Дж |
|
||||||||||
Вычисления: A = |
|
|
|
|
|
8,31 |
|
(340 К−320 К) = 831 Дж. |
|||||||||||||
32 10−3 кг/моль |
К моль |
||||||||||||||||||||
|
|
|
|
|
i |
5 |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
∆U = |
|
|
|
A = 2 831 ДЖ = 2078 Дж. |
|||||||||||||||
|
|
|
2 |
||||||||||||||||||
|
|
Q = |
i + 2 |
A |
= |
5 + 2 |
|
831 ДЖ = 2909 Дж. |
|||||||||||||
|
|
|
|
||||||||||||||||||
|
|
2 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
||||
ПРИМЕЧАНИЯ 2.3: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
1. |
Решение задачи 2.23 упрощается, если конечное изменение |
||||||||||||||||||||
внутренней энергии ∆U и количество теплоты Q выразить так же, как и работу А через параметры p и V, используя уравнение Менделеева - Клапейрона.
2. Решая задачу 2.29, учтите, что нормальные условия: Tн.у = 273 К, pн.у = 105 Па.
4. Задачи 2.31-2.40 на тему «Тепловые машины. Цикл Карно»
[1, §56-59]; [2, §11.1, 11.2]; [3, §11].
В этой теме рассмотрены задачи на определение коэффициента полезного действия (КПД) тепловой машины, работающей по циклу Карно (рис. 2.2).
