
Дипломы-2 / ВЗД-172 / Документы / Производство / ВЫСОКИЕ ТЕХНОЛОГИИ
.pdf
ВТСНТ – 2013
I

 (CH2)4COOH
(CH2)4COOH  123I
123I

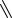
 (CH2)4COOH
(CH2)4COOH
Рис. 5. Введение иозотопной метки
Список литературы
1.Чайковский В.К., Юсубов М.С. Синтез и использование арилиодидов: учебное пособие. Томск: Изд. ТПУ, 2006. 123 с.
2.Stang P.J., Zhdankin V.V. // Chem. Rev. 1996.(96) P. 1123–1178.
3.Kitamura T., Fujiwara Y. // Organic Preparations and Procedures Int., 1997. V. 29. N 4. P. 409–458.
4.Zhdankin V.V., Stang P.J. // Tetrahedron, 1998. V. 57, N 54. P. 10927–10966.
5.Grushin V.V. // Chem. Soc. Rev., 2000. N 29. P. 315–324.
6.Skulski L. // Molecules, 2000. N 5. P. 1331–1371.
7.Zhdankin V.V., Stang P.J. // Chem. Rev., 2002. (102). P. 2523–2584.
8.Victor N.Nemykin, A.Koposov, B.Netzel, M.Yusubov,V.Zhdankin, Inorg.Chem. 2009, V 48 Р. 4908-4917
ИССЛЕДОВАНИЕ ВЛИЯНИЯ ВОДНОГО ЭКСТРАКТА КОРЫ ОСИНЫ НА АКТИВНОСТЬ ФЕРМЕНТОВ
Л. К. Мингажева, студент гр. 4ГМ21 Национальный исследовательский Томский политехнический университет,
634050, г. Томск, пр. Ленина, 30,тел. (3822)-563-861
E-mail: vinsent_422@mail.ru
Описторхоз является одним из самых распространенных и социально значимых гельминтозов в России. Очаги описторхоза имеются в бассейнах рек Обь, Иртыш, Енисей, Волга, Кама, Днепр, Урал, Северная Двина. Регион Западной Сибири признан в числе чрезвычайно напряженных очагов описторхозной инвазии. Пораженность населения самого большого очага описторхоза Обь-Иртышского бассейна рек среди коренных жителей колеблется от 50 до 100%. [1]. Помимо механического повреждения слизистой желчевыводящих путей, аллергических реакций и нарушения функций желудочно-кишечного тракта описторхоз может стать причиной возникновения холангиокарциномы [2].
Препараты коры осины (Populus tremula) используются как противоописторхозное средство [3]. Фитохимическое исследование показало наличие в коре осины салирепозида (1), салицилоил-салицина (2), салицина (3),тремулацина (4), кофейной кислоты (5), феруловой кислоты (6), ванилиновой кислоты (7) и др.[4].
89

Секция 4. Химические и биотехнологии.
С целью изучения фермент ингибирующей активности водного экстракта коры осины и соединений, входящих в ее состав было изучено in vitro их влияние на активность лейцинаминопептидазы, АТФ-азы и амилазы, играющих важную роль в процессах генерирования энергии организма паразита. В качестве источника ферментов были использованы для лейцинаминопептидазы и АТФ-азы - дрожжевой экстракт, для амилазы - слюна.
Анализ ингибирующей активности проводился по методикам, приведенным в [5]. Результаты исследования представлены в таблице 1.
|
|
|
|
|
|
|
|
Таблица1 |
|
Влияние водного экстракта коры осины и некоторых его компонентов |
|||||||||
|
|
на активность ферментов |
|
|
|
||||
Фермент |
Лейцинамино- |
|
АТФ-аза дрожжей |
Слюнная амилаза |
|||||
|
пептидаза дрожжей |
|
|
|
|
|
|
||
|
% инги- |
концент- |
% инги- |
концент- |
% |
концент- |
|||
Ингибитор |
бирова- |
рация, |
бирова- |
рация,мМ |
инги- |
рация, |
|||
ния |
мг/мл |
ния |
|
|
биро- |
мМ |
|
||
|
|
(мМ) |
|
|
|
вания |
|
|
|
Экстракт |
46,8 |
0,53 |
(-) |
16,5 |
0,04 |
(-) |
48,2 |
1,11 |
(-) |
коры осины |
|
|
|
|
|
|
|
|
|
Тремулацин |
49,67 |
0,53 |
(1,01) |
19,07 |
0,04 |
(0,08) |
0 |
0,22 |
(0,54) |
Салирепози |
55,95 |
0,53 |
(1,31) |
0 |
0,04 |
(0,10) |
0 |
0,22 |
(0,70) |
д |
|
|
|
|
|
|
|
|
|
Кофейная |
77,78 |
0,53 |
(2,96) |
15,5 |
0,04 |
(0,23) |
0 |
0,22 |
(1,59) |
кислота |
|
|
|
|
|
|
|
|
|
Салицилоил |
25,88 |
0,53 |
(1,31) |
4,6 |
0,04 |
(0,10) |
0 |
0,22 |
(0,70) |
- салицин |
|
|
|
|
|
|
|
|
|
Салицин |
0 |
0,53 |
(1,86) |
20 |
0,04 |
(0,15) |
0 |
0,22 |
(0,10) |
90 |
|
|
|
|
|
|
|
|
|

ВТСНТ – 2013
Процент ингибирования определялся по формуле 1 для лейцинаминопептидазы и АТФ-азы, и по формуле 2 для амилазы.





























 (1)
(1)
|
|
|
(2), |
|
|
||
где |
– оптическая плотность ферментативной реакции, |
||




 – оптическая плотность при добавлении ингибитора,
– оптическая плотность при добавлении ингибитора,


 - оптическая плотность контрольного образца.
- оптическая плотность контрольного образца.
Экстракт коры осины ингибирует действие всех трех ферментов. Не одно из исследованных веществ не ингибирует действие слюнной амилазы. Тремулацин выступает как эффективный ингибитор лейцинаминопептидазы и АТФазы. Салицилоил-салицин и кофейная кислота ингибируют оба фермента. Салирепозид не эффективен как ингибитор АТФ-азы, но в то же время активно ингибирует лейцинаминопептидазу. Салицин же, напротив, не является ингибитором лейцинаминопептидазы, но инигибирует АТФ-азу на 20%.
Таким образом, ни одно из протестированных индивидуальных соединений не обладает ярко-выраженным ингибирующим действием, превосходящим экстракт (в пересчете на содержание вещества в экстракте). Видимо имеет место потенцированное действие нескольких или многих компонентов экстракта, либо существуют более активные ингибиторы, с неустановленной структурой или известным строением, но не выявленной ферментингибирующей активности.
Список литературы
1.Бронштейн A.M., Токмалаев К.М. Паразитарные болезни человека: протозоозы и гельминтозы. М.: Издательство РУДН, 2002.207с.
2.Smout M. J., Sripa B., Laha T., Mulvenna J., Gasser R. B., Young N. D., ethony J. M., Brindleye P. J., Loukas A. // Mol. BioSyst. 2011. №7.P. 1367–1375.
3.Патент РФ 2162701 «Способ получения средства, обладающего противоописторхозным действием». - БИ. 2001. №4
4.Thieme H., Benecke R. // Die Pharmazie. 1970,№ 25.P. 780.
5.Биссвангер Х. Практическая энзимология. М.: Бином Лаборатория знания, 2010. 328с.
ДИХЛОРКАРБЕНИРОВАНИЕ 1,3-ДИХЛОРПРОПЕНОВ И ИХ ПРОИЗВОДНЫХ
Н.Н.Михайлова, к.х.н., доц., А.Н. Казакова, к.х.н., с.н.с., А.С. Гусева, студент 5 курса ФГБОУ ВПО Уфимский государственный нефтяной технический
университет, 450062, г.Уфа, ул. Космонавтов, 1, тел. (347)242-09-35
E-mail: ximik2008@mail.ru
Дихлоркарбены успешно присоединяются по двойным связям олефинов в условиях межфазного катализа с образованием замещенных гем- дихлорциклопропанов [1-5].
91

Секция 4. Химические и биотехнологии.
Было проведено дихлоркарбенирование стереоизомерных 1,3- дихлорпропенов и их производных в условиях межфазного катализа в результате, которого были получены соответствующие замещенные гем-дихлорциклопропаны (схема 1).
Cl Cl
R |
Cl |
: CCl2 |
R
 Cl
Cl
R=Cl; ОPh; ОBu
Результаты реакции присоединения дихлоркарбена при использовании катализатора триэтилбензиламмоний хлорида (ТЭБАХ) показали, что выход целевых продуктов не превышал 10%. При замене наиболее часто используемого ТЭБАХ на промышленно доступный катализатор – катамин АБ было обнаружено, что выходы продуктов увеличились до 90 %.
Конкурентное карбенирование стереоизомерных 1,3-дихлорпропенов и их производных с хлоралкенами позволило оценить их относительную реакционную способность. Определение реакционной способности по выходу продуктов реакции было проведено при конверсии реагентов менее 35% (таблица 1).
Было определено, что транс-изомер примерно в 2 раза уступает по активности хлористому аллилу и в 20 раз менее активен, чем металлилхлорид. В тоже время изомер совпадает по активности с хлористым аллилом и в 9 раз уступает металлилхлориду. Таким образом, цис-изомер в данной реакции в 2 раза активнее, чем транс-изомер. Видимо это объясняется тем, что в цис-изомере облегчен подход карбена :СCl2 с одной стороны двойной связи, где отсутствуют заместители, тогда как в транс-изомере образованию цикла с одной стороны двойной связи мешает СН2Cl-группа, а с другой стороны атом хлора.
Металлилхлорид почти на порядок активнее хлористого аллила в реакции дихлоркарбенирования.
Доказано, что для дихлокарбена характерно присоединение по двойной связи алкена с полным сохранением геометрии при двойной связи. Была определена относительная реакционная способность цис- и транс- 1,3-дихлорпропенов в реакции дихлоркарбенирования.
Таблица 1
Относительная реакционная способность сis-, trans олефинов
в реакциях дихлоркарбенирования. (0,01 моль олефинов; 60 мл CHCl3 , 64 мл NaOH (50%-ный водный раствор), 0,02 г катамина АБ; 40 ˚С)
|
Исходные соединения |
|
|
Продукты реакции |
|
А/В |
|||||||||||||
|
А |
|
|
|
В |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
CH2 |
Cl |
|
|
|
|
H |
Cl |
|
|
Cl Cl |
Cl |
|
|
Cl Cl |
H |
1,7 |
||
|
|
|
|
||||||||||||||||
Cl |
|
H |
|
|
Cl |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
Cl |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Катамин АБ – торговое наименование. Химическое название – четвертичная аммонийная соль смеси алкилдиметилбензиламмоний хлоридов, где алкил – смесь нормальных алкильных радикалов С10 – С18 или С12 – С14.
92

ВТСНТ – 2013
|
|
|
|
Cl Cl |
Cl Cl |
Cl |
|
||
Cl |
CH2 |
Cl |
Cl |
Cl |
|
Cl |
|
H |
1,0 |
|
H |
H |
|
|
|
||||
|
|
|
|
|
H |
|
|
||
|
|
|
|
|
|
|
|
|
|
Cl |
CH2 |
Cl |
H |
Cl Cl |
Cl Cl |
|
|||
|
|
|
Cl |
|
H |
18 |
|||
|
|
|
|
|
|||||
|
CH3 |
|
|
Cl |
|
|
|
||
|
H |
Cl |
|
|
|
|
|||
|
|
|
|
Cl |
|
||||
|
|
CH3 |
|
H |
|
||||
|
|
|
|
|
|
|
|||
|
CH |
|
|
Cl |
Cl |
Cl |
Cl |
|
|
Cl |
2 |
|
CH2 |
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
11 |
||
|
CH3 |
Cl |
|
|
|
|
|||
|
|
Cl |
|
|
|
|
|||
|
|
|
|
|
|
|
|
||
|
|
|
H |
CH3 |
H |
|
Cl |
|
|
|
|
|
O |
|
Cl |
|
|||
|
|
O |
3C |
|
|
|
H |
|
|
H3C |
O |
Cl |
|
|
H |
O |
|
||
|
|
|
|
|
|
||||
|
H |
|
|
|
|
|
|||
|
|
H |
|
|
Cl Cl |
Cl |
|
||
|
|
|
|
|
H |
1,8 |
|||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
Cl |
Cl |
|
Cl |
Cl |
|
Cl |
H |
O |
Cl |
Cl |
|
H |
O |
H |
|
|
|
|
|||||||
|
|
|
H |
|
|
Cl |
|
||
|
|
|
|
|
|
H |
1,3 |
||
H |
Cl |
|
|
|
|
Cl |
|||
|
|
H |
|
|
|||||
|
|
|
|
|
|
||||
|
|
H |
H |
Cl |
Cl |
Cl |
Cl |
|
|
|
|
|
|
Cl |
|
|
H |
H |
|
Cl |
Cl |
|
|
|
|
|
|
||
|
|
|
|
|
O |
|
|
||
|
|
O |
Cl |
|
|
|
Cl |
|
|
|
|
|
|
H |
|
2,0 |
|||
H |
H |
|
Cl |
|
|
|
|
||
|
|
|
|
|
|
|
|||
|
|
|
|
H |
|
|
|
|
|
|
|
|
H |
Cl |
Cl |
Cl |
Cl |
|
|
Cl |
Cl |
O |
|
Cl |
|
|
|
H |
|
Cl |
|
|
|
O |
|
||||
|
|
|
|
|
|||||
|
|
H |
Cl |
|
|
H |
H |
Cl |
2,3 |
|
H 1 |
|
|
|
|
||||
H |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
||
|
|
|
|
H |
|
|
|
|
|
Работа выполнена в рамках федеральной целевой программы «Научные и научно-педагогические кадры инновационной России» на 2009-2013 гг. по теме: «Создание инновационных высокоэффективных путей получения многофункциональных органических соединений с использованием в качестве сырьевой базы доступного отечественного нефтехимического сырья» (гос. контракт № 14.В37.21.0805 от 31 августа 2012 г.).
93

Секция 4. Химические и биотехнологии.
ОСОБЕННОСТИ ТЕРМИЧЕСКОГО ПОВЕДЕНИЯ НАНОТРУБЧАТЫХ ПОКРЫТИЙ TIO2, ДОПИРОВАННЫХ ФТОРОМ И АЗОТОМ
А.Н. Морозов, аспирант, А.И. Михайличенко, д.х.н., профессор Российский химико-технологический университет имени Д.И. Менделеева, 125480, г.Москва, ул. Героев Панфиловцев, д. 20, тел.(965)-230-66-24
E-mail: smallevil.666@mail.ru
Разработка фотокатализаторов на основе диоксида титана в настоящее время является перспективным направлением. Это обусловлено тем, что TiO2 обладает высокой фотокаталитической активностью и благодаря этому используется в процессах очистки воды и воздуха [1]. Особый интерес представляют композитные катализаторы на основе нанотрубчатых покрытий TiO2, допированных азотом и фтором НТП TiO2(N,F), которые получают анодным окислением титана [2-3]. Для достижения необходимых функциональных свойств после получения допированной структуры следует отжиг, в процессе, которого структура пленок изменяется от аморфной до кристаллической, а допирующие добавки меняют свое химическое состояние.
Целью настоящей работы было исследование процессов, происходящих при отжиге нанотрубчатых покрытий оксида титана, допированного азотом и фтором, а также определение оптимальных условий обработки, при которых наблюдается максимальная фотокаталитическая активность покрытий.
В качестве исходного материала для синтеза НТП TiO2(N,F) был использован технически чистый титан марки ВТ1-0 толщиной 300 мкм. Образцы анодировали в этиленгликоле, содержащем 0,5% масс. NH4F и 4% масс. H2O. Анодное окисление титана производилось в потенциостатическом режиме при 60 В и 25 °С. Продолжительность процесса составляла 3 часа.
Морфологию катализатора изучали с помощью сканирующей электронной микроскопии (СЭМ) и просвечивающей электронной микроскопии (ПЭМ) на микроскопах JSM 6510 LV и LEO - 912АВ Omega соответственно (рис.1).
Полученная структура состоит из прямолинейных нанотрубок TiO2, расположенных перпендикулярно поверхности титана, имеющих длину 28 мкм, с внутренним диаметром 105 нм и толщиной стенок 5 нм. На внутренней поверхности нанотрубок находятся нанокристаллы гексафторотитаната аммония со средним размером 1,85 нм. Данные нанокристаллы являются прекурсом для допирования поверхности НТП TiO2 атомами фтора и азота, которое производится пирогидролизом с образованием нестехиометрического соединения TiOxNyFz [4-5]. Также установлено, что полученное покрытие оксида титана является рентгеноаморфным до проведения отжига (рис. 2 а). Поэтому выбор температуры для обработки покрытия является очень важным параметром, определяющим его дальнейшие свойства.
С этой целью методами дифференциальной сканирующей калориметрии (ДСК), термогравиметрии (ТГ) и рентгенофазового анализа (РФА) исследовано изменение состояния покрытия при нагреве. Оценку фотокаталитической активности покрытия проводили в реакции окисления метиленового голубого (10 мг/л). В качестве источника света использовали облучатель OSRAM ULTRAVITALUX (300 Вт), который генерирует смешанное излучение, схожее с излучением солнца.
94

ВТСНТ – 2013
Рис.1. Морфология НТП TiO2(N,F): вид сверху(а), скол покрытия (б), наночастицы (NH4)2[TiF6] на НТП TiO2(в), наночастицы TiOxNyFz на НТП TiO2(г), НТП TiO2 до отжига (д), НТП TiO2 отожжённые при
500 °С(е).
Рис.2. Результаты термического анализа в режимах ТГ/ДСК и рентгенофазового анализа НТП TiO2(N,F), отожженного при разных температурах.
Установлено, что кристаллизация НТП TiO2(N,F) начинается при 300 – 305 °С и заканчивается при 450 - 455°С с образованием фазы анатаз. При дальнейшем нагревании происходит спекание образовавшихся частиц с получением кристаллитов большего размера, что приводит к появлению видимых дефектов в структуре нанотрубок при 600 °С и разрушению НТП TiO2 при температурах выше 700 °С из-за образования кристаллитов большего размера, чем толщина стенки. Данное утверждение основано, в первую очередь, на результатах РЭМ и расчете областей когерентного рассеяния по данным РФА с помощью формулы ДебаяШеррера.
Согласно данным РФА (рис.2б) в структуре присутствует примесь второй фазы, которая относится к TiOF2 (JSPDS 08-0060). Интенсивность рефлексов
95

Секция 4. Химические и биотехнологии.
отнесенных к TiOF2 уменьшается при отжиге выше 500 °С, что вероятно связано с разложением оксодифторида титана.
Согласно результатам термического анализа (рис. 2a), процесс термообработки НТП TiO2(N,F) происходит в несколько этапов. Начальный этап 25-200 °С соответствует испарению влаги и частичному удалению этиленгликоля. Далее следует потеря массы при температурах 200-440 °С и наблюдаются значительные экзотермические пики (максимумы при 277,4 °С, 365,8 °С, 386,8 °С), что, вероятно, связано с процессами дегидратации во время кристаллизации рентгеноаморфной фазы, разложением комплекса (NH4)2[TiF6] и последовательным разложением этиленгликоля и удалением образовавшихся продуктов окисления из нанотрубок. Так как процессы дегидратации и разложения (NH4)2[TiF6] вызывают поглощение тепла, то на кривой ДСК наблюдается интегральная характеристика тепловых процессов, происходящих в данном интервале температур. Вид характеристики обусловлен более мощным экзотермическим процессом (кристаллизация рентгеноаморфной фазы) по сравнению с эндотермическим вкладом. Другие два экзотермических пика, наблюдаемые на кривой ДСК с максимумами при 504,8 и 581,4°С, связаны с замещением азота на кислород и разложением TiOF2 соответственно. Первый процесс протекает без изменения массы, что связано с близкой атомной массой кислорода и азота, а второй имеет убыль массы, что связано с удалением TiF4 как продукта термолиза TiOF2. Оба процесса сопровождаются выделением тепла, которое наблюдается на кривой ДСК. Это подтверждается данными элементного анализа и РФА. С дальнейшим ростом температуры отжига не наблюдается значительных экзоили эндотермических эффектов, а масса образца постепенно уменьшается. Это соответствует процессам роста кристаллитов и удалению химически связанной воды из структуры НТП TiO2.
Таким образом было установлено, что полное удаление электролита из структуры наблюдается уже при температуре 400 °С (рис.2а). Предварительно проведенные исследования показали, что полное разложение комплекса (NH4)2[TiF6] до TiOxNyFz достигается при 440 °С и это согласуется с литературными данными [5]. Исходя из термической стабильности покрытия и температуры удаления допирующих добавок, для исследования влияния температуры отжига покрытия на его фотокаталитическую активность был выбран диапазон 450-600 °С.
В ходе исследования установлено, что наибольшей активностью обладают покрытия обработанные при 450-500 °С в потоке воздуха. Степень окисления МГ составляет 99% за 1 час процесса. При этой температуре происходит полное разложение комплекса (NH4)2[TiF6] с образованием соединения TiOxNyFz, нанотрубки имеют структуру анатаза и наблюдается полное удаление электролита из структуры. Покрытие имеет состав 31,95 ат. % Ti, 63,79 ат. % O, 0,92 ат. % N и 2,54 ат. % F. При использовании более высоких температур для отжига наблюдается обесцвечивание покрытия, что, вероятно, связано с удалением азота из структуры. В свою очередь, это приводит к отсутствию поглощения в видимой части спектра.
Список литературы:
1. Артемьев Ю. М., Рябчук В. К. Введение в гетерогенный фотокатализ: учебное пособие. – СПб.: Изд-во С.-Петербурского университета, 1999. – 304 с.
96

ВТСНТ – 2013
2.Yaling Su, Xingwang Xhang, Minghua Zhou, Song Han, Lecheng Lei. Preparation of high efficient photoelectrode of N-F-codoped TiO2 nanotubes // Journal of Photochemistry and Photobiology A. – 2008. – 194. – P.152–160.
3.Qi Li, Jian Kus Hang. Composite photocatalyst of nitrogen and fluorine codoped titanium oxide nanotube arrays with dispersed palladium oxide nanoparticles for enhanced visible light photocatalytic performance // Environ. Sci. Technol. – 2010,
– №44, – P.3493–3499.
4.Harry A., Seibel H., Karen P., Timothy R., Patrick M. Synthesis and characterization of color variants of nitrogenand fluorine-substituted TiO2 // J. Mater. Chem. – 2009. – №19. –P.471–477.
5.Di Li, Naoki Ohashi, Shunichi Hishita, Taras Kolodiazhnyi, Hajime Haneda. Origin of visible-light-driven photocatalysis: A comparative study on N/F-doped and N–F-codoped TiO2 powders by means of experimental characterizations and theoretical calculations // Journal of Solid State Chemistry. – 2005. – 178. – P.3293–3302.
РАЗРАБОТКА СОВРЕМЕННОГО СОРБЕНТА ДЛЯ ОЧИСТКИ СТОЧНЫХ ВОД ОТ РАДИОАКТИВНЫХ ЗАГРЯЗНЕНИЙ
Ю.А. Муксунова, студент гр. 4ГМ21 Томский политехнический университет, 634050, г.Томск, пр.Ленина,30,
тел. 8-953-913-90-71
E-mail: muksunovayulya@mail.ru
С бурным развитием промышленности в мире проблемы охраны окружающей среды становятся проблемами глобального масштаба. Одной из таких проблем является загрязнение воды промышленными стоками, которые содержат ионы радиоактивных и тяжелых металлов. Ее решение состоит в разработке дешевых и эффективных методов удаления ионов металлов из загрязненных водоемов. В настоящее время существует множество методов очистки сточных вод:
электролитические (электролиз, электродиализ);
биологические (использование микроорганизмов [1-4], хитина грибов и насекомых);
физико-химические (флотация, коагулирование, сорбция, ионообмен, экстрагирование, выпаривание).
Вчисле перечисленных методов особо выделяют метод сорбентов - твердых тел или жидкостей, избирательно поглощающих из окружающей среды, растворённые в ней вещества. Благодаря тому, что этот способ привлекателен своей высокой эффективностью и является экономически выгодным, свойства многих видов сорбентов уже изучены и введены в коммерческое использование.
Так, например, для извлечения радионуклидов из водных сред широко применяются различные сорбционные материалы: природные и синтетические ионообменники, комплексообразующие, модифицированные, композиционные сорбенты, а также биологические сорбенты [5].
Внашей работе мы соединили наноматериалы и плесневые грибы, исходя из того, что каждый из компонентов способен поглощать радиоактивные ионы из
97

Секция 4. Химические и биотехнологии.
водного раствора, а их комбинация позволит повысить эффективность сорбции. Наночастицы, как известно, адсорбируют загрязняющие вещества благодаря своей высокой удельной площади поверхности. Но их трудно утилизировать из очищенной воды, что может привести к загрязнению воды еще и наноматериалами. Решением проблемы безопасного извлечения наночастиц стало нанесение наноматериалов на носители, которые было бы удобно извлекать из очищаемой среды. В качестве таких носителей были выбраны плесневые грибы. Поэтому новым направлением является разработка методов очистки сточных и промышленных вод от радиоактивных загрязнителей при помощи осажденных на микробной биомассе наночастиц. Способность плесневых грибов сорбировать ионы тяжелых и радиоактивных металлов из раствора и накапливать их внутри клетки обеспечивает дополнительную адсорбцию радиоактивных материалов из загрязненной среды.
Это направление является очень актуальным, поскольку загрязнение окружающей среды радиоактивными ионами, производными от процессов обработки урана или утечки ядерных реакторов, представляет собой серьезную угрозу здоровью человека. Радиоактивные вещества могут попадать в грунтовые воды и загрязнять запасы питьевой воды в зонах большой плотности населения.
Целью данной работы является получение сорбента на основе наноматериалов и плесневых грибов для удаления радиоактивных ионов из загрязненных вод. В качестве наноматериалов были использованы нанопорошки оксидов металлов 


























 uO и AlOOH), которые осаждали на мицелии плесневых грибов из рода аспергилл (Aspergillus niger). Культивирование грибов проводилось на основе стандартных методик [6] в круглодонных колбах на жидкой питательной среде с соблюдением условий стерильности. По окончании культивирования проводили осаждение нанопорошков на мицелии плесневых грибов согласно следующей методике: в колбы с дистиллированной водой добавили нанопорошок и небольшие фрагменты промытого мицелия. При этом содержимое колб периодически перемешивали на шейкере.
uO и AlOOH), которые осаждали на мицелии плесневых грибов из рода аспергилл (Aspergillus niger). Культивирование грибов проводилось на основе стандартных методик [6] в круглодонных колбах на жидкой питательной среде с соблюдением условий стерильности. По окончании культивирования проводили осаждение нанопорошков на мицелии плесневых грибов согласно следующей методике: в колбы с дистиллированной водой добавили нанопорошок и небольшие фрагменты промытого мицелия. При этом содержимое колб периодически перемешивали на шейкере.
Полученный сорбирующий материал был исследован методом просвечивающей электронной микроскопии (Растровый электронный микроскоп JEOL JSM-7500FA) для определения локализации наноматериалов после осаждения на мицелии плесневых грибов (рис.1).
Рис.1. Снимок композитного сорбента (Asp. niger+нанотрубки 





 )
)
Также в ходе работы было проведено поглощение урана полученными сорбентами и оценена их эффективность с помощью показателя относительной сорбции (табл.1,2).
Таблица 1
98
