
- •Анализ органических лекарственных веществ по функциональным группам
- •Введение
- •Основная литература
- •Дополнительная литература
- •Теоретические сведения
- •3. Прочие фг, которые нельзя обобщить по одному признаку:
- •Анализ органических лекарственных веществ по фг Спиртовый гидроксил
- •Енольный гидроксил
- •Фенольный гидроксил
- •Карбонильная группа (альдегидная и кетонная)
- •Α-Кетольная группа
- •Пирокатехиновое кольцо
- •Гидразидная группа
- •1. Реакции окисления
- •Карбоксильная группа
- •Α-Аминокарбоксильная группа
- •1. Метод формольного титрования (метод Серенсена).
- •Сложноэфирная (лактонная) и амидная (лактамная) группы
- •1. Метод щелочного гидролиза, вариант обратного титрования
- •2. Метод Кьельдаля после щелочного гидролиза (для амидов)
- •Α– Гидроксикарбоксильная группа
- •Первичная ароматическая аминогруппа
- •Вторичная ароматическая аминогруппа
- •2. Обратная иодометрия
- •3. Метод Кьельдаля
- •R – sh Меркаптогруппа (сульфгидридная группа) Качественный анализ Реакция комплексообразования
- •Количественный анализ Метод Фольгарда
- •Пиразол (1,2-диазол)
- •Вопросы для самоподготовки
- •Вопросы для подготовки к коллоквиуму
- •Оглавление
1. Метод щелочного гидролиза, вариант обратного титрования
Основан на свойстве сложноэфирной и лактамной групп гидролизоваться раствором щелочи, избыток которой оттитровывают кислотой.

![]()
Э = М
2. Метод Кьельдаля после щелочного гидролиза (для амидов)
2.1. Если амид образован аммиаком или алкиламином, то образующийся при гидролизе амин (аммиак, алкиламин) перегоняют с водяным паром, улавливают раствором борной кислоты и затем титруют раствором хлороводородной кислоты (видоизмененный метод Кьельдаля).

![]()
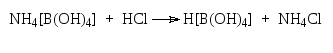
![]()
Если после гидролиза образуется ароматический амин, то определение заканчивают реакцие диазотирования (нитритометрия).
П![]() ростая
эфирная группа
ростая
эфирная группа
Качественный анализ
Реакция образования оксониевых солей
Простые эфиры обладают слабыми основными свойствами, поэтому они способны протонироваться с образованием оксониевых солей желтого цвета.

Методика. На часовое стекло наносят 3-4 капли концентрированной серной кислоты и прибавляют 0,02 г димедрола: появляется ярко-желтое окрашивание, постепенно переходящее в кирпично-красное.

Реакция гидролиза
Простые эфиры более устойчивы к гидролизу, чем сложные, поэтому их расщепление происходит лишь при нагревании с концентрированным раствором H2SO4 или HI.

В случае Alk- и Ar-замещенных простых эфиров, а также гликозидных связей гидролиз осуществляется под действием разбавленных минеральных кислот. Далее проводят анализ по продуктам гидролиза.
Методика. 0,1 г димедрола растворяют в 5 мл воды, прибавляют 2 мл разведенной хлористоводородной кислоты и кипятят в течение 3 минут. После охлаждения кристаллы отфильтровывают и перекристаллизовывают из небольшого количества воды. Температура плавления полученного бензгидрола 62-67 °С.


Количественный анализ ФЭК по оксониевой соли.
Α– Гидроксикарбоксильная группа
Качественный анализ
1. Реакция окисления
α-оксикислоты
при нагревании с сильными минеральными
кислотами способны окисляться с
последующим разложением до карбонильных
соединений (альдегидов, кетонов) и
муравьиной кислоты. 
Соли молочной
кислоты окисляются перманганатом калия
в кислой среде, при этом фиолетовая
окраска перманганата исчезает. 

![]()
2. Реакция
образования ауринового красителя Винная
кислота (адреналина гидротартрат,
платифиллина гидротартрат и др.)
окисляется серной кислотой при нагревании
до глиоксаля и муравьинной кислоты.

Муравьиная кислота,
как альдегид, вступает в реакцию
коденсации с фенолами с образованием
ауринового красителя.  Методика.
0,01 препарата (платифиллина г/т,
адреналинаг/т) растворяют в фарфоровой
чашке в 10 кап. конц. серной кислоте,
прибавляют несколько крупинок β-нафтола
и нагревают на водяной бане; появляется
зеленое окрашивание.
Методика.
0,01 препарата (платифиллина г/т,
адреналинаг/т) растворяют в фарфоровой
чашке в 10 кап. конц. серной кислоте,
прибавляют несколько крупинок β-нафтола
и нагревают на водяной бане; появляется
зеленое окрашивание.
Первичная ароматическая аминогруппа
Качественный анализ
Первичная ароматическая аминогруппа, являясь ориентантом I рода (как и фенольный гидроксил), повышает электронную плотность в орто-и пара-положениях бензольного кольца.

Поэтому ароматические амины легко вступают в реакции электро-фильного замещения.
Реакции электрофильного замещения
1.1 Реакция образования азокрасителя
Протекает в две стадии: диазотирования и азосочетания. Ароматический амин взаимодействует с нитритом натрия в солянокислой среде с образованием соли диазония (I) (стадия диазотирования), которая при сочетании с фенолами в щелочной среде или ароматическими аминами в нейтральной и слабощелочной среде образуют азокраситель (II) оранжево- или вишнево-красного цвета (стадия азосочетания).

Реакция азосочетания с фенолами проходит в щелочной среде, так как образующие феноляты легче вступают в реакции SE, чем фенолы.

С Ar-NH2 азосочетание нельзя проводить в кислой среде, поскольку в этом случае происходит протонирование аминогруппы, а протонированный ароматический амин теряет способность участвовать в реакциях SE:

В качестве азокомпоненты применяют разнообразные фенолы и ароматические амины:

Механизм реакции диазотирования
Диазотирующим реагентом является нитрозилхлорид (I), образующийся из азотистой кислоты в солянонокислой среде:
![]()

Нитрозилхлорид атакует ароматическую аминогруппу с образованием нестойкого N-нитрозамина (II), который изомеризуется в диазогидрат (III). Последний под действием кислоты превращается в соль диазония.


Механизм реакции азосочетания
Диазотирующий агент (соль диазония) атакует азокомпоненту (фенол, ароматический амин) по механизму SE с образованием -комплекса, который стабилизируется отщеплением протона, образуя азокраситель.
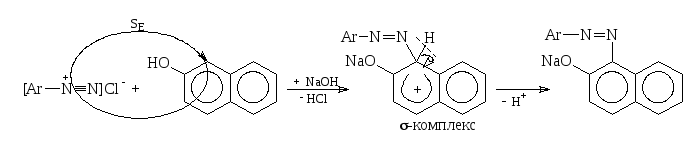
М е т о д и к а
1. К 1 мл 0,25 % раствора норсульфазола, сульфадимезина, натрия пара-аминосалицилата, анестезина в разведенной хлороводородной кислоте (1:2) прибавляют 1 каплю раствора нитрита натрия. Через 1 минуту полученный раствор каплями вливают в 0,5 мл щелочного раствора -нафтола. Появляется оранжево-красное окрашивание.
Ацильные производные ароматических аминов (парацетамол, фенацетин, ксикаин, тримекаин, фталазол) дают эту реакцию после кислотного гидролиза.
2. Около 0,05 г парацетамола, фенацетина, ксикаина, фталазола кипятят с 2 мл разведенной хлороводородной кислоты в течение 2-3 минут, охлаждают, прибавляют 2-3 капли раствора нитрита натрия, несколько капель полученного раствора осторожно вливают в 1 мл щелочного раствора -нафтола: появляется красное окрашивание.


Реакция образования бромпроизводных
Ароматические амины замещают атомы водорода бензольного кольца в орто- и пара- положениях на галоген, образуя нерастворимые соединения.

1.3. Реакция с 2,4-динитрофтор (хлор) бензолом
Ароматические амины образуют с 2,4-динитрохлорбензолом красители желтого цвета, которые экстрагируют в слой органического растворителя, например бензола.

Реакции окисления
Первичные ароматические амины легко окисляются, даже кислородом воздуха, с образованием окрашенных продуктов:

В качестве окислителей применяют хлорамин, хлорную известь, бихромат калия в кислой среде. Появление окраски обусловлено не только продуктами окисления, но и веществами, получившимися в результате последующей конденсации окисленных соединений с ароматическими аминами.
Эта реакция рекомендуется для определения анестезина, парацетамола (после гидролиза).

Методика
1. 0,05 г препарата (анестезин, норсульфазол, фенацетин, парацетамол) растворяют в 2 мл разведенной хлороводородной кислоты, прибавляют 5 мл воды и 2-3 капли раствора бихромата калия.
2. 0,02 г препарата растворяют в 1 мл разведенной хлороводородной кислоты, прибавляют 3 мл 2 % раствора хлорамина, смесь нагревают на кипящей водяной бане. Результаты исследований сводят в таблицу (см. карбоксильная группа, п. 2).
Реакции конденсации с альдегидами
Первичные ароматические амины конденсируются в кислой среде с ароматическими альдегидами, образуя основания Шиффа. Продукты реакции ароматических аминов с n-диметиламинобензальдегидом или ванилином в среде хлороводородной кислоты окрашены в желто-оранжевые оттенки.


Методика. К 0,01-0,02 г препарата (анестезин, новокаин, натрия пара-амносалицилат, норсульфазол) прибавляют 0,5 мл раствора n-диметиламинобензальдегида, 1 мл концентрированной хлороводородной кислоты, появляется желтое или оранжевое окрашивание.
Капельная реакция, основанная на образовании оснований Шиффа (реакция Овчинникова, лигниновая проба), состоит в том, что крупинку исследуемого препарата – ароматического амина – помещают на бумагу, содержащую лигнин, и прибавляют каплю разведенной соляной кислоты. Появляется желто-оранжевое окрашивание в результате конденсации амина с альдегидами, содержащимися в лигнине, в частности с конифериловым альдегидом.

Количественный анализ
Нитритометрия
Метод основан на свойстве препаратов, содержащих первичную ароматическую аминогруппу, диазотироваться нитритом натрия в солянокислой среде. Последняя нужна для образования диазотирующей частицы. Титрование проводят в присутствии катализатора – бромида калия.

В присутствии КВг образуется диазотирующая частица – нитрозилбромид BrN=O, скорость образования которой в 300 раз выше, чем нитрозилхлорида, а, следовательно, и скорость реакции диазотирования резко возрастает. Титруют медленно, так как скорость реакции диазотирования мала. Определение проводят на холоду, поскольку соль диазония при нагревании в водных растворах неустойчива и легко разлагается с выделением азота.

При определении ацильных производных ароматических аминов предварительно проводят кислотный гидролиз.


Индикация основана на окислительных свойствах титранта – нитрита натрия. Применяются:
1) внутренний индикатор – тропеолин 00 (изменение окраски – от красной до бесцветной или желтой вследствие окисления красителя) либо смесь тропеолина 00 с метиленовым синим (изменение окраски – от фиолетовой до изумрудно-зеленой);
2) внешний индикатор – йодкрахмальная бумага, на которую наносят каплю анализируемой смеси. При избытке нитрита натрия йодид восстанавливается до I2, который дает синее окрашивание с крахмалом.

![]()
Методы галогенирования
Основаны на электрофильном замещении атомов водорода ароматического кольца, активированного ароматической аминогруппой, на атомы галогена. Применяется для анестезина, новокаина, стрептоцида, натрия пара-аминосалицилата. Индикаторы – метиловый оранжевый, метиловый красный. Избыточная капля брома необратимо окисляет индикатор.
2.1. Броматометрия
Прямое титрование.


2.2. Йодхлорметрия
Обратное титрование. Избыток ICl определяют йодометрически (индикатор – крахмал).

![]()
![]()
![]()
Фотоэлектроколориметрический метод на основе реакции образования азокрасителя
