
- •Министерство образования российской федерации
- •В в е д е н и е
- •Техника безопасности при выполнении лабораторных работ
- •Методы анализа и методика отбора проб древесного сырья
- •Лабораторная работа № 1 Определение влажности древесины высушиванием
- •Коэффициент сухости древесины вычисляют по формуле
- •Лабораторная работа № 2 Определение зольности древесины
- •Лабораторная работа № 3 Определение веществ, экстрагируемых органическими растворителями
- •Методика экстрагирования в аппарате Сокслета
- •Лабораторная работа № 4 Определение веществ, экстрагируемых водой
- •Лабораторная работа № 5 Определение таннинов
- •Лабораторная работа № 6 Определение целлюлозы
- •Лабораторная работа № 7 Определение легко– и трудногидролизуемых полисахаридов
- •Лабораторная работа № 8 Определение лигнина
- •Требование к оформлению отчёта
- •Л и т е р а т у р а
- •Луговых Юрий Михайлович
- •3 Курса
Лабораторная работа № 7 Определение легко– и трудногидролизуемых полисахаридов
Определение легко– и трудногидролизуемых полисахаридов в древесине основано на реакциях их гидролиза с последующим нахождением общего количества образовавшихся моносахаридов по редуцирующей (восстановительной) способности. Легко– и трудногидролизуемые полисахариды разделяют, используя различные условия гидролиза.
Метод определения полисахаридов заключается в последовательной обработке исследуемого растительного сырья сначала 2% соляной кислотой ( или 5% серной кислотой ) при температуре около 100ОС, а затем 80% серной кислотой при комнатной температуре.
Методика определения легкогидролизуемых полисахаридов. Навеску около 5 г исследуемого материала нагревают с 200 мл 2% - ной соляной кислотой в конической колбе на 500 мл с обратным холодильником при слабом кипении в течении 3 часов. По окончании нагревания раствор фильтруют через бумажный фильтр. Остаток на фильтре промывают горячей водой до отрицательной реакции на кислоту (индикатор метилоранж). Фильтрат и промывные воды сливают вместе и доливают водой в мерной колбе до 500 мл.
Содержимое редуцирующих веществ (РВ) определяют эбулиостатическим методом, разработанным Низовкиным и Емельяновой.
Эбулиостатический метод определения РВ основан на применении прямого титрования. Горячий меднощелочной раствор титруют раствором сахара в эбулиостате, устройство которого позволяет проводить анализ в токе водяного пара без доступа воздуха к поверхности реагирующей жидкости. Обогрев осуществляется через паровую рубашку и пропусканием пара через реагирующую жидкость.
 Индикатором
является метиленовая синь, которая в
окислительной среде имеет синюю окраску,
а в восстановительной среде бесцветна.
По изменению окраски метиленовой сини
определяют конец титрования меднощелочного
раствора раствором сахара. Для растворения
осадка Cu2O
в меднощелочной раствор добавляют
желтую кровяную соль K4[Fe(CN)6].
Индикатором
является метиленовая синь, которая в
окислительной среде имеет синюю окраску,
а в восстановительной среде бесцветна.
По изменению окраски метиленовой сини
определяют конец титрования меднощелочного
раствора раствором сахара. Для растворения
осадка Cu2O
в меднощелочной раствор добавляют
желтую кровяную соль K4[Fe(CN)6].
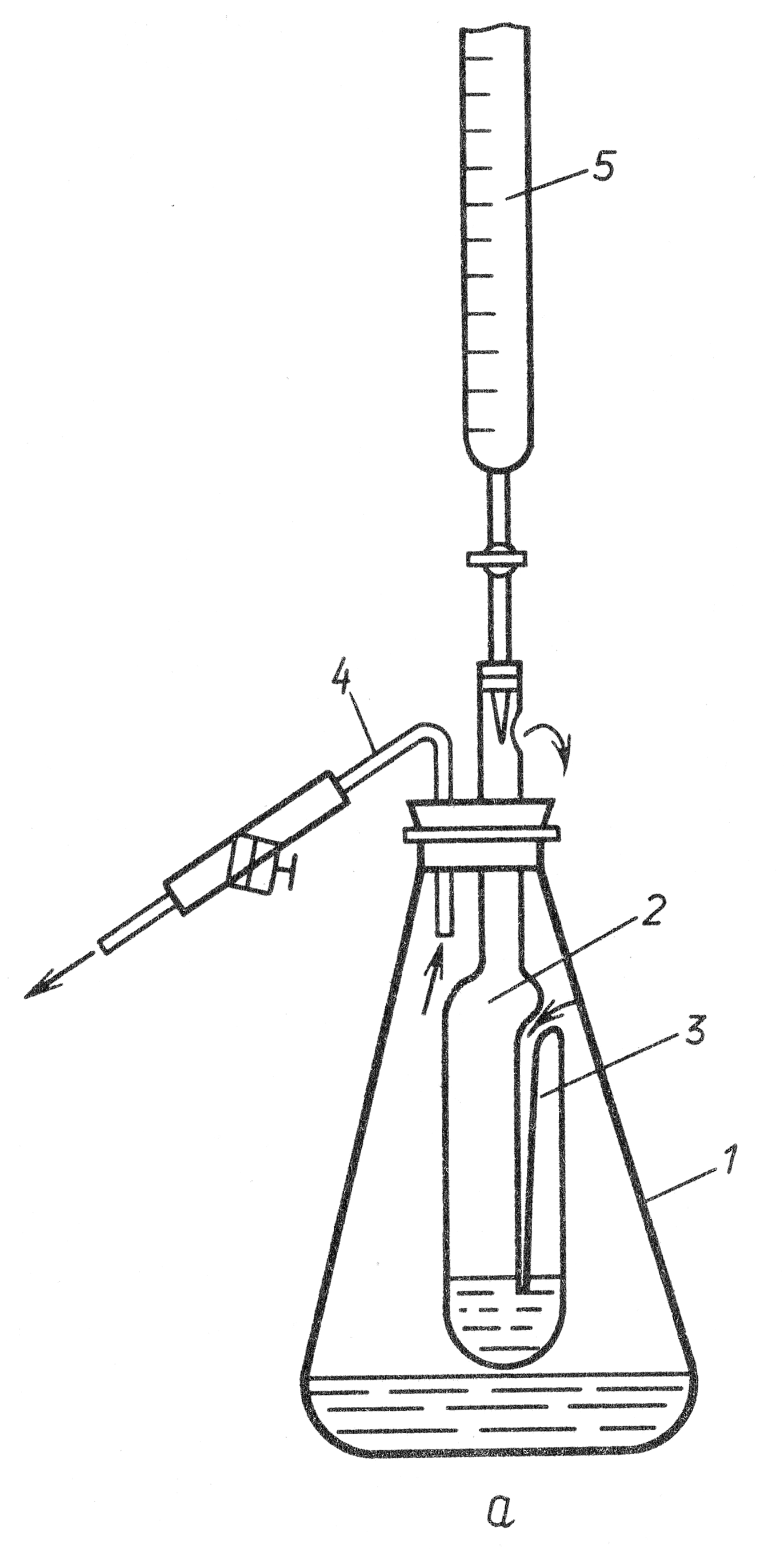
Прибор для титрования состоит из внешнего сосуда – конической колбы 1 и внутреннего сосуда – эбулиостата 2 с впаянной в его боковую стенку трубкой, доходящей почти до дна сосуда. Суженный конец эбулиостата вставлен в колбу 1 на резиновой пробке и имеет отверстие для выхода пара 3. В резиновую пробку вставлена стеклянная трубка 4 для отвода избытка пара из колбы 1. Струю пара регулируют винтовым зажимом на резиновой трубке, надетой на конец стеклянной трубки. Во время титрования верхний конец эбулиостата закрывают резиновой пробкой, в которую вставлен конец бюретки 5 для раствора сахара.
Для анализа приготавливают растворы А и Б . Раствор А - 10 г CuSO4.5H2O и 0,04 г метиленовой сини (или метиленовой голубой) в 1 л раствора. Раствор Б – 50 г сегнетовой соли, 75 г NaOH и 4 г K4[Fe(CN)6] в 1 л раствора.
Титр меднощелочного раствора устанавливают по глюкозе. Для его установления растворяют около 0,1 г безводной глюкозы в мерной колбе на 100 мл. Затем 10 мл меднощелочного раствора, отмеренного пипеткой (или специальным дозатором), титруют раствором глюкозы, концентрацию которой вычисляют по навеске. Зная концентрацию глюкозы, вычисляют количество глюкозы, которое расходуется на восстановление 10 мл меднощелочного раствора. Это и будет титром меднощелочного раствора по глюкозе. Он определяется по формуле
Т = С . V ,
где С – концентрация глюкозного раствора, мг/л;
V – расход глюкозного раствора на титрование, мл.
Определение редуцирующих веществ в растворе. Во внешний сосуд прибора наливают дистиллированную воду и прибор ставят на электроплитку. Для равномерного образования пара на дно колбы помещают кусочки пористого стекла (капилляры) или пористой керамики. Когда вода закипит, эбулиостат вынимают и в него наливают при помощи пипеток (или дозаторов) 5 мл раствора А и 5 мл раствора Б .Смесь взбалтывают и осторожно вставляют в сосуд с водой. Верхнее отверстие эбулиостата закрывают пробкой, надетой на кончик бюретки с анализируемым раствором сахара, и ждут, когда пар начнёт проходить (барбатировать) через меднощелочной раствор (через 0,5…1 мин). Если пар не будет долго проходить через реагирующую жидкость, при помощи зажима уменьшают выход пара через отводящую трубку.
Как только пар начнёт проходить через реагирующую жидкость, постепенно прибавляют сахарный раствор. Сначала проводят ориентировочное определение, а затем окончательное. При ориентировочном определении к 10 мл меднощелочного раствора, находящегося в эбулиостате, прибавляют по каплям со скоростью 1 капля в 1…2 с сахарный раствор до появления желтой окраски реагирующей жидкости от одной капли этого раствора. Замечают объем сахарного раствора, израсходованного на титрование. При окончательном определении к 10 мл меднощелочного раствора в эбулиостат прибавляют из бюретки сразу 80…90% того количества сахарного раствора, которое пошло на ориентировочное определение, ждут 2 мин (по секундомеру или песочным часам), а затем прибавляют сахарный раствор со скоростью 1 капля в 6…7 с до появления желтой окраски. По бюретке замечают объём сахарного раствора, израсходованного на титрование.
Массовую долю РВ, %, в гидролизате легкогидролизуемых полисахаридов, рассчитывают по формуле
![]() ,
,
где Т – титр меднощелочного раствора по глюкозе, мг;
Vг – объём гидролизата, израсходованного на титрование 10 мл медноще- лочного раствора, мл.
Массовая доля легкогидролизуемых полисахаридов, % к абсолютно сухой древесине, определяется по формуле
![]() ,
,
где Сл – массовая доля РВ в гидролизате легкогидролизуемых полисахаридов,
% ;
V – объём гидролизата, V=500 мл;
КЛ – коэффициент пересчёта моносахаридов в полисахариды, Кл=0.89;
g – масса абсолютно сухой навески древесины, г;
n – разбавление гидролизата при нейтрализации, n = 100/50 = 2;
КЭ – коэффициент экстрагирования.
Методика определения трудногидролизуемых полисахаридов. Для определения трудногидролизуемых полисахаридов остаток на фильтре после удаления легкогидролизуемых полисахаридов количественно переносят в стакан на 100 мл и подсушивают при температуре 50…60°C до воздушно – сухого состояния, а затем обрабатывают 15…20 мл 80% раствором серной кислоты при комнатной температуре в течении 2 ч, периодически перемешивая стеклянной палочкой. Смесь из стакана переносят в коническую колбу на 500 мл, смывая её 200 мл воды. Затем колбу присоединяют к обратному холодильнику и нагревают на электроплитке (при слабом кипении ) в течении 3ч. Раствор после нагревания фильтруют через бумажный фильтр, остаток на фильтре промывают горячей водой до отрицательной реакции на серную кислоту (по метилоранжу).
Фильтрат и промывные воды соединяют вместе и доводят раствор водой в мерной колбе до 500 мл. Нейтрализуют 25 мл этого раствора 2н раствором NaOH (по метилоранжу) и доводят объём водой в мерной колбе до 100мл.
Содержание РВ определяют эбулиостатическим методом, описанным выше.
Массовую долю РВ, %, в гидролизате трудногидролизуемых полисахаридов рассчитывают по формуле
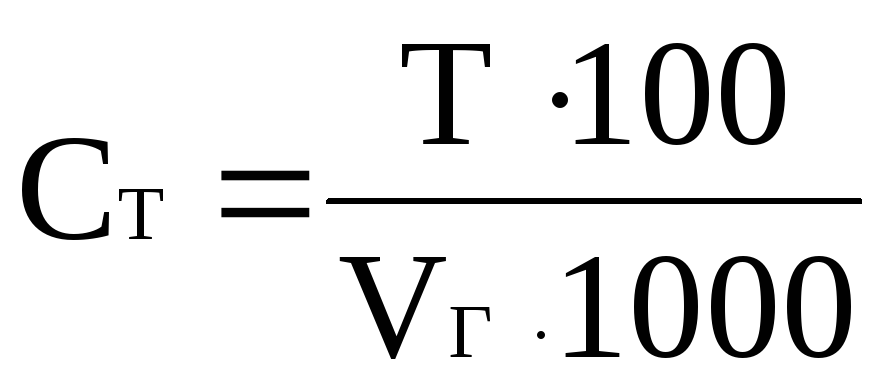 ,
,
где Т – титр меднощелочного раствора по глюкозе, мг;
V – объём гидролизата израсходованного на титрование 10 мл меднощелочного раствора, мл.
Массовая доля трудногидролизуемых полисахаридов, % к абсолютно сухой древесине, определяется по формуле
![]() ,
,
где Ст – массовая доля РВ в гидролизате трудногидролизуемых полисахаридов,
%;
V – объём гидролизата, V = 500 мл;
КТ – коэффициент перерасчёта моносахаридов в полисахариды, КТ=0,90;
g – масса абсолютно сухой навески древесины, г;
n – разбавлении гидролизата при нейтрализации, n = 100/25 = 4;
КЭ – коэффициент экстрагирования.
Примечание. Общий выход РВ определяют как сумму редуцирующих веществ, полученных при определении легко– и трудногидролизуемых полисахаридов.
