
- •«Дальневосточный федеральный университет»
- •Оглавление
- •Аннотация учебно-методического комплекса дисциплины «Химия»
- •«Дальневосточный федеральный университет»
- •Школа естественных наук двфу
- •Рабочая программа учебной дисциплины (рпуд)
- •180100.62 – Кораблестроение, океанотехника и системотехника объектов морской инфраструктуры Форма подготовки (очная)
- •Оборотная сторона титульного листа рпуд
- •Введение
- •1. Цели освоения дисциплины
- •2. Место дисциплины в структуре ооп бакалавриата
- •3. Начальные требования к освоению дисциплины
- •3А. Компетенции обучающегося, формируемые в результате освоения дисциплины
- •4. Структура и содержание дисциплины
- •Краткое содержание лекционного курса
- •1. Строение вещества
- •2. Химическая термодинамика, энергетика процесса, кинетика и химическое равновесие
- •3. Жидкие системы – растворы
- •4. Окислительно-восстановительные процессы
- •5. Конструкционные материалы
- •5. Образовательные технологии
- •Самостоятельной работы студента (срс)
- •6. Учебно-методическое и информационное обеспечение дисциплины
- •1. Основная литература:
- •2. Дополнительная литература:
- •3. Справочная литература:
- •7. Материально-техническое обеспечение и электронные средства обучения, иллюстрационный материал, специализированное и лабораторное оборудование
- •8. Текущий и итоговый контроль
- •Перечень типовых экзаменационных вопросов
- •9. Рейтинговая оценка по дисциплине
- •«Дальневосточный федеральный университет»
- •Тема 2. Основные понятия и законы химии
- •Раздел 2. Строение атома и химическая связь (6 часов)
- •Тема 1. Строение атома, периодический закон д.И. Менделеева
- •Тема 2. Химическая связь
- •Раздел 1 Межмолекулярное взаимодействие (6 часов)
- •Тема 1. Межмолекулярное взаимодействие
- •Тема 2. Агрегатные состояния вещества
- •Раздел 1. Химическая термодинамика (18 часов)
- •Тема 1. I и II закон термодинамики
- •Раздел 2. Химическая кинетика (18 часов)
- •Тема 1. Кинетика химических процессов и химическое равновесие
- •Раздел 1. Общие сведения о растворах (12 часов)
- •Тема 1. Физико-химические свойства растворов
- •Выводы по теме:
- •1. Растоворы – сложные системы, состоящие из растворителя, растворенных веществ и продуктов их взаимодействия.
- •Тема 2. Растворы электролитов
- •Выводы по теме:
- •Раздел 2. Дисперсные системы (8 часов)
- •Тема 1. Коллоидные растворы
- •Раздел 1. Окислительно–восстановительные процессы (6 часов)
- •Тема 1. Окислительно–восстановительные реакции
- •Раздел 2. Гетерогенные окислительно-востановительные процессы (12 часов)
- •Тема 1. I род электродных процессов. Электродные процессы и электродвижущие силы в гальванических элементах.
- •Тема 2. Электролиз
- •Тема 3. Коррозия и защита металлов
- •Раздел 1. Высокомолекулярные соединения (8 часов)
- •Тема 1. Полимерные материалы
- •1. Основная литература:
- •2. Дополнительная литература:
- •3. Справочная литература:
- •«Дальневосточный федеральный университет»
- •Школа естественных наук материалы лабораторных занятий
- •180100.62 – Кораблестроение, океанотехника и системотехникаобъектов морской инфраструктуры
- •Лабораторная работа №1 Определение молярной массы эквивалента металла
- •Экспериментальная часть
- •Лабораторная работа №2 Комплексные соединения
- •Экспериментальная часть
- •Лабораторная работа №3 Определение теплового эффекта реакции нейтрализации
- •Экспериментальная часть
- •Лабораторная работа №4 Химическая кинетика
- •Экспериментальная часть
- •Лабораторная работа №5 Гидролиз солей
- •Экспериментальная часть
- •Лабораторная работа № 6 Коллоидные растворы
- •Экспериментальная часть
- •Лабораторная работа № 7 Электрохимические процессы
- •Экспериментальная часть
- •Лабораторная работа № 8 Коррозия металлов
- •Экспериментальная часть
- •Опыт 4. Ингибиторная защита металла от коррозии в кислой среде
- •Лабораторная работа № 9 Общие свойства металлов
- •Экспериментальная часть
- •«Дальневосточный федеральный университет»
- •2.Закон эквивалентов
- •Элементы химической термодинамики
- •Химическая кинетика
- •Модуль 4. Растворы Способы выражения состава растворов
- •Равновесия в растворах электролитов
- •Коллигативные свойства растворов
- •Модуль 5. Основы электрохимии
- •1. Основная литература:
- •2. Дополнительная литература:
- •3. Справочная литература:
- •«Дальневосточный федеральный университет»
- •II. Строение атома. Периодическая система
- •III. Химическая связь
- •IV. Химическая термодинамика
- •V. Химическая кинетика и равновесие
- •VI. Растворы неэлектролитов
- •VII. Растворы электролитов
- •VIII. Ионообменные реакции
- •3. Какие пары ионов могут быть использованы при составлении молекулярного уравнения, которому отвечает ионное уравнение
- •IX. Дисперсные системы и поверхностные явления
- •X. Окислительно-восстановительные процессы
- •XI. Электрохимические процессы
- •XII. Коррозия
- •«Дальневосточный федеральный университет»
- •2. Дополнительная литература:
- •3. Справочная литература:
- •«Дальневосточный федеральный университет»
- •Школа естественных наук глоссарий
- •180100.62 – Кораблестроение, океанотехника и системотехникаобъектов морской инфраструктуры
- •«Дальневосточный федеральный университет»
- •Константы диссоциации слабых оснований
- •Стандартные окислительно-восстановительные потенциалы некоторых систем в водных растворах при 25 с
- •Потенциалы металлов
- •Произведение растворимости веществ в воде
- •Термодинамические константы некоторых веществ и ионов
Модуль 4. Растворы Способы выражения состава растворов
Раствораминазывают гомогенные системы, состоящие из двух и более компонентов. Компонент, агрегатное состояние которого не изменяется при образовании раствора, принято называтьрастворителем, а другой компонент –растворенным веществом. При одинаковом агрегатном состоянии компонентов растворителем считают то вещество, которое преобладает в растворе.
Способы выражения состава раствора:
Массовая доля
С![]() (Х)
илиW(X)
– число граммов растворенного
вещества, содержащееся в 100 г раствора.
(Х)
илиW(X)
– число граммов растворенного
вещества, содержащееся в 100 г раствора.
С![]() (Х)
=
(Х)
=![]() 100% илиС
100% илиС![]() (Х)
=
(Х)
=![]() 100%,
100%,
где m(Х) – масса растворенного вещества Х, г
m(раствора) - масса раствора, г
V![]() -
объем раствора, см
-
объем раствора, см![]()
![]()
![]() - плотность раствора, г/см
- плотность раствора, г/см![]() .
.
Молярная
концентрация С![]() илиС(Х) – число моль растворенного
вещества Х, содержащееся в 1дм
илиС(Х) – число моль растворенного
вещества Х, содержащееся в 1дм![]() или 1 л раствора ( молярность М ).
или 1 л раствора ( молярность М ).
С(Х) =
![]() или С(Х)
=
или С(Х)
=![]() [
[![]() ],
],
где n(Х) – количество растворенного вещества, моль
V–
объем раствора, дм![]() или
л
или
л
М(Х) – молярная масса растворенного вещества, г/моль.
Раствор, содержащий
1 моль растворенного вещества в 1 дм![]() ,
называется одномолярным (1М), содержащий
0,1 моль вещества – децимолярным (0,1М),
содержащий 0,01 моль вещества – сантимолярным
(0,01М) и т. д..
,
называется одномолярным (1М), содержащий
0,1 моль вещества – децимолярным (0,1М),
содержащий 0,01 моль вещества – сантимолярным
(0,01М) и т. д..
Молярная
концентрация эквивалента С![]() илиС (
илиС (![]() Х)
–число моль эквивалентов растворенного
вещества, содержащееся в 1 дм
Х)
–число моль эквивалентов растворенного
вещества, содержащееся в 1 дм![]() или
1 л раствора (нормальность раствора Н).
или
1 л раствора (нормальность раствора Н).
С (![]() Х)
=
Х)
= или С
(
или С
(![]() Х)
=
Х)
= ,
,
где n(![]() X)
– количество эквивалентов вещества Х,
моль;
X)
– количество эквивалентов вещества Х,
моль;
V-
объем раствора, дм![]() (л);
(л);
М (![]() Х)
– молярная масса эквивалента вещества
Х, г/моль.
Х)
– молярная масса эквивалента вещества
Х, г/моль.
Раствор, содержащий
1 моль эквивалентов растворенного
вещества в 1 дм![]() раствора, называется однонормальный
(1Н), содержащий 0,1 моль эквивалентов –
децинормальным (0,1Н) и т.д..
раствора, называется однонормальный
(1Н), содержащий 0,1 моль эквивалентов –
децинормальным (0,1Н) и т.д..
Для перевода одного способа выражения концентрации раствора в другой используются соотношения:
С(Х) =
![]() ; С(
; С(![]() Х)
=
Х)
= ; С(
; С(![]() Х)
=z C(X).
Х)
=z C(X).
Мольная доля– отношение числа моль данного вещества к сумме числа моль всех веществ, находящихся в растворе.
![]() =
=![]() ,
,
где n(X) – количество вещества Х в растворе, моль
N(X) – общее количество всех веществ в растворе, моль.
Моляльная концентрация Сm- число моль растворенного вещества Х приходящееся на 1 кг чистого растворителя.
Сm
=![]() ,
[
,
[![]() ]
]
Если для расчетов
используются массы всех веществ в
граммах, то формула имеет вид Сm
=
![]() , [
, [![]() ]
]
Пример 1.Вычислить массу гидроксида натрия и воды, необходимые для приготовления 2 л 10% раствора гидроксида натрия (плотность раствора равна 1,109 г/мл).
Решение:
а) Зная объем и плотность, находим
массу раствора, который необходимо
приготовитьm![]() =V
=V![]()
![]()
![]()
m![]() =
2000 мл ∙1,109 г/мл = 2218 г
=
2000 мл ∙1,109 г/мл = 2218 г
10% раствор NaOHв 100 г раствора содержит 10 гNaOH,
следовательно в 2218 г раствора содержится х г NaOH
x=![]() = 221,8 (г)
= 221,8 (г)
Массу воды, в
которой необходимо растворить 221,8 г
NaOH, находим по формулеm(H![]() O)
=m(раствора) –m(NaOH)
= 2218 – 221,8 = 1996,2 (г).
O)
=m(раствора) –m(NaOH)
= 2218 – 221,8 = 1996,2 (г).
б) Задачу можно решить, используя формулу массовой доли
C![]() (NaOH)
=
(NaOH)
=
![]() 100%, откуда
100%, откуда
m(NaOH) =![]()
m(NaOH)
=
![]() = 221,8 г
= 221,8 г
m(H![]() O)
=m(раствора) –m(NaOH)
= 2000 мл ∙ 1,109 г/мл – 221,8 г = 1996,2 г.
O)
=m(раствора) –m(NaOH)
= 2000 мл ∙ 1,109 г/мл – 221,8 г = 1996,2 г.
Ответ:221,8 гNaOHи 1996,2 гH![]() O
O
Пример 2.К 200 мл 28 % раствора соляной кислоты (плотность раствора равна 1,142 г/мл) добавили 500 мл воды. Вычислить молярную концентрацию полученного раствора и определить массовую долюHClв растворе.
Решение:Находим массу 28 % раствора соляной кислоты
m![]() =V
=V![]()
![]()
![]() = 200 мл ∙1,142 г/мл = 228,4 г
= 200 мл ∙1,142 г/мл = 228,4 г
Исходя из формулы
массовой доли C![]() (HCl)
=
(HCl)
=
![]() 100%,
100%,
находим m(HCl)
=
![]() =
=
![]() = 63,952 г.
= 63,952 г.
После добавления 500 мл воды количество HClне изменилось.
С(HCl)
=
![]() =
=
![]()
С(HCl)
=
![]() = 2,5 моль/л
= 2,5 моль/л
В 1 л раствора соляной кислоты содержится 2,5 моль HCl.
Массовую долю HClв полученном растворе находим по формуле
C![]() (HCl)
=
(HCl)
=
![]() 100%, =
100%, =![]() 100% = 8,78 %, в т.ч.m(воды) =V(воды)
100% = 8,78 %, в т.ч.m(воды) =V(воды)![]() (воды)
= 500 мл ∙1 г/мл = 500 г.
(воды)
= 500 мл ∙1 г/мл = 500 г.
В 100 г полученного раствора содержится 8,78 г HCl.
Ответ:С(HCl)
= 2,5 моль/л,C![]() (HCl)
= 8,78 %
(HCl)
= 8,78 %
Пример 3.Сколько мл 96 % серной кислоты (плотность равна 1,84 г/мл) нужно взять для приготовления 500 мл 0,1Hраствора серной кислоты?
Решение: Исходя из формулы молярной концентрации эквивалента,
С(![]() H
H![]() SO
SO![]() )
=
)
=

рассчитываем массу серной кислоты в 0,1 Н растворе
m(H![]() SO
SO![]() )
=C(
)
=C(![]() H
H![]() SO
SO![]() )∙M(
)∙M(![]() H
H![]() SO
SO![]() )∙V
)∙V
m(H![]() SO
SO![]() )
= 0,1моль/л
∙ 49 г/моль
0,5 л =2,45 г
)
= 0,1моль/л
∙ 49 г/моль
0,5 л =2,45 г
M(![]() H
H![]() SO
SO![]() )
=
)
=
![]() M(H
M(H![]() SO
SO![]() )
=
)
=
![]() 98 г/моль = 49 г/моль
98 г/моль = 49 г/моль
Из определения
массовой доли следует, что в 100 г раствора
содержится 96 г H![]() SO
SO![]() ,
а необходимая нам масса кислоты 2,45 г
содержится в х г 96 % раствора . 100 г раствора
- 96 гH
,
а необходимая нам масса кислоты 2,45 г
содержится в х г 96 % раствора . 100 г раствора
- 96 гH![]() SO
SO![]()
х г раствора -
2,45 г H![]() SO
SO![]()
х =
![]() = 2,55 г раствора 96 %H
= 2,55 г раствора 96 %H![]() SO
SO![]()
Разделив массу
раствора на его плотность, получим объем
96 % раствора H![]() SO
SO![]() .
.
V![]() =
=
![]() =
=
![]() = 1,39 мл
= 1,39 мл
Если для решения использовать формулу массовой доли
С![]() (H
(H![]() SO
SO![]() )
=
)
=
![]() 100 % , тоV
100 % , тоV![]() =
=
![]() 100 %
100 %
V![]() =
=
![]() = 1,39 мл
= 1,39 мл
Ответ:нужно
взять 1,39 мл 96 % раствораH![]() SO
SO![]() и
и
разбавить водой до 500 мл.
Пример 4.Для нейтрализации раствора, содержащего 0,04 г гидроксида натрия, потребовалось 10 мл раствора соляной кислоты. Вычислить молярную концентрацию эквивалента соляной кислоты.
Решение:NaOH+HCl=NaCl+H![]() O
O
Cогласно
закону эквивалентов, число моль
эквивалентов всех веществ, участвующих
в химической реакции одинаково:n(![]() NaOH)
=n(
NaOH)
=n(![]() HCl)
HCl)
или С(![]() NaOH)
∙V(NaOH) =C(
NaOH)
∙V(NaOH) =C(![]() HCl)
∙V(HCl).
HCl)
∙V(HCl).
Отсюда
C(![]() HCl)
=
HCl)
= =
=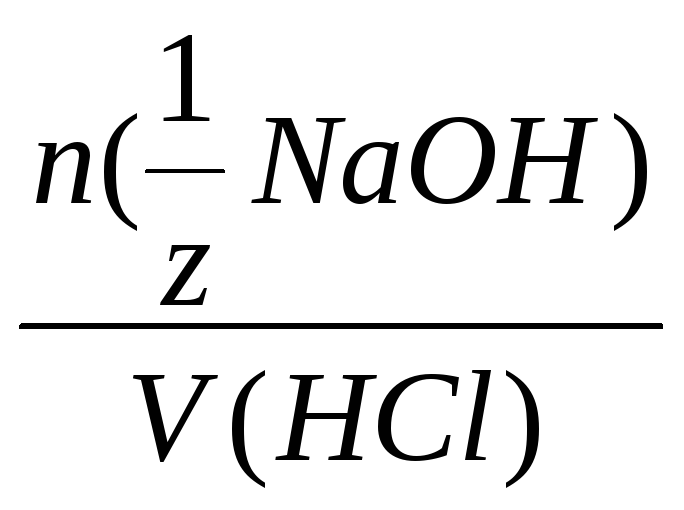 .
.
Зная массу гидроксида
натрия, определяем n(![]() NaOH)
=
NaOH)
= =
=
=
 = 0,001 моль.
= 0,001 моль.
Следовательно,
C(![]() HCl)
=
HCl)
=![]() = 0,1 моль/л.
= 0,1 моль/л.
Ответ: C(![]() HCl)
= 0,1 моль/л
HCl)
= 0,1 моль/л
Задания для самостоятельного решения:
1. Сколько граммов воды нужно взять для растворения 1 кг сахара, чтобы получить его 5 % раствор?
2. Определить молярную концентрацию эквивалента 8 % раствора серной кислоты (плотность раствора равна 1,06 г/мл).
3. Плотность 30 % раствора хлорида натрия равна 1,18 г/мл. Выразить состав раствора в мольных долях и в молях на 1 л раствора.
4. Плотность 2,3 % раствора аммиака равна 0,99 г/мл. Рассчитать молярную и моляльную концентрации раствора.
5. Сколько хлороводорода растворено в 50 мл 10 % раствора соляной кислоты (плотность раствора равна 1,05 г/мл)? Найти молярную концентрацию эквивалента соляной кислоты.
6. Сколько мл 70 % раствора нитрата калия (плотность раствора равна 1,6 г/мл) нужно взять, чтобы приготовить 500 мл раствора нитрата калия с молярной концентрацией 0,2 моль/л?
7. Вычислить массовую долю гидроксида калия в растворе с молярной концентрацией эквивалента 4,2 моль/л и плотностью 1,176 г/мл.
8. В каком объеме 0,2 Н раствора содержится 16 г сульфата меди (II)?
9. Смешали 100 мл 20 % раствора (плотность равна 1,1г/мл) и 200 мл 10 % раствора соляной кислоты (плотность равна 1,06 г/мл). Вычислить массовую долю и молярную концентрацию полученного раствора соляной кислоты.
10. Какова массовая доля азотной кислоты в растворе с молярной концентрацией 14,8 моль/л и плотностью 1,4 г/мл?
11. К 40 г фосфата натрия прилили 500 г 5 % раствора этого вещества. Вычислить массовую долю фосфата натрия в полученном растворе.
12. Рассчитать молярную концентрацию эквивалента 30 % раствора фосфорной кислоты (плотность раствора равна 1,18 г/мл).
13. Сколько мл
раствора щелочи с молярной концентрацией
эквивалента 0,1 моль/л потребуется для
осаждения в виде Fe(OH)![]() всего железа, содержащегося в 250 мл
раствора хлорида железа (III)cмолярной концентрацией
эквивалента 0,2 моль/л?
всего железа, содержащегося в 250 мл
раствора хлорида железа (III)cмолярной концентрацией
эквивалента 0,2 моль/л?
14. Сколько граммов 5 % раствора нитрата серебра требуется для обменной реакции со 120 мл раствора хлорида алюминия с молярной концентрацией эквивалента 0,6 моль/л?
15. Определить массовую долю, моляльную концентрацию и молярную концентрацию эквивалента следующих растворов:
а) в 600 мл раствора находится 5 г сульфата алюминия;
б) в 100 г воды растворили 1,71 г гидроксида бария;
в) 50 г хлорида кальция растворили в 250 мл воды;
г) 2,5 г карбоната калия в 400 мл раствора;
д) в воде объемом 300 мл растворили 50 г хлорида хрома (III).
Плотность растворов считать равной 1г/мл.
