
[Rukavishnikov_A.I.]_Azbuka_raka(BookFi.org)
.pdf
у шести из семи лабораторных мышей. При этом мыши не испытывали никаких неудобств от того, что этот фермент в их организмах не работает».
Анализ результатов позволил учѐным сделать вывод: раковые клетки не могут распространяться в отсутствие uPA, но «организму деятельность этого фермента не нужна». Эта идея затем была подтверждена в ходе новых экспери-
ментов: «мыши, которые в результате генетических манипуляций родились во-
все без uPA, никак не ощущали его отсутствия».
«Это значит, что мы можем блокировать этот фермент, – говорит один из учѐных, доктор М. Йонсен, – и таким образом предотвращать распространение раковых клеток без тяжѐлых побочных последствий для пациента, к которым приводят другие формы терапии».
Следующий шаг в этом направлении – создание препарата, который рабо-
тал бы на мышах. Только тогда можно приступать к решению вопроса о воз-
можности испытаний этого препарата на людях.
Доктор Т. Сковсгаард, специалист по раку из копенгагенской клиники
«Херлев», считает работу его коллег «очень многообещающей». «Если клини-
ческие испытания также покажут, что распространение раковых клеток может быть остановлено, – говорит он, – тогда станет ясно, что этой группе исследо-
вателей удалось найти ключ к этой проблеме».
«Это правда: терапия, которая предотвращала бы распространение рако-
вых клеток, стала бы большим шагом на пути лечения рака», – согласна К. Ло,
глава отдела клинических испытаний британского общества Cancer Research.
В заключение раздела, мы выделяем некоторые положения.
1. Утрата раковой клеткой контакта с соседними клетками и внеклеточ-
ным матриксом делает еѐ клеткой-организмом.
Опухолевая клетка без свойства инвазии создаѐт из себя незлокачествен-
ную опухоль. Удаление такой опухоли хирургическим методом обычно не-
трудно, и на этом прекращается сама болезнь.
Опухолевая клетка со свойством инвазии, т.е. раковая клетка, создаѐт из себя самую опасную болезнь – рак, которая пока неизлечимая.
140

2. Свойство инвазии раковой клетки делает еѐ смертельной для пациента,
страдающего от рака. Почему?
На этапе удаления первичного очага рака и регионарного метастазирова-
ния хирургическим методом невозможно удалить, не оставив хотя бы сколько-
то раковых клеток где-то в ткани. Из них, как клеток-организмов, нередко воз-
никает рецидив рака.
Проф. А.И. Барышников (2004) пишет так: «Как бы тщательно не удаляли рак, всегда остаются раковые клетки, из которых рак способен возродиться».
Объектом воздействия скальпеля хирурга является первичный очаг рака,
региональная клетчатка и другие ткани с лимфатическими узлами и незримые в границах операционного поля раковые клетки.
В настоящее время хирург-онколог, каждый в своей анатомической об-
ласти, достиг в технике операции предела, даже показывает чудеса в технике операции. Однако, для излечения рака с симптомами этого недостаточно, – да-
леко нередки рецидивы рака. Но главное другое.
Ведь рак в ткани до размера узелка 2 мм в диаметре – это ещѐ местная болезнь, а при размере больше этого, – становится системной болезнью из-за ангиогенеза и лимфангиогенеза в таком узелке, а значит, рассеивания клеток с кровью и лимфой.
Дж. Педжет (J. Paget, 1853), Н.Н. Петров (1910) и другие учѐные подчѐр-
кивали ограниченность хирургического метода для излечения от рака. Причина этого – инвазия раковых клеток в ткани органов не имеет границ и без конца.
Но молекулярные причины свойства к инвазии раковых клеток выяснены лишь теперь: молекула белка Src, ген инвазии и метастазирования mts1 и его белок – Мts 1, ген остеопонтин и его белок и другие.
Улучшение результатов хирургического метода лечения рака можно ожидать лишь, подавляя свойство к инвазии раковых клеток, действуя лекарст-
венными препаратами на эти молекулы, до операции и после операции. Пока это в практику врача-онколога не внедрено.
141

Если рак – это потомство из одной раковой клетки, то ясно, что для изле-
чения от него, необходимо уничтожить все раковые клетки. То есть путь к из-
лечению от рака один, и состоит в решении двух задач: 1) распознать в орга-
низме пациента каждую раковою клетку среди нормальных клеток и 2) унич-
тожить их все – «без остатка», не повреждая нормальные клетки.
Лучевое лечение и химиотерапия в стандартном виде неадекватны ни са-
мой ракой клетке, – эукариот среди нормальных эукариотов, составляющих ор-
ганизм человека, ни следствиям свойства к инвазии раковых клеток – инвазия в окружающие здоровые ткани и метастазы по всему организму.
В ближайшие годы XXI века к хирургическому методу лечения от рака будут добавлены новые методы, позволяющие решить эти две задачи.
Из новых методов – это экстракты из эмбриональных тканей или их бел-
ки, вакцины на основе дендритных клеток и другие вакцины, а также лекарства к генам-маркерам и белкам-маркерам раковых клеток, избирательно уничто-
жающие эти клетки, т.е. без побочных эффектов, ведь действовать они будут только на определѐнные гены и белки раковых клеток.
6.4. Метастазирование раковых клеток: молекулярные причины и
пути предотвращения
Другим, ещѐ более опасным следствием свойства инвазии раковых ство-
ловых клеток, является образование ими метастазов в различных органах паци-
ента.
Метастаз – это вторичный очаг рака, образующийся из-за метастазирова-
ния раковых клеток в отдаленные органы. Метастазирование (от греч. metastasis
– перемещение) – процесс переноса раковых клеток по кровеносным и ли-
мфатическим сосудам из первичного очага рака в другой орган или органы.
Ещѐ Ле Дран (H. Le Dran, 1685-1770) предположил, что рак может воз-
никнуть как локальная опухоль и лишь затем распространяется в регионарные лимфатические узлы.
142

В 1829 г. французский врач Ж.К. Рекамье (J. Recamier, 1774-1852) впе-
рвые доказал, что причиной метастазов являются раковые клетки. Он обнару-
жил инвазию вен раковыми клетками. Они переносятся в отдаленные участки тела. Из них там образуются «отдельные островки поражений», которые он на-
звал «метастазами». Как раковые клетки проникают в кровь и лимфу, долго ос-
тавалось не ясным.
Когда и в какой орган мигрировала первая раковая клетка, всегда не из-
вестно, как и возникновение первой раковой клетки где-то в ткани какого-либо органа. Если бы это знали, то могли бы уничтожить такую клетку, – не было бы ни рака, ни метастазов.
Причина в обоих случаях одна и та же – раковая клетка. Это объект мик-
роскопической величины, а поэтому невидимый глазом. Лишь при концентра-
ции в самом раке или метастазе 108–9 раковых клеток, они становятся видимыми глазом в органе при помощи методов – клиническое исследование, рентгено-
графия, УЗИ и др.
Метастазы раковой клетки – главная причина смерти пациентов при раке.
Причина в том, что лекарства стандартной химиотерапии неизбирательные, что не позволяет уничтожить все раковые клетки в организме пациента.
Ряд новых средств и методов от рака уже создан, но их лишь начинают внедрять в клиническую практику.
Метастазирование раковых клеток начинается с размера первичного узелка из раковых клеток размером 2 мм и даже 1 мм в диаметре, а к моменту видимых симптомов рака часть его клеток уже осела где-то в других органах
«как семена вторичного рака», т.е. метастазы. Это явление в литературе обо-
значается термином – диссеминация.
Из этого вывод: для адекватного лечения пациента только операции все-
гда недостаточно и необходимо дополнительное лечение – системное с помо-
щью лекарств.
Метастаз или метастазы образуется за счет инвазии раковых клеток сквозь стенку кровеносных и лимфатических капилляров и выходом в их про-
143

свет. С потоком лимфы клетки переносятся в лимфатические узлы, а с кровью – в различные отдаленные органы.
Метастазирование раковых клеток – это активный процесс и состоит из ряда этапов. Каждый этап контролируется разными генами через их продукт – белки в раковой клетке.
1-й этап. Некоторые клетки отделяются от первичного узелка из раковых клеток размером в 2 мм или 1 мм в диаметре и проникают через стенку питаю-
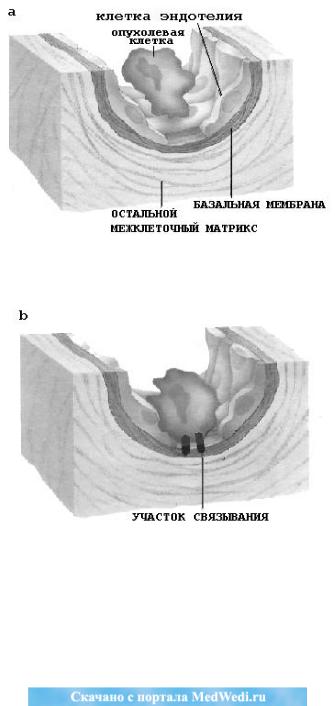
щих их капилляров, в их просвет. Они разносятся с кровью по организму до тех пор, пока не прикрепятся к эндотелию капилляров в каком-то органе или орга-
нах. В этом месте они вызывают сокращение клеток эндотелия и обнажают белковый матрикс – базальную мембрану (Рис. 1, а).
2-й этап. Раковые клетки прикрепляются к базальной мембране, связыва-
ясь с еѐ белками с помощью своих рецепторов, которыми распознают ко-
мпоненты базальной мембраны. Включив гены деструкции – протеиназ, они расщепляют белки матрикса и образуют в мембране отверстия (Рис. 2, b).
3-й этап. Раковые клетки вытягивают псевдоподии и проникают через от-
верстия, продолжая секретировать ферменты деструкции. Это позволяет им разрушать внеклеточный матрикс под базальной мембраной и затем внедряться в него (Рис. 3, c).
4-й этап. Для продвижения вперед в раковых клетках отключаются гены деструкции. Клетки утрачивают связь с матриксом на своей задней стороне, но цепляются псевдоподиями за матрикс впереди зоны лизиса, что приводит к ми-
грации самих клеток во внеклеточный матрикс и далее вглубь здоровой ткани
(Рис. 4, d).
Не все раковые клетки, проникшие в здоровую ткань, способны выжить.
За счѐт аутокринного стимула раковая клетка делится, образуя из своих потом-
ков узелок в 1-2 мм в диаметре – микрометастаз. В нѐм еще нет сосудов – ни кровеносных и ни лимфатических, и питательные вещества в него попадают через его поверхность путем диффузии (Г.П. Георгиев, 2000).
144
Из-за недостатка питания часть клеток в узелке «отмирает», но взамен их путѐм размножения клеток узелка образуются новые клетки. Это «дремлющий» микрометастаз или микрометастазы. Они могут оставаться в тканях органа
«многие годы», ни чем, не проявляя себя.
«Дремота» микрометастаза или микрометастазов «часто связана» с секре-
цией клетками первичного очага рака белков – ангиостатина и др., которые по-
давляют ангиогенез в микрометастазах (Г.П. Георгиев, 2000). В таком случае операция на первичном раке и путях лимфооттока вызывает ангиогенез в
«дремлющем» микрометастазе, и он начинает быстро расти за счет деления его клеток.
Рис.1, a. Сокращение клеток эндотелия, выстилающих кровеносные сосу-
ды, и обнажение базальной мембраны (рис. и цит. по: Л. А. Лиотта, 1992).
Рис. 2, b. Раковая клетка прикрепляется к базальной мембране, связываясь с определѐнными белками (рис. и цит. по: Л. А. Лиотта, 1992).
145

Рис. 3, c. Секретируемые раковой клеткой ферменты деструкции расщеп-
ляют белки матрикса, и в базальной мембране образуются отверстия (рис. и
цит. по: Л. А. Лиотта, 1992).
Рис.4, d. Раковая клетка внедряется во внеклеточный матрикс под базаль-
ной мембраной и затем вглубь ткани (рис. и цит. по: Л. А. Лиотта, 1992).
Для индукции ангиогенеза в раковой клетке включается ген фактора рос-
та эндотелия сосудов – VEGF, а также фактора роста фибробластов (FGFb).
Они синтезируются и выделяются раковой клеткой – это белки-лиганды.
Далее белок-лиганд вступает в контакт со своим рецептором на поверх-
ности клеток эндотелия мелких соседних венул окружающей ткани. По этому сигналу клетки эндотелия отделяются и мигрируют внутрь узелка и из них пу-
тѐм деления формируются кровеносные и лимфатические капилляры. Теперь при достатке питательных веществ и кислорода микрометастаз растѐт и превра-
щается в макрометастаз.
146

Как микрометастаз, так и макрометастаз являются новым местом, из ко-
торого раковые клетки мигрируют уже в другие органы и так без конца и гра-
ниц, что ускоряет ухудшение состояния пациента.
При ангиогенез в метастазах образуются кровеносные капилляры и сосу-
ды «мозаичного» типа, т.е. в их стенки встроены раковые клетки. Из стенок ка-
пилляров и сосудов раковые клетки ежедневно выходят в кровоток. Из этого важное следствие для практики: анализ на наличие раковых клеток в крови мо-
жет позволить выявлять рак в организме пациента на самом раннем этапе – при размере узелка из раковых клеток 1-2 мм в диаметре.
Познания этапов метастазирования раковой клетки и их молекулярных причин позволит: 1) найти гены-маркеры и белки-маркеры для предсказания метастазов у пациента; 2) использовать эти маркеры в качестве мишеней для приготовления избирательно действующих лекарств, и предотвращать ими ме-
тастазы и 3) уничтожать уже существующие у пациента микрометастазы и мак-
рометастазы.
В настоящее время учѐные, в том числе нашей страны, дали уже немало знаний о молекулярных причинах метастазирования раковой клетки.
1. П.С. Стиг (P.S. Steeg, 1991) и еѐ группа открыла ген и его продукт – бе-
лок nm23 в раковой клетке разного типа. Этот белок подавляет инвазию и мета-
стазирование раковых клеток. По этой причине белок nm23 получил название антиметастатический (от англ. – nonmetastatic).
Ген этот отсутствует или неактивен в раковых клетках, поэтому его про-
дукт белок nm23 в таких клетках отсутствует или дефектен. Это создаѐт свой-
ство инвазии раковой клетки и вызывает следствие этого, – образование мета-
стазов.
Низкое содержание белка nm23 в клетках первичного рака явно связано с метастазированием, а высокий уровень коррелирует с отсутствием метастазов раковой клетки и благоприятным прогнозом. Отсюда: белок nm23 может быть использован не только для ранней диагностики, но и для лечения от рака.
147

Так, П.С. Стиг вводила ген, кодирующий nm23 в культивируемые мета-
стазирующие клетки, что усиливало его экспрессию, т.е. синтез белка. Инъек-
ции таких раковых клеток мышам приводила к тому, что эти клетки оказыва-
лись «неспособными к образованию метастазов».
П.С. Стиг и еѐ группа считают, что метастазирование раковых клеток можно подавлять с помощью генотерапии, т.е. введением гена nm23 в раковые клетки. Теперь введение генов в клетки упрощается, если взять в качестве век-
тора вирус Т4.
2. Акад. Г.П. Георгиев и его группа (1999, 2000) открыли ген mts1 и его продукт – белок Mts1 или метастазин 1. Этот ген не является онкогеном, так как учѐные обнаружили, что при больших количествах белка Мts1 в нор-
мальной клетке, она не превращается в раковую клетку.
Ген mts1 экспрессируется во многих типах раковых клеток, а также в не-
которых нормальных клетках – в активированных макрофагах. В большинстве нормальных клеток ген «молчит» и его белок Mts1 отсутствует.
Введение конструкции: ген mts1 и регуляторный фрагмент в опухолевые клетки вызывало продукцию белка Mts1, и это резко усиливало способность клеток создавать метастазы при подкожной инъекции таких клеток мышам.
Введение конструкций, подавляющих синтез белка Mts1 в раковые клетки,
снижало способность клеток метастазировать.
Mts1 способен вызывать ангиогенез через «дезагрегацию клеток эндо-
телия и их активную пролиферацию».
Подавление гена или связывание его белка в раковых клетках будет по-
давлять метастатический фенотип раковых клеток.
Ген mts1 и его белок – Mts1 необходимо использовать также для ди-
агностики рака и контроля лечения пациента. На биочипах по титру иРНК этого гена и его белка Mts1 в образце крови от пациента удастся диагностировать ме-
тастазы рака.
148

Кроме этого, изменения в содержании гена и его белка в образце крови от пациента позволят следить за процессом лечения рака, а по отсутствию гена и его белка после лечения, – регистрировать излечение от метастазов рака.
3.Проф. Р. Бенезра (1999) и его группа из США открыли гены: JD-1 и JD-
3.Эти гены в норме экспрессируются в клетках эмбрионов мышей и человека.
Они через свой продукт – белки отвечают за рост и развитие кровеносной сис-
темы плода, но у взрослого человека они не зкспрессируются.
Однако, раковые клетки вновь «включают» эти гены и используют для размножения себя. JD-гены индуцируют ангиогенез в узелке из раковых клеток,
что препятствует их отмиранию.
Учѐные надеются разработать лекарства против этих мишеней – генов и их продукта, – белков. «Избавиться от самого гена, вместо того чтобы бороться с продуктами его работы, означает по-настоящему сделать человечество неуяз-
вимым для рака», – заявляют авторы открытия.
4. Молекулярный «переключатель» метастазирования раковых клеток.
Учѐные центра по изучению рака Техасского университета расшифровали молекулярные причины, вызывающие отделение раковых клеток от первичного очага рака и метастазирование в «различные части тела организма». Они под-
черкивают, что метастазирование сильно затрудняет лечение и зачастую при-
водит к смерти пациентов даже в случае успешного удаления первичного рака.
Исследователи называют открытый ими механизм «молекулярным пере-
ключателем» и утверждают, что это открывает большие возможности для раз-
работки новых методов против возникновения метастазов.
«Переключатель» представляет собой фермент GSK-3?, способный изме-
нять функции белков и может стать ключом к разработке эффективных средств лечения рака.
Было известно, что в эпителиальных клетках содержится много белка Е-
кадгерина, функция которого, – прикрепление клеток друг к другу.
Другой важный белок – фактор транскрипции, названный «снейл». Он контролирует ген, ответственный за синтез Е-кадгерина. Этот белок способен
149
