
- •Введение
- •Обзор литературы
- •1.1 Наиболее распространенные заболевания XXI века
- •1.2 Краткое описание лекарственных растений и входящих в их состав
- •Характеристика лекарственных растений и их химический состав
- •1.2.2 Биологически активные вещества (бав) лекарственного растительного сырья
- •1.3 Способы применения лекарственного растительного сырья
- •1.4 Примеры использования лекарственных растений в производстве мучных изделий
- •1.6 Использование лекарственных растений в производстве кондитерских изделий
- •1.7 Использование лекарственных растений в других пищевых производствах
- •1.8 Использование лекарственных растений в производстве макаронных изделий
- •Заключение по обзору литературных источников
- •2.3.1.5 Определение свойств крахмала по методике, разработанной на кафедре «Технология хлебопекарного производства» мгупп
- •2.3.1.6 Метод определения взаимодействия лекарственных сборов с крахмалом пшеничной муки
- •2.3.3.4 Определение кислотности (по гост р 52377–2005)
- •2.3.3.6 Определение содержания бав в макаронных изделиях
- •3 Экспериментальная часть
- •3.1.6 Влияние различных дозировок сборов на реологические показатели макаронного теста
- •3.1.7 Влияние различных дозировок сборов на качественные показатели готовой продукции и выбор оптимальных дозировок сборов
- •3.1.8 Определение содержания пищевых веществ в сборах, сухих и сваренных макаронных изделиях
2.3.3.6 Определение содержания бав в макаронных изделиях
Определение содержания суммы флавоноидов (ГОСТ 21908–93)
Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 1 мм. Около 1 г измельченного сырья помещают в коническую колбу вместимостью 100 см3 и прибавляют 50 см3 этилового спирта с объемной долей 60%, содержимое колбы встряхивают и взвешивают. Колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане 1,5 ч с момента закипания содержимого колбы. Колбу охлаждают до комнатной температуры, вновь взвешивают и при необходимости добавляют этиловый спирт с объемной долей 60 % до первоначальной массы. Извлечение фильтруют через складчатый бумажный фильтр в коническую колбу вместимостью 50 см3, отбрасывая первые 10 см3 фильтрата.
1 см3 фильтрата помещают в мерную колбу вместимостью 50 см3, прибавляют 4 см3 раствора алюминия хлорида с массовой долей 2 % в этиловом спирте с объемной долей 95 %, объем раствора доводят тем же спиртом до метки и перемешивают. Через 30 мин определяют оптическую плотность на ФЭКе при длине волны 440 нм в кювете с толщиной слоя 1 см.
Массовую долю суммы флавоноидов (Х) в процентах в пересчете на абсолютно сухое сырье вычисляют по формуле (8):
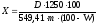 (9)
(9)
где D – оптическая плотность испытуемого раствора;
m – масса сырья, г;
W – потеря в массе при высушивании сырья, %.
Определение содержания аскорбиновой кислоты(витамина С)
Навеску сырья 1 г взвешивают и растирают в ступке с 15 мл 2 % раствора соляной кислоты. Полученный экстракт фильтруют и переносят по 1 мл фильтрата в 2 конические колбы на 50 мл. Добавляют в каждую колбу по 10 мл дистиллированной воды и титруют 0,001Н раствором 2,6 – дихлорфенолиндофенола из микробюретки. Окончание титрования узнают по появлению устойчивого розового окрашивания.
Содержание витамина С в 100 г определяют по формуле (9):
Х = 132*(а/Н) (10)
где а – объем раствора 2,6 – дихлорфенолиндофенола, пошедшего на титрование, мл;
Н – навеска сырья, г.
Определения содержания β-каротина в продукте с помощью ФЭКа (ГОСТ 8756.22 – 80)
Метод определения β-каротина в пищевых продуктах основан на измерении интенсивности светопоглощения его растворов. Как соединения с сопряженными двойными связями каротиноиды имеют характерные спектры поглощения в ультрафиолетовой и видимой областях. Максимум поглощения каротиноидов зависит от числа сопряженных двойных связей и от растворителя. Каротиноиды экстрагируют органическими растворителями, отделяют β-каротин от других каротиноидов с помощью адсорбционной хроматографии и измеряют поглощение его растворов на фотоэлектроколориметре при длине волны 450 нм.
В первую очередь необходимо построить градуировочный график. Для этого готовят стандартные растворы следующим образом: 36 мг бихромата калия растворяют в мерной колбе вместимостью 100 см и доводят объем до метки; 1 см3 такого раствора по окраске соответствует 2,08 мкг β-каротина в 1 см3. Далее готовят серию растворов сравнения. Для этого в ряд пробирок наливают 1,0; 1,5; 2,0; 2,5; 3,0; 3,5; 4,0 см свежеприготовленного стандартного раствора и доводят объем растворов до 10 см3 водой. Полученные растворы содержат соответственно 0,208; 0,312; 0,416; 0,52; 0,624; 0,728; 0,832 мкг каротина в 1см3. Измеряют на фотоэлектроколориметре оптическую плотность полученных растворов по отношению к воде в кюветах с расстоянием между рабочими гранями 1 см при длине волны 450 нм. Строят график зависимости оптической плотности раствора от массовой концентрации каротина (мкг/см3) D=f(c).
Далее осуществляют экстракцию каротина: из пробы продукта берут в ступку навеску массой 1-3 г с погрешностью не более ±0,01 г. Растирают в ступке с равным количеством кварцевого песка и 5-7 см3 ацетона. Ацетоновую вытяжку, не затрагивая осадка, фильтруют в делительную воронку через стеклянный фильтр. Экстракцию проводят до обесцвечивания последней порции ацетона. Ацетоновый фильтрат встряхивают в делительной воронке с 15 см3 второго экстрагента, в качестве которого используют гексан. Каротин переходит из нижнего ацетонового слоя в верхний гексановый слой. Если после встряхивания слои не разделяются, добавляют 1-2 см3 воды. После разделения слоев нижний водоацетоновый слой отбрасывают, а верхний слой промывают водой до полного удаления ацетона.
Измеряют оптическую плотность исследуемого раствора на фотоэлектроколориметре при длине волны 450 нм в кюветах с расстоянием между гранями 1 см против чистого растворителя (гексана).
По градуировочному графику находят массовую концентрацию каротина.
Массовую долю каротина (X) в процентах вычисляют по формуле (10):
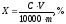 (11)
(11)
где С – концентрация каротина по графику, мкг;
V – объем элюата каротина, мл;
m – масса навески продукта, г.
Определение содержания органических кислот [18]
Свежие плоды, овощи или листья растений тщательно измельчают на терке или в ступке. Растительную массу перемешивают и берут навеску 20 г и переносят ее без потерь в коническую колбу на 200 мл. В колбу приливают 150 мл дистиллированной воды и выдерживают в течение 30 мин на водяной бане при температуре 80-90 ºС. Затем колбу охлаждают водопроводной водой, доводят до метки и фильтруют в сухой стакан. Полученный фильтрат служит для определения общей кислотности. 50 мл фильтрата переносят в коническую колбу емкостью 200-250 мл и добавляют в нее 50 мл 1н NaOH. Колбу нагревают на водяной бане при 80-90 ºС в течение 10 мин. Затем в колбу добавляют 50 мл 1,2н HCl и снова нагревают на бане в течение 10 мин. Затем раствор в колбе охлаждают. Наряду с определением свободной кислотности проводят «холодное» определение. Для этого вместо раствора берут 50 мл 1н NaOH, нагревают на бане, затем вносят 1,2 н HCl и снова нагревают.
После охлаждения растворов приступают к титрованию. Для этого в обе колбы добавляют по несколько капель спиртового раствора фенолфталеина и титруют 0,1 н NaOH до ярко-розового оттенка раствора. Если раствор сильно окрашен и переход окраски раствора при добавлении щелочи определить трудно, то при титровании пользуются лакмусовой бумажкой.
Количество миллиэквивалентных кислот, содержащихся в 100 мл раствора (в 10 г образца), определяем по формуле (11):
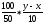 (12)
(12)
где у – число мл 0,1 н NaOH, затраченное на титрование исследуемого образца;
х – число мл 0,1 н NaOH, затраченное на титрование контроля.
Определение содержания дубильных веществ (ГОСТ 24027.2 – 80)
Навеску сырья 2 г помещают в коническую колбу вместимостью 500 см3, заливают 250 см3 нагретой до кипения воды и нагревают с обратным холодильником на кипящей водяной бане в течение 30 мин при периодическом перемешивании. Жидкость отстаивают, охлаждая до комнатной температуры и фильтруют около 100 см3 в коническую колбу вместимостью 200–250 см3 через вату, чтобы частицы сырья не попали в колбу. Затем отбирают пипеткой 25 см3 полученной жидкости в другую коническую колбу вместимостью 750 см3, добавляют 500 см3 воды, 25 см3 раствора индигосульфокислоты и титруют при постоянном перемешивании 0,1 н раствором калия марганцовокислого до золотисто-желтого окрашивания, сравнивая его с окраской раствора контрольного испытания.
Для проведения контрольного испытания в коническую колбу вместимостью 750 см3, добавляют 525 см3 воды, 25 см3 раствора индигосульфокислоты и титруют при постоянном перемешивании 0,1 н раствором калия марганцовокислого до золотисто-желтого окрашивания.
Содержание дубильных веществ (Х) в процентах в абсолютно сухом сырье вычисляют по формуле (12):
 (13)
(13)
где V – объем 0,1 н марганцовокислого калия, пошедшего на титрование извлечения, мл;
V1 - объем 0,1 н марганцовокислого калия, пошедшего на титрование в контрольном анализе, мл;
0,004157 – количество дубильных веществ, соответствующее 1 см3 0,1 н раствора марганцовокислого калия, г;
m – масса сырья, г;
W – потеря в массе при высушивании сырья, %;
250 – вместимость мерной колбы, см3;
25 – объем жидкого извлечения, взятого для титрования, см3.
