
- •Токсикологическая химия
- •1. Основы токсикологической химии. Организация и основы судебно-медицинской экспертизы в Российской Федерации
- •2. Биохимическая токсикология
- •2.1. Токсикокинетика чужеродных соединений. Общие закономерности распределения веществ в организме
- •2.2. Метаболизм чужеродных соединений.
- •3. Выделение чужеродных соединений.
- •3. Группа веществ, изолируемых минерализацией («металлические яды»
- •3.1. Общая характеристика группы
- •3.2. Токсидинамика и токсикокинетика металлических ядов
- •3.3.Методы минерализации
- •3.3.1.Методы мокрой минерализации
- •Метод минерализации смесью концентрированных серной, азотной кислот и воды (1:1:1)
- •3.4. Дробный метод анализа «металлических ядов»
- •3.4.1.Маскировка ионов в дробном анализе
- •3.4.2.Применение органических реагентов в дробном анализе "металлических ядов"
- •3.4.3.Применение диэтилдитиокарбаминовой кислоты и её солей
- •3.4.4.Применение дитизона
- •3.6.1.Свинец
- •3.6.2.Барий
- •3.6.3.Марганец
- •3.6.4.Хром
- •3.6.5.Серебро
- •3.6.6.Цинк
- •3.6.7.Медь
- •3.6.10.Ртуть
- •1. Сборка прибора и вытеснение из него воздуха водородом
- •2. Проверка прибора и реактивов на отсутствие мышьяка
- •Современные методы анализа металлов, используеме в аналитической и токсикологической химии (краткий обзор)
- •Группа веществ, изолируемых дистилляцией («летучие яды»)
- •4.1. Общая характеристика группы
- •4.2. Современные методы изолирования «летучих ядов»
- •4.3. Токсикологическое значение некоторых летучих ядов
- •4.3.1.Синильная кислота (цианистый водород, нитрил муравьиной кислоты)
- •4.3.2. Алкилгалогениды
- •4.4.Спирты
- •4.4.2. Химические свойства спиртов. Методы анализа в судебно-химической экспертизе отравлений и экспертизе алкогольного опьянения
- •5. Группа веществ, изолируемых из биологического материала экстракцией и сорбцией (лекарственные и наркотические вещества)
- •5.1.Общая характеристика группы. Номенклатура и классификация веществ
- •5.2. Методы изолирования веществ и их теоретические основы
- •5.2.1.Общие и частные методы изолирования
- •5.3. Аналитический скрининг лекарственных веществ, имеющих токсикологическое значение
- •5.4.1. Барбитураты и методы их исследования
- •1. Коматозное состояние и другие неврологические расстройства (оглушённость, сон, отсутствие рефлексов).
- •5.4.2. Кислота салициловая
- •5.4.3. Антипирин
- •5.4.4. Амидопирин
- •5.4.5. Кофеин
- •5.4.6. Теобромин
- •5.4.7. Теофиллин
- •5.5. Алкалоиды
- •5.5.1. Атропин
- •5.5.2. Скополамин
- •5.5.3. Кокаин
- •5.5.4. Новокаин
- •5.5.5. Дикаин
- •5.5.6. Платифиллин
- •5.5.7. Хинин
- •5.5.8. Резерпин
- •5.5.9. Стрихнин
- •Алкалоиды, производные изохинолина
- •5.5.10.Морфин
- •5.5.11. Кодеин
- •5.5.12. Этилморфин
- •5.5.13. Апоморфин
- •5.5.14. Промедол
- •5.5.15. Папаверин
- •5.5.17. Наркотин
- •5.5.18. Кониин
- •5.5.19. Ареколин
- •5.5.20. Никотин
- •5.5.21. Анабазин
- •5.5.22. Вератрин
- •5.5.23. Эфедрин
- •5.5.24. Производные фенотиазина
- •5.5.25. Производные 1.4-бензодиазепина
- •I этап Гидролиз 1,4-бенз-диазепина
- •II этап Гидролизат
- •III этап Экстракция 1,4-бенздиазепинов из гидролизата
- •IV этап
- •5.6. Аналитическая диагностика острых отравлений, наркотического опьянения. Анализ отдельных групп наркотических средств
- •5.6.1. Понятие о веществах, вызывающих одурманивание
- •5.6.2. Классификация наркотических и одурманивающих веществ
- •5.6.3. Особенности химико-токсикологического анализа на содержание одурманивающих средств
- •5.6.4. Требования, предъявляемые к работе лабораторий, занимающихся анализом наркотических и других одурманивающих веществ
- •5.6.5. Особенности интерпретации результатов при анализе биологических объектов на содержание веществ, вызывающих одурманивание
- •5.6.6. Правила отбора проб на обнаружение наркотических средств, психотропных и других токсических веществ
- •5.6.8. Характеристика биологических объектов. Пробоподготовка
- •5.6.9. Особенности исследования мочи на присутствие наркотиков
- •5.6.10. Экстракция как метод изолирования наркотических и одурманивающих средств. Основные понятия экстракции
- •5.7. Ненаправленный анализ наркотических и одурманивающих веществ
- •5.8. Химико-токсикологический анализ отдельных групп наркотических и одурманивающих веществ (направленный анализ)
- •5.8.1. Производные барбитуровой кислоты
- •5.8.2.Алкалоиды группы опия
- •5.8.3. Производные 1,4-бензодиазепина
- •5.8.4. Производные фенотиазина
- •5.8.5. Каннабиноиды
- •5.8.6. Кокаин
- •5.8.7. Амитриптилин
- •5.8.8. Димедрол (дифенгидрамин)
- •5.8.9. Промедол
- •5.8.10. Эфедрин, эфедрон
- •6. Группа веществ, изолируемых экстракцией и сорбцией. Пестициды
- •6.1. Пестициды как химические загрязнители
- •7. «Химико - токсикологический анализ веществ, изолируемых из объекта настаиванием с водой, с последующим диализом а также требующих или нетребующих особых методов изолирования»
3.6.2.Барий
Токсикологическое значение
Из соединений бария токсикологическое значение имеют его гидроксид, хлорид, нитрат, карбонат, хлорат и др. Все растворимые соли бария ядовиты. Соединения бария применяю для получения препаратов бария, в керамическом и стекольном производстве (ВаСОз), в текстильной и резиновой промышленности, в сельском хозяйстве (ВаС12) для борьбы с вредителями растений; селенит бария (BaSeО3) и бария карбонат применяют для дератизации. Некоторые препараты бария, например бария хлорид, гидрат окиси бария, имеют применение в аналитических лабораториях. Бария сульфат, применяемый при рентгеноскопии, практически нетоксичен. Смерть наступает от паралича сердца.
В истории отравлений барием различают два периода: первый - до введения бария сульфата в качестве контрастного вещества при рентгенологическом исследовании желудочно-кишечного тракта, второй - после введения бария сульфата в рентгеноскопию. В первом периоде отравления соединениями бария были редкими. Причиной их было применение бария карбоната в смеси с мукой для отравления крыс или бария хлорида для аппретуры белья. С момента внедрения бария сульфата в медицинскую практику отравления солями бария стали встречаться чаще. Причиной этих интоксикаций, как правило, является бария сульфат, нерастворимый в воде и в жидкостях организма, а растворимые соли его, содержащиеся в бария сульфате в виде примесей, или ошибочное применение растворимых солей бария вместо бария сульфата. Известны случаи отравления бария карбонатом, находящимся в бария сульфате в виде примесей. Такие отравления объясняются тем, что для рентгеноскопии используют большие (до 100 г и более) количества бария сульфата, который по способу своего получения может содержать бария карбонат, переходящий в организме под влиянием соляной кислоты желудочного сока в растворимый бария хлорид.
При приеме внутрь ядовитых соединений бария возникают жжение во рту, боли в области желудка, слюнотечение, тошнота, рвота, головокружение, мышечная слабость, одышка, замедление пульса и падение артериального давления. Основной метод лечения отравлений барием - промывание желудка и употребление слабительных средств. Основными источниками поступления бария в организм человека являются пища (особенно морепродукты) и питьевая вода. По рекомендации Всемирной организацией здравоохранения содержание бария в питьевой воде не должно превышать 0,7 мг/л, в России действуют гораздо более жесткие нормы - 0,1 мг/л.
Соединения бария оказываются нейротоксическое (паралитическое), кардиотоксическое, гемотоксическое действия. Основные симптомы: жжение во рту и пищеводе, боли в животе, тошнота, рвота, диарея, головокружение; кожные покровы бледные, покрыты холодным потом. Пульс медленный, слабый; экстрасистолия, мерцание предсердий, возможна остановка сердца; снижение АД; одышка, цианоз. Через 2-3 ч после отравления - нарастающая мышечная слабость (особенно мышц верхних конечностей и шеи), иногда гемолиз.
Соединения бария выделяются из организма главным образом через кишечник. Следовые количества этих соединений выводятся через почки и частично откладываются в костях. Сведения о содержании бария как нормальной составной части клеток и тканей организма в литературе отсутствует.
Патологоанатомическая картина неспецифична: наблюдаются гиперемия и кровоизлияния в слизистой оболочке желудка, кишках, серозных покровах и в легких, жировое перерождение печени. Химико-токсикологическое исследование оказывает серьезную помощь в диагностике отравлений. Выделение бария происходит главным образом через желудочно-кишечный тракт. Ва2+ в незначительных количествах содержится во всех органах и тканях живых существ в качестве естественной составной части организма (А. О. Войнар).
Исследование фильтрата на барий
1. Реакция перекристаллизации BaSО4 из концентрированной кислоты серной.
Часть исследуемого осадка на фильтре переносят на предметное стекло и слегка подсушивают. Затем к осадку прибавляют 2 капли концентрированной кислоты серной и осторожно нагревают до появления паров. (Кислота серная не должна растекаться на предметном стекле). При наличии в осадке бария сульфата на стекле через 15 – 20 мин после охлаждения появляются бесцветные кристаллы, имеющие форму квадратов с вытянутыми углами или в виде мелких крестов и прямоугольных пластинок.
2. Реакция образования бария йодата
BaSO4
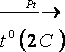 BaS + 2 CO2
BaS + 2 CO2
BaS + 2 HCl ® BaCl2 + H2S
BaCl2 + 2 KIO3 ® Ba(IO3)2 + 2 KCl
На предметное стекло наносят несколько капель 10 % раствора кислоты хлороводородной. Затем платиновой петлёй забирают часть исследуемого осадка и нагревают его в восстановительной части пламени горелки. При этом бария сульфат восстанавливается в бария сульфид, а пламя горелки окрашивается в зелёный цвет.
При исследовании больших количеств осадка и при поступлении на химико–токсикологический анализ химических соединений бария возможно проведение дополнительных подтверждающих реакций.
3. Реакция с калия бихроматом
2 BaCl2 + K2Cr2O7 + H2O![]() 2
BaCrO4 ¯ + 2 KCl + 2 HCl
2
BaCrO4 ¯ + 2 KCl + 2 HCl
Выпадает жёлтый кристаллический осадок.
Реакция с кислотой серной
BaCl2 + H2SO4 ® BaSO4 ¯ + 2 HCl
Выпадает белый кристаллический осадок.
5. Реакция с натрия родизонатом
В присутствии катиона бария на бумаге появляется красновато–коричневое пятно не исчезающее от добавления капли кислоты хлороводородной (отличие от стронция).
Объектами исследования на наличие бария могут быть не только органы трупов и биологические жидкости, но и химические соединения этого металла, которые в народном хозяйстве широко используются для борьбы с вредителями сельскохозяйственных культур и для других целей.
Исследование минерализата после отделения осадка
(BaSО4 и PbSО4)
Исследование обычно начинают с Mn2+ и Cr 3+, так как определенное мешающее влияние оказывают Cl-. В основу обнаружения и определения этих катионов положены реакции окисления – восстановления.
