
- •ПРЕДИСЛОВИЕ
- •ГЛАВА 1. ВЫСОКОТЕМПЕРАТУРНАЯ ФИКСАЦИЯ АЗОТА
- •ХОЛОДИЛЬНЫЕ ЦИКЛЫ
- •Холодильный цикл среднего давления с расширением воздуха в детандере (цикл Клода)
- •ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ ПРОЦЕССОВ КОНВЕРСИИ ПРИРОДНОГО ГАЗА
- •РАВНОВЕСИЕ РЕАКЦИЙ КОНВЕРСИИ МЕТАНА ВОДЯНЫМ ПАРОМ
- •КАТАЛИЗАТОРЫ КОНВЕРСИИ МЕТАНА
- •Кинетика конверсии метана
- •КОНВЕРСИЯ ОКСИДА УГЛЕРОДА (II)
- •КАТАЛИЗАТОРЫ КОНВЕРСИИ ОКСИДА УГЛЕРОДА (II)
- •КИНЕТИКА КОНВЕРСИИ ОКСИДА УГЛЕРОДА (II)
- •ТЕХНОЛОГИЧЕСКИЕ СХЕМЫ КОНВЕРСИИ ПРИРОДНОГО ГАЗА
- •ОСНОВНОЕ ТЕХНОЛОГИЧЕСКОЕ ОБОРУДОВАНИЕ ПРОЦЕССОВ КОНВЕРСИИ ПРИРОДНОГО ГАЗА
- •Очистка газов от диоксида углерода водными растворами аминоспиртов
- •Очистка газов от диоксида углерода водными растворами карбонатов щелочных металлов
- •ОЧИСТКА КОНВЕРТИРОВАННОГО ГАЗА ОТ ОКСИДА УГЛЕРОДА (II)
- •РАВНОВЕСИЕ РЕАКЦИИ СИНТЕЗА АММИАКА
- •КАТАЛИЗАТОРЫ СИНТЕЗА АММИАКА
- •КИНЕТИКА СИНТЕЗА АММИАКА
- •ВЫДЕЛЕНИЕ АММИАКА ИЗ ПРОРЕАГИРОВАВШЕЙ АЗОТОВОДОРОДНОЙ СМЕСИ
- •ТЕХНОЛОГИЧЕСКИЕ СХЕМЫ СИНТЕЗА АММИАКА
- •ТЕХНОЛОГИЧЕСКОЕ ОБОРУДОВАНИЕ БЛОКА СИНТЕЗА АММИАКА
- •Теплообменная аппаратура
- •Аппаратура для выделения жидкого аммиака
- •Пути совершенствования схем синтеза аммиака
- •ГЛАВА 6. ПРОИЗВОДСТВО АЗОТНОЙ КИСЛОТЫ
- •ОКИСЛЕНИЕ АММИАКА
- •ОКИСЛЕНИЕ ОКСИДА АЗОТА (II)
- •ТЕХНОЛОГИЧЕСКИЕ СХЕМЫ ПОЛУЧЕНИЯ АЗОТНОЙ КИСЛОТЫ
- •ПРОИЗВОДСТВО КОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТЫ
- •Прямой синтез концентрированной азотной кислоты
- •ГЛАВА 7. ПРОИЗВОДСТВО АЗОТНЫХ УДОБРЕНИЙ
- •ПРОИЗВОДСТВО СУЛЬФАТА АММОНИЯ
- •ПРОИЗВОДСТВО НИТРАТА АММОНИЯ
- •ПРОИЗВОДСТВО КАРБАМИДА
- •ТЕХНОЛОГИЧЕСКИЕ СХЕМЫ СИНТЕЗА КАРБАМИДА
- •ЖИДКИЕ АЗОТНЫЕ УДОБРЕНИЯ
- •ЛИТЕРАТУРА
- •ОГЛАВЛЕНИЕ

30 |
Глава 2 |
Для адиабатического (изоэнтропного) расширения газов абсолютные температуры и давления в начале и конце процесса связаны следующим соотношением:
K 1
T2 P2 K ,
T1 P1
где T1, Т2 – начальная и конечная температура, К; Р1, P2 – начальное и конечное давление; K – показатель адиабаты расширения, равный отношению Cp : CV. Для воздуха K = 1,4.
Для воздуха, расширяющегося от 8 до 0,1 МПа при начальной температуре 20°С, конечная температура T2, рассчитанная по указанному уравнению, равна 84 К, или –189°С. В действительности достигаемое понижение температуры меньше вычисленного.
В практических расчетах изменение температур и энтальпий газов в процессе их расширения определяют по термодинамическим диаграммам, в частности по энтропийной диаграмме S – T.
ХОЛОДИЛЬНЫЕ ЦИКЛЫ
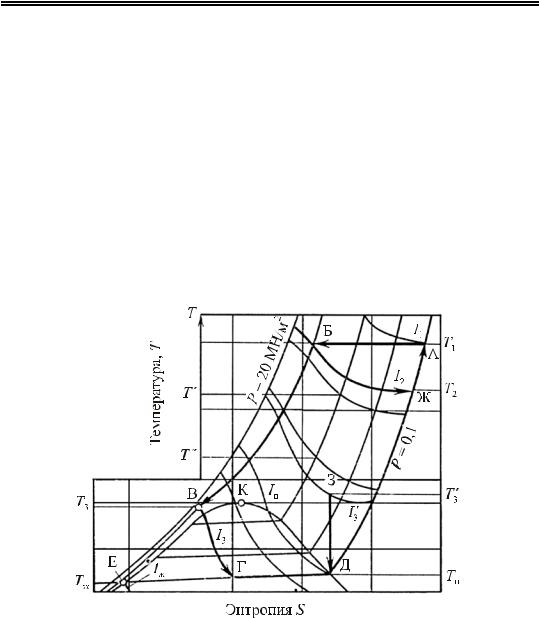
Для охлаждения и сжижения газов в технике применяют холодильные циклы. Холодильным циклом называется замкнутый процесс последовательного сжатия и расширения газов, который сопровождается их нагреванием и охлаждением. Тепловые процессы, происходящие при этом, наиболее удобно изучать с помощью энтропийных диаграмм S – T. Диаграмма S – T для воздуха представлена на рис. 5.
По этой диаграмме можно проследить ход процессов, протекающих при постоянных температуре, давлении, энтальпии, энтропии, а также определить интегральный эффект Джоуля – Томпсона, изотермический эффект дросселирования, эффекты адиабатического и политропического расширения воздуха в детандерах, долю воздуха, сжижаемого при дросселировании. На этой диаграмме нанесены:
–AБ – линия изотермического сжатия при температуре Т1;
–БЖ – линия дросселирования газа при I2 = const; интегральный эффект дросселирования ∆Т' = Т1 – Т2; изотермический эффект дросселирования ∆I = I1 – I2, Дж/кг;
–БВ – линия охлаждения газа в теплообменнике при р = const от температуры Т1 до Т3;
Производство азота и кислорода из воздуха криогенным методом 31
– ВГ – линия дросселирования при I3 = const в области влажного пара ∆Т" = Т3 – Тж;
–ГД – линия испарения жидкости после дросселирования, отношение ГД / ЕД определяет долю жидкости x (кг жидкости / кг сжатого газа) в конце процесса дросселирования;
–ЕГД – линия испарения сжиженного газа (теплота испарения жидкости r = Ip – Iж, Дж/кг;
–ДА – линия нагрева в теплообменнике сухого насыщенного пара до начальной температуры Т1 при р = const;
–ЗД – линия адиабатического расширения газа с совершением
внешней работы; изменение температуры при этом ∆Т = Т3' – Тр; изменение энтальпии ∆I = I3' – Ip, Дж/кг.
Рис. 5. Диаграмма S – T для воздуха
Таким образом, зная параметры воздуха до и после расширения, можно определить долю сжиженного воздуха, а также энергетические затраты на сжижение.
Холодильные циклы, применяемые для сжижения газов, можно разделить на две группы – дроссельные циклы, основанные на использовании эффекта Джоуля – Томпсона, и детандерные, основанные на расширении газов с совершением внешней работы.
В промышленности применяется большое количество холодильных циклов. Рассмотрим некоторые из них.
32 |
Глава 2 |
Холодильный цикл высокого давления с однократным дросселированием сжатого воздуха
(цикл Линде)
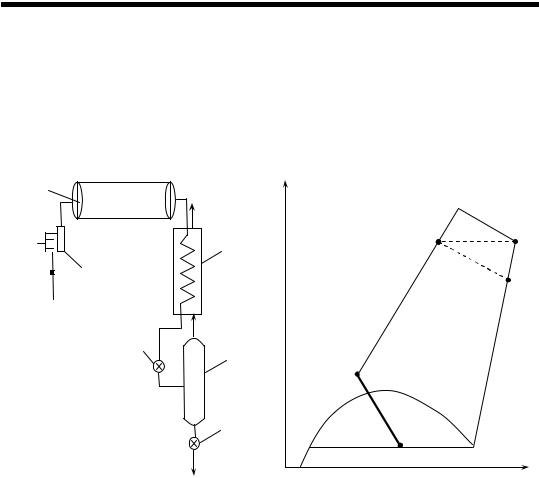
Схемы этого цикла и его изображение на диаграмме S – T представлены на рис. 6.
2 |
|
Т |
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
i1 |
|
|
|
|
3 |
|
|
|
|
3 |
|
|
|
1 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
1 |
|
|
|
|
i3 |
1' |
|
|
|
i2 |
|
|
|
Воздух |
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
5 |
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
Жидкий воздух |
6 |
0 |
5 i0 |
|
|
6 |
|
|
|
|
|||
а |
|
|
б |
|
|
S |
|
|
|
|
|
Рис. 6. Схема цикла с однократным дросселированием воздуха (а) и его изображение на диаграмме S – T (б):
1 – компрессор; 2 – водяной холодильник; 3 – противоточный теплообменник; 4 – дроссельный вентиль;
5 – сборник жидкого воздуха; 6 – вентиль слива жидкого воздуха
Воздух сжимается в компрессоре до давления 20 МПа, проходит водяной холодильник 2, где охлаждается до исходной температуры и поступает в трубное пространство противоточного теплообменника 3, где охлаждается обратным потоком несконденсировавшейся части воздуха до температуры, близкой к температуре конденсации.
Затем охлажденный воздух дросселируется в вентиле 4 до исходного давления и сильно охлаждается. При этом часть воздуха конденсируется и выводится на ректификацию. Несконденсировавшаяся часть воздуха поступает в межтрубное пространство противоточного теплообменника 4, где отдает свой холод сжатому

Производство азота и кислорода из воздуха криогенным методом 33
воздуху и нагревается до исходной температуры, после чего выбрасывается в атмосферу. Изображение этого цикла на диаграмме S – T представлено на рис. 6, б.
На этом рисунке линия 1–2 изображает сжатие воздуха в компрессоре; 2–3 – охлаждение воздуха в водяном холодильнике до исходной температуры; 1–3 – изотермическое сжатие воздуха; 3– 4 – охлаждение сжатого воздуха в противоточном теплообменнике; 4–5 – дросселирование сжатого воздуха до исходного давления, в результате чего температура снижается и часть воздуха конденсируется; линия 5–6–1 – испарение жидкого воздуха и нагревание несконденсировавшейся части воздуха в противоточном теплообменнике до исходной температуры. Долю сжиженного воздуха x можно определить по соотношению отрезков 5–6 и 0–6:
x 50––66 .
Для определения доли сжиженного воздуха составим тепловой баланс цикла на 1 кг воздуха.
Обозначим x – доля сжиженного воздуха; i0 – энтальпия жидкого воздуха, кДж/кг; i1, i2 – энтальпия воздуха при P1 и P2. С учетом тепла, отводимого в водяном холодильнике, приход тепла
Q1 = i3.
Расход тепла составит
Q2 = xi0 + (1 – x)i1.
Q1 = Q2, следовательно
i3 = xi0 + (1 – x)i1.
Решая это уравнение, получим:
x i1 i3 . i1 i0
Однако данное уравнение не учитывает потери холода. В действительности всегда наблюдаются потери холода через теплоизоляцию и за счет недорекуперации, так как температура расширившегося воздуха на выходе из теплообменника всегда ниже исходной температуры.
С учетом потерь холода
