- •Классификация аминокислот.
- •4. Простые и сложные белки, их классификация. Характер связей простетических групп с белком. Биологические функции белков. Способность к специфическим взаимодействиям с лигандом.
- •5. Углеводсодержащие белки: гликопротеины, протеогликаны. Основные углеводы организма человека: моносахариды, дисахариды, гликоген, гетерополисахариды, их структура и функции.
- •8. Хромопротеины, их классификация. Флавопротеины, их структура и функции. Гемопротеины, структура, представители: гемоглобин, миоглобин, каталаза, пероксидаза, цитохромы. Функции гемопротеинов.
- •13. Энзимопатия у детей и важность их биохимической диагностики (на примере нарушения азотистого и углеводного обмена).
- •14. Витамины, классификация витаминов (по растворимость и функциональная). История открытия и изучения витаминов.
- •15. Витамин а, структура, участие в обменных процессах. Гипо- гипер- и авитаминоз а, их причины и особенности проявления. Пищевые источники, суточная потребность.
- •17. Витамин рр, структура коферментов, участие в обменных процессах. Гипо - и авитаминоз рр. Пищевые источники, суточная потребность.
- •18. Витамин в2, структура коферментов, участие в обменных процессах. Гиповитаминоз и авитаминоз в2. Суточная потребность, пищевые источники.
- •19. Витамин с, структура, участие в обменных процессах. Гипо- и авитаминоз с. Пищевые источники, суточная потребность.
- •20. Витамин в1, структура кофермента, участие в обменных процессах. Гиповитаминоз и авитаминоз в1. Пищевые источники, суточная потребность.
- •21. Витамин в6, структура кофермента, участие в обменных процессах. Гиповитаминоз и авитаминоз в6. Пищевые источники, суточная потребность.
- •22. Пантотеновая кислота и биотин, их участие в обменных процессах. Гиповитаминозы и авитаминозы в3 и н. Суточная потребность, источник этих витаминов.
- •23. Фолиевая кислота и кобаламин, их участие в обменных процессах, авитаминозы. Пищевые источники, суточная потребность.
- •24. Витамин е и к, участие их в обменных процессах. Гиповитаминозы и авитаминозы этих витаминов. Пищевые источники, суточная потребность.
- •25. Возрастные потребности в отдельных витаминах у ребенка. Особенности проявления гипо- и авитаминозов в раннем детском возрасте.
- •27. Гормоны гипоталамуса – либерины и статины. Химическая природа. Механизм их действия на молекулярном уровне, биологический эффект.
- •29. Гормоны задней доли гипофиза: вазопрессин, окситоцин. Химическая природа. Механизм их действия, биологический эффект. Нарушения функций организма, связанные с недостатком выработки этих гормонов.
- •32. Паратгормон и кальцитонин. Химическая природа. Механизм действия на молекулярном уровне. Влияние на обмен кальция, гиперкальциемия и гипокальциемия.
- •35. Половые гормоны: андрогены, эстрогены. Химическая природа. Механизм действия на молекулярном уровне, влияние на обмен веществ. Нарушения обмена при недостатке и избытке этих гормонов в организме.
- •45. Свободно-радикальное окисление. Токсичность кислорода: образование активных форм кислорода, их действие на липиды и другие вещества клетки. Механизм защиты: антиоксидантные системы
- •58. Своеобразие метаболизма гликогена в печени у ребенка. Патология обмена гликогена (гликогенозы).
- •60. Лабильность уровня глюкозы в крови у детей раннего возраста. Наклонность к гипогликемии. Своеобразие учета результатов нагрузной пробой сахара у детей.
- •62. Особенности переваривания и всасывания жиров в организме ребенка.
- •72. Повышенная активность биосинтеза и распада нейтральных жиров в тканях ребенка. Бурый жир, его значение.
- •73. Неустойчивость липидного обмена, связанная с недостаточно сформированной нейроэндокринной регуляцией. Кетонемия и ацетонемия у детей. Факторы, способствующие их развитию.
- •75. Патология обмена холестерина у детей. Наследственные нарушения липидного обмена: семейная гиперхолестеринемия и семейная триглицеридемия.
- •76. Обмен аминокислот и белков в питании ребенка. Понятие об азотистом балансе. Физиологическая азотемия новорожденных.
- •79. Замедленное переваривание белков в желудке у детей. Особенности исследования функции желудка в детском возрасте.
- •84. Обмен фенилаланина и тирозина. Образование катехоламинов, гормонов щитовидной железы, меланина. Нарушения процессов распада тирозина: фенилкетонурия, алкаптонурия, альбинизм.
- •85. Лабильность дезаминирования в гепатоцитах ребенка. Повышенная концентрация аминокислот в крови и моче ребенка раннего возраста. Своеобразие обмена некоторых аминокислот. Фенилаланин, тирозин.
- •89. Биосинтез пиримидиновых нуклеотидов, этапы этого процесса. Оротацидурия. Распад пиримидиновых нуклеотидов. Биосинтез дезоксирибонуклеотидов. Участие утф и цтф в обменных процессах.
- •91. Обмен нуклеиновых кислот и нуклеотидов у ребенка. Генетические нарушения, связанные с наследственными заболеваниями.
- •92. Биосинтез днк (репликация): стехиометрия реакций, днк-полимераза, матрица. Повреждение и распад днк.
- •93. Биосинтез рнк (транскрипция): рнк-полимераза, стехиометрия реакции, днк как матрица. Регуляция транскрипции. Посттранскрипционная достройка рнк. Молекулярные мутации. Наследственные болезни.
- •94. Биосинтез белков (трансляция). Стадии биосинтеза белка на рибосоме. Универсальность биологического кода и
- •96. Распад гема. Билирубин как продукт распада гема. Метаболизм билирубина. Нарушение его обмена. Желтухи и их биологическая диагностика.
- •97. Физиологическая желтуха новорожденных, ее причины.
- •98. Обмен гемоглобина у детей. Типы и виды гемоглобина. Его возрастная эволюция. Возрастные особенности 2,3-дфг эритроцита. Гемоглобинопатии.
- •101.Возрастные колебания общего белка крови и его фракции. Наличие фетальных белков в крови. Иммуноглобулины. Неспецифические факторы защиты.
- •103.Возрастные особенности содержание и распределения воды в организме ребенка. Лябильность водного обмена. Физиологическая потеря жидкости новорожденными.
- •106.Важность минеральных солей для обменных процессов у детей (пластическая и регуляторная роль). Значение прикорма ребенка для уменьшения дефицита минеральных солей.
- •110. Мукополисахаридоз у детей – наследственная лизосомальная болезнь накопления.
- •113.Роль креатинфосфата в мышечном сокращении у ребенка. Физиологическая креатинурия. Врожденные энзимопатии (фосфорилаза и фосфоглюкомутаза), приводящие к патологии мышечной системы.
- •114.Биохимия мышечной ткани у детей.
- •118.Своеобразие химического состава и метаболических процессов мозга плода и у ребенка раннего возраста.
- •120.Важность определения функционального состояния печени в детском возрасте.
- •121.Возрастные особенности процессов гниения в желудочно-кишечном тракте ребенка.
- •123.Характеристика периода новорожденности и его биохимические аспекты. Биохимические сдвиги новорожденного впервые часы постнатального периода.
- •124.Своеобразие метаболизма ребенка и его регуляция в различные возрастные периоды. Биохимические критерии, характеризующие отдельные возрастные этапы.
- •126.Особенности обмена веществ у ребенка раннего возраста. Несовершенство высших форм регуляции. Своеобразие гормональной регуляции.
- •127.Изменения ферментативных систем в ходе индивидуального развития организма как проявление биохимической адаптации. Срочная и замедленная адаптация.
91. Обмен нуклеиновых кислот и нуклеотидов у ребенка. Генетические нарушения, связанные с наследственными заболеваниями.
Обмен нуклеиновых кислот. В клетках тканей нуклеиновые кислоты распадаются под влиянием ферментов. Ферменты, расщепляющие полинуклеотидные цепи, называют нуклеазами, или фосфодиэстеразами, так как они ускоряют реакции разрыва межнуклеотидных фосфодиэфирных связей в молекулах нуклеиновых кислот. Различают эндонуклеазы и экзонуклеазы. Эндонуклеазы действуют на внутренние межнуклеотидные связи в молекулах ДНК и РНК. Таким образом, при их участии осуществляется деполимеризация нуклеиновых кислот, в основном до олигонуклеотидов. Экзонуклеазы отщепляют нуклеотиды с 3′- или 5'-конца полинуклеотидной цепи и обеспечивают распад нуклеиновых кислот до свободных нуклеотидов. По специфичности действия различают дезоксирибонуклеазы (ДНКазы, расщепляющие ДНК) и рибонуклеазы (РНКазы, гидролизующие РНК). В результате их действия образуются олигонуклеотиды и лишь небольшое количества мононуклеотидов. Рибо- и дезоксирибонуклеозидфосфаты расщепляются до нуклеозидов и фосфорной кислоты под действием фосфатаз (нуклеотидаз). Нуклеозиды могут расщепляться гидролитическим путем с участием фермента нуклеозидазы: Аденозин + Н2О → Аденин + рибоза Пентозы окисляются до CO2 и H2O; фосфорная кислота используется для фосфорилирования органических соединений или выводится из организма. Азотистые основания превращаются в конечные продукты обмена и выделяются с мочой. Продукты гидролиза нуклеиновых кислот поступают в клетки организма, где используются для синтеза нуклеотидов, нуклеиновых кислот, или же для удовлетворения энергетических потребностей клетки и организма.
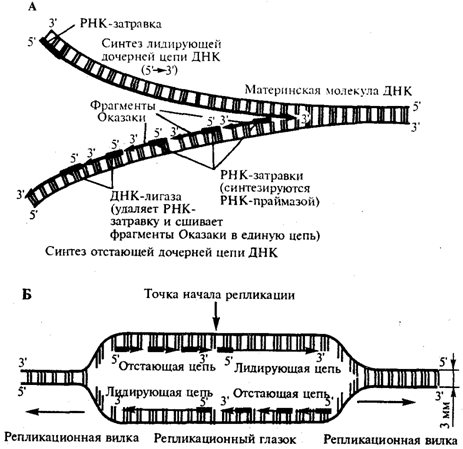
92. Биосинтез днк (репликация): стехиометрия реакций, днк-полимераза, матрица. Повреждение и распад днк.
Источником
энергии в реакциях полимеризации
мононуклеотидов является энергия,
освобождаемая всеми четырьмя типами
дезоксирибонуклеозидтрифосфатов,
участвующих в синтезе ДНК. Образующийся
пирофосфат под действием пирофосфатазы
также расщепляется на две молекулы
ортофосфата, давая дополнительную
энергию для биосинтеза ДНК. Помимо
энергии, биогенез ДНК требует наличия
специфических ферментов, катализирующих
отдельные этапы синтеза, и множества
белковых факторов, абсолютно необходимых
для регулирования процесса репликации
и проявления каталитической активности
ферментов. По имеющимся данным, в
репликации ДНК, включающей узнавание
точки начала процесса, расплетение
родительских цепей ДНК в репликационной
вилке, инициацию биосинтеза дочерних
цепей и дальнейшую их элонгацию и,
наконец, окончание (терминация) процесса,
участвует более 40 ферментов и белковых
факторов, объединенных в единую ДНК
репликазную систему,
называемую реплисомой.
Основным ферментом, катализирующим
биосинтез новообразованной ДНК (точнее,
стадию элонгации репликации ДНК),
является ДНК-полимераза III, представляющая
собой мультимерный комплекс собственно
ДНК-полимеразы (мол. масса около 900000) и
ряда других белков.
ДНК-полимераза
III катализирует сопряженный синтез
ведущей (лидирующей) и отстающей цепей
ДНК при репликации. ДНК-полимераза I
катализирует отщепление
затравочного
олигорибонуклеотидного праймера и
заполнение образующихся после этого
пробелов (ниш) дезоксирибонуклеотидами.
Важную функцию соединения двух цепей
ДНК или замыкания двух концов одной
цепи ДНК в процессе репликации либо
репарации ДНК выполняет особый фермент
– ДНК-лигаза, катализирующая за счет
энергии АТФ образование фосфодиэфирной
связи между 3'-ОН-группой дезоксирибозы
одной цепи и 5'-фосфатной группой другой
цепи ДНК. Функцию раскручивания
(расплетения) двойной спирали ДНК в
репликационной вилке, происходящего
за счет энергии гидролиза АТФ, выполняет
специфический rep-белок, названный
хеликазой (мол. Масса 300000). Этапы
биосинтеза ДНК. Этап
I – инициация биосинтеза ДНК
– является началом синтеза дочерних
нуклеотидных цепей; в инициации участвует
минимум восемь хорошо изученных и разных
ферментов и белков. Первая фаза – это
ферментативный биосинтез на матрице
ДНК необычного затравочного
олигорибонуклеотида (праймера) со
свободной гидроксильной группой у С-3'
рибозы. При инициации к цепям ДНК
последовательно присоединяются
ДНК-раскручивающие и ДНК-связывающие
белки, а затем комплексы ДНК-полимераз
и праймаз.
Этап II – элонгация синтеза ДНК
– включает два кажущихся одинаковыми,
но резко различающихся по механизму
синтеза лидирующей и отстающей цепей
на обеих материнских цепях ДНК. Синтез
лидирующей цепи начинается с синтеза
праймера (при участии праймазы) у точки
начала репликации, затем к праймеру
присоединяются дезоксирибонуклеотиды
под
действием
ДНК-полимеразы III; далее синтез протекает
непрерывно, следуя шагу репликационной
вилки. Синтез отстающей цепи, напротив,
протекает в направлении, обратном
движению репликационной вилки и
начинается фрагментарно. Этап
III – терминация синтеза ДНК
– наступает, скорее всего, когда
исчерпана
ДНК-матрица и трансферазные реакции
прекращаются. Точность репликации ДНК
чрезвычайно высока, возможна одна ошибка
на 1010 трансферазных реакций, однако
подобная ошибка обычно легко исправляется
за счет процессов репарации.