
Uchebnik
.pdf
основной цепи, сфингозины растений - дополнительную спиртовую группу. Как правило, жирная кислота, взаимодействуя со сфингозинами по аминогруппе, образует соответствующий замещенный амид, а фосфорная кислота этерифицирует первичную спиртовую группу, остальные спиртовые группы (одна или две) – обычно свободны. Если, все спиртовые группы остаются свободными, эту группу липидов называют церамидами.
Все сфинголипиды делят на сфингомиелины, цереброзиды, ганглиозиды и сульфолипиды. Три последние группы сфинголипидов содержат в структуре сахара и называются гликолипидами или липополисахаридами. В природе эти соединения распространены очень широко – они обнаружены в растениях, животных и микроорганизмах.
Галактоглицериды имеют состав:
они найдены в липидах зеленых листьев, в пшеничных зернах, в водорослях, в бактериях, в нервных тканях животных.
Цереброзиды: френозин, керазин, нервон имеют общую формулу:
|
O |
|
CH3 |
|
|
HN |
|
(CH2)13 |
|
HO |
|
CH3 |
||
O |
OH |
|||
|
||||
HO |
O |
|
(CH2)8 |
|
OH |
|
|
||
HO |
OH |
|
|
|
|
|
|
Сояцереброзид найден в составе Glycine max, Tetragonia tetragonoides, Prunus jamasakura, Dimocarpus Fumatus.
Воска - жироподобные производные жирных кислот, являются сложными эфирами неразветвленных жирных кислот и спиртов. В состав восков, чаще всего, входят пальмитиновая, церотиновая и маноцериновая кислоты, а также цетиловый и цериловый спирты (неразветвленные первичные). Иногда в образовании восков участвуют первичные спирты эйкозанол-2 и октадеканол-2. В состав некоторых животных восков (ланолин) входят сложные эфиры обычных жирных кислот и циклического спирта холестерола. Сложные эфиры холестерола и редких жирных кислот (например, фурановые жирные кислоты)
271

достаточно часто встречаются в морских организмах, входят в состав плазмы крови человека.
Растительные воски, покрывающие в виде тонкого налета или пленки листья, стебли и плоды растений, защищают последние от излишней потери влаги. Их примерами являются карнаубский воск, покрывающий листья бразильской пальмы Copernicia cerifera и пальмовый воск, покрывающий ствол пальмы Geroxilon ondlicoka.
По химическим и физико-химическим свойствам воски близки к жирам, отличаясь от последних большей инертностью, особенной устойчивостью к гидролизу – они могут быть гидролизованы с трудом и только в щелочной среде. Для них также нехарактерно окисление по типу «прогоркания». Гидрофобность восков также более ярко выражена по сравнению с глицеридами, фосфолипидами и другими жироподобными соединениями. Их состав представлен ниже:
Жирная кислота R-CO-O-R’ пальмитиновая
СН3-(СН2)14-СООН тетракозановая (лигноцериновая)
СН3-(СН2)22-СООН гексакозановая (церотиновая)
СН3-(СН2)24-СООН
С15Н31-СОО-С16Н33 |
Цетин – главная компонента (98%) |
С25Н51-СОО-С16Н33 |
спермацета китов и кашалотов |
Основной эфир (98%) китайского воска, |
|
С25Н51-СОО-С30Н61 |
вырабатывается червецом Coccus ceriferus |
Входит в состав пальмового воска (80%) |
|
|
Восковые покрытия туберкулезных |
|
бактерий и бактерий лепры |
|
В плазме крови человека |
Из растительного сырья жирные кислоты и липиды извлекают двумя основными методами, позволяющими количественно экстрагировать липиды практически всех групп: экстракцией смесью хлороформ - метанол (2:1) и (1:1) и солюбилизацией. Для повышения выхода полярных липидов предложено заменять смесь хлороформ-метанол на хлороформ - 2% уксусная кислота или хлороформ-метанол-1М соляная кислота (4:2:3).
Для анализа состава и структуры различных липидов используют основное свойство - сложных эфиров - разлагаться под действием кислот,
272
щелочей, ферментов, а полученный жирнокислотный состав определяют методом ГЖХ, ЖЖХ и ВЭЖХ.
Из трех видов гидролиза, ферментативный является наиболее специфичным.
Фосфолипиды хорошо растворяются во многих органических растворителях (хлороформ, бензол, эфир и спирт) и в воде, в которой они образуют коллоидные растворы.
Сложность выделения фосфолипидов растений заключается в одновременном присутствии в них ферментов-липаз, гидролизующих фосфолипиды, с образованием свободных жирных кислот. Поэтому выбор растворителя для экстракции фосфолипидов, одновременно ингибирующего их ферментативное разложение, имеет особое значение.
Наиболее часто для предварительной обработки растительного материала используют изопропиловый спирт или ацетон.
В этом случае воздушно-сухое сырье обрабатывают в течение 5-10 минут горячим изопропиловым спиртом. Горячую смесь фильтруют, остаток на фильтре промывают сначала горячим изопропиловым спиртом, затем смесью хлороформ-пропанол-2 (1:1) и хлороформом. Объединенные фильтраты упаривают под вакуумом, остаток растворяют в хлороформе. Полученный раствор несколько раз промывают водой очищенной и концентрируют.
Согласно альтернативному методу, фосфолипиды из измельченных и обезжиренных ацетоном частей растения извлекают смесью хлороформметанол (2:1). Растворители отгоняют под вакуумом в мягких условиях, остаток растворяют в хлороформе и фильтруют; фильтрат сгущают до небольшого объема. Для предварительной очистки суммы фосфолипидов от сопутствующих веществ (масла, пигменты, углеводы, стероиды и др.) сухой экстракт обрабатывают ацетоном. Нерастворимый в ацетоне остаток растворяют в смеси хлороформ-метанол-вода (90:10:1) и для окончательной очистки от углеводов пропускают эту смесь через колонку с предварительно набухшим в той же смеси молселектом Г-25. Полноту очистки от углеводов проверяют методом ТСХ элюата в системе: хлороформ-метанол-вода 65:25:4.
Для фракционного разделения суммы фосфолипидов, полученный экстракт растворяют в хлороформе и наносят на колонку с силикагелем. Элюирование компонентов осуществляют ацетоном, хлороформом, затем смесью хлороформ-метанол возрастающей полярности. При этом ацетоном извлекают вещества стероидного характера, хлороформом - нейтральные липиды. Смесь хлороформ-метанол (4:1) позволяет выделить фосфатидилэтаноламины и фосфатидилхолины; а тот же элюент состава (2:1) будет содержать фосфатидилэтаноламины и фосфатидилинозиты, после чего в метанольной фракции остаются лишь лизофосфатидилхолины.
Для проведения контроля за ходом разделения фосфолипидов оптимальным является использование метода хроматографии в тонком слое сорбента в следующих системах:
хлороформ-метанол-аммония гидроксид 65:35:8, 65:30:2 либо 65:25:4
хлороформ-метанол-вода 65:35:5
273
2% гидроксид аммония-метанол 2:3
2-пропанол-аммония гидроксид-вода 5:4:1 либо 49:7:14
н-бутанол-пиридин-вода 6:4:3
Сравнительный качественный анализ и препаративное выделение компонентов фосфолипидной фракции растений целесообразно осуществлять с использованием метода ВЭЖХ.
Для разделения и анализа фосфолипидов в растительных экстрактах применимы два основных типа хроматографических колонок: SiO2-содержащие и диольные.
Анализ фосфолипидов на кремнийсодержащих колонках (Lichrospher Si60, Supelcosil LC-Si) проводится с использованием одной из подвижных фаз:
изооктан-тетрагидрофуран 99:1
2-пропанол-хлороформ 80:20
2-пропанол-вода 50:50
ацетонитрил-метанол-вода 61:21:4
ацетонитрил-метанол-серная кислота 100:2.1:0.05
дихлорметан-метанол-вода 45:45:10, содержащая 1% муравьиной кислоты
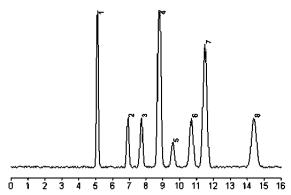
Эффективного разделения компонентов фосфолипидной фракции удалось достичь на указанной колонке с использованием градиента подвижных фаз А: хлороформ-метанол-аммония гидроксид 80:19.5:0.5 и В: хлороформ-метанол- вода-аммония гидроксид 60:34:5.5:0.5 за 16 минут от А:В 50:50 до 100% В.
1:фосфатидилэтаноламин
2:фосфатидил-линоситол
3:фосфатидилсерин
4:фосфатидилхолин
5:фосфатидиновая кислота
6 и 7: сфингомиелин 8: лизофосфатидилхолин.
Для разделения фосфолипидов на диольных колонках (Nucleosil 100-7 OH DIOL) предложены 2 наиболее эффективные подвижные фазы:
гексан-2-пропанол-бутанол-тетрагидрофуран-изооктан-вода
64.5:17.5:7:5:5:1
2-пропанол-бутанол-тетрагидрофуран-изооктан-вода 73:7:5:5:10 (v/v) с добавле-нием 180 мг/л аммония ацетата в обе хроматографические системы.
Для выделения отдельных групп липидов обычно используют адсорбционную или распределительную хроматографию на колонках на таких сорбентах как силикагель, кремниевая кислота или флоризил. Элюирование, как правило, осуществляют хлороформом, содержащим некоторое количество метанола, а также чистым хлороформом, диэтиловым эфиром, смесью диэтиловый эфир-метанол в различных соотношениях.
274
На газовом хроматографе липиды разделяют при следующих условиях:
колонка капиллярная кварцевая размером 25м х 0.20 мм;
неподвижная фаза – SE-54 с толщиной слоя 0.25 мкм или аналогичная, для которой выполняются требования теста «Проверка пригодности хроматографической системы»;
температура колонки – 1700С;
температура испарителя – 2200С;
температура детектора - 2200С;
скорость газа-носителя (азот) - 0.85 мл/хв;
коэффициент разделения потока - 1:100.
Хроматографируют по 1 мкл раствора сравнения, получая не менее 5 хроматограмм.
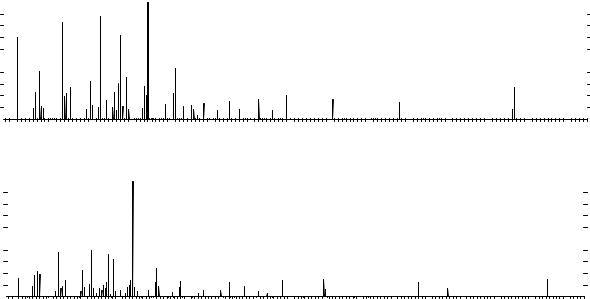
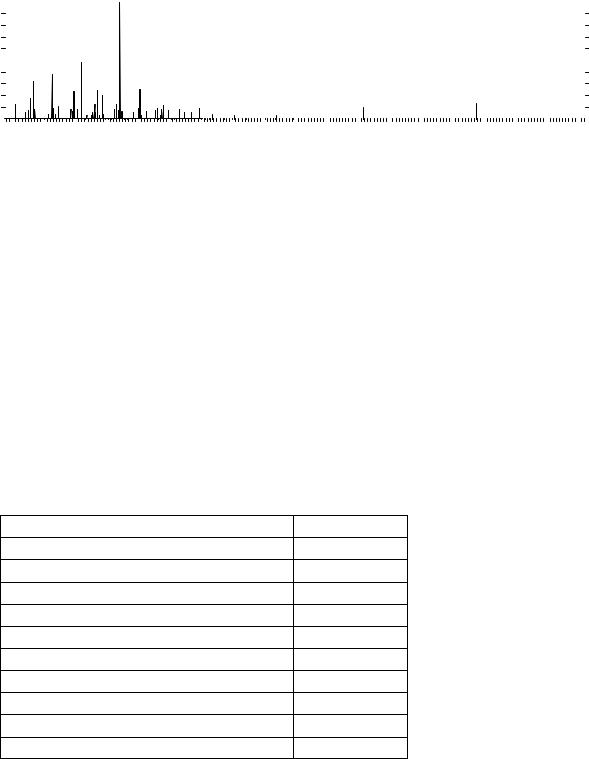
Достоверную информацию о структурах липидов получают комплексом химических (разные виды гидролиза), хроматографических, хромато-масс- и масс-13С-ЯМР-методов. Так, методом хромато-масс-спектрометрии петролейноэфирных фракций спиртового концентрата проведен анализ компонентного состава и количественного содержания жировых кислот и липидов многих растений, что позволило идентифицировать сопутствующие вещества липидных фракций, высокомолекулярные кислоты и основные пути их фрагментации. При исследовании корней кермека Гмелина найдены редкие, обнаруженные в цереброзидах С24 кислоты нервоновая (С24:1) и лигноцериновая (С24:0), а также кислоты с нечетным числом углеродных атомов – трикозановая
(С23:0) и трикозен-14-овая (С23:1) кислоты. В качестве примера приведены хромато-масс-спектры 3 кислот:
100 |
|
|
|
|
|
55 |
74 |
|
|
|
98 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
32 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
50 |
|
|
|
|
|
43 |
|
|
|
|
|
|
|
|
|
|
112 |
|
|
|
138 |
154 |
168 |
191 |
|
|
|
226 |
|
|
|
|
|
|
283 |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
126 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
337 |
|
|
|
|
|
|||||||||||||||||||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M/Z |
30 |
50 |
70 |
90 |
110 |
|
130 |
|
150 |
170 |
190 |
210 |
230 |
|
|
250 |
|
270 |
290 |
310 |
|
|
|
||||||||||||||||||||||||||||||
100 |
|
|
|
|
|
|
|
|
|
|
|
98 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
50 |
|
|
|
|
|
55 |
74 |
|
|
|
112 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
32 |
|
|
|
|
|
|
|
|
|
126 |
|
|
154 |
|
|
|
185 |
208 |
|
|
|
264 |
|
|
|
|
|
|
|
337339 |
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
281 |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
163 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M/Z |
30 |
50 |
70 |
|
90 |
|
110 |
130 |
150 |
170 |
190 |
210 |
230 |
|
250 |
|
270 |
290 |
310 |
330 |
350 |
|
|
|
|||||||||||||||||||||||||||||
275
100 |
|
|
|
|
|
74 |
98 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
50 |
|
|
|
43 55 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
126 |
149 |
177 |
|
|
210 |
|
|
|
253 |
|
|
292 |
|
|
325 |
|
337367 |
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
334 |
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M/Z |
30 |
50 |
70 |
90 |
110 |
130 |
150 |
170 |
|
190 |
210 |
230 |
250 |
270 |
290 |
310 |
330 |
350 |
370 |
390 |
|||||||||||||||||||||||||||
Хромато-масс-спектры гексадекандиовой, эйкозандиовой и докозандиовой кислот
Исследован петролейно-эфирный экстракт Glycyrrhiza glаbra (сем. Fabaceae), содержащий 70% нейтральных и 30% полярных липидов. Идентифицированы: углеводороды, эфиры стеринов, триацилглицерины, свободные жирные кислоты, свободные стерины, диацилглицерины, фосфо - и гликолипиды.
Определен жирнокислотный состав ацилсодержащих липидов. Идентифицировано 14 кислот; основная ненасыщенная кислота составляла
18:2, а насыщенная - 16:0.
Липиды и жирные кислоты корней солодки фракционировали на силикагеле L100/160 мк, элюируя смесью гексан-эфир в соотношении от 99:1
до 1:99.
Жирнокислотный состав всех фракций липидов определяют ГЖХ.
Классы липидов корней Glycyrrhiza glаbra (в % к сумме липидов)
Класс липида |
Содержание |
Углеводороды |
0.5 |
Эфиры стеринов |
27.5 |
Метиловые эфиры жирных кислот |
следы |
Триацилглицерины |
10.0 |
Свободные жирные кислоты |
10.5 |
Свободные стерины |
11.5 |
Диацилглицерины |
6.2 |
Гликолипиды |
19.0 |
Фосфолипиды |
10.1 |
Неидентифицированные |
4.7 |
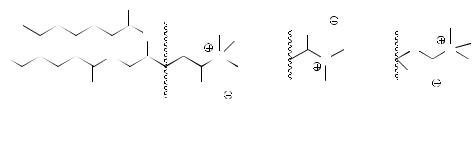
Среди полярных липидов более 30% приходится на долю бетаиновых липидов:
1(3),2-диацилглицеро-3(1)-О-4’-(N,N,N-триметил)гомосерин (1)
1(3),2-диацилглицеро-3(1)-О-2’-(оксиметил)-(N,N,N-триметил)-β-аланин
(2)
1(3),2-диацилглицеро-3(1)-О-карбокси(оксиметил)холин (3) и их мезоформы:
276
Простые и сложные липиды – это поставщики атомов углерода, запаса энергии, компоненты мембран, предшественники простагландинов, стероидных гормонов, желчных кислот, витаминов D, F и др.
Все липиды выполняют защитную роль от термических, электрических, лучевых и механических воздействий.
Химическими и фармакологическими исследованиями установлено, что комплекс липидов растений проявляет значительно большую биологическую активность, чем его составные индивидуальные компоненты, хотя каждый из классов липидной фракции выполняет свою специфичную биологическую роль. Например, семена дальневосточного растения Coix lachryma, содержащие глицеролипиды, проявляют способность тормозить рост некоторых злокачественных образований, обусловленную содержанием в них нейтрального вещества коиксенолида, смешанного эфира мезо-2,3-бутандиола с пальмитиновой и транс-вакценовой кислотами.
Церебролецитин, фосфрен, липоцеребрин, феррокаль, холецин, тестобромлецитин, интралипос, мирестерал созданы на основе фосфолипидов и играют важную роль в борьбе с атеросклерозом, инфарктом миокарда, заболеваниями печени и обмена веществ, в лечении центральной нервной системы и в процессах свертывания крови. Предложены составы, содержащие лизофосфолипиды, обладающие противораковой, иммуностимулирующей активностью и для лечения лейкемии. Рекомендовано «средство для лечения атеросклероза», содержащее смесь фосфолипидной фракции соевого масла, негидролизованной части кукурузного масла, а также витамины В и Е. Препараты «Липостабил» и «Эссенциале», приготовленные на основе фосфолипидов, применяются при гиперлипемии, атеросклерозе, жировой эмболии, заболеваниях печени.
Являясь хорошими эмульгаторами, липиды используются при создании жировых эмульсий для парентерального питания больных, а также кровозаменителей. Фосфатидилхолин в виде изотонических растворов, содержащих до 20% липидов, применяют при заболеваниях желудочно-кишечного тракта.
На основе нейтральных липидов морозника кавказского и абхазского создан препарат «Геллипол», рекомендованный в качестве радиосенсибилизатора при лучевой терапии злокачественных опухолей. Установлен вирусингибирующий эффект нейтральных липидов семян наперстянки (Digitalis) и противоопухолевая активность семян маклюры оранжевой (Maclura). Нейтральные липиды плодов держи-дерева обладают ранозаживляющим и противовоспалительным действиями, а суммарный препарат плодов держидерева «Христобол» (спиртово-водное извлечение), содержащий до 8% нейтральных липидов и до 7% фосфолипидов, рекомендован в качестве желчегонного и гепатопротекторного средства.
277
Кроме того, нейтральные липиды обладают высококачественными питательными свойствами и используются в композициях косметических кремов.
Воздействие на репродуктивную систему, гипотензивный эффект, противоопухолевое и др. действие выявлено у липидов, выделенных из пантов пятнистого и северного оленей и входящих в состав фармацевтических препаратов «Пантокрин» и «Ранторин».
Вопросы для самоконтроля студентов
1Классифицируйте карбоновые кислоты.
2Опишите особые свойства оксикислот.
3Напишите уравнение реакции кето-енольной таутомерии аскорбиновой кислоты.
4Опишите сходства и различия в химических свойствах альдегидо- и кетонокислот.
5Напишите реакции сахарных кислот в открытой и циклической форме.
6Опишите строение и химические свойства жирных кислот.
7Перечислите особенности методов гидрогенизации жиров и масел.
8Опишите строение, классификацию, биологические функции липидов.
9Перечислите особые свойства липидов.
10Перечислите основные промышленно-важные представители окси-, оксо- и жирных кислот, фосфолипидов.
Галогенкарбоновые кислоты
В ряду природных метаболитов описаны разнообразные галогенокислоты, выделенные из грибов, высших растений и морских организмов.
Так, из южноафриканского молочая Dichapetalum выделена фторуксусная кислота и ее ацетат. Позже из многих видов молочая (листья, семена) были
выделены -фторалифатические кислоты, а фторацетат описан во многих видах бобовых и акациях.
Влипидах угря Anguilla идентифицированы индивидуальные диастереомеры 3,4-дихлортридекановой кислоты, изомерные кислоты с разным положением хлора, а также изомерные 5,8,9,10-; 9,10,12,13 – и другие тетрахлордекановые кислоты.
Вморских ежах, различных сортах рыбы, моллюсках и в морском желуде Balanus описаны хлорсодержащие ненасыщенные карбоновые кислоты.
Пунагландины – это простагландинподобные хлорсодержащие кислоты впервые описанные из морского коралла. Морская сине-зеленая водоросль Lyngbua продуцирует амиды галогенкарбоновых кислот – малингамиды, их ацетаты и восстановленные аналоги.
Красные водоросли продуцируют бромкарбоновые кислоты и др. природные группы соединений: хлоруксусная, хлоракриловая, 3-бромнонен-2-
278
овая, 3-бромгептен-2-овая, 3,3-дибром-2-н-гексилакриловая кислоты, а 9,10- дибромстеариновая и 9,10,12,13тетрабромстеариновая кислоты выделены из масла семян пустыноколосника широкочашечного.
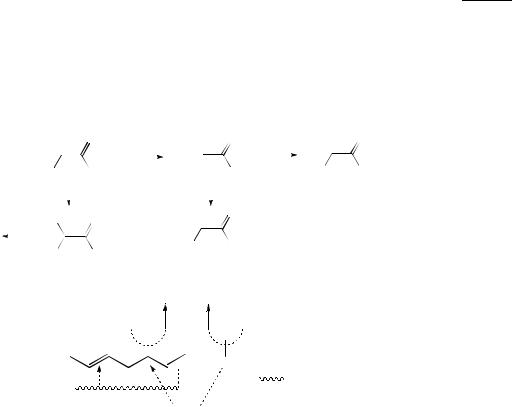
На основе природных галогенокислот получено множество продуктов их химической модификации, из которых наибольшей биоактивностью обладали продукты аминирования и окисления по С=С связям, амиды, сложные эфиры и соли:
|
|
|
O |
NH3 |
O |
t0 |
O |
||
|
|
|
|
||||||
|
|
F |
OH |
|
H2N |
ONH4 |
|
H2N |
NH2 |
|
|
|
|
||||||
|
|
|
Hal |
|
|
t0 / OH- |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
ROH Hal |
O |
|
|
O |
|
|
|
||
|
|
|
|
|
|
||||
|
|
F |
OH |
|
H2N |
OH |
|
|
|
|
|
|
|
|
|
|
|
||
р. обмена
-р. присоединения
-р. окисления
-р. полимеризации
Br Br

 COOH
COOH  р. кислот
р. кислот
р. электрофильного замещения
Морские губки оказались продуцентами целого комплекса БАВ, в том числе гомологического ряда 6-бромдиеновых, ди- и трибромкарбоновых кислот состава С16 с 4 и 5 С=С или С=С и С≡С связями, которые обладают цитотоксичностью по отношению к опухолевым КВ-клеткам.
В высокогорном лишайнике Acorospora и др. также содержатся бромпроизводные высшие кислоты.
Значительно реже встречаются йодкарбоновые кислоты (красные морские водоросли Asparagopsis), способствующие авторегуляции щитовидной железы.
Редкими (около 20 структур) являются карбоновые кислоты, содержащие несколько различных атомов галогенов в различном сочетании.
Процесс введения галогенов проходит с участием пероксидаз и/или других строго специфических ферментных систем.
Кислоты ароматические имеют состав С6Н5СООН или С6НnRnСООН и отличаются низкой растворимостью в воде без нагревания за счет наличия ароматического кольца. Бензойная, изомерные толуиловые и фталевые кислоты накапливаются в корнях и корневищах растений, обладают бактерицидным действием и защищают растение-хозяина от вредителей.
По химическим свойствам они повторяют все свойства СООН-группы образуя соли, сложные эфиры, амиды, галогенангидриды, ангидриды и свойства ароматического кольца (электрофильный обмен в мета-положения, относительно карбокси-группы). Например:
279
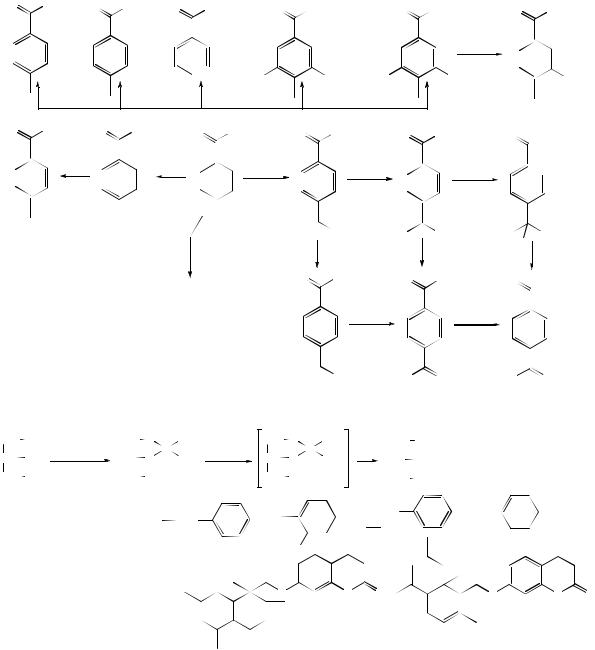
L-моноглицериды ароматических и кумариновых кислот и их производных получены по схеме:
Аминокислоты, бетаины, пептиды, белки
Названные соединения образуют группу химически и биологически родственных соединений, которым принадлежит исключительная роль во многих жизненно важных процессах. Аминокислоты присутствуют во всех органах всех растений. В различном сочетании и в составе белков аминокислоты присутствуют и в животных организмах.
От других карбоновых кислот их отличает наличие двух функциональных группNH2- амино- и СООНкарбоксильной, которые могут быть у соседних углеродных атомов или удалены друг от друга на различное число атомов углерода и, в зависимости от этого, все аминокислоты делят на α, β, γ, σ- и т.д., например:
280
