
Uchebnik
.pdf1 ■ по молекулярной массе (ди-, три-, тетра-… полимеры)
по типу связи между мономерами (С-С (В); С-С и С-О-С (А, Т))
по природе мономеров
по числу и расположению заместителей в мономерах.
2 ■ При кислотном гидролизе, гидролизуемые дубильные вещества распадаются на углевод и различные фенолокислоты, тогда как конденсированные – на мономерные флавонольные молекулы (антоцианидины).
С раствором ЖАК и железа окисного хлорида – гидролизуемые дубильные вещества образуют черно-синее окрашивание, а конденсированные – черно-зеленое.
С раствором нитрозометилуретана при нагревании и с бромной водой, конденсированные дубильные вещества выпадают в осадок.
3 ■ Реакции гидролиза на тип связи С-С, С-О-С и др.
■ Реакции алкилирование и ацилирование - на число ОН-групп. 4 ■ Масс-спектры, реже 13С-ЯМР-спектроскопия.
Комплекс химических, хроматографических и спектральных данных (13С-ЯМР-; масс-).
Рекомендуемая литература к главе
Основная
1Д.Ю.Корулькин, Ж.А.Абилов, Р.А.Музычкина, Г.А.Толстиков. Природные флавоноиды. Новосибирск, 2007, 232с.
2J.B.Harborne. The flavonoids: Advances in research. London: Charman and Hall, 1982, Р. 261-311
3А.Блажей, Л.Шутый. Фенольные соединения растительного происхож-
дения. М., 1977, 240с.
4Р.А.Музычкина, Д.Ю.Корулькин, Ж.А.Абилов и др. Биологически активные вещества растений. Выделение, разделение, анализ. Алматы, 2006, 438с.
Дополнительная
1В.А.Куркин. Фармакогнозия. Самара, 2007, 1236с.
2В.П.Георгиевский, А.И.Рыбаченко, А.Л.Казаков. Физико-химические и аналитические характеристики флавоноидных соединений. Ростов-на-Дону, 1988, 144с.
3Н.И.Гринкевич, Л.Н.Сафронич. Химический анализ лекарственных растений. М., 1983, 176с.
4М.Н.Запрометов. Фенольные соединения. М., 1993, 245с.
5J.B.Harborne, T.J.Mabry, H.Mabry. The flavonoids. 1974, London, 1202p.
6E.Haslam. The flavonoids. London: Chapman and Hall, 1975, Р. 505-559
7Дж.Харборн. Биохимия фенольных соединений. М.: Мир, 1968, 452с.
8Э.Хефтман. Хроматография. Практическое приложение метода. М., 1986, ч. 2, 336с.
151
Глава 5. ИЗОПРЕНОИДЫ
Это огромная группа природных соединений, чрезвычайно распространенных как в мире животных, так и в мире растений и которые являются продуктами вторичного биосинтеза. Многие из них содержатся в очень малых количествах, другие составляют до нескольких процентов в расчете на сухой вес той части растения, откуда они извлекаются. Изопреноидами эти соединения называются в связи с тем, что углеродный скелет этих молекул как бы составлен из изопреновых (изопентановых) фрагментов, чаще всего соединенных между собой по принципу «голова к хвосту» («изопреновое правило» Ружички).
Все изопреноиды делят на 3 большие группы:
терпены (терпеноиды)
стероиды
каротиноиды
Термин терпены применяется для обозначения соединений, содержащих целое число изо-С5-фрагментов независимо от того, содержатся ли в их молекулах другие элементы, чаще всего кислород. Терпеноиды - это соединения с различным числом углеродных атомов, но структурными их предшественниками являются «правильные» терпены, образованные реакциями вторичного метаболизма терпенов. Иногда терпенами называют только углеводороды соответствующего состава и структуры, а терпеноидами – любые их производные.
Терпены и терпеноиды - это эфирные масла практически всех пахнущих растений (запах розы, полыни и т.д.) и смоловыделения хвойных растений под общим названием «живица». Живицы хвойных являются наиболее богатыми источниками самых различных терпенов, как по номенклатуре, так и по количественному содержанию. В животных организмах терпены являются минорными компонентами, но продукты их метаболизма (это касается, в первую очередь, высших изопреноидов - ди-, три- и тетратерпенов) - явление для многих животных, включая человека, обязательное и значительное (витамины, гормоны и др.).
Классификация терпенов основана на количестве изо-С5-остатков в молекуле, при этом за единицу терпена принят фрагмент (молекула) из двух изопреновых звеньев – в силу исторических причин. До недавнего времени найденные в природе терпены имели минимальный углеродный состав С10. И только недавно во многих растениях в очень малых концентрациях были найдены собственно изопрен и его производные.
Простейшие терпены и терпеноиды делят на:
алифатические С10 с 2-3 С=С связями (мирцен хмеля, гераниол, цитраль, линалоол);
моноцикличекие с 2-мя С=С связями;
бициклические с одной С=С связью;
трициклические без двойных связей.
152
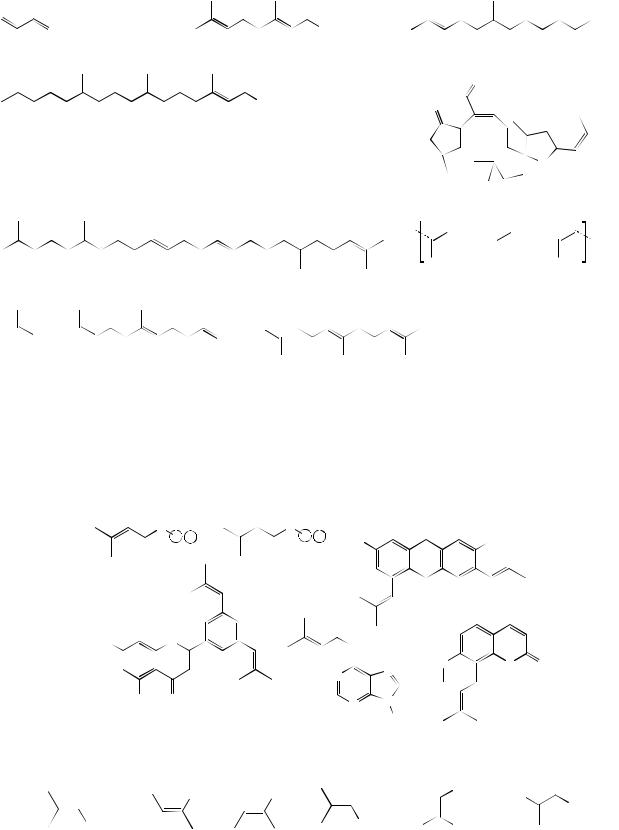
Другая классификация за основу использует число углеродных атомов:
С5- |
гемитерпены |
С10- монотерпены |
С15- сесквитерпены |
(полутерпены) изопрен |
гераниол |
фарнезол |
|
С20-дитерпены геранил-гераниол
С25- сестертерпены офноболин А
С30- тритерпены |
Политерпены |
сквален |
n = от 7 103 до 3 105 каучуки |
|
С40- тетратерпены |
|
фитоин |
Гемитерпены в растениях присутствуют в следовых количествах, их спутниками являются фосфорилированные гемитерпены - ∆2-изоамилпиро- фосфат и ∆3-изоамил- и изопентенилпирофосфат, являющиеся ключевыми интермедиатами в биосинтезе всех терпенов. В растениях часто обнаруживают связанные гемитерпены, т.е. соединения другого класса, содержащие изо-С5- заместитель. Это некоторые алкалоиды, пурины, пирановые гетероциклы, флавоноиды, антраценовые и т.д. Например:
На основании структуры углеродного скелета к гемитерпенам формально относят природные кислоты состава С5:
|
COOH |
COOH |
|
OH |
HOOC |
|
|
|
|
COOH |
|||
|
|
|
|
|
|
|
COOH |
|
|
COOH |
COOH |
|
|
изо- |
ангеликоваятиглиновая |
сенециноваясерациновая итаконовая |
||||
валериановая |
||||||
В природе не обнаружена н-валериановая и пиволиновая кислоты ((СH3)3C-COOH), тогда как изовалериановая и 2-метилмасляная с изопреноидным скелетом описаны во многих растениях.
153
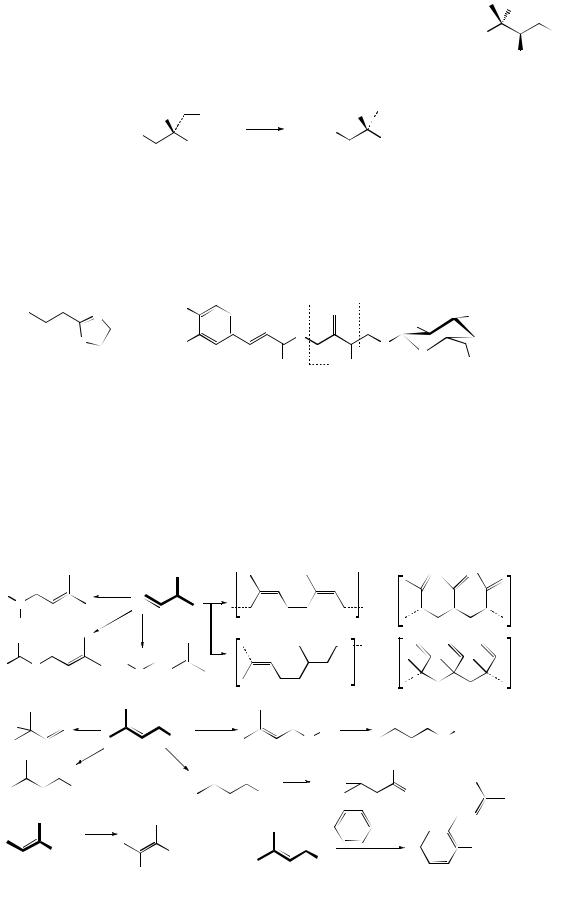
Очень многие растения синтезируют изопрен, который выделяется в атмосферу, образуя «легкую дымку», особенно над лесами.
В масле хмеля, в корнях, в чайном листе, в цитрусовых, в гераниевом масле содержатся изовалериановая и тиглиновая кислоты.
В тропическом растении Leucaena обнаружена гемитерпеновая оксикислота в виде калиевой соли, которая регулирует движение листьев растения, в зависимости от суточного освещения и закрывает листья на ночь.
К гемитерпеновым кислотам относится лимоннояблочная кислота:
Большая часть гемитерпеновых кислот представлена структурами с геминальным расположением COOH и CH3-групп.
Вразличных природных источниках образуются гемитерпеновые кислоты
ввиде тиазолов, например, в томатах изовалериановая кислота образует 2- изобутилтиазол (компонент запаха); из растения падуб пушистый выделены гликозиды изопренилтриола, этерифицированного кофейной кислотой; ингибирующие агрегацию склеротических бляшек:
Кгемитерпенам может быть отнесен ряд соединений сопряженного
биосинтеза или меротерпенов с фрагментом изо-С5, связанным с другими природными фрагментами. N-гемитерпены найдены во многих растениях, грибках, бактериях, водорослях, морских организмах - это класс фитогормонов, которые вместе с ауксинами вызывают деление клеток, дифференцировку стеблевых почек, активизируют рост листьев, задерживают старение срезанных листьев травянистых растений.
Химические свойства гемитерпенов - это свойства структурных элементов изопренильного фрагмента (С=С) и функциональных групп, например:
154
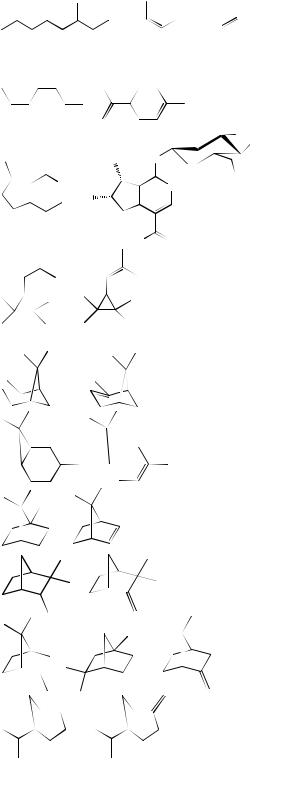
Монотерпены занимают лидирующее положение среди всех терпенов; в живице хвойных количество некоторых из них достигает 50% при наличии нескольких десятков представителей этого класса в смеси. Монотерпены, как важные компоненты эфирных масел, широко представлены у высших растений в особых секреторных железках. Эфирные масла продуцируются чаще всего у растений семейств Labiatae, Pinaceae и Umbelliferae. По-видимому, только растения из класса Violales не синтезируют монотерпены в заметных количествах. Все монотерпены делят на:
Ациклические
2,6-диметилоктаны (октены, октандиены, октатриены и т.д.)
Моноциклические
Ментаны (циклогексановые, циклогексеновые)
Ириданы (циклопентановые)
Хризантематы (циклопропановые)
Бициклические
Пинаны (2,6,6-триметилбицикло- [3.1.1]- гептаны)
Караны (3,7,7-триметилбицикло- [4.1.0]-гептаны, гептены)
|
Камфаны (1,7,7- |
|
|
триметилбицикло-[2.2.1]-гептаны, |
|
|
гептены) |
борнилен |
|
Изокамфаны (2,2,3-триметил- |
|
|
бицикло-[2.2.1]-гептаны) |
|
Фенханы (триметилбицикло- |
|
|
|
[2.2.1]-гептаны) |
|
|
Туйаны (1-изопропил-4- |
|
|
метилбицикло-[3.1.0]-гексаны) |
|
155
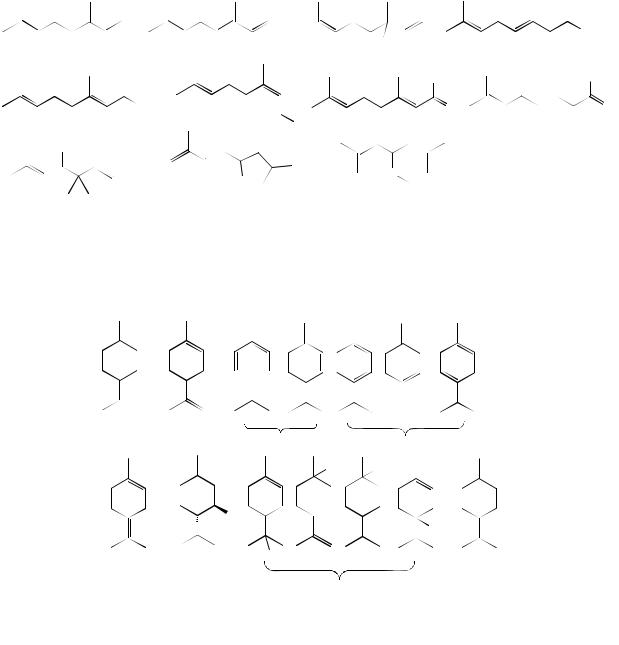
Ациклические природные монотерпены (всегда представленные ненасыщенными соединениями) различают между собой количеством и положением двойных связей, а также присутствием функциональных групп; в основном спиртовых, реже - карбонильных, еще реже - карбоксильных. Их углеродный скелет, обычно, имеет структуру 2,6-диметилоктана образованную в соответствии с правилом сочленения изопреновых фрагментов «голова к хвосту», иногда более разветвленную углеродную структуру или структуру с 2,7-диметилоктановым скелетом, например:
Обладая специфическими запахами все названные вещества используются в парфюмерии, пищевой и фармпромышленности.
Моноциклические терпены относят к производным ментана (в мяте перечной сумма их достигает 40-70%):
Наиболее распространены лимонен и ментол.
Ментол используется для ароматизации пищевых продуктов, в фармацевтической промышленности, входит в состав парфюмерных композиций. Однако, он существует в виде четырех изомеров, каждый из которых также может существовать в виде пары оптических антиподов. Свойства этих веществ существенно зависят от их пространственного строения: например, только (-)-ментол обладает чистым мятным запахом, холодящим вкусом и антисептической активностью:
156
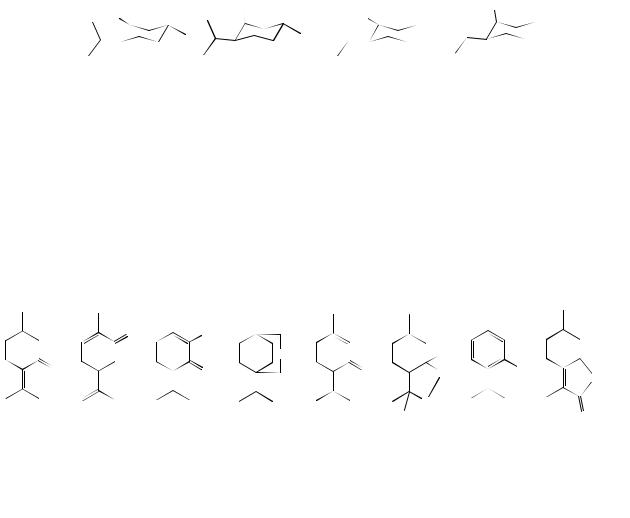
Непредельные спирты этого ряда, представленные α-, β- и γ-терпинеолами, обладают запахами сирени, гиацинта и розы соответственно. В эфирном масле грейпфрута носителем характерного запаха является 8-меркаптоментан. Среди других кислородных производных более или менее часто встречаются карбонильные производные (пулегон, карвон), циклические эфиры (1,8- цинеол), лактоны, перекиси, фенолы.
Многие кислородные производные ментанового ряда обладают определенной биологической активностью: пиперитон активен как репеллент насекомых, тимол - мягкий антисептик и антигельминтное средство; выделенные из цитварной полыни (Chenopodium anthelminticum) 1,8-цинеол – антисептик, муколитик, а аскаридол - эффективное антигельминтное средство:
Следует отметить, что в природе они чаще всего существуют в виде (+)- и (-)-изомеров. Но в каждом отдельном источнике они обычно представлены одним энантиомером. Так, из мяты перечной добывается (-)-ментол; (+)- камфору выделяют из камфорного лавра, тогда как (-)-камфору получают при окислении борнеола пихты сибирской; во всех растительных источниках найден 3-карен только (+)-конфигурации, тогда как в защитной секреторной жидкости термитов (Nasufitermes) обнаружен (-)-3-карен.
(-)-Лимонен входит в состав живицы всех хвойных, тогда как (+)-лимонен составляет основу эфирного масла лимона, запах которого и обусловлен его присутствием. В виде рацематов в природных источниках монотерпены (а возможно, и вообще терпены) не образуются, или это случается чрезвычайно редко.
По химическим свойствам моноциклические терпеноиды не имеют специфических особенностей и проявляют свойства структурных элементов своих молекул: тимол проявляет свойства фенола, пиперитон, пулегон, карвон, диосфенол - свойства С=С и С=О групп и т.д.
Практически все основные типы монотерпенов с бициклическим углеродным скелетом представлены в живицах хвойных (часто в больших количествах). Летучая фракция живицы сосны мягкоигольчатой (Pinus muricata) и сосны алепской (Pinus halepensis Mill.) содержит α-пинена более 90%, 75% скипидара сосны песчаной (Pinus clousa Chapm.) составляет β-пинен,
а56% скипидара пихты Семенова (Abies Semenovii) – 3-карен.
Вмалых дозах эти терпены входят в состав эфирных масел многих других растений-эфироносов. Олефиновые бициклические терпены характеризуются
157
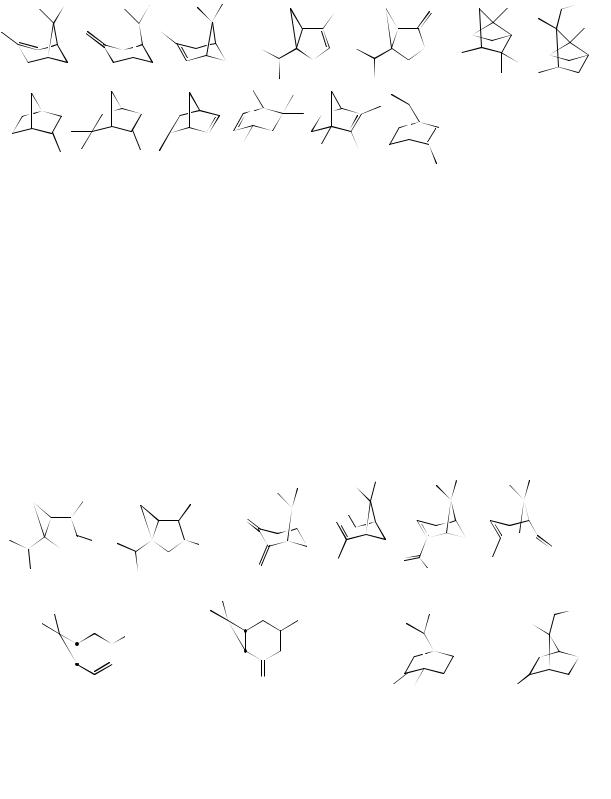
разнообразной изомерией положения двойной связи – она бывает как эндо-, так и экзоциклической, а иногда заменяется на дополнительную мостиковую связь, преобразуя, таким образом, бициклическую структуру терпена в трициклическую. Так, карены и замещенные карана имеют структуру «сломанной плоскости», т.е. плоскости циклопропанового и циклогексанового (циклогексенового) циклов:
Введение каких-либо функциональных групп в молекулы бициклических монотерпенов приводит к конфигурационной изомерии этих производных.
Кроме того, бициклические монотерпеноиды представлены большим разнообразием кислородных производных: в основном, спиртов и карбонильных соединений с разнообразной биологической активностью, например камфора - кардиотоническое и аналептическое средство – усиливает сердечную деятельность, возбуждает центральную нервную систему, стимулирует дыхание и кровообращение. Сильным возбуждающим действием на центральную нервную систему обладает и другой бициклический кетон - туйон, но, в отличие от камфоры, его действие носит наркотический характер; хамовая кислота обладает инсектицидной активностью, так же как и 3-карен; в тоже время пинены и их производные проявляют феромонную активность (вербенол - агрегационный феромон); викодиол - контрацептив в народной медицине Индии:
Из растений семейства Crysanthemum выделены эфиры хризантемовой кислоты, которая является циклопропановым монотерпеном.
Несколько более разнообразны циклопентановые монотерпены (иридоиды), производные иридана.
158
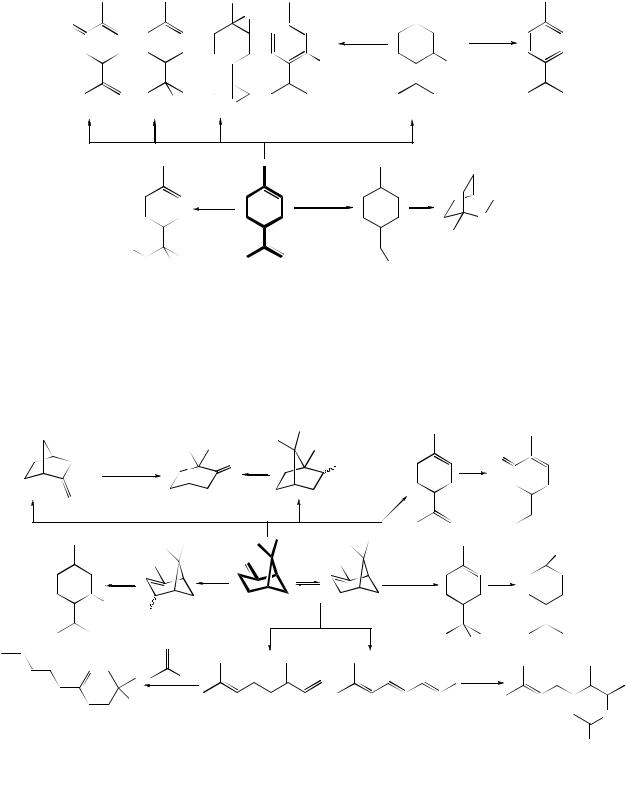
Особенностью их химических свойств является легкость окисления кислородом воздуха и перекисями:
Отличительной особенностью химических превращений бициклических монотерпенов является реакция Вагнера-Меервейна, по которой бициклы не расщепляются, меняется характер бициклизации. Часто эта перегруппировка сопровождается перегруппировкой Наметкина (камфеновая, I рода) с образованием камфена после отщепления протона.
α- и β-пинены часто используют в виде смеси изомеров, так как их взаимопревращения возможны в условиях проведения реакций:
Базируясь на использовании достаточно доступных природных терпеноидах, синтезирован ряд моно- и полифункциональных О-, N- и S- содержащих хиральных веществ.
Получение энантиомерно чистых веществ базируется на кинетическом и физико-химическом разделении в процессе синтеза полифункциональных производных:
159

[O] |
|
O |
; |
|
O |
; |
||||
|
|
|
|
|
|
|
||||
|
|
HO |
|
OH |
|
|
|
OHC |
||
|
|
|
HO |
HO |
|
HO |
||||
|
|
|
|
|||||||
X |
|
|
|
|
; |
|||||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
OH |
|
|
|
HO |
|
O |
|
|
|
|
O |
|
|
|
|
OH |
|
|
|
|
O |
|
|
|
OH |
||
|
|
|
|
|
|
|
|
|||
Сесквитерпены представляют собой самую обширную группу среди всех терпенов как по количеству соединений, обнаруженных в природе (их несколько тысяч), так и по множеству структурных вариантов и разнообразию типов углеродного скелета (их более двухсот). В наибольшем количестве и разнообразии сесквитерпены присутствуют в растениях семейств Magnoliaceae, Rutaceae, Cornaceae и Asteraceae. По-видимому, только Ranunculales является единственным классом, в котором сесквитерпены не накапливаются.
Классификация сесквитерпенов, в принципе, построена так же, как и у монотерпенов - по степени циклизации углеродного скелета.
Ациклические сесквитерпены – фарнезаны, являются производными 2,6,10-триметилдодекана. В природе найдены фарнезен (живица хвойных семейства Pinaceae, масло хмеля), нероледол, фарнезол (эфирное масло липы и ландыша ) и некоторые другие оксипроизводные этого ряда:
Моноциклические  сесквитерпены
сесквитерпены  -
-  представлены несколькими группами, различающимися по размеру цикла. Это соединения с циклогексановым фрагментом – циклофарнезаны, бисаболены, элеманы; соединения 1- изопропил-4,8-диметилциклодекановой структуры - гермакраны; сесквитерпены гумуланового типа с 1,1,4,8-тетраметилциклоундекановым скелетом.
представлены несколькими группами, различающимися по размеру цикла. Это соединения с циклогексановым фрагментом – циклофарнезаны, бисаболены, элеманы; соединения 1- изопропил-4,8-диметилциклодекановой структуры - гермакраны; сесквитерпены гумуланового типа с 1,1,4,8-тетраметилциклоундекановым скелетом.
Соединения гермакрановой группы интересны тем, что среди их функциональных производных на первое место выходят лактоны. Они многочисленны также во многих других группах сесквитерпенов, что и послужило причиной выделения их в отдельный класс природных соединений - сесквитерпеновые лактоны цис-транс конфигураций:
160
