
Uchebnik
.pdf
|
|
|
|
O |
|
|
||
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
||
|
С4-С8 |
|
|
|
|
O |
OH |
С4-С8 |
|
|
|
|
|||||
|
|
|
|
|
С4-С8 |
|||
|
|
|
|
|
|
|||
|
O |
|
|
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
O |
|
O |
|
|
O |
O |
O |
C5'-C8 |
|
|
|
|
||||
|
|
O |
|
O |
||||
|
|
|
|
|
||||
|
|
|
|
C6-C8 |
|
C6-C8 |
||
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
C6'-C8 |
|
O |
|
|
|
O |
O |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
C8-C8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
O |
|
|
|
|
|
C3-C3 |
|
|
|
O |
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
||
|
|
|
O |
|
|
|
|
O |
|
O |
|
|
|
|
O |
|
C4'-O-C8 |
|
|
|
O |
|
||||
|
|
|
|
|
|
|||
|
|
|
O |
|
|
|
|
|
|
O |
C |
-O-C |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
4' |
6 |
|
|
|
|
|
С4-С8
O 
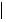
 O
O
O 
 O
O
O
O


C6-C8

 O
O

O

 C2'-C2'
C2'-C2'
O
O
 O
O
O
C4'-O-C5' O
Большой биологической активностью отличаются димеры флавоноидов представленные ниже:
131

|
|
OH |
|
|
|
|
|
|
HO |
O |
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
||
|
|
OH |
HO |
|
O |
|
|
|
|
|
|
OH |
|
|
|
|
|
OH |
O |
OH |
|
|
|
OH |
O |
|
|
O |
|
OH |
O |
O |
|
|
|
|
|
O |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
O |
O |
HO |
O |
|
|
|
|
|
|
HO |
O |
|
|||
HO |
|
|
|
|
|
|||
|
HO |
|
|
|
|
|
|
|
3,8-нарингенин- |
|
|
|
4',6-О-биапигенин |
OH |
|||
апигенин |
6,6-бинарингенин |
OH O |
|
|||||
(волкенсифлавон) |
(сукциданофлавон) |
|
|
|
|
|||
Помимо димеров, в растениях описаны тримеры, типа указанного выше и тетрамеры, объединенные в подгруппу «проантоцианидинов группы Т» (флаволаны), описанные, например, в Pavetta owariensis и др.:
Полифенолы корней герани кровянокрасной представлены 2 катехинами и 3 новыми глюкозидированными проантоцианидинами, структуры которых доказаны комплексом химических и спектральных данных:
132

Стадийный кислотный гидролиз позволил определить соотношение фенольных и углеводных компонент этих соединений – 1:1.5 (1), 1:1 (2), 1:2 (3) и тип связей между мономерами.
Основная роль конденсированных дубильных веществ в растениях – защитная от патогенов и механических повреждений, а для человека и животных – это своеобразные мембраны, осуществляющие процессы диализа, в том числе на опухолях.
Для многих мономерных структур и их димерных аналогов характерно наличие асимметрических атомов углерода и связанных с этим оптических изомеров и рацематов, которые обуславливают различия не только в физических и химических свойствах, но и в биодоступности и биоактивности.
Например, при ферментации чая из различных форм катехинов образуются оптически активные продукты конденсации – теафлавины с бензотрополоновым фрагментом и теарубигены (димерные и полимерные формы).
Под действием желудочного сока и повышенной кислотности, в организме димеры расщепляются до красителей – антоцианов, что делает их более биодоступными, повышая растворимость, способствуя укреплению стенок кровеносных сосудов и связыванию с металлами и анионами.
Наиболее распространенными бифлавоноидами являются структуры с
3,8’-, 6,8’-, 8,8’-, 5’,8’-, 5’,6-типами связи С-С и 4’,6-, 4’,4’-, 3,8’-, 6,6’-типами С-
О-С связей, причем мономерные фрагменты могут быть одинаковыми или разными: флавон-флавон, флаванон-флаванон, флавон-флаванон, флавонфлавонол и теафлавины 18 различных видов чая, содержание которых может увеличиваться при воздействии УФ-света, температуры и ферментов:
133

С наличием большого числа фенольных ОН-групп, особенно с рядовым расположением, связывают возможность дубильных веществ образовывать комплексы, хелаты или соли с белками, протеинами, алкалоидами, тяжелыми металлами, либо выводя их из организма или способствуя их биоактивности. Конденсированные дубильные вещества ограниченно растворимы в воде, поэтому их выделение из растений проводят экстракцией ацетоном или метанолом. Из сухого остатка экстракцией этилацетатом выделяют сумму димеров, дальнейшее отделение от мономеров и полимеров проводят на колонках капрона, перлона, сефадекса, целлюлозы, ионообменных смол. Сумму полученных димеров сразу же переводят в ацильные производные, а затем перацетаты разделяют на колонках кремневая кислота : целит 545 (1:1) из неполярных растворителей или вариантом препаративной хроматографии в тонком слое или на бумаге. Перацетаты разделяются достаточно хорошо, за исключением профизетинидина и пробинетидина, димеров брусники и конского каштана (тип А1 И А2).
Дубильные вещества конденсированного и смешанного типа отделяют от гидролизуемых добавлением 10% уксусной кислоты и 10% раствора ацетата свинца. При этом в осадок выпадают гидролизуемые дубильные вещества и остается черно-зеленый фильтрат при наличии конденсированных дубильных веществ.
Суммарные извлечения дубильных веществ можно разделять на индивидуальные компоненты с помощью хроматографических методов: адсорбционно-распределительной хроматографии на колонках целлюлозы, силикагеля или полиамида, ионообменной хроматографией на колонках катионита (Dauex-50), гель-хроматографией на колонках сефадекса G-50 или G-100.
134
Для предварительной очистки может быть использован метод диализа, лучшие результаты, при этом, получены при выделении высокомолекулярных флавоноидов и танинов, растворимых в воде и для смесей с сахарами и полисахаридами, а также растворимыми неорганическими компонентами растительных экстрактов.
Оптимальных результатов в разделении конденсированных дубильных веществ удалось достичь на неподвижной фазе Лихросорб RР8 с (10 мкм), Сферисорб гексил (5 мкм) и Гиперсил SАS (5 мкм) с УФ-детектором 280 нм. Предложена методика анализа и разделения конденсированных дубильных веществ на колонке [250x4] с Нуклеосилом-5 С18 при 450С с применением в качестве подвижной фазы смеси ацетонитрила и 0.5М раствора фосфорной кислоты при повышении концентрации ацетонитрила и расходе подвижной фазы 0.75 мл/мин.
Применяя колонку [250x4.6] с Сферисорбом ODS (5мкм) при анализе конденсированных танинов в соке некоторых сортов французских яблок, удалось получить достаточно хорошие результаты при градиентном элюировании смесями: А (вода - 1М НСl 99.8:0.2) и В (метанол - 1М НСl 99.8:0.2) с повышением содержания В в А от 0 до 50% в течение 85 минут при расходе подвижной фазы 1.8 мл/мин и использовании УФ-детектора с переменной длиной волны.
При разделении и анализе смешанных танинов хороших результатов удалось достичь на колонке с Лихросфером RР18 (5 мкм) при повышении концентрации уксусной кислоты в смеси её с водой от 2 до 10% за 99 минут, при расходе подвижной фазы 0.5 мл/мин и на колонке Diasorb-130-С16Т при повышении концентрации ацетонитрила в 0.1М ортофосфорной кислоте от 0 до 15% за 180 минут, с дальнейшим элюированием смесью ацетонитрила и муравьиной кислоты при повышении концентрации ацетонитрила от 0 до 30% за 80 мин при расходе подвижной фазы 4 мл/мин при использовании УФдетектора 280 нм.
В качестве сорбентов для выделения, разделения и очистки дубильных веществ широко используются варианты жидкость-жидкостной хроматографии с использованием в качестве неподвижных фаз, помимо названных выше, адсорбентов аффинного типа. Перспективность использования химически модифицированных сорбентов связана со способностью дубильных веществ образовывать комплексы не только с биополимерами (эластазой, коллагеназой, желатином, альбумином и др.), но и с алкалоидами и другими азотсодержащими лекарственными веществами. Описано разделение компонентов дубильных веществ из корневища бадана, кровохлебки, лапчатки, змеевика, коры дуба методом нетрадиционной аффинной хроматографии.
Различить катехины, димерные проантоцианидины и конденсирован-
ные флаваны можно по их положению на бумажной хроматограмме: высокомолекулярные флаваны образуют «дорожки» от точки нанесения по движению водных систем, в зависимости от молекулярной массы - чем ниже масса, тем выше фронт «дорожки».
135

Бифлавоноиды, их перметиловые эфиры, хинокифлавоны (4-O-8’-, 4-
О-6’-межфлавановые связи), аментофлавоны (3,8’-, 3,6’- связи) делят в системе бензол - пиридин - этилформиат – диоксан 5:1:2:2 в тонком слое силикагеля.
Для варианта двумерной хроматографии на бумаге используют системы растворителей: н-бутиловый спирт - уксусная кислота - вода в соотношениях 6:1:8, 4:1:5, 40:12.5:29, в одном направлении и кислота уксусная 2%, 6% и 15% - во втором. Для одномерной бумажной хроматографии применяют системы соляная кислота - уксусная кислота - вода (3:3:1), н-бутиловый спирт - уксусная кислота - вода - этиленгликоль (4:1:5:1), муравьиная кислота - соляная кислота - вода (5:3:2), н-бутиловый спирт - соляная кислота - вода (7:2:5).
Для хроматографии в тонком слое сорбента более пригодны системы: ацетон - вода - пиридин (20:4:1), бензол - метиловый спирт - пиридин (16:2:1), бензол - этиловый спирт (1:1), бензол-ацетон (1:5, 1:4, 1:3).
Ниже приведена схема разделения катехинов и гликозидов, которую можно использовать для любого катехин-содержащего сырья:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СЫРЬЕ |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
бензол |
|
|
хлороформ |
|
|
|
метанол |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Смолы, |
|
|
|
|
Смолы, воска, |
|
|
Флаваны |
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
агликоны |
|
|
|
|
терпеноиды |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
эфир |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
этилацетат |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
(+)-катехин; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(+)-катехин; (-)-эпикатехин; |
|
||||||||||||||||||||
|
|
|
|
(-)-эпикатехин |
|
|
|
|
|
|
|
|
|
|
гликозиды 1,2; флуор. в-ва |
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
полиамид |
|
|||||||
|
хлороформ |
|
20% МеОН/хлф |
30% МеОН/хлф |
|
|
метанол |
||||||||||||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
Смолы, |
|
|
|
|
|
|
|
Гликозид 1; |
|
|
|
|
|
|
|
|
Гликозид 2; |
|
|
|
|
|
Гликозид 2; |
|||||||||||||||||
|
флуор. в-ва |
|
|
|
|
( )-катехины |
|
|
|
|
|
|
|
|
( )-катехины |
|
|
|
|
|
( )-катехины |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
эфир |
|
|
|
|
|
|
|
|
|
силикагель |
|
|
|
|
|
метанол |
LH-20; метанол |
|||||||||||||||||||||||
|
|
|
|
|
ЭА |
|
|
ацетон |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
( )-ка- |
|
|
( )-ка- |
|
|
|
( )-ка- |
|
|
|
|
Гл.1 + |
|
|
Смолы; |
|
|
Гл.2 + |
||||||||||||||||||||||
|
техины |
|
|
техины |
|
|
|
техины |
|
|
|
|
|
сопут. |
|
|
|
|
|
смолы; |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
в-ва |
|
|
( )-ка- |
|
сл.( )-ка- |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ следы |
|
|
|
|
|
|
техины |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Гл.1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
техины |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
LH-20; метанол |
|
|
ТСХ |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ТСХ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
целлюлоза |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
Смолы |
|
|
|
Гл.1 + |
|
целлюлоза |
|
|
|
|
|
|
Гликозид 1 |
|
|
|
Гликозид 2 |
|||||||||||||||||||||||
|
|
|
|
|
|
|
смолы |
|
|
|
|
|
|
|
|
|
|
|
|
(-)-эпикатехина |
|
|
|
(+)-катехина |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
136

Химические свойства конденсированных дубильных веществ
По химической природе дубильные вещества являются полифенолами и для них характерны все реакции, указанные в разделах: фенолы, фенолокислоты и флавоноиды. При этом, поскольку основу гидролизуемых дубильных веществ чаще составляют галловая, м-дигалловая и эллаговая кислоты, которые являются производными пирогаллола, с раствором ЖАК и солей железа окисного они дают черно-синее окрашивание или осадки, как и пирогаллол.
Конденсированные дубильные вещества содержат звенья пирокатехина и с указанными реагентами дают темно-зеленое окрашивание или осадки.
Достаточно надежной для различия пирогалловых и пирокатехиновых танинов является реакция с нитрозометилуретаном, который осаждает
пирокатехиновые дубильные вещества при кипячении.
К извлечению добавляют по каплям бромную воду (5 г брома в 1 л воды) до появления запаха брома, выпадает осадок (конденсированные дубильные вещества и катехины).
Специфика химических свойств конденсированных дубильных веществ связана с молекулярной массой, количеством, расположением, природой заместителей и типом связи. В кислой среде, особенно при нагревании связь С-О-С разрывается быстро и полное расщепление проходит в течение 2-10 часов в растворе от 7 до 20% концентрации кислоты.
Полимерные флавоноиды (флаволаны) трудно растворимы в воде,
лучше при нагревании и в водно-органических растворителях. При температурах выше 800С и при действии кислот выше 7% концентрации флаволаны превращаются в продукты более высокой степени конденсации - флобафены и осаждаются.
Флаволаны образуют нерастворимые окрашенные комплексы с солями алюминия, железа, тяжелых металлов.
При кислотном гидролизе менее 7% концентрации кислоты из флаволанов образуются антоцианидины, например:
137

Проантоцианидины образуют перацетаты, соответственно по всем ОНгруппам, а при реакции метилирования диазометаном образуется метоксипроизводное на 2 ОН группы меньше, т.к. алифатические ОН-группы в эту реакцию не вступают. Это же свидетельствует и о том, что эти две ОН-группы не участвуют в межфлавановой связи.
В проантоцианидинах этой группы 5 асимметрических атомов углерода и теоретически возможны 32 оптических изомера. Но так как мономеры, соответствующие этим димерам, встречаются в растениях обычно в двух наиболее устойчивых формах – транс-форме с 2R3S-конфигурацией ((+)- катехин) или цис-форме с 2R3Rконфигурацией ((-)-эпикатехин), то количество возможных изомеров сокращается до восьми.
Редким является процианидин пальмы, образованный конденсацией (+)- эпикатехина. Четыре из возможных 8 димеров группы В названы условно В1- В4:
При кислотном гидролизе из димера В1 образуется цианидин и (+)- катехин, из димера В2 в тех же условиях получается вместо (+)-катехина - (-)- эпикатехин и т.д.
Стерическое строение «верхних» половин молекул димеров группы В определяют по реакции расщепления с тиогликолевой кислотой. Таким образом, зная химические особенности поведения мономерных молекул, можно предположить возможные направления в реакциях их полимеризации и конденсации. Хэслам, исследовав 29 видов различных растений, обнаружил еще 4 диастереоизомера, которые при детальном изучении их свойств оказались парными, к указанным выше димерам, т.е. димер В5 соответствует
димеру В2, В6 В3, В7 В1, и В8 В4.
138

Эти димеры различаются либо формой межфлавановой связи С8-С4 или С6- С4, либо конфигурацией асимметрического центра у С4, или они являются ротационными изомерами по межфлавановой связи В2 и В5, В1 и В7 - «верхняя» часть молекул - (-)-эпикатехин; В3 и В6. В4 и В8 - «верхняя» часть молекул - (+)- катехин:
В растениях димеры группы А образуются, вероятно, по схеме:
Соединения этой группы под действием минеральных кислот расщепляются с образованием красителя – антоцианидина и флаван-3-ола, однако для гидролиза требуется большая концентрация кислоты (0.5н НСl).
При ацилировании всех димеров группы А получены нонацетаты, а при метилировании диазометаном образуются гептаметиловые эфиры. Если после метилирования проводить реакцию ацилирования, это приводит к получению диацетилгептаметилового эфира. Структура этих соединений не может быть однозначно определена на основании химических свойств полифенолов, поэтому для димеров каштана, как наиболее вероятная предложена формула:
139

Для определения конфигурации молекул предложено проводить расщепление димеров толуолтиолом, при этом тиоэфир «верхней» молекулы при восстановлении никелем Ренея образует соответствующий катехин. Схема реакции изображена ниже:
HO |
|
O |
|
H |
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2N2 |
|
|
|
|
|
|
HO |
O |
|
H |
OH |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
OH |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H+ HO |
|
O |
|
|
|
|
|
|
H+ |
|
|
|
|
|
|
OH |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
||||||||||||||||||||||||
OH |
|
|
|
|
|
OH |
|
|
OH |
|
|
|
|
|
|
H |
OH |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|||
HO |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
O |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(+)-катехин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
||||||
|
|
|
OH |
|
|
|
|
|
OH |
B3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
OH |
|||
|
|
|
|
|
|
|
|
|
|
|
CH N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
B1 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 2 |
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
O |
|
|
|
|
|
|
|
|
HO |
O |
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
HSCH2COOH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
SHCH3Ph |
|
|
|
|
|
|
||||||||||||||||
|
|
HSCH2COOH |
OH |
|
|
SCH2Ph |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
HO |
|
O |
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
HO |
|
O |
|
OH |
|
|
|
|
HO |
|
|
|
O |
H |
||||||||||||||||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H+ [O] |
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
H+ [O] |
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||||||||
OH |
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
H |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
цианидин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Димерные проантоцианидины группы А имеют на 2 атома водорода меньше, чем проантоцианидины группы В, это наводит на мысль о существовании второй межфлавановой связи. Из 12 атомов кислорода 9 соответствуют ОН-группам, что подтверждается в реакциях ацилирования.
140
