
- •Лекция 1 Тема: основные химические понятия и законы. Цель: Ознакомить студентов с оснровными законами и понятиями, лежащими в основе химии.
- •Химия как наука и ее задачи.
- •Важнейшие законы, лежащие в основе химии.
- •Основные понятия химии
- •Закон Авогадро.
- •Уравнение состояния газа. Уравнение Менделеева-Клапейрона.
- •Лекция 2
- •2.Образование атомной кристаллической решетки
- •Лекция 3. Тема: Классификация неорганических соединений. Цель: Ознакомить студентов с разнообразием, строением и свойствами неорганических соединений
- •Кислота основание основание кислота
- •Лекция 4
- •Лекция 5
- •Лекция 6
- •2.Энергия активации. Энтропия активации
- •3.Факторы, влияющие на скорость гомо- и гетерогенных химических реакций. Катализ.
- •Лекция 7
- •2.Изменение энтропии в химическом процессе. Энергия Гиббса
- •Лекция 8
- •2. Коллигативные свойства растворов
- •3.Сильные и слабые электролиты
- •4. Растворы электролитов
- •5. Процесс диссоциации
- •6. Константа диссоциации. Смещение ионного равновесия
- •7. Особенности воды как электролита. Ионное произведение воды . РН раствора. Буферные растворы
- •8. Гидролиз солей. Расчёт концентрации ионов водорода в растворах
- •Лекция 9
- •2.Окислители и восстановители
- •1)Окислители
- •2)Восстановители
- •3)Окислительно-восстановительная двойственность
- •3.Составление уравнений окислительно-восстановительных реакций
- •1.Метод электронного баланса.
- •2.Метод полуреакций, или ионно-электронный метод.
- •Электрохимические процессы
- •2.Направление протекания овр
- •3.Электролиз
- •4.Законы электролиза
- •5.Применение электролиза
- •Лекция 10
- •2.Атомно-молекулярное учение. Основные химические понятия и определения
- •3.Строение атома
- •4. Квантовые числа. Правила заполнения электронных орбиталей
- •Периодический закон и периодическая система элементов д. И. Менделеева.
- •2.Свойства атомов
- •Лекция 11
- •2.Типы химической связи
- •3.Гибридизация атомных орбиталей
- •4.Метод валентных связей
- •Лекция 12
- •Комплексные соединения, их строение и номенклатура. Химическая связь в комплексных соединениях.
- •Устойчивость комплексных ионов. Константа нестойкости. Комплексные химические соединения.
- •Лекция 13
- •2. Водород
- •3. Вода
- •4. Пероксид водорода
- •5. Элементы viiа группы
- •6. Элементы viа группы
- •Общая характеристика элементов vа, ivа групп
- •1. Элементы vа группы.
- •2.Элементы ivа группы.
- •Характеристика металлов
- •1. Строение металлов.
- •2. Физические свойства металлов.
- •3. Химические свойства металлов.
- •Уменьшение химической активности нейтральных атомов
- •Уменьшение способности ионов к присоединению электронов
- •Характеристика элементов второй группы периодической системы
- •Стеарат натрия стеарат кальция
- •Сода осаждает кальций и магний тоже в виде карбонатов:
- •Характеристика элементов третей группы периодической системы
Основные понятия химии
Атомная масса (или атомный вес) — масса 1 атома элемента, выраженная в углеродных единицах. Углеродная единица —1/12 часть массы атома изотопа углерода С12. 1 углеродная единица (сокращенно: уг. ед.) = 1,66-10-24г; 1 г = 6 • 1023 уг. ед. (округленно). Число 6-1023 носит название числа Авогадро.
Грамм-атом — количество элемента, выраженное в граммах и численно равное массе 1 атома в уг. ед. Пример: масса 1 атома серы —32 уг. ед.; грамм-атом серы весит 32 г. Килограмм-атом (кг-атом) = 1000 г-атом; 1 миллиграмм-атом = 0,001 грамм-атома.
Молекулярная масса (или молекулярный вес) —масса 1 молекулы вещества в углеродных единицах. Грамм-молекула, или моль,— количество вещества, выраженное в граммах и численно равное молекулярному весу. Пример: масса 1 молекулы Н2О равна 18 уг. ед.; .1 грамм-молекула (1 моль) воды весит 18 г.
1 грамм-атом содержит Авогадрово число (6-1023) атомов;
1 моль вещества содержит Авогадрово число (6-1023) молекул.
Число Авогадро является важной константой для физики и химии. Это число обозначается через (NA — 6-1023; более точно, NA = 6,0229-1023).
Закон Авогадро.
В отношении идеальных газов, а также газов и паров, близких к этому состоянию, установлен следующий закон Авогадро: при данных условиях температуры и давления в равных объемах всех газов содержится одинаковое число молекул.
Одно из важнейших следствий из этого закона: грамм-молекулы всех веществ в газообразном или парообразном состоянии при нормальных физических условиях занимают одинаковые объемы, а именно: 22,4 л/моль, или 22,4 м3/кмоль, или 22,4 см3/миллимоль.
Нормальные физические условия: температура 0° С (или 273° по абсолютной шкале = 273° К), давление 760 мм ртутного столба.
Из закона Авогадро вытекают также следующие два положения:
1. Молекулярная масса вещества М численно равна удвоенной его плотности D в газообразном или парообразном состоянии по водороду: М = 2D, точнее, М = 2,016 D).
2. Молекулярная масса вещества численно в 29 раз больше, чем относительная плотность его D' в газообразном или парообразном состоянии по отношению к воздуху: М = 29 D'.
В этих формулах:
D = Вес 1 л данного газа; D' = Вес 1 л данного газа (1-1)
Вес 1 л водорода Вес 1 л воздуха
При нормальных условиях 1 л водорода весит 0,09 г, а 1 л воздуха— 1,293 г.
Из формулы М = 29D' получаем: D' = М/29. Из последнего соотношения вытекает, что все газы и пары, у которых М > 29, тяжелее воздуха, а у которых М < 29—легче воздуха.
Уравнение состояния газа. Уравнение Менделеева-Клапейрона.
Выше приводились данные в отношении газов, находящихся при нормальных физических условиях (температура 0°, давление 760 мм рт. ст.). На практике большей частью приходится вести работу с газами, находящимися при иных условиях температуры и давления.
Для производства расчетов с газами, находящимися при разнообразных физических условиях, служит уравнение Клапейрона — Менделеева, которое в математической форме устанавливает связь между величинами (параметрами), определяющими состояние газа,— объемом, давлением и температурой:
pV = nRT. (1-2)
В этой формуле р — давление газа, выраженное либо в мм рт. ст., либо в атм; V — объем газа в л; п —число молей газа; R — универсальная газовая постоянная; Т —абсолютная температура, которая связана со шкалой Цельсия равенством:
Т = t + 273, где t — температура по шкале Цельсия.
Число молей газа п может быть вычислено по одному из соотношений:
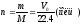 (1-3)
(1-3)
где m —данная масса газа в г; М —r-молекулярное количество газа, согласно его химической формуле, также в г; Vo — объем данной массы газа при нормальных условиях в л.
Универсальная газовая постоянная R вычисляется для 1 моля газа, находящегося при нормальных условиях:
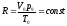 (1-4)
(1-4)
В последней формуле р0 — нормальное давление (р0 = 760 мм рт. ст. == 1 атм), V0 —молярный объем газа при нормальных условиях (Vo = 22,414 л/моль) и То—нормальная температура (для t = 0°С имеем Т0=273°К).
Численная величина газовой постоянной R зависит от того, в каких единицах выражаются объем и давление газа. Если объем выражен в литрах (Vo = 22,414 л/моль), а давление в атмосферах (р0 — 1 атм), то для газовой постоянной получаем:
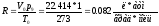 (1-5)
(1-5)
Если объем газа по-прежнему выражен в литрах, а давление в миллиметрах ртутного столба {р0 = 760 мм рт. ст.), то газовая постоянная окажется равной:
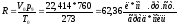 (1-6)
(1-6)
Газовая постоянная имеет размерность работы (представляет собой работу расширения 1 моля газа при нагревании его на 1°-при постоянном давлении). В связи с этим величину R можно выражать и в других энергетических единицах.
Литература:
Ахметов, Н.С. Общая и неорганическая химия / Н.С.Ахметов. – 3-е изд. – М.: Высшая школа, 2000. – 743с.
Т.Браун. Химия – в центре наук / Браун.Т, Лемей Г.Ю. – М.: Мир, 1983. – тт. 1–2.
Карапетьянц М.Х. Общая и неорганическая химия / М.Х. Карапетьянц, С.И.Дракин. – М.: Высшая школа, 2002.
Коровин Н.В. Общая химия / Н.В.Коровин. – М.: Высшая школа, 2006. – 557 с.
Кузьменко Н.Е. Краткий курс химии / Н.Е. Кузьменко, В.В Еремин, В.А. Попков. – М.: Высшая школа , 2002. – 415 с.
