- •60 Химическое строение и свойства витамина b1
- •Нехватка витамина b1, причины, симптомы
- •Нарушение обмена тиамина в организме
- •Суточная потребность в витамине b1, пищевые источники витамина b1
- •Продукты, богатые витамином b1
- •Химическое строение и свойства витамина b2 (рибофлавина)
- •Биохимические свойства витамина b2
- •Гиповитаминоз и гипервитаминоз витамина b2 Гиповитаминоз
- •Гипервитаминоз
- •Метаболизм пантотеновой кислоты (витамина b3)
- •Биохимические функции пантотеновой кислоты
- •Гиповитаминоз и гипервитаминоз пантотеновой кислоты
- •Суточная потребность и пищевые источники пантотеновой кислоты
- •Продукты, богатые пантотеновой кислотой (витамином b3)
- •Химическое строение и свойства витамина pp
- •Метаболизм витамина pp
- •Биохимические функции никотиновой кислоты
- •Гиповитаминоз витамина b5
- •Гипервитаминоз витамина b5
- •Оценка обеспеченности организма витамином pp
- •Суточная потребность и пищевые источники витамина b5
- •Продукты,богатые витамином pp (b5)
- •Гиповитаминоз пиридоксина (витамина b6)
- •Гипервитаминоз пиридоксина (витамина b6)
- •Врожденные нарушения обмена витамина b6
- •Гомоцистинурия
- •Цистатионинурия
- •Наследственная ксантуренурия (синдром Кнаппа)
- •Пиридоксинзависимый судорожный синдром
- •Пиридоксинзависимая анемия
- •Суточная потребность в витамине b6, пищевые источники пиридоксина
- •Метаболизм фолиевой кислоты
- •Биохимические функции и свойства витамина b9
- •Гиповитаминоз фолацина
- •Врождённые нарушения обмена витамина b9
- •Обеспеченность организма фолиевой кислотой
- •Суточная потребность в витамине b9, пищевые источники фолиевой кислоты
- •Продукты,богатые витамином b9
- •Химическое строение и свойства витамина b12 (кобаламина)
- •Метаболизм кобаламина в организме
- •Биохимические свойства и функции кобаламина (b12)
- •Недостаток кобаламина (витамина b12) в организме
- •Избыток витамина b12
- •Как проводят оценку?
- •Суточная потребность витамина b12, пищевые источники кобаламина
- •Продукты,богатые витамином b12
- •Химическое строение и свойства витамина h
- •Метаболизм биотина (витамина h)
- •Биохимические функции биотина
- •Врожденные нарушения обмена биотина, гипервитаминоз и гиповитаминоз витамина h Гиповитаминоз
- •Врожденные нарушения обмена биотина
- •Суточная потребностьи пищевые источники биотина
- •Продукты,богатые витамином h
- •Витамин с (аскорбиновая кислота), химическое строение и свойства
- •Метаболизм аскорбиновой кислоты в организме
- •Биохимические функции аскорбиновой кислоты
- •Гиповитаминоз и гипервитаминоз аскорбиновой кислоты Гиповитаминоз
- •Суточная потребность и источники аскорбиновой кислоты
- •Продукты, богатые витамином c
- •Химическое строение и свойства витамина а.
- •Метаболизм витамина а в организме человека
- •Биохимические функции ретинола
- •Участие витамина а в процессе зрения
- •Участие витамина а в антиоксидантной защите организма
- •Гиповитаминоз и гипервитаминоз ретинола Гиповитаминоз витамина а
- •Гипервитаминоз витамина а
- •Оценка обеспеченности организма ретинолом
- •Врожденные нарушения обмена ретинола
- •Суточная потребность витамина а, пищевые источники витамина а
- •Продукты, богатые витамином а
- •Химическое строение и свойства каротинов (провитаминов а)
- •Биохимические функции провитаминов а
- •Суточная потребность и пищевые источники каротинов
- •Продукты, богатые каротинами
- •Химическое строение и свойства витамина е
- •Метаболизм токоферола
- •Биохимические функции токоферола
- •Гиповитаминоз токоферола
- •Гипервитаминоз токоферола
- •Врождённые нарушения обмена токоферола
- •Оценка обеспеченности организма витамином е
- •Суточная потребность и пищевые источники токоферола
- •Продукты, богатые витамином е
- •Витамин д (кальциферол), химическое строение и свойства
- •Метаболизм витамина д
- •Биохимические функции кальциферола
- •Гиповитаминоз витамина д
- •Врожденные нарушения обмена кальциферола Семейный гипофосфатемический витамин-д-резистентный рахит.
- •Врожденный псевдодефинитный витамин-д-зависимый рахит.
- •Гипервитаминоз витамина д
- •Суточная потребность в витамине д и его источники
- •Метаболизм и биохимические функции витамина k Метаболизм витамина к
- •Биохимические функции витамина к
- •Недостаточность витамина к
- •Врожденные нарушения обмена витамина к
- •Оценка обеспеченности организма витамином к, суточная потребность
- •Продукты богатые витамином к
- •Метаболизм витамина f метаболизм витамина f
- •Биохимические функции витамина f
- •Недостаточность витамина f
- •Суточная потребность и источники витамина f
- •Продукты богатые витамином f
- •Химическое строение и свойства инозита (витамина b8)
- •Метаболизм витамина b8 (инозита)
- •Суточная потребность и источники витамина b8
- •Недостаточность карнитина
- •Потребность и пищевые источники липоевой кислоты
- •Потребность и источники парааминобензойной кислоты.
- •Суточная потребность и пищевые источники рутина
- •Продукты, богатые витамином p
Как проводят оценку?
Для этой цели служит определение содержания витамина в сыворотке крови, либо определение суточной экскреции метилмалоновой кислоты, которая возрастает при низкой обеспеченности организма кобаламином в десятки и сотни раз. Иногда применяется также метод нагрузки с помощью парентерального введения меченного по кобальту витамина В12.
Суточная потребность витамина b12, пищевые источники кобаламина
Синтез кобаламинов в природе осуществляется исключительно микроорганизмами. Животные и растительные клетки такой способностью не обладают. Основные пищевые источники витамина — печень, мясо (в нем кобаламина в 20 раз меньше, чем в печени), морские продукты (крабы, лососевые, сардины), молоко, яйца. У строгих вегетарианцев, исключающих из пищи не только мясные, но и молочные продукты, рано или поздно развивается В12-дефицитная анемия.
Суточная потребность — 3 мкг.
Продукты,богатые витамином b12






Химическое строение и свойства витамина h
Биотин был выделен в 1935 г. из яичного желтка. Свое название витамин получил от греч. bios — жизнь из-за его способности стимулировать рост дрожжей и бактерий.
Молекула витамина Н состоит из имидазольного и тетрагидротио-фенового колец, боковая цепь представлена валериановой кислотой.
N1-имидазольного кольца является местом карбоксилирования. Связываясь с ионом гидрокарбоната (НС03-), биотин становится кофер-ментом, называемым карбоксибиотином.

Биотин плохо растворяется в воде, но хорошо в спирте. Он устойчив при нагревании и в растворах слабых шелочей и оснований.
Биотин способен образовывать с авидином — гликопротеином белка куриного яйца — прочный комплекс, который не может расщепляться пищеварительными ферментами. Поэтому при частом употреблении сырых яиц прекращается всасывание присутствующего в пище биотина. Способность молекул авидина и биотина специфически связываться друг с другом используется в некоторых методах очистки в биотехнологии.
Метаболизм биотина (витамина h)
С растительной пищей витамин Н поступает преимущественно в свободном состоянии. Биотин животной пищи освобождается гидролазами от связи с различными белками и в свободном виде всасывается в тонком кишечнике. В кровяном русле биотин переносится альбумином и аккумулируется главным образом в печени. В тканях биотин находится в виде карбоксибиотинил-ферментов: СОО- группа валериановой кислоты карбоксибиотина ковалентно присоединена карбамидной связью к e-NH2-rpynne лизина, входящего в состав активного центра биотинзависимого фермента.
Выводится биотин в свободном виде с мочой и экскрементами, причем с последними его выводится больше, чем поступает с пищей. Объясняется это способностью микрофлоры кишечника синтезировать биотин.
Биохимические функции биотина
Витамин Н способствует усвоению тканями ионов бикарбоната (но не СO2) и активирует реакции карбокси-лирования и транскарбоксилирования в составе следующих карбо-ксибиотинил-ферментов:
Пируваткарбоксилазы — фермента, катализирующего АТФ-зависимое образование оксалацетата из пирувата и НСО3- .

Пируваткарбоксилаза является тетрамерным белком, несущим четыре молекулы биотина, каждая из которых связана с остатком лизина алофермента. Пируваткарбоксилазная реакция является наиболее важной анаплеротической реакцией, особенно в печени и почках (к анаплеротическим относятся возмещающие, пополняющие, реакции). Так, пируваткарбоксилаза восполняет запас оксалацетата, необходимый для функционирования цикла Кребса.
Пируваткарбоксилаза является важным митохонлриальным ферментом глюконеогенеза (новообразования глюкозы).
Ацетил-КоА-карбоксилазы — первого фермента в реакциях биосинтеза жирных кислот. Активная форма энзима представляет собой множество длинных мономерных нитей. При ферментативном катализе отдается карбоксильная группа бикарбоната ацетил-коэнзиму А с образованием малонил-КоА:

Пропионил-КоА-карбоксилат — фермента, участвующего в окислении жирных кислот с нечетным числом атомов углерода. При этом происходит стереоспецифический перенос активированной карбоксильной группы от карбоксибиотина к пропионил-КоА с образованием метил малонил-КоА:

Следует отметить, что ион бикарбоната может утилизироваться клеткой без участия биотина, как, например, это имеет место в карбомоилфосфатсинтетазной реакции при синтезе пиримидинов:
![]()
Бета-метилкротоноил-КоА-карбоксилазы — фермента, участвующего в реакциях окислительного распада лейцина.
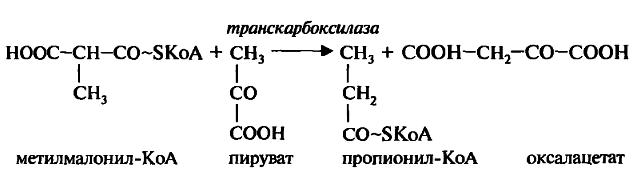
Метилмалонил-ЩУК-транскарбоксилазы — фермента, катализирующего реакцию транскарбоксилирования, а именно, обратимое превращение пирувата и оксалацетата (другие транскарбоксилазные реакции также протекают с участием биотина):