
6 курс / Неонатология / Неонатология_Н_П_Шабалов_7_е_издание_Том_2_2020
.pdfалкалоз, гипохлоремия, гипокалиемия, гипо-натриемия. Позднее уровень сывороточного натрия нормализуется благодаря развитию вторичного гиперальдостеронизма.
Клиническая картина. Болезнь проявляется уже внутриутробно многоводи-ем, что свидетельствует о начале диареи еще до рождения. У новорожденных отсутствует меконий. Дети обычно рождаются недоношенными, нередко с явлениями пренатальной гипотрофии. Уже при рождении отмечается увеличение живота, связанное с парезом кишечника, который продолжается в течение нескольких недель и не зависит от уровня калия.
С первых дней жизни наблюдается рвота фонтаном после каждого кормления, жидкий очень водянистый, похожий на мочу стул 10-20 раз в сутки. Диарея носит профузный упорный характер, приводя к тяжелой дегидратации, гипотрофии, мышечной гипотонии. В крови - тяжелая гипохлоремия, алкалоз. Обычная инфузионная терапия достаточного эффекта не дает. Отмена молочного питания также неэффективна.
Диагностика. Основное диагностическое значение имеют:
1)повышение экскреции хлоридов с фекалиями (более 1 г/сут);
2)выраженная гипохлоремия, гипокалиемия;
3)тяжелый алкалоз (pH крови до 7,7-7,8; ВЕ до +30,0).
Лечение. Тяжелое состояние ребенка требует назначения парентерального искусственного питания. После периода парентерального питания обычно состояние ребенка стабилизируется. Для коррекции потерь хлора рекомендуется пожизненное замещение электролитов в виде смеси NaCl и KCl, требуется несколько грамм хлоридов в день, доза подбирается индивидуально. Питание ребенка обычное.
Прогноз благоприятный после периода парентерального питания.
Врожденная натриевая диарея - редкое аутосомно-рецессивное заболевание, связанное с нарушением транспортного белка, обеспечивающего обмен иона натрия на ион водорода в энтероците. Усиленная секреция натрия с калом сопровождается потерей воды. Нарушение Na+/H+ обмена способствует задержке в организме водородных ионов и развитию метаболического ацидоза.
Клиническая картина. Симптоматика заболевания очень похожа на врожденную хлоридную диарею. Подобно ей, в последнем триместре беременности может наблюдаться многоводие, ребенок рождается с задержкой внутриутробного развития. С рождения наблюдается профузная диарея с выделением очень жидких водянистых фекалий, имеющих упорное течение без какого-либо эффекта от диетической коррекции. В крови развиваются тяжелая гипонатрие-мия, метаболический ацидоз.
Диагностика. Диагностическое значение имеют: упорный профузный понос с рождения, повышение экскреции натрия с калом, гипонатриемия и метаболический ацидоз.
Заболевание следует дифференцировать от сольтеряющей формы адреноге-нитального синдрома (по уровню 17-гидроксипрогестерона в крови), а также врожденной хлоридной диареи. При проведении дифференциальной диагностики с последней решающее значение имеет определение электролитов в кале:
•для хлоридной диареи характерно: Cl- > Na+ + K+;
•для натриевой диареи характерно: Na+ > Cl- + K+.
Лечение. Тяжелая профузная диарея и дегидратация требуют перевода ребенка на парентеральное питание, после которого состояние ребенка несколько улучшается, хотя персистирующая диарея остается. С целью восполнения потерь натрия назначают натрия
цитрат и глюкозо-солевые растворы для оральной регидратации, так как всасывание натрия при назначении их происходит по другому, глюкозо-натриевому каналу энтероцита.
Прогноз. Персистирующая секреторная диарея сохраняется, но после периода парентерального питания обычно не имеет жизнеугрожающего характера.
Первичные аномалии энтероцитов. Раннее начало тяжелой водянистой диареи должно наводить на мысль об интестинальной патологии, обусловленной нарушениями эпителия тонкой кишки. На сегодняшний день известно несколько типов первичных аномалий интестинального эпителия, обусловливающих клинические проявления.
Атрофия микроворсинок (болезнь включения микроворсинок). Этиология. Причина заболевания не ясна. Предполагается аутосомно-рецессивный путь наследования, так как описаны случаи поражения нескольких детей в одной семье. Существует мнение, что заболевание ассоциировано с патологией энтеро-цитарного цитоскелета, который продуцирует аномальные микроворсинки. В пользу этой теории свидетельствует обнаруженный дефицит миозина энте-роцитарного цитоскелета. Предполагают также нарушения экзоцитоза глико-каликса.
Возможным вариантом заболевания является описанная недавно дистрофия интестинальных микроворсинок.
Морфология. Световая микроскопия биоптатов тонкой кишки выявляет гипопластическую атрофию ворсин с истончением слизистой оболочки. Окраска реактивом Шиффа (+ PAS-реакция) позволяет увидеть аномально окрашенные включения в апикальной части цитоплазмы эпителия.
При электронной микроскопии микроворсинки на поверхности энтероци-тов в области ворсин отсутствуют или имеют аномальную конфигурацию, а в цитоплазме энтероцитов обнаруживают везикулы с находящимися там (включенными) микроворсинками. Клетки крипт почти нормальны и не содержат везикулярных включений. Аналогичные изменения присутствуют и в эпителии толстой кишки.
Вышеописанные структурные нарушения щеточной каймы энтероцитов приводят к тяжелым нарушениям мембранного транспорта.
Клиническая картина. Тяжелая секреторная диарея обычно развивается через несколько дней после рождения, хотя описаны случаи более позднего начала заболевания. Стул водянистый и очень обильный, его объем составляет иногда более 250-300 мл/кг в сутки, соотношение электролитов при этом обычное
(в отличие от врожденной хлоридной или натриевой диареи). На фоне массивной потери жидкости и электролитов развивается тяжелая дегидратация. Отмена энтерального питания и инфузионная заместительная терапия не купируют диарею.
Диагноз устанавливают по морфологическим данным: атрофии ворсин без воспалительной инфильтрации и обнаружению характерных включений с элементами щеточной каймы внутри энтероцитов.
Лечение и прогноз. Без парентерального искусственного питания (ПИП) болезнь имеет фатальный характер. Однако и современные достижения ПИП не позволяют продлить жизнь больным с АМ, большинство детей погибают в раннем возрасте. Попытки лечения кортикостероидами, молозивом, эпителиальным фактором роста оказались безуспешными. Единственно возможным методом лечения больных с АМ является пересадка тонкой кишки.
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
Интестинальная эпителиальная дисплазия (пучковая энтеропатия). Инте-стинальная эпителиальная дисплазия (ИЭД) - энтеропатия, при которой происходит патологическое слущивание кишечного эпителия, является более частой аномалией энтероцитов, чем атрофия микроворсин, особенно на Ближнем Востоке.
Этиология. В последних исследованиях доказаны изменения структуры кишечного α2β1- интегрина, обеспечивающего взаимодействие эпителиальных клеток с различными компонентами базальной мембраны, такими как ламинин и коллаген, вдоль оси криптаворсинка. Образующиеся «пучки» представляют собой группы клеток, не подвергшихся апоптозу, но и не связанных с базальной мембраной. Таким образом, снижение апоптоза сопровождается усилением межклеточных связей.
Большинство больных ИЭД - дети от родственных браков, описаны случаи заболевания у нескольких детей в одной семье. Это предполагает вероятность аутосомно-рецессивного пути наследования патологии.
Морфология. При морфологическом исследовании биоптатов тонкой кишки всегда обнаруживают атрофию ворсин различной степени тяжести. Аномалия характеризуется дезорганизацией поверхностных энтероцитов с локальными их скоплениями, похожими на пучки. Эти «пучки» слущивающихся клеток располагаются преимущественно у верхушек ворсин, но могут захватывать до 70% их поверхности. Крипты могут быть разветвленными, аномально расширенными, содержать псевдокисты, что свидетельствует о нарушениях процессов регенерации кишечного эпителия. Изменения не ограничиваются тонкой кишкой, подобные скопления обнаруживают и на поверхности толстой. Описан случай поражения всего ЖКТ.
Клиническая картина. Заболевание проявляется в первые недели жизни тяжелой водянистой диареей. Диарея резистентна к терапии и требует постоянного парентерального питания. Однако описаны случаи более мягких клинических проявлений. Возможно, фенотипические различия обусловлены различиями мутаций патологического гена.
У некоторых больных ИЭД может сочетаться с другими аномалиями: атре-зией хоан, ректальной атрезией, пилоростенозом, кератитом.
Диагностика. Диагностика ИЭД может быть сложной по нескольким причинам. Несмотря на раннее начало тяжелой постоянной диареи, характерные «пучки» слущивающихся клеток при морфологическом исследовании не всегда удается обнаружить. Первоначально может выявляться лишь умеренная атрофия ворсин, и только повторные биопсии и исследование в динамике позволяют найти морфологическое подтверждение болезни. Вторая сложность состоит в том, что хотя ИЭД не является воспалительным заболеванием, при исследовании биоптатов иногда обнаруживают инфильтрацию собственной пластинки Т-лимфоцитами, часть которых активирована. Эта инфильтрация является следствием повышенной проницаемости кишечного барьера в условиях нарушенной клеточной адгезии к базальной мембране, т. е. инфильтрация вторична по отношению к первичной аномалии энтероцитов.
Лечение и прогноз. Дети с ИЭД требуют постоянного парентерального питания. Консервативная терапия неэффективна. Возможным методом лечения является трансплантация тонкой кишки.
Синдромальная энтеропатия (СЭ) характеризуется сочетанием трудноизлечимой упорной диареи и внешних аномалий.
Этиология. Причина СЭ неизвестна, и взаимосвязь между основными симптомами - низкой массой при рождении, дисморфизмом, тяжелой диареей, трихорексисом и иммунодефицитом остается не ясной. Возможны два генетических варианта - либо
одновременная мутация нескольких генов, контролирующих вышеописанные признаки, либо (что более вероятно) нарушения на более высоком уровне моделирующих генов.
Клиническая картина. Симптомы ТМД проявляются в первые 6 мес жизни, но чаще - уже на 1-м месяце. Диарея носит водянистый характер, без патологических примесей, объем потерь со стулом составляет 50-100 мл/кг в сутки. Исключение энтерального питания и перевод ребенка на парентеральное не уменьшают диарею. Обычно дети рождаются малыми к сроку гестации и имеют определенные внешние аномалии или стигмы: лицевой дизморфизм - выдающийся лоб, широкий нос, гипертелоризм, а также отчетливую аномалию волос, которая носит название trichorrhexis nodosa, при которой волосы выглядят наподобие шерсти, трудно укладываются, легко выпадают и плохо пигментированы, даже у детей из южных регионов. Подобная аномалия волос встречается и при других патологических состояниях. У всех описанных пациентов СЭ отмечены нарушения иммунной защиты, несмотря на нормальный уровень сывороточных иммуноглобулинов, отрицательные антигенспецифичные кожные пробы. Характер иммунодефицита остается неуточненным.
Диагноз основывается на характерном сочетании симптомов: задержки внутриутробного развития, внешних аномалий лица и волос, ТМД и иммунодефицита. Морфологическое исследование биоптатов СОТК во всех случаях показало наличие атрофии ворсин II-III степени с непостоянной мононуклеарной инфильтрацией собственной пластинки без каких-либо эпителиальных аномалий.
Прогноз этого типа ТМД плохой, так как большинство пациентов умирают в возрасте от 2 до 5 лет. Лечение не разработано, в первые месяцы жизни проводится парентеральное питание.
20.2.14. Некротический энтероколит
Некротический энтероколит (НЭК) - это одно из наиболее частых и серьезных приобретенных заболеваний ЖКТ у недоношенных детей с ЭНМТ и ОНМТ, сопряженное с высоким риском осложнений и высокой летальностью.
Эпидемиология. В 2013 г. заболеваемость НЭК в Санкт-Петербурге была 1,4 на 1000 живорожденных. Болезнь преимущественно развивается у детей с ЭНМТ и ОНМТ в ОРИТН в период выздоровления от кардиопульмональных заболеваний. Примерно 5-10% больных НЭК - доношенные новорожденные с «синими» пороками сердца, полицитемией, ЗВУР, тяжелой асфиксией, ЗПК или обструктивной мальформацией ЖКТ. При этом у них чаще отмечается спонтанная перфорация кишечника (СПК).
Сообщения о групповой заболеваемости НЭК в отделениях патологии новорожденных редки, но описаны вспышки заболевания в ОРИТН, которые обрывались вслед за введением строгих противоэпидемических мер. Если у доношенных новорожденных НЭК обычно развивается в первые 3-4 дня жизни, то у недоношенных менее 28 нед гестации - между 2-й и 4-й неделями постна-тальной жизни (Caplan M., 2012). Чем меньше масса при рождении, тем чаще, но позднее может развиться НЭК.
M. Caplan (2012) подчеркивает, что по сущности и прогнозу НЭК и СПК различаются, но и у детей с ЭНМТ и ЭНМТ в первые 2 нед жизни может развиться СПК (табл. 20.9). И ближайший, и отдаленный прогноз при СПК достоверно лучше по сравнению с прогнозом у больных НЭК.
Частота. Подавляющее большинство больных НЭК (90%) - недоношенные дети с массой тела менее 1500 г, поэтому НЭК называют «болезнью выживших недоношенных». Из недоношенных близнецов НЭК чаще развивается у первого ребенка, хотя второй обычно более слабый. С.А. Караваева (2002) отмечает, что у 4,7% новорожденных, поступивших в 80-90-е годы прошлого века в городской центр реанимации и интенсивной терапии
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
новорожденных при ДГБ № 1 Санкт-Петербурга, выявлен НЭК. Среди 432 больных НЭК, наблюдавшихся ею, 78% были недоношенными и 54,6% имели срок гестации 32 нед и менее.
Таблица 20.9. Клинические различия между некротическим энтероколитом и спонтанной перфорацией кишечника (Caplan M., 2012)
Признак |
Некротический |
Спонтанная |
|
энтероколит |
перфорация кишечника |
Частота у детей с ЭНМТ и ОНМТ |
7-10% |
2-3% |
Возраст начала |
2-6-я недели |
0-14-й дни |
Пневматоз |
Да |
Нет |
Энтеральное питание |
Да |
Нет |
Гистологические доказательства |
Да |
Нет |
некроза ворсинок |
|
|
Летальность |
На 10-30% выше |
На 5-10% выше средней |
|
средней |
|
Среди пациентов с массой 500-750 г частота НЭК может доходить до 1320%. В 2013 г. частота НЭК в Санкт-Петербурге у детей с массой тела при рождении менее 750 г составила 18,5%, 751-1000 г - 13%, 1001-1500 г - 12% (Федорова Л.А., 2014). Согласно M. Caplan (2012) 50% больных с НЭК требуется хирургическое вмешательство, а летальность при НЭК - 25-30%.
Этиология и патогенез. НЭК поражает выживающих, поправляющихся после тяжелой болезни новорожденных. Большинство из них переносят респираторный дистресссиндром (РДС, внутричерепные кровоизлияния и родовую травму) за несколько дней или недель до начала НЭК. Поскольку заболевание обычно наблюдается у недоношенных детей, многие факторы, ассоциированные с недоношенностью, рассматриваются как факторы риска НЭК.
Ишемия кишечника. Факторы риска включают асфиксию, РДС, гипоксию, гипотензию, открытый артериальный проток (ОАП), полицитемию, анемию, катетеризацию пупочной артерии (в меньшей степени пупочной вены), замен-ное переливание крови (ЗПК). Действительно, каждый из указанных факторов способен вызвать ишемию кишечника, но контролируемые исследования показали, что эти заболевания с равной частотой встречаются и у детей с НЭК, и в контрольной группе (Kleiman R.М., 1997), поэтому не рассматриваются как прямые патогенетические факторы НЭК, а лишь как частые атрибуты недоношенности. Главный фактор риска НЭК - недоношенность в сочетании с незрелостью иммунного ответа и гастроинтестинальных функций.
Некоторые факторы могут инициировать недостаточность мезентериального кровообращения уже внутриутробно - плацентарная недостаточность, употребление матерью кокаина. Дети с кокаиновой интоксикацией имеют более высокий риск развития НЭК, хотя и рождаются с относительно большей массой.
Врезультате гипоперфузии резко снижается местная резистентность слизистой оболочки, ишемические участки ее становятся более подверженными воздействию агрессивной микрофлоры, что завершает патологический процесс.
Внормальном организме поступление пищи вызывает расширение мезен-териальных сосудов, что регулируется местными гастроинтестинальными гормонами и обеспечивает секрецию пищеварительных ферментов в просвет кишки и доставку кислорода к работающему органу. Этот процесс может нарушаться в условиях незрелости ЖКТ и нарушенного местного и системного кровотока.
Нарушение механизмов ауторегуляции кишечного кровотока как в связи с изменениями центрального кровотока, так и в связи с кормлением - одно из узловых звеньев патогенеза НЭК.
Бактериальная колонизация и провоспалительный ответ. Многие эпидемиологические исследования подтверждают, что НЭК ассоциирован с одним или несколькими бактериальными агентами. У большинства детей при бактериологическом исследовании кала наблюдается рост таких микроорганизмов, как кишечная палочка, фекальный стрептококк, серрация, клебсиелла, эпи-дермальный стафилококк, клостридии и грибы рода Candida. В 25% случаев высеваются ассоциации этих агентов (Караваева С.А., 2002).
Единый идентифицированный бактериальный агент отсутствует (Норманн Э. и др., 2013), однако в некоторых экспериментальных и сравнительных исследованиях предполагается важная роль анаэробов в генезе этой патологии, в частности, Clostridium perfringens типа С и Clostridium difficile. Это доказывается типичным для НЭК пневматозом кишечника, напоминающим газовую гангрену, а также опытами на животных.
У 20-30% пациентов микробный агент выделяется из культуры крови. Чаще это грамотрицательные микробы (E. сoli, Streptococcus faecies, Serratia marcescens, Acinetobacter, Proteus mirabilis, Klebsiella) или Staph. epidepmalis. Остается не выясненным, является ли микроорганизм, высеваемый из крови или перитоне-альной жидкости, первичным патогеном или вторично внедрившимся, который попадает в циркуляцию вследствие повреждения слизистой оболочки кишки.
Определенное значение имеет контаминация несколькими нормальными аэробными грамотрицательными симбионтами. Эндотоксины этих бактерий, обычно неопасные, при слабой элиминации или повышенной проницаемости эпителиального барьера могут вызывать воспалительные изменения слизистой оболочки кишечника с избытком синтеза провоспалительных цито-кинов и дефицитом противовоспалительных. Более того, в настоящее время установлено, что при глубокой недоношенности дети, как правило, рождаются с признаками «системного фетального воспалительного ответа» (подробнее см. главу 14).
Энтеральное питание. Несколько рандомизированных исследований конца 1980-х - начала 1990-х годов показали высокую ассоциацию частоты НЭК и раннего начала (на первых днях жизни) энтерального питания глубоко недоношенных детей, а также повышенного количества жира и белка в смесях для вскармливания. В дальнейшем, правда, выяснилось, что дело скорее в интенсивности увеличения энтеральной нагрузки (25 мл/кг в сутки и более). Установлено, что раннее начало энтерального «трофического питания» (см. главы 6, 8) уменьшает вероятность развития НЭК. Гиперосмолярные смеси и назначенные внутрь лекарства усиливают воздействие на кишечный кровоток и моторику. Превышая возможности пищеварения и всасывания, непереваренные компоненты пищи, особенно углеводы, способствуют развитию метеоризма. Высокое давление в просвете кишки при этом может редуцировать местный кровоток. При повреждении эпителия газ из полости кишки может проникать под слизистую оболочку и вызывать типичный симптом кишечного пневматоза, а в случае проникновения в сосуды - воздушную эмболию v. hepatica и v. porta. Анализ газа из пневматических кист показал, что его состав типичен для бактериальной ферментации неабсорбированных углеводов и содержит водород, углекислый газ, метан. В то же время отсрочка перевода на энтеральное питание детей, перенесших тяжелую асфиксию, катетеризацию пупочной вены и РДС, не сопровождается достоверным снижением частоты НЭК и скорее усугубляет риск осложнений, так как способствует развитию атрофии слизистой оболочки тонкой кишки, холестазу, остеопении и др.
Постпрандиальная гипоксия может вызывать нарушение пищеварения и всасывания, нарушение перистальтики и реализоваться в повреждение кишки, повышение ее
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
проницаемости и язвообразование. Возможно, именно пост-прандиальная гипоперфузия создает у пациентов с НЭК несоответствие между повышенными потребностями в кислороде и энергии после приема пищи и недостаточными возможностями их доставки.
НЭК обычно ассоциирован с искусственным вскармливанием, он развивается у 1,2% недоношенных, получающих материнское молоко, и у 7,2%, получающих молочные смеси. По этой причине родился афоризм: «НЭК - болезнь глубоко недоношенных детей, питающихся формулами (смесями для искусственного вскармливания)».
Установлена ассоциация повышения частоты развития НЭК с применением некоторых медикаментов (индометацина, Эуфиллина♠, натрия гидрокарбоната, препаратов кальция, высокоосмолярных растворов, антибиотиков широкого спектра, кортикостероидов и др.), наркоманией у матери.
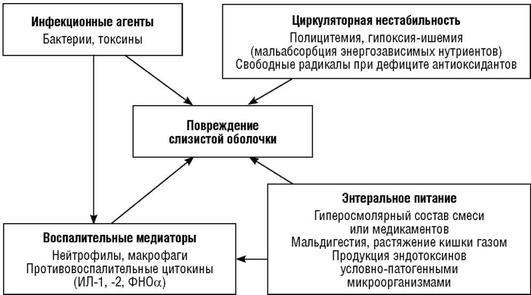
Таким образом, в генезе НЭК нельзя выделить какого-либо одного причинно-значимого фактора. Скорее, совокупность воздействия группы энтеропато-генов на фоне незрелого иммунного и функционального ответа кишечника и реализуется в конечном итоге в болезнь (схема 20.1).
Схема 20.1. Взаимодействие факторов патогенеза НЭК
Морфология. Морфологически НЭК характеризуется воспалением и коа-гуляционным некрозом. Последний является следствием ишемии и воспаления. Осмотр поврежденных резецированных участков или аутопсийных образцов обнаруживает изъязвления слизистой оболочки кишки, геморрагии, отек и наличие подслизистых или подсерозных кист, заполненных газом, - инте-стинальный пневматоз. У 50% детей в процесс вовлекаются и тонкая, и толстая кишка (чаще илеоцекальная область), у 25% - только толстая кишка, у 25% - только подвздошная. Реже наблюдается поражение тощей кишки, желудка, иногда
процесс захватывает весь кишечник - от связки Трейтца до прямой кишки, что обычно заканчивается фатально. Поражение может быть как непрерывным, так и прерывистым.
Гистологическое исследование резецированных тканей выявляет коагу-ляционный некроз в 90% случаев, выраженное воспаление - в 90%, в 15% - эозинофилы в инфильтрате, в 75% - изъязвление, в 70% - геморрагии. Пнев-матоз при гистологическом исследовании наблюдается в половине случаев. В крупных мезентериальных сосудах тромбы находят нечасто, в мелких - в 30% наблюдений.
Репаративные процессы характеризуются регенерацией эпителия, образованием грануляционной ткани и фиброзом. Последний может в дальнейшем приводить к формированию стриктур.
В общепринятой практике в зависимости от распространенности процесса выделяют локализованную форму - поражение ограничено небольшим участком киши или
желудка; мультисегментарную форму - поражено несколько участков кишки; тотальное поражение кишечника, или паннекроз.
Клиническая картина. Ранние симптомы НЭК часто неспецифичны и включают признаки общей интоксикации и слабые гастроинтестинальные проявления. Диарея нечасто бывает первым признаком НЭК. Интоксикация может проявляться апноэ, брадикардией, вялостью, нарушением терморегуляции, цианозом и «мраморностью» кожного покрова, похолоданием конечностей. При появлении интестинальных симптомов живот становится вздутым и напряженным, кишечные шумы ослабевают. Может наблюдаться рвота, по желудочному зонду отходит обильное застойное желудочное содержимое. Иногда бывает гематеме-зис, но чаще - стул с кровью (в 80%). Однако на первом этапе болезни кровь в стуле может быть скрытой.
По мере прогрессирования болезни развиваются артериальная гипотензия, шок, ДВСсиндром. Возможны асцит, перитонит, перфорация кишки. На передней брюшной стенке могут появляться красные стрии и гиперемия вокруг пупка и по ходу пупочной вены. Может быть гиперемия в правой подвздошной области с наличием пальпируемых масс там. Это проявление перфорации с формированием локального абсцесса.
Различают три стадии развития НЭК по модифицированной классификации M.J. Bell и
соавт. (табл. 20.10).
I стадия - субклиническая, при которой не обнаруживается явных диагностических, рентгенологических или ультразвуковых признаков. На этой стадии трудно дифференцировать НЭК от других гастроинтестинальных заболеваний.
II и III стадии - это несомненный документированный НЭК. Прогрессирова-ние и переход от одной стадии к другой обычно происходит в течение 24-48 ч после начала симптомов. Однажды стабилизируясь, пациент редко переходит в следующую стадию. Большинство эпизодов перфорации наблюдается у больных IIIА-В стадии. Перфорация чаще происходит через 48-72 ч у детей с IIIА стадией.
Выделение стадий болезни позволяет более точно оценить тяжесть состояния ребенка и более четко сформулировать показания к хирургическому лечению.
Таблица 20.10. Классификация НЭК у новорожденных (Bell М.J. et al., 1978; Wаlsh М.C. et al., 1986)
Стадия |
Общие |
Интестинальные |
Рентгенологическая |
|
симптомы |
симптомы |
картина |
IА (подозрение на НЭК) |
Нестабильность |
Незначительное |
Норма или |
|
температуры, |
вздутие живота, |
некоторое вздутие |
|
апноэ, брадикар- |
рвота. Скрытая |
петель кишечника |
|
дия, вялость |
кровь в стуле |
|
IБ (предполагаемый НЭК) |
То же |
То же + примесь |
То же |
|
|
ярко-красной |
|
|
|
крови в стуле |
|
IIА (определенный НЭК, легкая |
То же + |
То же + парез |
Расширение |
форма, обратимая стадия) |
незначительный |
кишечника, т. е. |
кишечных петель с |
|
метаболический |
снижение или |
множественными |
|
ацидоз и |
отсутствие |
горизонтальными |
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/

|
незначительная |
кишечных |
уровнями, пневма- |
|
|
тромбоцитопенияшумов с |
тоз кишечной |
||
|
|
реакцией на |
стенки |
|
|
|
пальпацию или |
|
|
|
|
без таковой |
|
|
IIБ (определенный НЭК, среднетя- |
То же + |
То же + |
То же с (или без) |
|
желая форма, необратимая |
метаболический |
выраженное |
газом в v. porta, с |
|
стадия) |
ацидоз и |
вздутие и |
(или без) асцитом |
|
|
тромбоцитопениянапряжение |
|
||
|
|
живота с (или |
|
|
|
|
без) |
|
|
|
|
абдоминальным |
|
|
|
|
целлюли-том |
|
|
|
|
или |
|
|
|
|
пальпируемыми |
|
|
|
|
массами в |
|
|
|
|
правом нижнем |
|
|
|
|
квадранте |
|
|
IIIА (прогрессирующий НЭК, |
То же + |
То же + |
То же + всегда газ |
|
тяжелая форма) |
смешанный |
симптомы |
в v. porta и |
|
ацидоз, |
перитонита, |
выраженный асцит |
||
|
||||
|
артериальная |
гиперемия |
|
|
|
гипотензия, |
передней |
|
|
|
брадикардия, |
брюшной |
|
|
|
повторные апноэ, стенки, |
|
||
|
нейтропения, |
кровавый стул, |
|
|
|
анурия, |
парез |
|
|
|
коагуляци-онные кишечника с |
|
||
|
нарушения |
реакцией на |
|
|
|
|
пальпацию |
|
|
|
|
живота |
|
|
IIIБ (прогрессирующий НЭК, |
То же + |
Разлитой |
То же + пневмопе- |
|
перфорация) |
декомпен- |
перитонит, |
ритонеум |
|
|
резкое вздутие |
|
||
|
сированный |
|
||
|
живота, |
|
||
|
|
|
||
|
ДВС-синдром |
кровавый стул, |
|
|
|
|
парез |
|
|
|
|
кишечника с |
|
|
|
|
реакцией на |
|
|
|
|
пальпацию |
|
|
|
|
живота |
|
|
Течение. С.А. Караваева (2002) выделила три варианта течения НЭК: молниеносное, острое и подострое.
Молниеносное течение характерно для доношенных крупных детей, перенесших в родах асфиксию, травму головного и/или спинного мозга, а также для новорожденных с гемолитической болезнью (особенно после повторных ЗПК) и для больных с пороками ЖКТ (острая форма болезни Гиршпрунга, гастро-шизис). От первых нечетких симптомов дискомфорта в состоянии ребенка, которые появляются на 3-5-й дни жизни, до возникновения перфорации проходит не более 1,5-2 сут. Своевременная диагностика этой формы заболевания может быть затруднена из-за преморбидного фона и очень тяжелого общего состояния
ребенка, что иногда затушевывает признаки надвигающейся катастрофы. Однако
появление вздутия живота, беспокойство ребенка, резкое ухудшение лабораторных данных, свидетельствующих о воспалительном процессе, должны навести на мысль о возможном развитии НЭК. Такие дети требуют срочного осмотра хирурга и рентгенологического обследования.
Острое течение НЭК характерно для недоношенных детей с массой тела при рождении менее 1500 г. Заболевание развивается на 2-4-й неделях жизни с ярко выраженных симптомов со стороны брюшной полости: срыгивания и рвота, отказ от еды, вздутие живота, нарушение пассажа по кишечнику, что соответствует стадии заболевания IА. Вскоре присоединяются общесоматические симптомы, свидетельствующие об интоксикации и дисфункции жизненно важных органов и систем. При отсутствии адекватной терапии НЭК переходит в необратимую стадию развития процесса, что требует незамедлительного хирургического вмешательства.
Подострое течение особенно характерно для пациентов с экстремально низкой массой тела. Болезнь развивается постепенно с 3-й недели жизни: ребенок перестает усваивать питание, начинает срыгивать, возникает вздутие живота, меняется характер стула - он учащается, в нем появляется примесь зелени и слизи, крови, а иногда, наоборот, он становится более редким и вообще прекращается. Симптомы со стороны ЖКТ имеют перемежающийся характер: периоды внешнего благополучия сменяются ухудшением и возвратом кишечного синдрома.
Диагностика. С самого начала заболевания необходимо частое повторное исследование ребенка (каждые 6-8 ч), которое включает пальпацию живота и лучевые исследования брюшной полости (УЗИ и по показаниям рентгенография), чтобы не пропустить ухудшение состояния и развитие осложнений. Наблюдение за ребенком осуществляют совместно неонатолог и хирург.
Абсолютными рентгенологическими признаками обратимой стадии НЭК являются:
•неравномерное вздутие кишечных петель;
•ограниченный пневматоз кишечной стенки;
•отдельные паретические уровни в кишечнике.
К абсолютным рентгенологическим признакам некроза кишки относятся:
•статичная, «стабильная» петля кишки на рентгенограммах, сделанных с интервалом 6-12 ч;
•обширный пневматоз кишечника;
•газ в воротной вене;
•асцит;
•пневмоперитонеум.
С.А. Караваева (2002) пришла к заключению, что при неясной клинической картине НЭК и анатомических особенностях, обусловленных врожденными пороками развития (атрезия пищевода и др.), как средство диагностики необходимо применять лапароцентез с целью ранней диагностики некроза кишки.
Лабораторные данные помогают в оценке состояния ребенка: тромбоци-топения в сочетании или без ДВС-синдрома, ацидоз, анемия, нейтропения с резким сдвигом влево являются тревожными признаками прогрессирующего НЭК.
Дифференциальную диагностику следует проводить с целым рядом системных и гастроинтестинальных заболеваний (табл. 20.11).
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
