
6 курс / Неонатология / Неонатология_Н_П_Шабалов_7_е_издание_Том_2_2020
.pdfпоследнюю очередь - предсердий. При повышенной нагрузке в гипертрофированной мышце количество этого изомера достигает 50% актина.
3.Уменьшением функции белков ионной помпы. По Л. Мэнони (1988), в раннем возрасте относительно снижена удельная плотность кальциевого насоса на мембране и малоэффективно сопряжение транспорта иона и гидролиза АТФ. Для неонатального сердца характерно относительно сниженное количество саркоплазматического ретикулума (органеллы, регулирующей концентрацию цитоплазматического кальция и его утилизацию) и большая зависимость цитоплазматической концентрации кальция от внеклеточной. Переход от неонатальной изоформы миозина к зрелой сопровождается утилизацией большего количества этого иона.
4.Структурными и биохимическими особенностями миокарда новорожденного, которые обусловливают, в сравнении со взрослыми, менее активное напряжение для данной длины миофибрилл на фоне сниженной скорости сокращения и повышенного остаточного натяжения при любой данной длине волокон. Все это объясняет, с одной стороны, относительно низкую сократительную способность миокарда, с другой стороны - отсутствие четкой зависимости эффективности сокращения от величины преднагрузки (диастоличе-ского наполнения сердца), т. е. ослаблено действие закона Старлинга («все или ничего»).
5.У новорожденного ребенка инотропная эффективность 1 г миокарда меньше, чем у взрослого человека, также за счет того, что относительное содержание стромы в нем существенно больше, чем сократительных элементов (70% - в первые месяцы жизни, 40% - в более старшем возрасте). По этой же причине миокард новорожденного менее податлив, чем у взрослых, и в 2 раза менее активно отвечает приростом сердечного оттока на стандартную тестовую преднагрузку.
6.Уменьшение постнагрузки на сердце ребенка существенно не влияет на сердечный отток, но в то же время ее дополнительное увеличение значительно его снижает.
7.Адаптацию сердечного оттока к повышающимся потребностям в кислороде новорожденный ребенок обеспечивает преимущественно за счет частоты сердечных сокращений (ЧСС), однако компенсаторные возможности этого пути ограничены как из-за малых запасов норадреналина в миокарде и сниженной способности симпатических рецепторов к захвату и связыванию этого медиатора, так и из-за сокращения времени диастолического наполнения сердца при тахикардии, а отсюда - снижения коронарного кровотока.
8.У новорожденных при рождении - относительно большой сердечный отток (400 и 100 мл/кг в минуту у взрослого), однако он используется почти в 2 раза менее эффективно, чем у взрослого человека: на обеспечение потребления тканями 1 мл/кг в минуту кислорода новорожденному требуется 52 мл крови, взрослому - 24 мл.
При сердечной недостаточности, помимо изменений миокарда и работы сердца, в организме происходит также ряд компенсаторных сдвигов гемодинамики и нейроэндокринной регуляции в виде повышения активности симпатической нервной системы в ответ на недогрузку барорецепторов за счет сниженного АД и СО, централизации кровообращения, активации системы ренин-ангиотензин-альдостерон, задержки воды и натрия почками, гипер-волемии. Включение этих механизмов зависит от степени и скорости снижения сердечного оттока.
При быстром (в течение минут или часов) снижении сердечного индекса (СИ) сердечный отток в расчете на 1 м2 поверхности тела (норма у новорожденных 5 л/мин на м2) - менее 2 л/мин на м2, и компенсация не помогает обеспечить адекватную системную и тканевую перфузию, развивается СН с малым сердечным выбросом, или кардиогенный шок. При постепенном нарастании СН (сутки или недели) эти механизмы успевают поддержать
сердечный отток или скомпенсировать его уменьшение так, чтобы поддержать системный кровоток. На первый план выступает относительная или абсолютная диастоличе-ская перегрузка, возникает застойная сердечная недостаточность (ЗСН).
19.4.1. Застойная сердечная недостаточность
У новорожденных в соответствии с основным патофизиологическим механизмом ее возникновения может быть обусловлена:
1)чрезмерной пред- и постнагрузкой, перегрузкой давлением или объемом, ВПС и транзиторными расстройствами кровообращения;
2)нарушением сократимости миокарда - миокардиопатии, миокардиты, метаболические расстройства (ацидоз, гипогликемия, гипокальциемия, гипокалиемия и др.), перикардиты;
3)тахи- и брадиаритмиями.
Эти причины приводят к декомпенсации в различные сроки после рождения ребенка, поэтому возраст должен быть первым признаком, который позволяет их дифференцировать. В 1-й день жизни ЗСН может быть либо следствием внутриутробного миокардита, либо недостаточности предсердно-желу-дочковых
клапанов, атрезии аорты или синдрома гипоплазии левого желудочка; к началу 2-3-х суток после рождения - постасфиксической транзиторной ишемии миокарда, кардиомиопатии у детей от матерей, страдающих диабетом, метаболических расстройств. В это же время к ЗСН приводят тяжелая анемия (уровень гемоглобина <70-100 г/л) и аритмии. К середине - концу 1-й недели жизни ЗСН осложняются транзиторные расстройства переходного кровообращения (ПФК, широкий ОАП) и транспозиции крупных сосудов, широкие артериовенозные свищи. Всего на первые 7 дней постнатального периода, по Д. Сэниэл (1988), приходится 20% всех случаев сердечной недостаточности при ВПС у детей раннего возраста. В течение 8-30 дней после рождения основной причиной ЗСН являются ВПС с нарушением выхода из левого желудочка или с перегрузкой объемом, увеличивающимся по мере возрастного снижения давления в легочной артерии. Чаще всего в этот период ЗСН сопровождает коарк-тацию и стеноз аорты, на втором месте стоит транспозиция магистральных сосудов со значительным дефектом межжелудочковой перегородки. Всего в течение 2-4-й недели жизни ЗСН составляет 18% общего числа случаев этой патологии в раннем возрасте.
При дифференциальной диагностике причин ЗСН у новорожденных следует также учитывать реакцию на гипероксидную пробу.
Если на фоне ЗСН ребенок реагирует на ингаляцию кислорода 100% концентрации (PaО2 >150 мм рт.ст.), то недостаточность кровообращения является осложнением ВПС с обогащением легочного кровотока либо кардиомиопа-тии или миокардитов. Если при
отрицательной пробе цианоз сохраняется (PаО2 <150 мм рт.ст. при FiО2 = 1,0), это значит, что причины ЗСН - легочная гипертензия или ВПС с обеднением малого круга кровообращения либо со значительным право-левым шунтированием кровотока. Причины ЗСН ниже расположены по нисходящей частоте.
Причины ЗСН у новорожденных
При отсутствии цианоза |
При наличии цианоза |
|
Коарктация аорты. Стеноз аорты. Перерыв |
Синдром гипоплазии левого желудочка. |
|
дуги аорты. |
Тотальный аномальный венозный |
|
Транзиторная ишемия миокарда. Кардио- |
легочный дренаж с обструкцией. Общий |
|
артериальный ствол. Транспозиция |
||
миопатия (диабет у матери) ОАП и |
магистральных сосудов |
|
миокардит. ДМЖП. |
||
|
||
|
|
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
Аортолегочное окно. Артериовенозный с ДМЖП, ПФК. |
|
свищ |
Атрезия трикуспидального клапана |
|
|
|
с ДМЖП. |
Единственный желудочек Патогенез. Сердечная недостаточность у новорожденных первично чаще всего
развивается как левожелудочковая. Это обусловлено двумя причинами: во-первых, левый желудочек, толщина стенки и масса которого не отличаются от таковых правого, характеризуется меньшей мышечной силой; во-вторых, процессы, приводящие к перегрузке объемом и давлением, прежде всего,
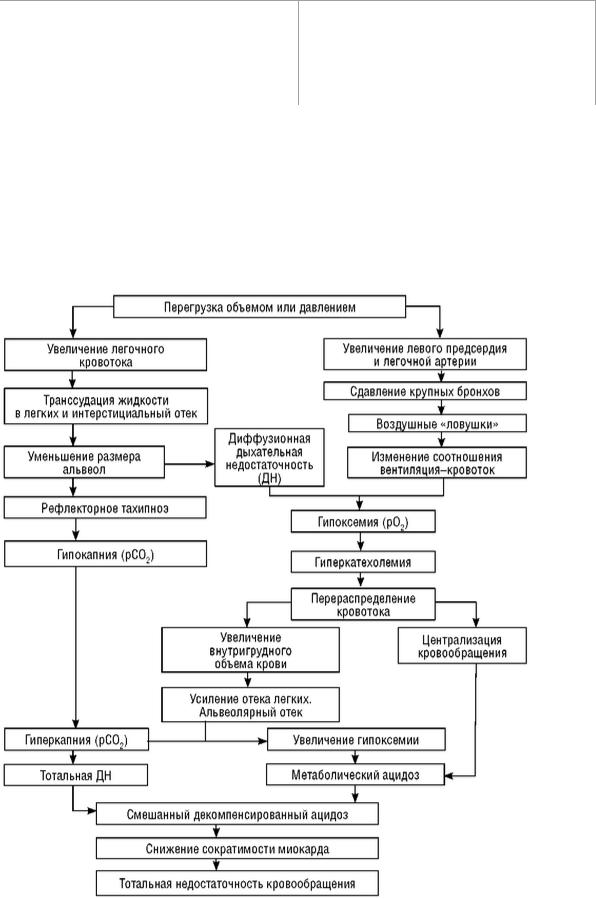
оказывают влияние на левые отделы сердца. В подобной ситуации ведущим звеном патогенеза всегда является перегрузка малого круга кровообращения, т. е. недостаточность проявляется в виде сочетанного сердечно-легочного повреждения (схема
19.3).
Схема 19.3. Патогенез сердечной недостаточности у новорожденных
Сугубо условно в развитии СН можно выделить несколько этапов. Увеличение легочного кровотока и интерстициальный отек легких на раннем этапе приводят к рефлекторному тахипноэ, гипокапнии и гипоксии. Одновременно сдав-ление крупных бронхов расширенным левым предсердием и легочной артерией нарушает соотношение вентиляция/кровоток и усугубляет гиперкатехолемию,
которая обеспечивает поддержание сердечного оттока за счет тахикардии и централизации кровообращения. Вместе с тем увеличивается внутригрудной объем крови, возникает альвеолярный отек, ранним симптомом которого может быть смена гипокапнии на гиперкапнию. В ее генез свою долю также вкладывает усталость (истощение) дыхательной мускулатуры. Централизация кровообращения вместе с гипоксией приводят к метаболическому ацидозу и последующему снижению сократимости миокарда. Наступает окончательная декомпенсация. Подобные представления о патогенезе СН объясняют закономерности развития ее клинической картины у новорожденных и намечают основные пути терапии. На первом этапе - уменьшение преднагрузки и дыхание под положительным давлением, на втором - ИВЛ, снижение постнагрузки и коррекция ацидоза, на заключительном этапе - присоединение инотропной терапии.
Симптоматика застойной сердечной недостаточности. ЗСН у новорожденных -
полиорганный синдром, который может проявляться как осложнение заболеваний сердца уже с первых суток жизни. Клиническая картина ранней стадии ЗСН несколько отличается от ее более поздних проявлений.
Самыми первыми признаками являются персистирующие тахикардия и та-хипноэ. Дыхание, частота которого обычно более 80 в минуту, первоначально не сопровождается ретракцией грудной клетки: на фоне нормальных движений диафрагмы быстро и поверхностно «дышит» передняя брюшная стенка, затем присоединяется сопение. В сочетании с частотой пульса (более 180-190 уд./мин) это должно наводить на мысль о СН. Кожа ребенка - бледная с положительным симптомом «растирания», особенно у недоношенных детей. На этом этапе чаще встречается периферический, чем центральный цианоз. Диагноз подтверждает сочетание этих симптомов с кардиомегалией, выраженным сердечным толчком, громким акцентуированным II тоном и коротким систолическим шумом на основании сердца. Обязательно сравнение давления на верхних и нижних конечностях. При отсутствии коарктации аорты диастолическое АД выше систолического только на 10 мм рт.ст.
В более позднем периоде у больного ребенка появляются затруднения с сосанием, чрезмерная прибавка массы тела, потливость головы. При относительно высокой частоте дыхания наблюдаются экспираторная одышка, ретракция грудной клетки, над легкими выслушиваются влажные хрипы. Часто наблюдается центральный цианоз, тоны сердца глухие, неблагоприятный признак - появление ритма галопа, исчезновение сердечного толчка. Развиваются гепа-томегалия (более 3 см ниже реберной дуги), олигурия (менее 0,5 мл/кг в час). Периферические отеки и асцит кардиогенного генеза у новорожденных редки, спленомегалия не характерна.
Лабораторные данные: достаточно частые и стойкие признаки - прогрессирующие метаболический ацидоз и гиперкапния. При цианотичных ВПС - рефрактерная гипоксемия с PaО2 менее 40 мм рт.ст. На рентгенограмме грудной клетки - кардиомегалия и признаки отека легких.
Появление перечисленных симптомов является показанием к электро-и эхокардиографическому обследованию, которые позволяют уточнить причину ЗСН.
По ЭКГ оценивают признаки перегрузки и гипертрофии желудочков сердца, нарушения субэндокардиального кровообращения и, при необходимости, - характер аритмии. Эхокардиограмма позволяет уточнить топику ВПС, характер и величину шунтирования кровотока.
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
19.4.2. Лечение сердечной недостаточности
Лечение сердечной недостаточности должно решать следующие задачи: улучшение производительности сердца, уменьшение постнагрузки и венозного застоя в малом и большом кругах кровообращения. Последовательность их решения зависит от тяжести СН
инепосредственной причины ее возникновения. При умеренной СН нередко достаточно снизить сердечную преднагрузку умеренным ограничением поступления воды и электролитов (до 80% от возрастных потребностей). В тех случаях, когда это не обеспечивает уменьшения перегрузки, больному назначают диуретики (табл. 19.4), которые особенно показаны при перегрузке малого круга кровообращения с клинической
ирентгенологической картиной интерстициального отека легких.
Таблица 19.4. Назначение диуретиков новорожденному при застойной сердечной недостаточности
Показания |
Препарат |
Относительная |
Пик |
Доза |
|
|
активность |
действия |
|
Экстренная |
Фуросемид |
+++ |
1-2 ч |
1-3 мг/кг |
ситуация |
|
|
|
внутривенно per os |
Длительное |
Тиазиды |
++ |
2-8 ч |
1-3 мг/кг гидро- |
лечение СН и |
|
|
|
рохлортиазида per os |
особенно |
|
|
|
|
артериальной |
|
|
|
|
гипертензии |
|
|
|
|
Для сочетания с |
К+-сберегаю-щие |
+ |
2-3 сут |
3 мг/кг в сутки |
другими |
диуретики |
|
|
(Верошпирон♠), 0,3 |
диуретиками и |
(Верошпирон♠, |
|
|
мг/кг в сутки |
сохранения К+ |
триамтерен) |
|
|
(триамтерен) per os |
при СН и |
|
|
|
|
болезнях печени |
|
|
|
|
Если перечисленные мероприятия не купируют СН и возникает необходимость наращивать активность терапии, ее усиливают в нескольких направлениях, учитывающих причины возникновения синдрома. Однако в любом случае новорожденному ограничивают физическую нагрузку с исключением акта сосания (кормление через зонд) и проводят оксигенотерапию с дыханием под положительным давлением при FiО2 не больше 0,5. Вопрос об увеличении производительности сердца традиционно решали при помощи сердечных глико-зидов. При СН у новорожденных на фоне ВПС с лево-правым шунтированием кровообращения либо при миокардитах и дилатационных кардиомиопатиях (постасфиксических, при фиброэластозе эндокарда) их применяют длительно в течение нескольких месяцев и даже лет. Однако по мере разработки представления о диастолической сердечной недостаточности, особенно при гипертрофических кардиомиопатиях (диабетическая и при болезни Помпе), основу терапии стали составлять средства, способствующие диастолическому наполнению сердца (β-адренолитики, препараты, ингибирующие ангиотензин, конвертирующие энзимы). Этот же механизм, по-видимому, является основой
положительного эффекта других сосудорасширяющих препаратов, улучшающих постнагрузку.
Для инотропной поддержки при СН, не сопровождающейся СМСВ, у новорожденных используют дигоксин, насыщение которым осуществляют, как правило, внутривенно, а при поддерживающей терапии при улучшении состояния ребенка препарат чаще всего назначают per os. С учетом биодоступности дигоксина соотношение между оральной и внутривенной дозами составляет 1:0,6. Методика дигитализации в неонатальном периоде такая же, как в более старшем возрасте. Период насыщения препаратом в течение 24-36 ч:
1/2+1/4+1/4 дозы насыщения с интервалом в 8-12 ч и последующим периодом поддержания терапевтической концентрации препарата в крови (1/8 дозы насыщения каждые 12 ч). Внутривенная доза насыщения для новорожденных колеблется от 0,03 до 0,04 мг/кг (30-40 мкг/кг). Необходимая концентрация препарата в плазме достигается через 60-180 мин. Терапевтический уровень дигоксина у новорожденных при сопоставимых дозах в 1,5-2 раза выше и составляет 1,1-2,2 нг/мл. Токсический уровень - более 3,5 нг/мл. Другими словами, чем младше ребенок, тем быстрее проявляются токсические эффекты дигоксина. К их возникновению предрасполагают гипоксия, ацидоз, гипока-лиемия. У детей малого гестационного возраста важно учитывать возможность усиления токсичности при сочетанном применении дигоксина и индометаци-на. Доза первого в подобных случаях должна быть уменьшена на 50%.
При интоксикации дигоксином состояние ребенка ухудшается, он отказывается от еды, появляются срыгивания, рвота. Одним из ранних объективных критериев интоксикации сердечными гликозидами у новорожденных являются ЭКГ-признаки: удлинение интервала P-Q, дугообразное изменение S-T, желудочковые аритмии. Начальные признаки интоксикации лечат унитиолом, поздние - антиаритмическими дозами лидокаина и Дифенина♠ (фенитоина) и применением антидигоксиновых антител.
При соблюдении режима дигитализации, своевременной ликвидации сопутствующих метаболических расстройств и профилактике токсичности препарата инотропная поддержка дигоксином при СН может быть продолжительной и удлиняет жизнь ребенка. В тех случаях, когда СН оказывается рефрактерной к сердечным гликозидам либо при гипертрофических кардио-миопатиях основой терапии является сочетание диуретиков с ингибиторами ангиотензинконвертирующих ферментов (каптоприл, Капотен♠) или с β-ад- реноблокаторами (Обзидан♠, пропренол). Дозы каптоприла для новорожденных (0,1-0,4 мг/кг каждые 6-24 ч) подбирают таким образом, чтобы у ребенка не возникала артериальная гипотензия и увеличивался диурез. Необходимо помнить, что из-за опасности гиперкалиемии каптоприл не сочетают с калий-сберегающими диуретиками. Доза Обзидана♠ 1-3 мг/кг в сутки per os. Контролируют эффект препарата по динамике частоты сердечных сокращений и уровню АД (опасны брадикардия и артериальная гипотензия). В отличие от детей грудного возраста с тяжелыми формами ВПС типа тетрады Фалло, у новорожденных β-блокаторы не купируют одышечно-цианотические приступы,
так как в раннем постнатальном периоде они имеют не миогенный, а клапанный генез.
Как и при лечении любого патологического состояния у новорожденных, фармакологическая терапия СН может быть успешна только в том случае, если ее
сочетать с адекватной возрасту поддерживающей терапией.
19.5. ШОК
В отечественной литературе долгое время бытовало мнение, что в связи с особенностями нейроэндокринной регуляции и болевой рецепции новорожденный не способен давать шокоподобные реакции. Мнение изменилось, когда наши исследователи, подобно зарубежным, начали рассматривать шок как прогрессирующую острую недостаточность тканевого кровообращения. Однако до настоящего момента истинная частота возникновения этого патологического синдрома в период новорожденности остается неизвестной. Этиопатогенетически у новорожденных могут возникать три вида шока.
1.Кардиогенный, обусловленный некомпенсированным синдромом малого сердечного выброса (см. ниже).
2.Гиповолемический геморрагический (чаще при родовой травме паренхиматозных внутренних органов и сосудов, реже - при антеили интранатальной фетоматеринской, фетоплацентарной или фето-фетальных трансфузиях) и ан-гидремический (при потерях
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
воды и электролитов при рвоте или диарее при заболеваниях желудочно-кишечного тракта или при перегреве).
3. Септический, связанный с инфицированием ребенка во время его прохождения через родовые пути матери (чаще стрептококком группы В) или в раннем постнатальном периоде (чаще условно-патогенной грамотрицательной бактериальной микрофлорой).
Причины синдрома малого сердечного выброса (кардиогенного шока) у новорожденных
Неэффективная сократимость миокарда:
•транзиторная ишемия миокарда при асфиксии;
•гипогликемия, гипокальциемия, ацидоз;
•миокардит.
Неэффективная диастола:
•гипертрофическая кардиомиопатия у детей от матерей, страдающих диабетом;
•тахиаритмия.
Нарушения переходного кровообращения ОАП и ПФК:
•ВПС;
•синдром малого левого желудочка; • ТБС;
•коарктация или стеноз аорты;
•общий артериальный ствол.
Механическое препятствие сердечной функции или венозному возврату:
•напряженный пневмоторакс;
•интерстициальная эмфизема и пневмомедиастинум;
•диафрагмальная грыжа;
•тампонада сердца (пневмо- и гидроперикард).
Патогенез. Острая прогрессирующая недостаточность периферического кровообращения первоначально возникает вследствие спазма сосудов микроциркуляции или централизации кровообращения. Последняя может быть либо компенсаторной и вторичной (при кардиогенном и гиповолемическом шоке), либо первичной патологической, обусловленной воздействием бактериального эндотоксина. Если централизация кровообращения вовремя не ликвидирована, тканевая гипоксия прогрессирует, усиливает метаболический ацидоз, в сочетании с тканевыми вазоактивными веществами (кинины, простагландины и др.) приводит к нарушению проницаемости капиллярной стенки, внутрисо-судистому свертыванию крови, ее секвестрации и гиповолемии. Возникает децентрализация кровообращения, системная артериальная гипотензия, что еще больше усиливает гипоксию. Замыкается порочный круг.
В клинической картине шока у недоношенных детей на первый план выступает синдром угнетения ЦНС с мышечной гипотонией, гипорефлексией. Нарушения гемодинамики никогда не превалируют, симптоматики централизации кровообращения нет. Прогрессирует гиповентиляционная дыхательная недостаточность с частыми длительными апноэ (более 15-20 с). Недостаточность периферического кровообращения проявляется в том, что ребенок перестает самостоятельно поддерживать постоянство
температуры тела, развиваются гипотермия, склерема. Кожа бледная или бледноцианотичная, несмотря на то, что максимальное артериальное давление длительно сохраняется на нижней границе возрастной нормы (в пределах 30 мм рт.ст.). У больного отсутствует диурез. В смешанной капиллярной крови рО2 на фоне оксигенотерапии с FiО2 0,6-0,8 не превышает 30 мм рт.ст. Исследование КОС, даже на фоне ИВЛ, выявляет стойкий декомпенсированный метаболический ацидоз, не поддающийся коррекции внутривенным введением растворов натрия гидрокарбоната. Подобное состояние «анабиоза» может сохраняться достаточно долго (в течение нескольких часов или суток) и в большинстве случаев завершается постепенным угасанием витальных функций.
У доношенных новорожденных, несмотря на то что централизация кровообращения при шоке также выражена слабо, тем не менее, шок как синдром проявляется более отчетливо (Хишфильд С.С., 1987). Недостаточность периферического кровотока проявляется бледной или серо-землистой окраской кожи, продолжительной олигурией и метаболическим ацидозом, степень которого не всегда объяснима клинической ситуацией, так же как у недоношенных новорожденных. Вместе с тем у детей, родившихся на поздних сроках гестации, в симптоматике шока чаще всего превалирует шунтодиффузная дыхательная недостаточность. На ранних стадиях она обусловлена легочной гипертензией с синдромом дыхательных расстройств и последующим интерсти-циальным отеком легких. На поздних стадиях по мере прогрессирования артериальной гипотензии ведущей причиной дыхательной недостаточности становится
синдром персистирующего фетального кровообращения с 5070% шунтированием кровотока справа налево через овальное окно и, в меньшей степени, через артериальный проток.
При септическом шоке быстро возникает ДВС. Летальный исход наступает в пределах суток.
Противошоковую терапию начинают с решения следующих вопросов:
1)нужна ли больному инфузионная терапия и каковы должны быть ее объем и состав?
2)подбор фармакологических средств для инотропной поддержки (табл. 19.5) и вазоактивной терапии;
3)определение характера необходимого респираторного обеспечения;
4)выбор дополнительных лечебных мероприятий с учетом этиологии шока. Для оценки необходимости инфузионной терапии следует провести тест
с разовой объемной нагрузкой и клинико-лабораторный контроль. В подавляющем большинстве случаев для тест-нагрузки выбирают кристаллоиды (изотонический раствор натрия хлорида) в дозе 10-20 мл/кг в течение 10-20 мин. Контроль включает измерение центрального венозного давления, АД, диуреза, температуры конечностей, определение количества эритроцитов, концентрации гемоглобина и гематокрита, электролитов плазмы и КОС крови. Если эти параметры улучшились, то весьма вероятно, что у больного гиповолемия, и инфузию следует продолжить. Дальнейший состав диктуют проведенные лабораторные исследования. При острой анемии с гематокритом менее 35 об.% ребенку необходима трансфузия эритроцитной взвеси в дозе 12-15 мл/кг, при гипонатриемии продолжают введение глюкозосолевой смеси (10% раствор Глюкозы♠ и 0,85% раствор натрия хлорида - 3:1) дополнительно 30 мл/кг. При декомпенсированном ацидозе и pH крови <7,2 снижено сосудоактивное влияние всех симпатомиметиков и катехоламинов. В подавляющем большинстве случаев препаратом выбора для первоначального поддержания гемодинамики является допамин. Его инфузия, так же как и Адреналина♠, проводится только в центральные (пупочная, подключичная) вены. Дозу подбирают методом титрования, т. е. начинают с 5-8 мкг/кг в минуту и корригируют так, чтобы
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/

добиться клинических и лабораторных признаков адекватности кровообращения (нормализация АД, температуры тела, диуреза, pH крови и рО2). Если эффекта не удается добиться путем повышения дозы допамина более 10 мкг/кг в минуту, то дополнительно начинают инфузию добутамина (5-10 мкг/кг в минуту) и при необходимости Адреналина♠ (0,05-1,0 мкг/кг в минуту). Если эта терапия стабилизирует систолическое АД на уровне более 60 мм рт.ст., но сохраняются олигурия и другие признаки централизации кровообращения, то в терапию включают сосудорасширяющие средства. Подобную комплексную терапию шока продолжают несколько суток и при улучшении состояния ребенка активность лечения снижают в последовательности, противоположной той, которая была при ее наращивании.
Перечисленные лечебно-тактические мероприятия всегда проводятся при гиповолемическом шоке. При септическом шоке в лечение дополнительно
Таблица 19.5. Инотропные и сосудоактивные препараты немедленного действия
Препарат |
Доза, |
Механизм действия и |
Особенности у |
Осложнения и |
|
мкг/кг |
эффекты |
новорожденных |
побочные эффекты |
|
в |
|
|
|
|
минуту |
|
|
|
Допамин |
1-4 |
Предшественник |
1. При перинатальных |
1. Суправентрикуляр- |
|
|
норадреналина. |
патологических |
ные тахикардии. |
|
|
Допаминергический |
состояниях и сепсисе |
2. Расстройства |
|
|
эффект, селективная |
из-за эндогенных |
|
|
|
периферического |
||
|
|
вазодилатация сосудов |
катехоламинов эффект |
|
|
|
кровообращения при |
||
|
|
почек и подкожной |
может проявляться |
|
|
|
гиповолемиях. |
||
|
|
клетчатки, мышц. |
только при дозе >10 |
|
|
|
|
||
|
|
Диуретический эффект |
мкг/кг в минуту. |
3. Гангрена |
|
|
β1-адренергический: |
2. α-Эффект созревает |
конечностей и некроз |
|
|
инотропный (слабый), |
сосудов, поэтому |
|
|
|
онтогенетически раньше |
||
|
|
уменьшение |
||
|
|
β-эф-фекта и |
инфузия только в |
|
|
|
системного сосудистого |
центральные вены |
|
|
|
сопротивления, |
проявляется при более |
|
|
|
низких дозах. |
|
|
|
|
увеличение сердечного |
|
|
|
|
|
|
|
|
|
оттока |
3. Большие дозы не |
|
|
10 и |
α-Адренергический |
изменяют легочного |
|
|
более |
спазм периферических |
сосудистого |
|
|
|
сосудов, повышение |
сопротивления, малые |
|
|
|
АД, сохранение слабого |
дозы могут нарушать |
|
|
|
β1-эффекта |
соотношение |
|
|
|
|
вентиляции и кровотока. |
|
|
|
|
4. Клиренс в 1,5 раза |
|
|
|
|
меньше, чем |
|
|
|
|
у взрослых |
|
Добута- |
2-10 |
Синтетический β1- |
1. Относительно низкая |
Доза >10 мкг/кг в |
мин |
|
адренергиче-ский - |
эффективность у |
минуту вызывает |
|
|
инотропный, |
новорожденных, так как |
тахикардию |
|
|
умеренный, |
обладает |
|
|
|
положительный, |
хронотроптроп-ным |
|
|
|
хронотроп-ный. При |
эффектом. |
|
|
|
больших дозах не |
|
|
|
|
увеличивает |
|
|
|
|
потребление кислорода |
2. После 3 сут |
|
|
|
миокардом |
применения возникает |
|
|
|
|
толерантность |
|
Адреналин♠ |
0,05- |
β1>β2 - инотроп-ный, |
1. Показан при |
Тахикардия, аритмии |
|
0,1 |
хронотропный |
артериальных гипотен- |
|
|
0,2-1,0 |
α>β - |
зиях, рефрактерных к 10 |
|
|
|
сосудосуживающий и |
мкг/кг |
|
|
|
инотроп-ный. |
в минуту допамина. |
|
|
|
Повышает потребление |
|
|
|
|
|
|
|
|
|
кислорода миокардом |
2. Усиливает эффект |
|
|
|
|
при сочетании с |
|
|
|
|
сосудорасширяющими |
|
|
|
|
препаратами. |
|
|
|
|
3. Быстрее всасывается |
|
|
|
|
при эндотрахе-альном |
|
|
|
|
введении |
|
Окончание табл. 19.5
Препарат |
Доза, |
Механизм действия и |
Особенности у |
Осложнения и |
|
|
мкг/кг |
эффекты |
новорожденный |
побочные |
|
|
в |
|
|
эффекты |
|
|
минуту |
|
|
|
|
Изадрин |
0,05- |
β1>β2, в низких дозах |
1. Снижает |
1. Повреждения |
|
(Изуп- |
0,5 |
преобладает |
легочную |
миокарда. |
|
|
положительный хроно- |
гипертензию |
|
|
|
|
|
2. Тахифилаксия |
|
||
рел♠, |
|
тропный эффект, |
|
|
|
|
на 25-115%. |
|
|
||
|
|
снижает системное |
|
|
|
Изопро- |
|
|
|
|
|
|
сосудистое |
2. Полезен при |
|
|
|
|
|
|
|
||
теренол♠) |
|
сопротивление, |
паренхиматозных |
|
|
|
|
повышает сердечный |
поражениях |
|
|
|
|
отток, бронходилататор |
легких |
|
|
Натрия нитро- |
0,5-8,0 |
Артериальное |
1. Может |
Переходит в |
|
пруссид |
|
сосудорасширяющее |
повышать |
тиоциа-нат и |
|
|
|
средство инотропно-го |
легочную гипер- |
цианиды |
|
|
|
действия |
тензию и |
|
|
|
|
|
усугублять ПФК |
|
|
|
|
|
(в эксперименте). |
|
|
|
|
|
2. В клинической |
|
|
|
|
|
картине давал |
|
|
|
|
|
положительный |
|
|
|
|
|
эффект при ПФК |
|
|
Нитроглицерин |
<2 |
Расширяющий вены |
|
|
|
|
3-5 |
Расширяющий артерии |
|
|
|
гемосорбция). При кардиогенном шоке целесообразно избегать инфузии Адреналина♠, а |
|||||
препаратом первого назначения может быть добутамин. После стабилизации |
|||||
гемодинамики дальнейшее инотропное воздействие осуществляют при помощи |
|||||
дигоксина. Насыщение им начинают на фоне постепенной отмены инотропных веществ немедленного действия.
19.6. ТРАНЗИТОРНЫЕ НАРУШЕНИЯ ПЕРЕХОДНОГО КРОВООБРАЩЕНИЯ
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
