
5 курс / Госпитальная педиатрия / 3 том Респираторная медицина
.pdf
Раздел 19
кприменению неинвазивной методики. Обычно больной находится в сознании и не нуждается в применении седативных и тем более миорелаксирующих препаратов. Масочная вентиляция является для пациента субъективно более комфортной процедурой, чем инвазивный вариант ИВЛ. Еще одно важное достоинство нИВЛ — возможность быстрого прекращения вентиляции при улучшении состояния пациента, а также немедленное ее возобновление, если в этом вновь появится необходимость.
При решении вопроса о переводе на нИВЛ пациента с ХОБЛ (при развитии синдрома ОДН на фоне выраженного обострения заболевания) в первую очередь ориентируются на клинические критерии оценки тяжести состояния. Показаниями
кначалу нИВЛ у данной категории пациентов можно считать: частоту дыхания более 24 в 1 мин, участие вспомогательной дыхательной мускулатуры, появление парадоксального дыхания.
При осуществлении нИВЛ основной целью является купирование выраженной гипоксемии, снижение работы дыхания, отдых диафрагмы, улучшение условий для газообмена в легких.
Наиболее подходящие режимы нИВЛ для пациентов с обострением ХОБЛ — CPAP и режим с двумя уровнями положительного давления. Примерные начальные параметры нИВЛ таковы.
При применении CPAP:
•уровень CPAP = 12–14 см вод.ст.;
•FiO2 — достаточное для поддержания SaO2 на уровне выше 90%.
При применении режима с двумя уровнями положительного давления:
•Phigh = 14–16 см вод.ст.;
•Plow = 4–6 см вод.ст.;
•FiO2 — достаточное для поддержания SaO2 на уровне выше 90%.
Следует иметь в виду, что проведение нИВЛ требует повышенного внимания со стороны медицинского персонала.
В случае перевода больного на инвазивную вентиляцию можно рекомендовать следующее. Режим ИВЛ — вентиляция, контролируемая по объему, с включенным тригером вдоха по давлению (2–3 см вод.ст.):
•дыхательный объем = 8–10 мл/кг идеальной массы тела;
•f = 10–12 в мин;
•отношение длительности вдоха и выдоха =
1:2,5–1:3,5;
•PEEP = 4–5 см вод.ст.;
•FiO2 — достаточное для поддержания SaO2 ≥90%;
•триггер вдоха (по давлению) = 2–3 см вод.ст.;
•пиковый инспираторный поток = 50–70 л/мин;
•ограничение по максимальному давлению в дыхательных путях — до 45 см вод.ст.
По мере улучшения состояния больного выраженность респираторной поддержки постепенно
снижают с переходом к полной, а в дальнейшем к частичной вспомогательной вентиляции.
Контроль пациентов, находящихся на искусственной вентиляции легких
Пациенты, находящиеся на ИВЛ, требуют к себе постоянного пристального внимания. Основанием для этого служит риск отказа в работе аппарата ИВЛ, разъединения элементов дыхательного контура, дислокации ЭТ, случаи самоэкстубации неадекватными больными, возникновения необходимости в срочной санации трахеобронхиального дерева, и т.д.
Недопустимо даже на непродолжительный отрезок времени оставлять пациента на ИВЛ без наблюдения медицинским работником!
Контроль за состоянием пациента должен включать внешний осмотр, использование аускультации и перкуссии грудной клетки, инструментальные методы контроля эффективности проводимой ИВЛ.
Внешний осмотр пациента позволяет оценить уровень сознания, степень двигательной активности, цвет и влажность кожных покровов, выраженность экскурсий грудной клетки, наличие
иэффективность попыток спонтанного дыхания. Цвет и влажность кожных покровов дают воз-
можность ориентировочной оценки адекватности выбора режима и параметров ИВЛ. Появление или прогрессирование цианоза, гипергидроза требует незамедлительной аускультации грудной клетки (исключение: дислокации ЭТ, развитие пневмоторакса), контроля герметичности дыхательного контура, проверки проходимости дыхательных путей (накопление мокроты), оценки необходимости в коррекции параметров проводимой респираторной поддержки.
При осмотре грудной клетки оценивается достаточность и равномерность дыхательных экскурсий. При гладком течении ИВЛ грудная клетка заметно расширяется в момент вдоха и спадается при выдохе. При отставании или отсутствии движений в правой или левой половине грудной клетки в первую очередь следует исключить дислокацию ЭТ. Другой, более редкой, причиной данного феномена может служить пневмоторакс или обтурация одного из главных бронхов инородным телом, мокротой. Осмотр в этих случаях следует дополнить аускультацией и перкуссией.
При однолегочной ИВЛ, обусловленной дислокацией ЭТ, требуется распустить герметизирующую манжету и подтянуть трубку кнаружи на 2–3 см. Как только звучность дыхательных шумов при аускультации в правой и левой подключичных областях выровняется, необходимо вновь раздуть манжету, а ЭТ надежно зафиксировать.
390

Дыхательная недостаточность
Инструментальный контроль в доступном объеме (SpO2, концентрации углекислого газа в выдыхаемом воздухе в конце выдоха, мониторирование ЭКГ, частоты пульса, АД) в процессе ИВЛ должен осуществляться у всех пациентов.
Прекращение искусственной вентиляции легких
Прекращение ИВЛ и перевод больного на спонтанную вентиляцию не всегда сопровождаются одновременным извлечением ЭТ (экстубация). Иногда требуется время для оценки эффективности спонтанной вентиляции и возможности экстубации. Что касается таких обязательных условий извлечения ЭТ как самостоятельное дыхание, стабильная гемодинамика, адекватное сознание, удовлетворительный мышечный тонус, то они понятны, не требуют дополнительного обсуждения и являются достаточными для того, чтобы экстубировать больного. Если в этом случае перед экстубацией измерить некоторые показатели спонтанной вентиляции и легочного газообмена, то они окажутся, скорее всего, такими:
•усилие вдоха <–20 см вод.ст.;
•дыхательный объем >5 мл/кг;
•ЖЕЛ >10 мл/кг;
•минутный объем вентиляции <10 л/мин;
•способность в 2 раза увеличить минутный объем вентиляции;
•Vd/дыхательный объем <0,60;
•альвеолярно-артериальная разница О2 (FiО2=1) <300–350 мм рт.ст.;
•paО2/FiО2 >200.
Если показатели спонтанной вентиляции и легочного газообмена соответствуют критериям, приведенным выше, то пациента можно экстубировать. Если существует сомнение в целесообразности извлечения ЭТ, то, скорее всего, через 15–30 мин самостоятельной вентиляции окажется, что:
•частота дыхания увеличилась на 10 и более дыханий в 1 мин;
•пульс участился на 10 и более ударов в 1 мин;
•изменилось АД в сторону увеличения или снижения;
•pаО2 оказалось меньше 60 мм рт.ст.;
•pаСО2 возросло на 10 мм рт.ст.;
•рН уменьшилось на 0,10.
В этом случае экстубация больного невозможна. Если у вас есть сомнения в возможности эффективной самостоятельной вентиляции пациента после экстубации, то безопаснее будет не спешить с извлечением ЭТ.
Обычно процедура отлучения (weaning) от респиратора связывается с переводом больного на самостоятельную вентиляцию с последующей экстубацией после длительного периода ИВЛ. Не
будет ошибкой заметить, что именно на этом, завершающем, этапе длительной ИВЛ нередко приходится испытывать наибольшие затруднения. Применяется различная тактика при отлучении больного от аппарата ИВЛ. Например, применение Т-образного адаптера. Если у вас не оказалось в наличии Т-образного адаптера, его можно изготовить у постели больного из 20-миллилитрового пластикового (одноразового) шприца. Вынимаем поршень, на боковой стенке цилиндра шприца, приблизительно посередине, вырезаем отверстие диаметром чуть больше широкой части коннектора ЭТ. Носик шприца и источник кислорода соединяем трубкой соответствующего диаметра. Т-образный адаптер через прорезанное боковое отверстие соединяется с ЭТ. Во время сеанса отключения от аппарата ИВЛ пациент дышит самостоятельно обогащенной кислородом и увлажненной дыхательной смесью через Т-образный адаптер; фракция кислорода
вдыхательной смеси должна быть увеличена на 10% по сравнению с используемой при ИВЛ; поток газа через Т-образный адаптер должен быть
в2 раза выше минутного объема вентиляции. При каждом последующем сеансе отключения время самостоятельного дыхания увеличивается. Т-образный адаптер также предупреждает на-
копление СО2 во вдыхаемой смеси (повторное вдыхание СО2). На протяжении сеанса отключения от аппарата ИВЛ требуется внимательное наблюдение за состоянием пациента, так как вначале они могут испытывать чувство дыхательного дискомфорта. В то же время, появление значительной одышки, снижение дыхательного объема являются достаточными основаниями для возобновления ИВЛ.
Продолжительность первого сеанса отключения от аппарата ИВЛ обычно ограничивается 15–30 мин. В это время необходимо регистрировать и оценивать субъективные ощущения больного, частоту пульса, дыхания, показатели АД. Удовлетворительные показатели свидетельствуют об успешности начала процедуры отлучения от респиратора. В дальнейшем продолжительность сеансов отключения и самостоятельного дыхания удлиняется. Жесткого протокола, регламентирующего частоту сеансов отключения и их продолжительность, нет. Для каждого случая протокол отлучения от аппарата ИВЛ с помощью Т-образного адаптера определяется индивидуальными характеристиками и состоянием больного.
ИВЛ при правильном ее применении позволяет спасти жизнь больного или, во всяком случае, дать такой шанс. Являясь мощным лечебным фактором, ИВЛ не прощает пренебрежительного, бездумного отношения к себе, превращаясь в этом случае в свою противоположность — изощренное орудие убийства.
391

Раздел 19
Таблица 19.15. Размеры воздуховодов
Категория больного |
Размер ISO |
|
Длина, мм |
Воздуховод Гведела |
Воздуховод Бермана |
|||||
|
|
|
|
|
|
|
|
|
|
|
Новорожденный |
4 |
|
40 |
Розовый |
|
Розовый |
|
|||
|
|
|
|
|
|
|
|
|
|
|
Младенец |
5 |
|
50 |
Голубой |
|
Бирюзовый |
|
|||
|
|
|
|
|
|
|
|
|
|
|
Маленький ребенок |
6 |
|
60 |
Черный |
|
Черный |
|
|||
|
|
|
|
|
|
|
|
|
|
|
Ребенок |
7 |
|
70 |
Белый |
|
Белый |
|
|||
|
|
|
|
|
|
|
|
|
|
|
Маленький взрослый |
8 |
|
80 |
Зеленый |
|
Зеленый |
|
|||
|
|
|
|
|
|
|
|
|
|
|
Средний взрослый |
9 |
|
90 |
Желтый |
|
Желтый |
|
|||
|
|
|
|
|
|
|
|
|
|
|
Взрослый |
10 |
|
100 |
Красный |
|
Фиолетовый |
|
|||
|
|
|
|
|
|
|
|
|
|
|
Крупный взрослый |
11 |
|
110 |
Оранжевый |
|
Оранжевый |
|
|||
|
|
|
|
|
|
|
|
|
|
|
Таблица 19.16. Клинки ларингоскопов |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||
Категория больного |
|
|
Miller |
Wisconsin |
Macintosh |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
размер |
|
длина, мм |
размер |
|
длина, мм |
размер |
|
длина, мм |
|
|
|
|
|
|
|
|
|
|
|
Недоношенный младенец |
|
0 |
|
75 |
0 |
|
75 |
– |
|
– |
|
|
|
|
|
|
|
|
|
|
|
Младенец |
|
1 |
|
102 |
1 |
|
102 |
1 |
|
91 |
|
|
|
|
|
|
|
|
|
|
|
Ребенок |
|
2 |
|
150 |
2 |
|
135 |
2 |
|
100 |
|
|
|
|
|
|
|
|
|
|
|
Взрослый |
|
3 |
|
190 |
3 |
|
162 |
3 |
|
130 |
|
|
|
|
|
|
|
|
|
|
|
Крупный взрослый |
|
– |
|
– |
4 |
|
199 |
4 |
|
190 |
|
|
|
|
|
|
|
|
|
|
|
Таблица 19.17. Подбор трубки при оротрахеальной интубации
Категория |
Внутренний |
Длина, см |
больного |
диаметр, мм |
|
|
|
|
Доношенный |
3,5 |
12 |
новорожденный |
|
|
|
|
|
Ребенок |
4+возраст |
14+возраст |
|
(годы)/4 |
(годы)/2 |
|
|
|
Взрослые: |
|
|
женщины |
7,0–7,5 |
24 |
мужчины |
7,5–8,0 |
24 |
|
|
|
Таблица 19.18. Выбор ларингеальной маски
Размер |
Категория |
Масса |
Объем |
маски |
больного |
больного, |
манжетки, |
|
|
кг |
мл |
1 |
Грудной |
<6,5 |
2–4 |
2 |
ребенок |
6,5–20 |
До 10 |
Ребенок |
|||
2,5 |
Ребенок |
20–30 |
До 15 |
3 |
Взрослый |
30–70 |
До 20 |
4 |
Взрослый |
>70 |
До 30 |
|
|
|
|
Таблица 19.19. Руководство по выбору эндотрахеальных трубок
|
Категория |
French |
Внутренний |
Длина (интубация |
Длина (интубация |
Санационный |
|
больного |
|
диаметр, мм |
через рот), см |
через нос), см |
катетер (French) |
|
|
|
|
|
|
|
<1000 г |
12 |
2,5 |
8 |
11 |
6 |
|
|
|
|
|
|
|
|
≥1000 г |
14 |
3,0 |
9 |
12 |
6 |
|
|
|
|
|
|
|
|
6 |
мес |
16 |
3,5 |
10 |
14 |
8 |
|
|
|
|
|
|
|
1 |
год |
18–20 |
4,0–4,5 |
12 |
16 |
8 |
|
|
|
|
|
|
|
2 |
года |
22–24 |
5,0–5,5 |
14 |
17 |
8 |
|
|
|
|
|
|
|
2–4 года |
24–26 |
5,5–6,0 |
15 |
18 |
10 |
|
|
|
|
|
|
|
|
4–7 лет |
26–28 |
6,0–6,5 |
16 |
19 |
10 |
|
|
|
|
|
|
|
|
7–10 лет |
28–30 |
6,5–7,0 |
17 |
21 |
10 |
|
|
|
|
|
|
|
|
10–12 лет |
30–32 |
7,0–7,5 |
20 |
23 |
10 |
|
|
|
|
|
|
|
|
12–16 лет |
32–34 |
7,5–8,0 |
21 |
24 |
12 |
|
|
|
|
|
|
|
|
Взрослая женщина |
34–36 |
8,0–8,5 |
22 |
25 |
12 |
|
|
|
|
|
|
|
|
Взрослый мужчина |
36–38 |
8,5–9,0 |
22 |
25 |
14 |
|
|
|
|
|
|
|
|
Примечание: размер подходящей эндотрахеальной трубки может варьировать в зависимости от размера и роста. На случай индивидуальных особенностей пациента необходимо иметь в запасе трубку на размер больше и на размер меньше.
392

Дыхательная недостаточность
Таблица 19.20. Примерные эквиваленты разных методов калибровки эндотрахеальных трубок
|
|
Диаметр |
|
Размер |
||
|
|
|
|
|
коннектора, |
|
внутренний, мм |
внешний, мм |
шкала Magill |
шкала French |
эквивалент манжет, дюймы |
||
мм |
||||||
|
|
|
|
|
||
|
|
|
|
|
|
|
2,5 |
4,0 |
|
12 |
|
3 |
|
|
|
|
|
|
|
|
3,0 |
4,5 |
0–0 |
12–14 |
|
|
|
|
|
|
|
|
|
|
3,5 |
5,0 |
0–0 |
14–16 |
3/16 |
4 |
|
|
|
|
|
|
|
|
4,0 |
5,5 |
0–1 |
16–18 |
3/16 |
|
|
|
|
|
|
|
|
|
4,5 |
6,0 |
1–2 |
18–20 |
1/4 |
5 |
|
|
|
|
|
|
|
|
5,0 |
6,5 |
1–2 |
20–22 |
1/4 |
|
|
|
|
|
|
|
|
|
5,5 |
7,0 |
3–4 |
22 |
1/4 |
6 |
|
|
|
|
|
|
|
|
6,0 |
8,0 |
3–4 |
24 |
1/4 |
|
|
|
|
|
|
|
|
|
6,5 |
8,5 |
4–5 |
26 |
1/4 |
7 |
|
|
|
|
|
|
|
|
7,0 |
9,0 |
5–6 |
28 |
5/16 |
|
|
|
|
|
|
|
|
|
7,5 |
9,5 |
6–7 |
30 |
5/16 |
8 |
|
|
|
|
|
|
|
|
8,0 |
10,0 |
7–8 |
32 |
5/16 |
9 |
|
|
|
|
|
|
|
|
8,5 |
11,5 |
8 |
34 |
3/8 |
|
|
|
|
|
|
|
|
|
9,0 |
12,0 |
9–10 |
36 |
3/8 |
10 |
|
|
|
|
|
|
|
|
9,5 |
12,5 |
9–10 |
38 |
3/8 |
11 |
|
|
|
|
|
|
|
|
10,0 |
13,0 |
10–11 |
40 |
7/16 |
12 |
|
|
|
|
|
|
|
|
10,5 |
13,5 |
10–11 |
42 |
7/16 |
|
|
|
|
|
|
|
|
|
11,0 |
14,5 |
11–12 |
42–44 |
1/2 |
13 |
|
|
|
|
|
|
|
|
11,5 |
15,0 |
11–12 |
44–46 |
1/2 |
|
|
|
|
|
|
|
|
|
Примечание: так как толщина трубок у разных производителей различна, эти значения отражают лишь основной принцип.
Таблица 19.21. Сравнение использования ларингеальной маски с лицевой маской и эндотрахеальной трубкой
По |
Преимущества |
|
Недостатки |
сравнению |
|
|
|
|
|
|
|
С лицевой |
Руки врача свободны. |
Выше риск травмы дыхательных путей из-за инвазивно- |
|
маской |
Легче поддерживать проходимость дыха- |
сти метода. |
|
|
тельных путей. |
Требуется введение гипнотических средств. |
|
|
Лучшая герметизация дыхательных путей |
Необходима подвижность в височно-нижнечелюстном |
|
|
и защита от аспирации глоточного секре- |
суставе |
|
|
та. |
|
|
|
Меньше риск травмирования глаз и лица |
|
|
|
больного |
|
|
|
|
|
|
С эндотрахеа- |
Альтернатива трудной интубации! |
Сброс дыхательной смеси, в том числе в желудок |
|
льной трубкой |
Меньшая инвазивность. |
с риском аспирации. |
|
|
Меньше риск травм губ, зубов, гортани, |
Дыхательные пути защищены хуже. |
|
|
развития ларинго- и бронхоспазма, попа- |
Ограничение Рpic. |
|
|
дания в пищевод, бронх. |
Больной может лежать только на спине. |
|
|
В ряде случаев не требуются миорелак- |
Опасно при ожирении. |
|
|
санты и большие дозы гипнотиков. |
Не предполагает длительного использования в респи- |
|
|
Часто возможно обойтись без разгибания |
раторной поддержке, а применяется только как сред- |
|
|
в атланто-окципитальном сочленении |
ство срочной помощи при трудной интубации |
|
|
|
|
|
Таблица 19.22. Соответствующие настройки для вакуум-аспиратора и санации |
|||
|
|
||
|
Параметры |
||
|
|
|
|
возраст |
переносной аспиратор, в мм рт.ст. |
|
стационарный аспиратор, мм рт.ст. |
|
|
|
|
Младенец |
3–5 |
|
60–100 |
|
|
|
|
Ребенок |
5–10 |
|
100–120 |
|
|
|
|
Взрослый |
7–15 |
|
120–150 |
|
|
|
|
393

Раздел 19
Таблица 19.23. Диаметр безманжеточных педиатрических трахеостомических трубок
Размер |
Внутренний диаметр, мм |
|
Внешний диаметр, мм |
Длина, мм |
|
|
|
|
|
|
|
Portex |
|
|
|
|
|
|
|
2,5 |
2,5 |
|
4,5 |
30 |
|
|
|
|
|
3,0 |
3,0 |
|
5,2 |
36 |
|
|
|
|
|
3,5 |
3,5 |
|
5,8 |
40 |
|
|
|
|
|
4,0 |
4,0 |
|
6,6 |
44 |
|
|
|
|
|
4,5 |
4,5 |
|
7,1 |
48 |
|
|
|
|
|
|
|
|
Shiley |
|
|||
3,0 |
3,0 |
|
|
4,5 |
|
39 |
|
|
|
|
|
|
|
|
|
3,5 |
3,5 |
|
|
5,2 |
|
40 |
|
|
|
|
|
|
|
|
|
4,0 |
4,0 |
|
|
6,0 |
|
41 |
|
|
|
|
|
|
|
|
|
4,5 |
4,5 |
|
|
6,5 |
|
42 |
|
|
|
|
|
|
|
|
|
5,0 |
5,0 |
|
|
7,1 |
|
44 |
|
|
|
|
|
|
|
|
|
Таблица 19.24. Размер трахеостомических трубок с манжетами низкого давления для взрослых |
|
||||||
|
|
|
|
|
|
|
|
Размер |
|
Внутренний диаметр, мм |
|
|
Наружный диаметр, мм |
|
Длина, мм |
|
|
|
|
|
|
||
|
|
Kamen-Wilkenson (Bivona) (надувная манжета) |
|
||||
|
|
|
|
|
|||
5 |
|
5,0 |
|
7,3 |
|
60 |
|
|
|
|
|
|
|
|
|
6 |
|
6,0 |
|
8,7 |
|
70 |
|
|
|
|
|
|
|
|
|
7 |
|
7,0 |
|
10,0 |
|
80 |
|
|
|
|
|
|
|
|
|
8 |
|
8,0 |
|
11,0 |
|
88 |
|
|
|
|
|
|
|
|
|
9 |
|
9,0 |
|
12,3 |
|
98 |
|
|
|
|
|
|
|
|
|
|
|
|
Portex |
|
|||
|
|
|
|
|
|||
6 |
|
6,0 |
|
8,3 |
|
55 |
|
|
|
|
|
|
|
|
|
7 |
|
7,0 |
|
9,7 |
|
75 |
|
|
|
|
|
|
|
|
|
8 |
|
8,0 |
|
11,0 |
|
82 |
|
|
|
|
|
|
|
|
|
9 |
|
9,0 |
|
12,4 |
|
87 |
|
|
|
|
|
|
|
|
|
|
|
|
Shiley |
|
|||
|
|
|
|
|
|||
4 |
|
5,0 |
|
9,4 |
|
65 |
|
|
|
|
|
|
|
|
|
6 |
|
6,4 |
|
10,8 |
|
76 |
|
|
|
|
|
|
|
|
|
8 |
|
7,5 |
|
12,2 |
|
81 |
|
|
|
|
|
|
|
|
|
10 |
|
8,9 |
|
13,8 |
|
81 |
|
|
|
|
|
|
|
|
|
Таблица 19.25. Приблизительные эквиваленты трахеостомических трубок разных производителей
Размер по Джексону |
Внешний диаметр, мм |
French |
Внутренний диаметр, мм |
|
|
|
|
0 |
4,3 |
13 |
2,5 |
|
|
|
|
0 |
5,0 |
15 |
3,0 |
|
|
|
|
1 |
5,5 |
16,5 |
3,5 |
|
|
|
|
2 |
6,0 |
18 |
4,0 |
|
|
|
|
3 |
7,0 |
21 |
4,5–5,0 |
|
|
|
|
4 |
8,0 |
24 |
5,5 |
|
|
|
|
5 |
9,0 |
27 |
6,0–6,5 |
|
|
|
|
6 |
10,0 |
30 |
7,0 |
|
|
|
|
7 |
11,0 |
33 |
7,5–8,0 |
|
|
|
|
8 |
12,0 |
37 |
8,5 |
|
|
|
|
9 |
13,0 |
39 |
9,0–9,5 |
|
|
|
|
10 |
14,0 |
42 |
10,0 |
|
|
|
|
11 |
15,0 |
45 |
10,5–11,0 |
|
|
|
|
12 |
16,0 |
48 |
11,5 |
|
|
|
|
Примечание: так как толщина трубок у разных производителей различна, эти значения отражают лишь основной принцип.
394

Дыхательная недостаточность
Таблица 19.26. Краткий список условных обозначений, используемых при механической вентиляции легких
Величина |
Подтип |
Обозначения |
|
Примеры |
|
|
|
|
|
Переменная |
Первичная |
Курсив, заглавные |
Р |
Давление |
|
|
буквы |
|
|
|
|
V |
Объем |
|
|
|
|
||
|
|
|
|
|
|
|
|
V· |
Поток |
|
|
|
С |
Концентрация |
|
|
|
|
|
|
|
|
Т |
Температура |
|
|
|
|
|
|
Разница (расстояние |
Курсив, заглавные |
P |
Давление в одной точке минус |
|
между точками в |
буквы, дельта |
|
давление в другой точке системы |
|
пространстве) |
|
|
|
|
|
|
|
|
|
Изменение (относи- |
Курсив, строчные |
p |
Давление, измеренное в сравне- |
|
тельно контрольной |
буквы |
|
нии с контрольной точкой |
|
точки) |
|
|
|
|
|
|
|
|
Аргумент (исполь- |
Не применяется |
Так же, как величина |
P(t) |
Давление как функция от времени |
зуется только с |
|
|
|
|
|
|
v(p) |
Изменение объема как функция от |
|
переменными, если |
|
|
||
|
|
|
изменения давления |
|
аргумент не обозна- |
|
|
|
|
|
|
|
|
|
|
|
Z(jω) |
Импеданс (сложное число, функ- |
|
чен, подразумевается |
|
|
||
время) |
|
|
|
ция от углового ускорения) |
|
|
|
|
|
Свойство |
Материальное |
Жирные, обычно гре- |
ε |
Эластичность |
|
|
ческие буквы |
|
|
|
|
η |
Вязкость |
|
|
|
|
||
|
|
|
|
|
|
Структурное |
Жирные, обычно |
C |
Растяжимость |
|
|
английский алфавит |
|
|
|
|
R |
Сопротивление |
|
|
|
|
||
|
|
|
|
|
|
|
|
τ |
Постоянная времени |
|
|
|
|
|
|
|
|
I |
Инертность |
|
|
|
|
|
|
|
|
D |
Диффузионная способность |
|
|
|
|
|
|
Системное |
Жирные, заглавные |
Z(jω) |
Импеданс (сложное число, функ- |
|
|
буквы греческого или |
|
ция от углового ускорения) |
|
|
английского алфавита |
|
|
Характеристика |
Системы в целом |
Заглавные и строчные |
PEEP |
Положительное давление в конце |
|
|
буквы |
|
выдоха |
|
|
|
|
|
|
|
|
MAP |
Среднее артериальное давление |
|
|
|
|
|
|
|
|
WOB |
Работа дыхания |
|
|
|
|
|
|
|
|
PIP |
Пиковое давление вдоха |
|
|
|
|
|
|
Ответа системы |
Заглавные и строчные |
FEV1 |
Объем форсированного выдоха за |
|
|
буквы |
|
первую секунду |
|
|
|
MV |
Минутная вентиляция |
|
|
|
|
|
|
|
|
FVC |
Форсированная жизненная |
|
|
|
|
емкость |
|
|
|
Cdyn |
Динамический комплаенс |
395

Раздел 19
Таблица 19.27. Краткий список условных обозначений модификаторов
Подтип |
|
Обозначения |
|
|
|
Примеры |
|
||
|
|
|
|
|
|
|
|||
Обозначение вещества |
|
Надстрочный |
|
pО2 |
Парциальное напряжение кислорода |
|
|||
|
|
|
|
|
= |
Среднее давление открытия дыхательных путей |
|||
Определение места, |
|
Подстрочный |
|
PAO |
|||||
направления |
|
|
|
|
|
|
|
|
|
|
|
|
|
RAW |
Сопротивление дыхательных путей |
|
|||
|
|
|
|
|
|
||||
|
|
|
|
|
paO2 |
Парциальное давление кислорода в артериальной |
|||
|
|
|
|
|
|
|
крови |
|
|
|
|
|
|
|
V (f) |
Поток выдоха (выражено как явная функция времени) |
|||
|
|
|
|
|
|
k |
|
|
|
Индекс времени |
|
Подстрочный |
|
Р0,1 |
Давление сопротивления дыхательных путей (occlusion |
||||
|
|
|
|
|
|
|
pressure) через 0,1 с после начала вдоха |
|
|
|
|
|
|
|
FEV1 |
Объем форсированного выдоха за первую секунду |
|||
|
|
|
|
|
tI |
Время вдоха |
|
||
|
|
|
|
|
tE |
Время выдоха |
|
||
|
|
|
|
|
τ |
Постоянная времени |
|
||
|
|
|
|
|
|
|
|||
|
|
|
|
|
ΔPTR,1 |
Разница транспульмонального давления за единицу |
|||
|
|
|
|
|
|
|
времени |
|
|
Указатель (содержит |
|
Маленькие буквы (не |
|
Cdyn |
Динамический комплаенс |
|
|||
часть термина) |
|
подстрочные) |
|
|
|
|
|
||
|
|
VD |
Объем мертвого пространства |
|
|||||
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
VT |
Дыхательный объем |
|
||
|
|
|
|
|
|||||
Таблица 19.28. Параметры давления, используемые при описании механики респираторной системы |
|
||||||||
|
|
|
|
|
|
|
|
|
|
Название |
|
Обозначение |
|
Определение |
|
||||
|
|
|
|
|
|
|
|
||
Давление открытия дыхательных |
Pao |
|
|
Давление, измеряемое во время открытия системы дыхатель- |
|||||
путей |
|
|
|
|
ных путей (рот/нос, открытие трахеостомы или конец ЭТ) |
||||
|
|
|
|
|
|
|
|
||
Внутриплевральное давление |
Ppl |
|
|
Давление, измеряемое в плевральной полости; изменения |
|||||
|
|
|
|
|
|
внутриплеврального давления часто оцениваются при помо- |
|||
|
|
|
|
|
|
щи измерения изменений давления в пищеводе |
|||
|
|
|
|
|
|
|
|
|
|
Альвеолярное давление |
|
Pa |
|
|
Давление в альвеолярной (воздухоносной) области легких |
||||
|
|
|
|
|
|
|
|
||
Давление поверхности тела |
Pbs |
|
|
Давление, измеряемое на поверхности тела |
|
||||
|
|
|
|
|
|
|
|
|
|
Абдоминальное давление |
|
Pab |
|
|
Давление в брюшной полости |
|
|||
|
|
|
|
|
|
|
|
||
Таблица 19.29. Разности давлений, используемые при описании респираторной системы |
|
||||||||
|
|
|
|
|
|
|
|
||
Определение |
|
|
|
|
Название |
Обозначение |
|||
|
|
|
|
|
|
|
|
||
Pao-Prs |
|
|
Трансреспираторная разница давления |
ΔP TR |
|||||
|
|
|
|
|
|
|
|
||
Pao-Pa |
|
|
Разница давления в дыхательных путях |
ΔP TAW |
|||||
|
|
|
|
|
|
|
|
||
Pao-Ppl |
|
|
Транспульмональная разница давления |
ΔP TP |
|||||
|
|
|
|
|
|
|
|
||
Pa-Ppl |
|
|
Трансальвеолярная разница давления |
ΔP TA |
|||||
|
|
|
|
|
|
|
|
||
Pa-Pbs |
|
|
Трансторакальная разница давления |
ΔP TT |
|||||
|
|
|
|
|
|
|
|
||
Ppl-Pbs |
|
|
Разница трансгрудностеночного давления |
ΔP TCW |
|||||
|
|
|
|
|
|
|
|
||
Ppl-Pab |
|
|
Трансдиафрагмальная разница давления |
ΔPtd |
|||||
|
|
|
|
|
|
|
|
||
Pab-Pbs |
|
|
Трансбрюшностеночная разница давления |
ΔP TabW |
|||||
|
|
|
|
|
|
||||
Торакальная трансмуральная (реберный кар- |
Разница давления мышц реберного каркаса |
ΔPmusc rc |
|||||||
кас, брюшная стенка, грудная стенка) разница |
|
|
|
|
|
||||
Разница давления мышц живота |
ΔPmusc ab |
||||||||
давления, которая осуществляет движения, |
|||||||||
|
|
|
|
|
|||||
идентичные движениям дыхательной мускула- |
Разница давления мышц диафрагмы |
ΔPmusc d |
|||||||
туры во время акта дыхания |
|
|
|
|
|
|
|||
|
Разница давления мышц грудной стенки (грудная |
ΔPmusc CW |
|||||||
|
|
|
|
||||||
|
|
|
|
стенка включает реберный каркас, брюшную |
|
||||
|
|
|
|
полость и диафрагму) |
|
||||
|
|
|
|
|
|
|
|
|
|
Список литературы
См. 
396
|
|
|
|
|
|
|
Дыхательная недостаточность |
|
|
14 |
|
|
|
|
|
|
|
|
12 |
|
|
|
|
|
|
|
|
|
|
|
|
Назотрахеальный |
|
|
|
см |
10 |
|
|
|
|
|
|
|
Длина, |
|
|
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
Оротрахеальный |
|
|
|
|
6 |
|
|
|
|
|
|
|
|
0,5 |
1,0 |
1,5 |
2,0 |
2,5 |
3,0 |
3,5 |
4,0 |
|
|
|
|
Масса тела, кг |
|
|
|
|
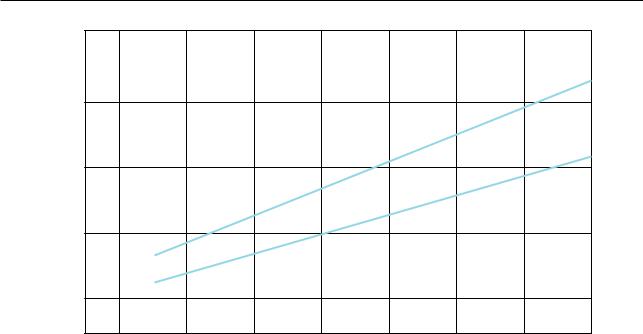
Рис. 19.15. График определения подходящей глубины введения эндотрахеальных трубок для младенцев с массой тела менее 750 г. Необходимо вычесть 0,5 см из полученной длины. Размер эндотрахеальной трубки для детей 1–12 лет может быть
рассчитан по формуле: Внутренний диаметр эндотрахеальной трубки (мм)
Возраст ( лет ) +16 4
19.4. Экстракорпоральная мембранная оксигенация
Е.В. Крюков, В.В. Моргачев, Р.Х. Шарипов, В.В. Стец, А.А. Зайцев
Введение
ЭКМО является методом искусственного увеличения уровня парциального напряжения О2 крови (оксигенации) и удаления (элиминации) из крови СО2, что достигается путем активного (с помощью аппарата ЭКМО) нагнетания венозной или артериальной крови в экстракорпоральный контур, ее последующего прохождения через оксигенатор и возврата оксигенированной и декарбоксилированной крови в системный кровоток. ЭКМО — это модифицированная искусственная система кровообращения, обеспечивающая замещение газообменной функции легких (оксигенация, элиминация СО2) и кровообращения, а также доставку О2 к периферическим тканям и системную перфузию для поддержания сердеч- но-легочной функции при крайне тяжелых расстройствах легочного газообмена и/или системной гемодинамики.
В настоящее время область применения ЭКМО чрезвычайно разнообразна, это кардиохирургия, анестезиология-реаниматология, медицина ката-
строф, трансплантология и донорство органов. В пульмонологической практике пристальный интерес к ЭКМО обусловлен недавней пандемией гриппа А/H1N1, и в настоящее время имеется достаточное количество данных, свидетельствующих о возможных перспективах данного метода в лечении пациентов с ОРДС и рефрактерной гипоксемией на фоне тяжелого вирусного поражения легких.
История искусственного кровообращения начинается с 1813 г., когда М. LeGallois предположил, что функция части тела, отделенной от организма, может восстановиться после проведения искусственной перфузии. А первая система оксигенации крови вне организма была сконструирована М. Von Frey и М. Gruber в 1885 г. для изучения метаболизма в отдельных органах, перфузия которых проводилась оксигенированной кровью. Газообмен в этой конструкции осуществлялся за счет непрерывного потока кислорода через вращающийся металлический цилиндр, внутренняя поверхность которого была покрыта тонкой пленкой крови.
В 1920 г. выдающийся русский ученый-патофи- зиолог С.С. Брюхоненко впервые предложил концепцию метода искусственного кровообращения, и в 1925 г. был впервые продемонстрирован созданный им аппарат искусственного кровообращения. Прибор состоял из двух механически управляемых насосов с системой клапанов. Удаленные легкие донорского животного служили оксиге-
397

Раздел 19
натором. Один насос доставлял венозную кровь
воксигенатор, другой перекачивал оксигенированную кровь из донорских легких в системную циркуляцию животного, которому осуществляли перфузию. Одновременно с СС. Брюхоненко над работой по созданию аппарата искусственного кровообращения трудился другой известный ученый С.И. Чечулин. Аппарат искусственного кровообращения был успешно применен в экспериментах на собаках.
Последующая история искусственного кровообращения связана с именем выдающегося американского ученого J. Gibbon, представившего миру
в1950 г. первый аппарат искусственного кровообращения, позволяющий проводить оперативные вмешательства на сердце. Длительное замещение оксигенирующей функции легких стало возможным после разработки качественно новых видов оксигенаторов, и в 1955 г. R. DeWall и С. Lillehei представили пузырьковый прямопоточный оксигенатор, в котором кровь и кислород непосредственно контактировали друг с другом. С 1956 г. стало возможным более длительное проведение искусственного кровообращения благодаря разработке мембранного оксигенатора G. Clowes с использованием полиэтилена в качестве мембраны. С этого времени началось применение мембранных оксигенаторов, которые в дальнейшем постоянно совершенствовались.
В1972 г. J. Hill и соавт. сообщили о первом успешном случае лечения 24-летнего пациента с ОРДС, возникшим в результате политравмы, с использованием экстракорпоральной мембранной оксигенации. На 4-е сутки пребывания в клинике больному в связи с развитием критической дыхательной недостаточности наладили периферическую вено-артериальную перфузию с использованием аппарата искусственного кровообращения и оксигенатора. Длительность процедуры составила 75 ч, объемная скорость перфузии — 3,0–3,6 л/мин. Это позволило снизить концентрацию кислорода на аппарате ИВЛ со 100 до 60%, увеличить парциальное давление кислорода в артериальной крови с 38 до 75 мм рт.ст., а в дальнейшем отключить систему ЭКМО и выписать пациента из клиники.
Последующие клинические наблюдения и исследования позволили продемонстрировать перспективность использования метода у больных с тяжелой дыхательной недостаточностью — как у детей, так и у взрослых. В нашей стране метод ЭКМО начали применять у пациентов с синдромом низкого сердечного выброса, развившегося после операции на закрытом сердце, с 1997 г. Первые случаи использования данного метода носили единичный характер, что было обусловлено высокой стоимостью оборудования, расходных материалов и применяемых медикаментов, а также значительной летальностью. Накопление опыта, расширение показаний и внедрение протоколов ведения больных на ЭКМО позволили
более активно применять данный метод вспомогательного кровообращения в лечении сердечной и/или дыхательной недостаточности.
Внастоящее время метод ЭКМО прочно вошел
вклиническую практику во всем мире, сформулированы показания и противопоказания к проведению данной процедуры, а появляющиеся новые технические разработки позволяют более безопасно и с меньшими затратами выполнять эту процедуру.
Показания и противопоказания
Теоретически ЭКМО может быть показана любому больному с рефрактерной к традиционным методам респираторной поддержки дыхательной недостаточностью, но с оговоркой о потенциально обратимой форме ДН. Очень важным является отбор пациентов для проведения ЭКМО. С одной стороны, необходимо правильно оценить степень снижения сердечно-легочной функции с целью определения показаний для применения этого метода, а с другой стороны, исключить группу больных, у которых прогноз является явно безнадежным и для которых проведение ЭКМО не имеет смысла. В целом, вопросы для отбора пациентов можно сформулировать следующим образом.
1.Является ли имеющаяся у больного легочная, сердечная или сердечно-легочная недостаточность потенциально обратимой?
2.Позволяет ли неврологический статус или функциональное состояние органов и систем надеяться на благополучный исход?
3.Имеются ли противопоказания для использования даже минимального уровня гепаринизации?
4.Можно ли достигнуть благополучного исхода, применяя консервативное или хирургическое лечение?
Согласно международным исследованиям, длительность ИВЛ является важным критерием для отбора больных. Максимально допустимая продолжительность ИВЛ у новорожденных составляет 10 дней, а у детей и взрослых — 7 дней. Проведение ИВЛ с большей продолжительностью часто сопровождается неблагоприятными исходами. Кроме того, важно учитывать повреждающее действие ИВЛ с высоким пиковым давлением.
Если ЭКМО используется при сердечной недостаточности, то она более эффективна в случае, когда у больного имеет место правожелудочковая недостаточность, которая является следствием ЛГ и сопутствующей гипоксии. Перед отбором больных для выполнения ЭКМО в качестве метода вспомогательного кровообращения важно правильно оценить функцию сердца. С развитием современных кардиохирургических методик случаи послеоперационной сердечной недостаточности, рефрактерной к инотропным препаратам, стали довольно редкими. Поэтому ЭКМО в качестве
398
Дыхательная недостаточность
Таблица 19.30. Показания и противопоказания к экстракорпоральной мембранной оксигенации
Показания/противопоказания |
Условия |
Потенциальные показания к ЭКМО |
● Рефрактерная гипоксемия paO2/FiO2 <50 мм рт.ст., персистирующая*, несмо- |
|
тря на FiO2 >80% + PEEP (≤20 cм H2O) при Pplat = 32 cм H2O + прональная пози- |
|
ция +/– ингаляционный NO. |
|
● Давление плато ≥35 cм H2O, несмотря на снижение PEEP до 5 cм H2O и сниже- |
|
ние дыхательного объема до минимального значения (4 мл/кг) и pH ≥7,15 |
|
|
Противопоказания к ЭКМО |
● Тяжелые сопутствующие заболевания с предсказанной продолжительностью |
|
жизни больного не более 5 лет. |
●Полиорганная недостаточность и SAPS II >90 баллов или SOFA >15 баллов.
●Немедикаментозная кома (вследствие инсульта).
●Решение об ограничении терапии.
●Техническая невозможность венозного или артериального доступа.
●ИМТ >40 кг/м2
* Характер персистирования зависит от динамики процесса (несколько часов для быстропрогрессирующих состояний и до 48 ч в случае стабилизации).
метода вспомогательного кровообращения чаще применяется при кардиальной патологии, по поводу которой не проводилось какого-либо лечения, как мост к пересадке сердца или в рамках сердечно-легочной реанимации.
Показания и противопоказания к ЭКМО у больных с ОРДС с тяжелым поражением легких при гриппозной инфекции, пневмонии представлены в табл. 19.30.
Принципы работы экстракорпоральной мембранной оксигенации
Наиболее важным компонентом экстракорпорального контура для ЭКМО является газообменное устройство или оксигенатор, остальные составляющие контура служат для обеспечения его работы. Современные оксигенаторы, предназначенные для проведения ЭКМО, имеют капиллярное или половолоконное строение. В зависимости от расположения крови по отношению к мембране капиллярного волокна выделяют два основных типа мембранных капиллярных оксигенаторов. Кровь поступает в оксигенатор или с внешней стороны капиллярного волокна, омывая его снаружи, или проходит внутри капиллярного волокна. При втором типе существует повышенный риск тромбоза капилляров и нарушения газообменной функции мембранного оксигенатора, в связи с чем в настоящее время выпускаются капиллярные оксигенаторы первого типа.
В современных мембранных капиллярных оксигенаторах газовый поток проходит внутри оксигенатора, а кровь — со стороны внешней поверхности капиллярного полиметилпептенового волокна с биосовместимым покрытием. Технология взаимно перпендикулярного направления потоков крови, газа и воды из теплообменника способствует улучшению физико-био- логических свойств капиллярной мембраны, повышению продолжительности ее оптимально-
го функционирования в целях длительного использования во время ЭКМО. Наличие тонкого слоя биосовместимого покрытия, прикрывающего микропоры капиллярной полиметилпептеновой мембраны, делает капиллярную мембрану истинно диффузионной.
При проведении ЭКМО, как правило, применяются центрифужные (ротационные) насосы, так как они меньше повреждают форменные элементы крови, имеют меньший объем заполнения и меньший размер. При их использовании необходимо осуществлять контроль давления в приточной линии, и если происходит снижение притока крови, а насос работает с высокой частотой оборотов, может возникать выраженное разрежение в головке насоса, сопровождающееся гемолизом.
В контур для ЭКМО, проводимых в стационарах, включается теплообменник для поддержания температуры больного. Теплообмен осуществляется между кровью и водой, циркулирующей в противоположном кровотоку направлении.
Компоненты контура для ЭКМО имеют свои технические особенности, они способны поддерживать нормотермию и функционировать длительное время. Магистрали контура для ЭКМО разработаны таким образом, что в них отсутствуют области застоя крови и они позволяют применять минимальный уровень гепаринизации.
Виды экстракорпоральной мембранной оксигенации
В зависимости от целей проведения выделяют следующие методики проведения ЭКМО.
•С использованием аппарата ЭКМО:
○вено-артериальная ЭКМО;
○вено-венозная ЭКМО;
○вено-артериовенозная ЭКМО.
•Без использования аппарата ЭКМО:
○артериовенозная самопоточная ЭКМО.
399
