
Полезные материалы за все 6 курсов / Учебники, методички, pdf / Вопросы_нейрохирургии_Выпуск_5_2020
.pdfОригинальные статьи |
Original articles |
зультатов радиохирургии на аппарате гамма-нож у 20 пациентов с НТН при ВБД (средний возраст — 74 года, 48—95 лет). Облегчение боли достигнуто по истечении 1 года у 53% больных, 2 лет — у 38%, 5 лет — у 10% пациентов. Следует уточнить понятие «облегчение боли»: радиохиругия считается эффективной, если соответствует I—IIIb степеням по шкале BNI, где IIIb означает сохранение приемлемой боли в лице на фоне приема препаратов. В 70% случаев (14 из 20) после лечения гамма-ножом пациенты проходили повторное хирургическое лечение (гамма-нож, радиочастотная термокоагуляция или МВД). Среднее время до снижения боли составило 5 нед, варьируя от 1 дня до 6 месяцев [31]. В работе S.E. Lakhan приведен случай одного пациента с НТН при ВБД с неэффективной операцией с использованием гамма-ножа [35]. Описания других случаев использования гамманожа у пациентов с ВБД в литературе мы не обнаружили. По-видимому, гамма-нож по эффективности уступает МВД в лечении НТН при ВБД, но является опцией при неэффективности МВД или при рецидиве после МВД [19].
Впервые принципы и технологию МВД при НТН описал нейрохирург P.J. Jannetta в 1967 г. [36]. Его главной идеей был принцип уязвимости «зоны входа» ТрН к пульсационным или непрерывным длительным механическим воздействиям, которые приводят к демиелинизации его волокон. В дальнейшем его идея стала известна как «периферическая теория». Несмотря на широкое распространение МВД, остается много вопросов относительно этой операции. Например, неясно, почему после МВД боли проходят сразу, ведь для восстановления миелина в нервных волокнах требуется время.
Операция МВД у пациентов с НТН вследствие ВБД производится через стандартный ретросигмоидный доступ. Описан лишь единичный случай с доступом по Kawase (птериональная краниотомия с передней петрозэктомией). По мнению авторов, такой доступ представлял больше возможностей для транспозиции и фиксации долихоэктазированной базилярной артерии. Боль в лице у пациента прошла, однако наблюдались осложнения — стволовой инсульт и парез отводящего нерва [37].
Способы разрешения нейроваскулярного конфликта при операции МВД с ВБД можно разделить на 2 группы — без фиксации и с фиксацией вертебробазилярного комплекса. Сторонники фиксации полагают, что внедрение изолирующего материала убирает раздражение ТрН, но усиливает сдавление ТрН и других черепных нервов и, следовательно, увеличивает вероятность послеоперационных осложнений, таких как гипестезия на лице, потеря слуха или диплопия. Они полагают, что экранирование ТрН не столько отводит крупнокалиберную ригидную артерию, сколько еще больше смещает и сдавливает нерв.
При простой МВД (без фиксации вертебробазилярного комплекса) в большинстве случаев используют тефлон. Значительно реже используют материал Ivalon, мышцу или мышцу вместе с жиром. От использования фрагментов аутологичной мышцы
восновном отказались из-за частых рецидивов [19]. Однако, по данным Ю.А. Григорян и соавт., у всех 10 пациентов с НТН при ВБД использование фрагмента мышцы с жиром привело к полному регрессу боли без рецидивов, хотя средний период наблюдения не указан [38]. В англоязычной литературе использование мышцы или Ivalon при МВД у пациентов с НТН при ВБД не упоминается с 1994 г.
От губки Ivalon также отказались в связи с большей частотой рецидивов по сравнению с тефлоном [2, 39]. Редко используют протезы из силикона. Тефлон используют в двух формах — в целой и разволокненной. Во всех случаях мы использовали разволокненный тефлон (структура ваты).
МВД при НТН, как известно, примечательна тем, что ее эффективность, в отличие от аналогичной операции при гемифациальном спазме, можно оценить сразу после операции. По данным работ, доступных
вPubMed к середине 2018 г., у всех пациентов с НТН при ВБД боль проходила сразу после МВД. Исключением стали только две работы по 2 пациента в каждой, причем у всех пациентов было сочетание с гемифациальным спазмом: 2 пациента из 10 у N.M. El-Ghandour (эффективность 80%) и 2 из 8 пациентов у J. Zhong и соавт. (эффективность 75%) [40, 41].
Таким образом, исходя из общего количества пациентов по данным опубликованной литературы к середине 2018 г. (около 180 пациентов), эффективность МВД при ВБД составляет 98%.
Ризотомия может быть использована как дополнение к МВД. Понятие «ризотомия» при НТН очень широко и варьирует у разных авторов от легкого «почесывания» или «массажа» ТрН до его пересечения (частичного или полного) или биполярной коагуляции. Ризотомия несет риск в лучшем случае онемения лица, а в худшем — деафферентационной боли, поэтому мы считаем, что от ризотомии в понимании частичного пересечения ТрН лучше отказаться вообще или использовать ее лишь в исключительных случаях. В нашей серии наблюдений ризотомия в виде частичного пересечения ТрН использована только у 1 пациентки как дополнение к МВД. Боль в лице у данной пациентки прошла, но возникло умеренное онемение лица.
Перемещение мегалоартерии с ее фиксацией несет риски перегиба со стенозом, повреждения перфорантных артерий и инфаркта в стволе мозга. Накладывать шов на твердую мозговую оболочку для фиксации часто очень неудобно и связано с опасностью повреждения нервов и сосудов. Самый простой, но и самый ненадежный способ — фиксация артерии фибриновым клеем, но фибриновый клей может не удержать столь крупную артерию, что приведет к раннему рецидиву
60 |
ВОПРОСЫ НЕЙРОХИРУРГИИ 5, 2020 |
Оригинальные статьи |
Original articles |
НТН [42]. Описаны способы фиксации мегалососуда при НТН с помощью петель (слинг-технология), фенестрированной клипсы, сочетания клипсы с петлей, фиксаторов из титана. Данные способы представлены в статьях в основном как единичные случаи с коротким периодом последующего наблюдения. Мы считаем фиксацию мегалососуда при НТН нецелесообразной. Работа в чрезвычайно тесном пространстве на глубине с множеством критических нейроваскулярных структур не позволяет, по нашему мнению, безопасно перемещать и фиксировать мегалоартерию. Такие манипуляции выходят за рамки «гарантированной хирургии». В качестве примера можно привести статью W. Taki с соавт., которые описали МВД при НТН с ВБД у двух пациентов. После безуспешной фиксации мегалососуда с помощью фибринового клея и петли авторы использовали длинную титановую пластинку, одним концом которой экранировали ТрН, а второй конец фиксировали к затылочной кости, так что длина титановой пластины в полости черепа в обоих случаях составила 10 см. У обоих пациентов боль прошла сразу после операции, без рецидивов при периоде наблюдения 1,5 года и 9 месяцев, однако не указано, имел ли место после операции какой-либо неврологический дефицит [33].
Многие авторы считают разумным выделять НТН, обусловленную ВБД, в отдельный тип [4]. Таким образом, можно предложить классифицировать НТН на «нормоваскулярный» и «долихоэктатический» типы компрессии. Некоторые авторы используют термин «макроваскулярная декомпрессия» при нейроваскулярном конфликте с ВБД [37, 43].
Таким образом, НТН у больных с ВБД при неэффективности медикаментозного лечения ставит пациента и его врача перед выбором нескольких хирургических опций, одной из которых является МВД. Данная опция привлекательна наибольшей эффективностью,
ЛИТЕРАТУРА/REFERENCES
1.Cruccu G, Gronseth G, Alksne J, Argoff C, Brainin M, Burchiel K, Nurmikko T, Zakrewska J. AAN-EFNS guidelines on trigeminal neuralgia management. European Journal of Neurology. 2008;15(10):1013-1028. https://doi.org/10.1111/j.1468-1331.2008.02185.x
2.Linskey ME, Jho HD, Jannetta PJ. Microvascular decompression for trigeminal neuralgia caused by vertebrobasilar compression. Journal of Neurosurgery. 1994;81(1):1-9.
https://doi.org/10.3171/jns.1994.81.1.0001
3.Yang XS, Li ST, Zhong J, Zhu J, Du Q, Zhou QM, Jiao W, Guan HX. Microvascular decompression on patients with trigeminal neuralgia caused by ectatic vertebrobasilar artery complex: technique notes. Acta Neurochirurgica. 2012;154(5):793-797.
https://doi.org/10.1007/s00701-012-1320-6
4.Ma X, Sun X, Yao J, Ni S, Gong J, Wang J, Li X. Clinical analysis of trigeminal neuralgia caused by vertebrobasilar dolichoectasia. Neurosurgical Review. 2013;36(4):573-577.
https://doi.org/10.1007/s10143-013-0468-8
5.Smoker WR, Corbett JJ, Gentry LR, Keyes WD, Price MJ, McKusker S. High-resolution computed tomography of the basilar artery: 2. Vertebrobasilar dolichoectasia: clinical-pathologic correlation and review. AJNR. American Journal of Neuroradiology. 1986;7(1):61-72.
но сопряжена с большей сложностью и риском. Следует учитывать, что ВБД не только локальная проблема лицевой боли, но и системное прогрессирующее заболевание. Тем не менее наши результаты дают некоторое основание считать операцию МВД у пациентов с НТН при ВБД достаточно эффективной и безопасной.
Заключение
Микроваскулярная декомпрессия является эффективным методом устранения боли у пациентов с невралгией тройничного нерва вследствие вертебробазилярной долихоэктазии. Операция технически сложнее, чем на сосудах нормального калибра, но гораздо эффективнее, чем все имеющиеся альтернативы. Возможности транспозиции сосуда при вертебробазилярной долихоэктазии с фиксацией или без фиксации последнего ограниченны и малоэффективны. Интерпозиция тефлоновой ваты в точках конфликта — эффективный и достаточный прием для полного устранения тригеминальной боли с минимальным риском для пациента.
Участие авторов:
Концепция и дизайн исследования — Шулев Ю.А.
Сбор и обработка материала — Печиборщ Д.А., Трашин А.В., Гордиенко К.С.
Статистическая обработка данных — Печиборщ Д.А.
Написание текста — Печиборщ Д.А., Трашин А.В., Гордиенко К.С.
Редактирование — Шулев Ю.А., Трашин А.В., Гордиенко К.С., Печиборщ Д.А.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflict of interest.
6.Giang DW, Perlin SJ, Monajati A, Kido DJ. Hollander Vertebrobasilar dolichoectasia: assessment using MR. Neuroradiology. 1988;30(6):518-523. https://doi.org/10.1007/bf00339693
7.Burchiel KJ. A new classification for facial pain. Neurosurgery. 2003;53(5):1164-1166; discussion 1166-1167. https://doi.org/10.1227/01.neu.0000088806.11659.d8
8.Flemming KD, Wiebers DO, Brown RD, Link M, Huston J, McClelland RL, Christianson T. The natural history of radiographically defined vertebrobasilar nonsaccular intracranial aneurysms. Cerebrovascular Diseases (Basel, Switzerland). 2005;20(4):270-279.
https://doi.org/10.1159/000087710
9.Kumral E, Kisabay A, Atac C, Kaya C, Calli C. The mechanism of ischemic stroke in patients with dolichoectatic basilar artery. European Journal of Neurology. 2005;12(6):437-444. https://doi.org/10.1111/j.1468-1331.2005.00993.x
10.Ikeda K, Nakamura Y, Hirayama T, Sekine T, Nagata R, Kano O, Kawabe K, Kiyozuka T, Tamura M, Iwasaki Y. Cardiovascular risk and neuroradiological profiles in asymptomatic vertebrobasilar dolichoectasia. Cerebrovascular Diseases (Basel, Switzerland). 2010;30(1):23-28. https://doi.org/10.1159/000313440
BURDENKO'S JOURNAL OF NEUROSURGERY 5, 2020 |
61 |
Оригинальные статьи |
Original articles |
11.Schievink WI, Torres VE, Wiebers DO, Huston J 3rd. Intracranial arterial dolichoectasia in autosomal dominant polycystic kidney disease. Journal of the American Society of Nephrology: JASN. 1997;8(8):1298-1303. https://doi.org/10.3171/jns.1995.83.6.1004
12.Laforet P, Petiot P, Nicolino M, Orlikowski D, Caillaud C, Pellegrini N, Froissart R, Petitjean T, Maire I, Chabriat H, Hadrane L, Annane D, Eymard B. Dilative arteriopathy and basilar artery dolichoectasia complicating late-onset Pompe disease. Neurology. 2008;70(22):2063-2066. https://doi.org/10.1212/01.wnl.0000313367.09469.13
13.Garzuly F, Marodi L, Erdos M, Grubits J, Varga Z, Gelpi E, Rohonyi B, Mázló M, Molnár A, Budka H. Megadolichobasilar anomaly with thrombosis in a family with Fabry’s disease and a novel mutation in the alphagalactosidase A gene. Brain. 2005;128(9):2078-2083. https://doi.org/10.1093/brain/awh546
14.Pico F, Labreuche J, Touboul PJ, Amarenco P. Intracranial arterial dolichoectasia and its relation with atherosclerosis and stroke subtype. Neurology. 2003;61:1736-1742. https://doi.org/10.1212/01.wnl.0000103168.14885.a8
15.Forrest KM, Siddiqui A, Lim M, Wraige E. Basilar artery dolichoectasia in childhood: evidence of vascular compromise. Child’s Nervous System. 2011;27(1):193-196.
https://doi.org/10.1007/s00381-010-1267-y
16.Victor J, Del Brutto, Jorge G. Ortiz. Intracranial Arterial Dolichoectasia.
Frontiers in Neurology. 2017;8:344. https://doi.org/10.3389/fneur.2017.00344
17.Passero S, Filosomi G. Posterior circulation infarcts in patients with vertebrobasilar dolichoectasia. Stroke. 1998;29(3):653-659. https://doi.org/10.1161/01.str.29.3.653.
18.Gutierrez J, Bagci A, Gardener H, Rundek T, Ekind M, Alperin N, Sacco R, Wright C. Dolichoectasia diagnostic methods in a multi-ethnic, stroke-free cohort: results from the northern Manhattan study. Journal of Neuroimaging. 2014;24(3):226-231.
https://doi.org/10.1111/j.1552-6569.2012.00781.x
19.Vanaclocha V, Herrera JM, Martínez-Gómez D, Rivera-Paz M, CalabuigBayo C, Vanaclocha L. Is There a Safe and Effective Way to Treat Trigeminal Neuralgia Associated with Vertebrobasilar Dolichoectasia? Presentation of 8 Cases and Literature Review. World Neurosurgery. 2016;96:516-529. https://doi.org/10.1016/j.wneu.2016.08.085
20.Miyazaki S, Fukushima T, Tamagawa T, Morita A. Trigeminal neuralgia due to compression of the trigeminal root by a basilar artery trunk. Report of 45 cases. Neurologia Medico-Chirurgica. 1987;27(8):742-748. https://doi.org/10.2176/nmc.27.742
21.Passero SG, Rossi S. Natural history of vertebrobasilar dolichoectasia. Neurology. 2008;70:66-72. https://doi.org/10.1212/01.wnl.0000286947.89193.f3
22.Han IB, Chang JH, Chang JW, Huh R, Chung SS. Unusual causes and presentations of hemifacial spasm. Neurosurgery. 2009;65(1):130-137. https://doi.org/10.1227/01.neu.0000348548.62440.42
23.Alabri H, Lewis WD, Manjila S, Alkhachroum AM, Georgia M. Acute Bilateral Ophthalmoplegia Due to Vertebrobasilar Dolichoectasia: A Report of Two Cases. The American Journal of Case Reports. 2017;18:1302-1308. https://doi.org/10.12659/ajcr.904395
24.Kawasaki A, Purvin V. Isolated IVth (trochlear) nerve palsy due to basilar artery dolichoectasia. Klinische Monatsblatter fur Augenheilkunde. 2006;223(5):459-461. https://doi.org/10.1055/s-2006-926576
25.Giray S, Pelit A, Kizilkilic O, Karatas M. Isolated abducens nerve palsy caused by contralateral vertebral artery dolichoectasia. Neurology India. 2005;53(2):246-247.
https://doi.org/10.4103/0028-3886.16433
26.Lin JY, Lin SY, Wu JI, Wang IH. Optic neuropathy and sixth cranial nerve palsy caused by compression from a dolichoectatic basilar artery. Journal of Neuro-Ophthalmology. 2006;26(3):190-191. https://doi.org/10.1097/01.wno.0000235579.57180.ae
27.Pham T, Wesolowski J, Trobe JD. Sixth cranial nerve palsy and ipsilateral trigeminal neuralgia caused by vertebrobasilar dolichoectasia. American Journal of Ophthalmology Case Reports. 2018;10:229-232. https://doi.org/10.1016/j.ajoc.2018.02.029
28.Holmes BB, Green WC, Kung NH, Goebel JA, Van Stavern GP. Vertebrobasilar Dolichoectasia Causing an Optic Tract Syndrome. Journal of NeuroOphthalmology. 2017;37(2):179-181. https://doi.org/10.1097/wno.0000000000000495
29.Ebrahimzadeh K, Bakhtevari MH, Shafizad M, Rezaei O. Hydrocephalus as a rare compilation of vertebrobasilar dolichoectasia: A case report and review of the literature. Surgical Neurology International. 2017;8:256. https://doi.org/10.4103/sni.sni_162_17
30.Mohammed K, Iqbal J, Kamel H, Mathew J, Al-Sulaiti G. Obstructive hydrocephalus and facial nerve palsy secondary to vertebrobasilar dolichoectasia: Case Report. Surgical Neurology International. 2018;9:60. https://doi.org/10.4103/sni.sni_37_17
31.Park KJ, Kondziolka D, Kano H, Berkowitz O, Ahmed SF, Liu X, Niranjan A, Flickinger JC, Lunsford LD. Outcomes of Gamma Knife surgery for trigeminal neuralgia secondary to vertebrobasilar ectasia. Journal of Neurosurgery. 2012;116(1):73-81.
https://doi.org/10.3171/2011.8.jns11920
32.Lye RH. Basilar artery ectasia: an unusual cause of trigeminal neuralgia. Journal of Neurology, Neurosurgery, and Psychiatry. 1986;49(1):22-28. https://doi.org/10.1136/jnnp.49.1.22
33.Taki W, Matsushima S, Hori K, Mouri G, Ishida F. Repositioning of the vertebral artery with titanium bone fixation plate for trigeminal neuralgia. Acta Neurochirurgica. 2003;145(1):55-61. https://doi.org/10.1007/s00701-002-1033-3
34.Noma N, Kobayashi A, Kamo H, Imamura Y. Trigeminal neuralgia due to vertebrobasilar dolichoectasia: three case reports. Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology, and Endodontics. 2009;108(3):50-55. https://doi.org/10.1016/j.tripleo.2009.04.039
35.Lakhan SE. Teaching NeuroImages: concurrent hemifacial spasm and trigeminal neuralgia due to vertebrobasilar dolichoectasia. Neurology. 2013;81(8):e52. https://doi.org/10.1212/wnl.0b013e3182a1aaeb
36.Jannetta PJ. Arterial compression of the trigeminal nerve at the pons in patients with trigeminal neuralgia. 1967. Journal of Neurosurgery. 2007;107(1):216-219.
https://doi.org/10.3171/jns.1967.26.1part2.0159
37.Yoon S, Mascitelli JR, Mooney MA, Gandhi S, Chen T, Cole TS, Lawton M. Kawase Approach for Dolichoectactic Basilar Artery Macrovascular Decompression in a Patient With Trigeminal Neuralgia: Case Report. Operative Neurosurgery (Hagerstown, Md.). 2019;16(6):178-183. https://doi.org/10.1093/ons/opy215
38.Григорян Ю.А., Ситников А.Р., Григорян Г.Ю. Тригеминальная невралгия и гемифациальный спазм при извитой вертебробазилярной артерии. Вопросы нейрохирургии имени Н.Н. Бурденко. 2016;80(1):44-56. Grigoryan YuA, Sitnikov AR, Grigoryan GYu. Trigeminal neuralgia and hemifacial spasm in convoluted vertebrobasilar artery. Zhurnal voprosy neirokhirurgii imeni N.N. Burdenko. 2016;80(1):44-56. (In Russ.) https://doi.org/10.17116/neiro201680144-56
39.Suzuki S, Tsuchita H, Kurokawa Y, Kitami K, Sohma T, Takeda T. New method of MVD using a vascular tape for neurovascular compression involving the vertebrobasilar artery — report of two cases. Neurologia MedicoChirurgica. 1990;30(13):1020-1203.
https://doi.org/10.2176/nmc.30.1020
40.El-Ghandour NM. Microvascular decompression in the treatment of trigeminal neuralgia caused by vertebrobasilar ectasia. Neurosurgery. 2010;67(2):330337.
https://doi.org/10.1227/01.neu.0000371978.86528.60
41.Zhong J, Zhu J, Li ST, Guan HX. Microvascular decompressions in patients with coexistent hemifacial spasm and trigeminal neuralgia. Neurosurgery. 2011;68(4):916-920.
https://doi.org/10.1227/neu.0b013e318208f5ac
42.Ohta M, Komatsu F, Abe H, Sakamoto S, Tsugu S, Oshiro S, Fukushima T. Complication caused by use of fibrin glue in vessel transposition for trigeminal neuralgia. Neurologia Medico-Chirurgica. 2008;48(1):30-32. https://doi.org/10.2176/nmc.48.30
43.Tabani H, Yousef S, Burkhardt JK, Gandhi S, Benet A, Lawton MT. Macrovascular Decompression of Facial Nerve with Anteromedial Transposition of a Dolichoectatic Vertebral Artery: 3-Dimensional Operative Video. Operative Neurosurgery (Hagerstown, Md.). 2018;16(1):E4. https://doi.org/10.1093/ons/opy117
Поступила 20.12.2018 Received 20.12.2018 Поступила после доработки 06.12.2019 Revised 06.12.2019 Принята к печати 03.07.2020 Accepted 03.07.2020
62 |
ВОПРОСЫ НЕЙРОХИРУРГИИ 5, 2020 |

Оригинальные статьи Original articles
Комментарий
Среди существующих методов лечения тригеминаль- |
боку на операционном столе, при котором риск воздуш- |
ной невралгии микроваскулярная декомпрессия (МВД) яв- |
ной эмболии сводится к нулю. Во-вторых, непонятно, по |
ляется наиболее эффективной независимо от характера |
какой причине авторами в одном клиническом случае про- |
компримирующего агента: артериального сосуда разного |
изведена ризотомия, в то время как в обсуждении приво- |
диаметра, вены. До 95% пациентов после пробуждения по- |
дятся абсолютные доводы о недопустимости такой мани- |
сле операции указывают на исчезновение боли или ее зна- |
пуляции. В-третьих, спорным является целесообразность |
чительное уменьшение. В большой степени это относится |
проведения пробы на адекватность гемостаза путем пере- |
и к невралгии тройничного нерва (НТН), обусловленной |
жатия шейных вен пациента. Все эти моменты требуют |
вертебробазилярной долихоэктазией (ВБД). Авторы вы- |
комментария. |
полнили 504 МВД, среди которых у 14 (2,8%) пациентов |
Особую ценность работе придает дискуссия относи- |
причиной стала именно ВБД. У всех пациентов этой не- |
тельно необходимости фиксации мобилизованного верте- |
большой, но особенной группы боль исчезла сразу после |
бробазилярного комплекса. Точнее, прекращение дискус- |
операции. Следует сразу отметить, что статья по своему со- |
сии с неоспоримыми аргументами в пользу «безфиксаци- |
держанию и подробному описанию оперативного вмеша- |
онной» технологии. Хочется выразить абсолютное согла- |
тельства фактически является методическим руководством |
сие с тем, что экранирование нерва на всем протяжении в |
для нейрохирургов. Авторами скрупулезно описана ВБД |
оральных отделах мостомозжечкового угла и прилежаще- |
как явление, оценена ее роль в развитии НТН и представ- |
го отдела ствола головного мозга позволяет добиться ис- |
лены этапы МВД именно при этом компримирующем |
чезновения боли во всех клинических случаях. Любые ма- |
агенте. Операции описаны и хорошо иллюстрированы ин- |
нипуляции (транспозиция сосудов, формирование фикси- |
траоперационными фотографиями. Каждый интрадураль- |
рующих петель из твердой мозговой оболочки и наложе- |
ный этап оперативного вмешательства подробно описан. |
ние на них швов или клипс) на вертебробазилярном ком- |
Обращает на себя внимание, что васкулярная декомпрес- |
плексе в условиях узкого операционного поля сопровожда- |
сия, произведенная тефлоновыми протекторами, допол- |
ются повышенным риском развития осложнений. По этой |
нялась установкой желатиновой губки. |
причине фиксация сосудов при МВД не может быть реко- |
Необходимы лишь незначительные дополнения, ко- |
мендована в нейрохирургической практике. |
торые внесут ясность при чтении статьи. Во-первых, оста- |
Статья представляет большой интерес, так как опыт |
ются вопросы, касающиеся положения пациента на опе- |
авторов и особенно литературный обзор по данной про- |
рационном столе. Не совсем понятно, что такое «боковая |
блеме являются весьма ценными для нейрохирургов. |
позиция». Скорее всего, это положение пациента лежа на |
В.Н. Шиманский (Москва) |
BURDENKO'S JOURNAL OF NEUROSURGERY 5, 2020 |
63 |
Оригинальные статьи |
Original articles |
Вопросы нейрохирургии им. Н.Н. Бурденко |
Burdenko's Journal of Neurosurgery |
2020, №5, с. 64-71 |
2020, №5, pp. 64-71 |
https://doi.org/10.17116/neiro20208405164 |
https://doi.org/10.17116/neiro20208405164 |
Лечение посттравматической невропатии седалищного нерва с использованием хронической нейростимуляции и эндоскопической техники
© А.В. Декопов, А.А. Томский, Э.Д. Исагулян, А.А. Огурцова, А.Б. Козлова
ФГАУ «Национальный медицинский исследовательский центр нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России, Москва, Россия
Резюме
Повреждения седалищного нерва в подъягодичной области представляют важную клиническую проблему из-за сложно-
сти хирургического доступа.
Цель исследования — разработка эндоскопического доступа к седалищному нерву, позволяющего проводить микрохирурги-
ческие манипуляции, нейрофизиологическое картирование и имплантацию электродов для хронической нейростимуляции.
Материал и методы. Прооперированы 3 больных с невропатией седалищного нерва. До операции во всех случаях отмечал-
ся нейрогенный болевой синдром по задней поверхности бедра и голени, достигавший 7—8 баллов по визуально-аналого-
вой шкале, парез двуглавой мышцы бедра и трехглавой мышцы голени. Мы применяли эндоскопический доступ к подъягодичной области через маленький разрез под ягодичной складкой. Под эндоскопическим контролем проводили наружный
и внутренний невролиз седалищного нерва. После этого осуществляли внутриствольное картирование нерва для визуали-
зации сенсорных волокон. Непосредственно на эти волокна имплантировали цилиндрический электрод для хронической
нейростимуляции.
Результаты. Во всех случаях после начала хронической нейростимуляции отмечено снижение болевого синдрома до 50%.
В течение 2—3 месяцев после операции происходило нарастание мышечной силы и увеличение объема движений. Клинический эффект был стабилен в катамнезе.
Заключение. Описанная нами техника, сочетающая минимально инвазивный доступ и применение интраоперационного
нейрофизиологического мониторинга, позволяет осуществить оптимальное позиционирование электрода как для дости-
жения противоболевого эффекта, так и для восстановления функции нерва.
Ключевые слова: посттравматическая невропатия, седалищный нерв, эндоскопическая техника, хроническая нейростимуляция.
Информация об авторах:
Декопов А.В. — https://orcid.org/0000-0002-3834-5579; e-mail: adekopov@nsi.ru* Томский А.А. — https://orcid.org/0000-0002-2120-0146
Исагулян Э.Д. — https://orcid.org/0000-0003-1191-9357 Огурцова А.А. — https://orcid.org/0000-0003-3595-2696 Козлова А.Б. — https://orcid.org/0000-0002-8366-8254 * — автор, ответственный за переписку
Как цитировать:
Декопов А.В., Томский А.А., Исагулян Э.Д., Огурцова А.А., Козлова А.Б. Лечение посттравматической невропатии седалищного нерва с использованием хронической нейростимуляции и эндоскопической техники. Вопросы нейрохирургии имени Н.Н. Бурденко. 2020;84(5):64–71. https://doi.org/10.17116/neiro20208405164
Treatment of sciatic posttraumatic neuropathy with chronic neuromodulation and endoscopic technics
© A.V. Dekopov, A.A. Tomsky, E.D. Isagulyan, A.A. Ogurtsova, A.B. Kozlova
Burdenko Neurosurgicai Center, Moscow, Russia
Abstract
Objective. Sciatic nerve injury in the deep gluteal space is a major clinical problem due to microsurgical manipulations in this region are limited in scope. We offer new endoscopic approach to the sciatic nerve in the deep gluteal space which allows to perform microsurgical manipulations, neurophysiological mapping and electrode installation for the chronic nerve stimulation.
Material and method. 3 patients with sciatic neuropathy have been operated. Before the operation they suffered from neuropathic pain in the the posterior thigh and calf, reaching 7-8 points on the visual analog scale (VAS). Paresis of triceps surae and biceps femur also was occurred. We performed endoscopic approach to the deep gluteal space through a small incision under the gluteal fold. Microsurgical external and internal decompression of sciatic nerve was performed under the endoscopic control. Next, intra-trunk nerve mapping was performed to visualize sensory fibers. Cylindrical electrodes for chronic neurostimulation were directly placed on the sensory fibers of sciatic nerve.
Results. Pain relief was obtained in all cases after activating the simulator, the patient noted a 50% reduction in pain. Muscle straight restoration was observed in all cases 2-3 months later. The clinical effect was stable in the follow up (6 months).
64 |
ВОПРОСЫ НЕЙРОХИРУРГИИ 5, 2020 |

Оригинальные статьи |
Original articles |
Conclusion. This technique, combining minimal invasiveness and intraoperative neurophysiological control, makes it possible to optimally position the electrode, both to achieve positive analgesic effect and for potential restoration of nerve function.
Keywords: posttraumatic neuropathy, sciatic nerve, endoscopic technics, chronic neurostimulation.
Information about the authors:
Dekopov A.V. — https://orcid.org/0000-0002-3834-5579; e-mail: adekopov@nsi.ru* Tomsky A.A. — https://orcid.org/0000-0002-2120-0146
Isagulyan E.D. — https://orcid.org/0000-0003-1191-9357 Ogurtsova A.A. — https://orcid.org/0000-0003-3595-2696 Kozlova A.B. — https://orcid.org/0000-0002-8366-8254 * — corresponding author
To cite this article:
Dekopov AV, Tomsky AA, Isagulyan ED, Ogurtsova AA, Kozlova AB. Treatment of sciatic posttraumatic neuropathy with chronic neuromodulation and endoscopic technics. Burdenko’s Journal of Neurosurgery = Zhurnal voprosy neirokhirurgii imeni N.N. Burdenko. 2020;84(5):64–71. (In Russ.) https://doi.org/10.17116/neiro20208405164
Список сокращений |
|
ВАШ — визуально-аналоговая шкала |
|
УЗИ — ультразвуковое исследование |
|
Повреждение седалищного нерва в подъягодич- |
ляции. Одним из путей решения вышеперечислен- |
ной области представляет собой актуальную клини- |
ной проблемы может быть применение эндоскопи- |
ческую проблему. Границы этой области составляют |
ческой техники. |
шейка бедра спереди, большая ягодичная мышца сза- |
Цель исследования — разработка эндоскопиче- |
ди, крестцово-бугорная связка медиально, нижний |
ского доступа к седалищному нерву, позволяюще- |
край седалищной вырезки сверху и мышцы задней |
го проводить микрохирургические манипуляции, |
группы бедра снизу. Из-за анатомических особен- |
нейрофизиологическое картирование и импланта- |
ностей седалищный нерв до выхода из-под большой |
цию электродов для хронической нейростимуляции. |
ягодичной мышцы труднодоступен прямому обзо- |
|
ру, что ограничивает объем возможных хирургиче- |
Материал и методы |
ских манипуляций. |
|
К повреждению седалищного нерва в этой обла- |
На сегодняшний день для эндоскопического до- |
сти может приводить травма, в том числе и тракци- |
ступа к седалищному нерву в подъягодичной области |
онная, поскольку нерв в подъягодичном простран- |
применяется артроскопическая методика с установ- |
стве наименее мобилен. К другим причинам отно- |
кой двух основных портов: переднелатерального и за- |
сят ортопедические вмешательства на тазобедренном |
днелатерального по отношению к большому вертелу |
суставе, инфекционно-воспалительные заболева- |
бедренной кости. Обычно их бывает достаточно для |
ния (постинъекционные абсцессы). При таком высо- |
полной ревизии ствола седалищного нерва, начиная |
ком уровне поражения развивается клиническая кар- |
от квадратной мышцы бедра до грушевидной мышцы |
тина невропатии седалищного нерва с выпадением |
[1]. Эта методика эффективно применяется для де- |
функции задней группы мышц бедра и мышц голени. |
компрессии седалищного нерва у больных с глубин- |
При этом нарушается сгибание ноги в коленном су- |
ным ягодичным синдромом (deep gluteal syndrome). |
ставе и развивается парез стопы, что инвалидизирует |
Его причиной является компрессия ствола седалищ- |
больных. Помимо моторного дефицита у больных ча- |
ного нерва фиброзным тяжом (анатомический вари- |
сто развивается нейрогенный болевой синдром. |
ант развития) или гипертрофированными отделами |
Нейрохирургическое лечение невропатии седа- |
грушевидной, близнецовой и внутренней запиратель- |
лищного нерва предполагает проведение ревизион- |
ной мышцы. В этих случаях эндоскопическая деком- |
ных операций, направленных на наружную и вну- |
прессия имеет хороший клинический эффект и мо- |
треннюю декомпрессию нерва и реконструктивных |
жет привести к полному регрессу симптоматики [2]. |
операций. Для купирования болевого синдрома ши- |
Однако у больных с посттравматическими невро- |
роко применяется методика хронической электрости- |
патиями седалищного нерва может оказаться недо- |
муляции периферических нервов. Однако в подъяго- |
статочно проведения только внешней декомпрессии |
дичной области возможности микрохирургических |
для достижения положительного эффекта. Это свя- |
манипуляций ограничены, а установка электродов на |
зано с развитием внутриствольного рубцово-спаеч- |
ствол седалищного нерва без прямого обзора и ней- |
ного процесса на большом протяжении. Для адек- |
рофизиологического картирования может привести |
ватной декомпрессии фасцикулярных пучков у та- |
к неэффективности противоболевой нейростиму- |
ких больных требуется выполнение эндоневролиза, |
BURDENKO'S JOURNAL OF NEUROSURGERY 5, 2020 |
65 |
Оригинальные статьи |
Original articles |
|
|
|
|
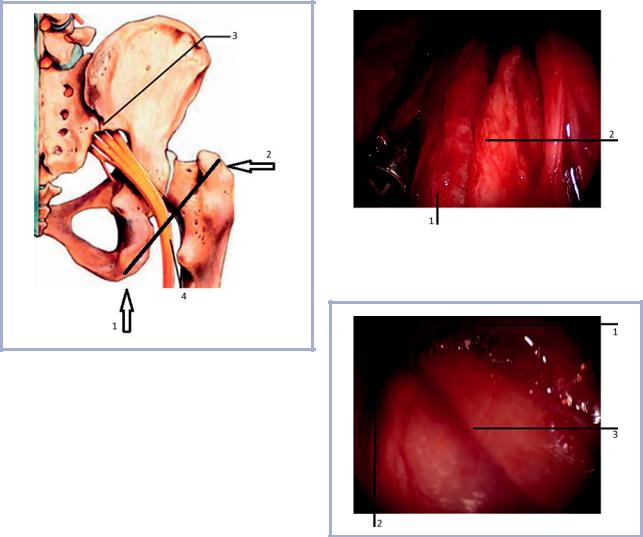
Рис. 1. Схема доступа к седалищному нерву. 1 — большой вертел; 2 — седалищный бугор; 3 — крестцово-подвздошное сочленение; 4 — направление доступа.
а для купирования нейрогенного болевого синдрома — применение методики хронической нейростимуляции [3].
В связи с необходимостью применения эндоневролиза при внутриствольных повреждениях нерва и позиционирования системы для нейростимуляции у таких больных нами предлагается вариант эндоскопического доступа к седалищному нерву в подъягодичной области.
Хирургическая техника
Хирургическое вмешательство выполнялось в условиях общего обезболивания с эндотрахеальной интубацией в положении лежа на животе. В ходе операции применялся интраоперационный нейрофизиологический мониторинг, включающий в себя стимуляционную электромиографию с регистрацией М-ответов мышц при электростимуляции моторных волокон седалищного нерва и регистрацию соматосенсорных вызванных потенциалов при электростимуляции сенсорных волокон седалищного нерва.
Игольчатые электроды для проведения стимуляционной электромиографии помещали в двуглавую мышцу бедра, полусухожильную мышцу, икроножную мышцу и переднюю большеберцовую мышцу.
Разрез кожи длиной 4 см выполняли в области пересечения ягодичной складки с проекционной линией ствола седалищного нерва, которая проходит от середины расстояния между седалищным бугром и большим вертелом бедренной кости (толстая линия
Рис. 2. Наружный невролиз седалищного нерва. 1 — ствол седалищного нерва; 2 — область рубца.
Рис. 3. Подгрушевидное отверстие и седалищный нерв. 1 — грушевидная мышца; 2 — подгрушевидное отверстие; 3 — седалищный нерв.
на рис. 1) к середине подколенной ямки. При этом доступе мы не использовали методику ультразвуковой навигации, так как анатомические ориентиры в этой области позволяют точно выйти на ствол нерва. После рассечения фасции визуализировался седалищный нерв латеральнее двуглавой мышцы бедра. Затем под большую ягодичную мышцу вводили ретрактор, создавая тем самым пространство для хирургических манипуляций. По ходу ствола седалищного нерва в краниальном направлении вводили эндоскоп (Karl Storz, Германия) 30° с рабочим каналом. Для улучшения видимости проводили ирригацию физиологическим раствором с одномоментной аспирацией отсосом. Ревизию седалищного нерва проводили на всем протяжении до уровня выхода из подгрушевидного отверстия. Во всех случаях седалищный нерв в подъягодичной области окружен плотной рубцовой тканью. Удаление посттравматического рубца проводилось при помощи ножниц и кусачек (рис. 2).
66 |
ВОПРОСЫ НЕЙРОХИРУРГИИ 5, 2020 |
Оригинальные статьи |
|
Original articles |
|
|
|
|
|
|
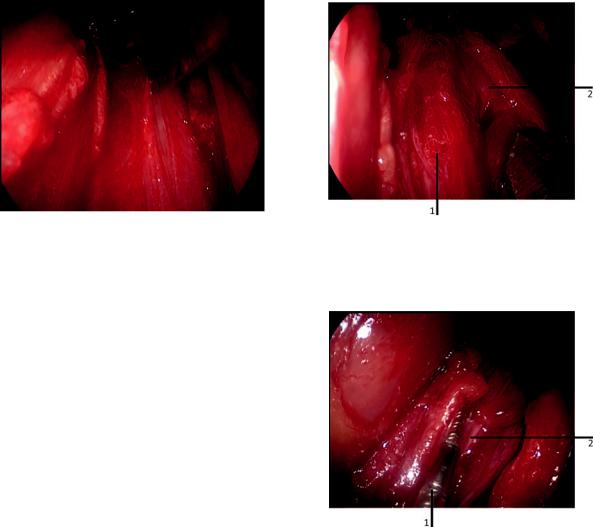
Рис. 4. Эндоневролиз седалищного нерва. Вскрытие эпиневрия. |
Рис. 5. Эндоневролиз седалищного нерва. Препаровка фасцикул. |
|
|
1 — большеберцовая порция; 2 — малоберцовая порция. |
|
Наружный невролиз выполняли до области подгру- |
|
|
шевидного отверстия. В области подгрушевидного |
|
|
|
||
отверстия нерв во всех случаях был интактен и окру- |
|
|
жен жировой тканью (рис. 3). После этого через ра- |
|
|
бочий канал эндоскопа вводили электрод для интра- |
|
|
операционной электростимуляции. |
|
|
Проводилась регистрация спонтанной и триггер- |
|
|
ной электромиограммы. Изменение фоновой элек- |
|
|
тромиограммы, появление выраженных осцилляций |
|
|
на спонтанной электромиограмме исследуемых групп |
|
|
мышц свидетельствовало о приближении к нерву. |
|
|
С целью идентификации ветвей седалищного нерва |
|
|
проводили прямую электростимуляцию с регистра- |
|
|
цией моторных вызванных ответов на исследуемых |
|
|
мышцах. Регистрацию соматосенсорных вызванных |
|
|
потенциалов проводили путем внутриствольной сти- |
|
|
муляции седалищного нерва и регистрации сомато- |
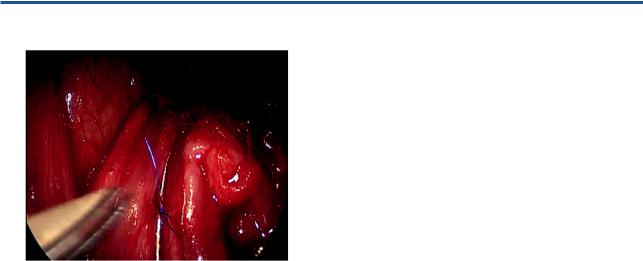
Рис. 6. Установка электрода. 1 — электрод; 2 — сенсорные фас- |
|
сенсорных вызванных ответов в проекции чувстви- |
||
цикулы. |
||
тельной зоны коры контралатерального полушария. |
||
|
||
Как правило, после выполнения наружного не- |
|
|
вролиза моторные ответы были низкоамплитудными |
ние системы производили на 2-е сутки после опе- |
|
и неустойчивыми. Поэтому во всех случаях выпол- |
рации. Хроническая стимуляция проводилась в по- |
|
няли эндоневролиз: на всем протяжении утолщения |
стоянном режиме с параметрами 80—130 Гц, 200— |
|
ствола седалищного нерва проводили вскрытие эпи- |
400 мкс, 2—4 В. |
|
неврия и препаровку на фасцикулярные пучки при |
|
|
помощи ножниц (рис. 4, 5). После эндоневролиза ам- |
Результаты |
|
плитуда моторных ответов во всех случаях нарастала. |
|
|
Далее проводилось внутриствольное картирование |
|
|
нерва для визуализации сенсорных волокон под кон- |
Клинический случай 1 |
|
тролем соматосенсорных вызванных потенциалов. |
Пациентке в возрасте 49 лет произвели внутри- |
|
Непосредственно на сенсорные волокна укладыва- |
||
лись цилиндрические электроды для хронической |
мышечную инъекцию анальгина в проекции про- |
|
нейростимуляции, которые вводились через рабочий |
хождения ствола седалищного нерва. После инъек- |
|
канал эндоскопа (рис. 6). Контакты электрода при |
ции появился болевой синдром в ягодичной области |
|
этом размещались проксимальнее уровня повреж- |
с иррадиацией по задней поверхности бедра. Затем |
|
дения. Фиксацию электрода к эпиневрию проводи- |
развился парез в задней группе мышц бедра и в мыш- |
|
ли узловыми швами нитью 6-0 (рис. 7). Импланта- |
цах голени. Консервативное лечение в течение 6 мес |
|
цию генератора импульсов осуществляли в верхнюю |
не дало клинического эффекта. Перед хирургическим |
|
ягодичную область. Включение и программирова- |
лечением в неврологическом статусе отмечался па- |
BURDENKO'S JOURNAL OF NEUROSURGERY 5, 2020 |
67 |
Оригинальные статьи Original articles
|
верхности бедра, голени и в стопе. Консервативное |
|
лечение в течение 6 мес не дало существенного кли- |
|
нического эффекта. Перед хирургическим лечением |
|
в неврологическом статусе отмечалось полное выпа- |
|
дение функции трехглавой мышцы голени и передней |
|
большеберцовой мышцы, глубокий парез двуглавой |
|
мышцы бедра со снижением силы до 2 баллов. От- |
|
мечался нейрогенный болевой синдром по задней |
|
поверхности бедра и голени, достигавший 7—8 бал- |
|
лов по ВАШ. При УЗИ седалищного нерва выявлены |
|
диффузные внутриствольные изменения седалищно- |
|
го нерва после выхода из подгрушевидного отверстия |
|
на протяжении 5 см. В течение первых суток после |
|
выполнения операции (15.02.2019) отмечалось умень- |
|
шение болевого синдрома на 1—2 балла по ВАШ. |
|
|
Рис. 7. Фиксация электрода. |
После включения системы для хронической нейро- |
|
стимуляции в течение двух суток больной отметил |
рез трехглавой мышцы голени со снижением силы |
уменьшение болевого синдрома на 50%. Нарастания |
до 3 баллов, парез передней большеберцовой мышцы |
мышечной силы в раннем послеоперационном пе- |
и разгибателя пальцев со снижением силы до 3 бал- |
риоде не было. Спустя 3 мес после операции у боль- |
лов и парез задней группы мышц бедра со снижением |
ного появились движения в стопе, начала нарастать |
силы до 4 баллов. Отмечался нейрогенный болевой |
сила в задней группе мышц бедра. При контрольном |
синдром в ягодичной области, по задней поверхно- |
осмотре через 9 мес после операции мышечная сила |
сти бедра и голени, достигавший 7—8 баллов по ви- |
в икроножной и передней большеберцовой мышце |
зуально-аналоговой шкале (ВАШ). При ультразву- |
выросла до 3 баллов, в бицепсе бедра — до 4 баллов. |
ковом исследовании (УЗИ) седалищного нерва от- |
На фоне хронической нейростимуляции уровень бо- |
мечались диффузные внутриствольные изменения |
левого синдрома составлял 3—4 балла по ВАШ. Па- |
седалищного нерва после выхода из подгрушевидно- |
циент продолжает хроническую нейростимуляцию |
го отверстия на протяжении 4 см. В течение первых |
в постоянном режиме. |
суток после выполнения операции (28.03.2018) от- |
|
мечалось уменьшение болевого синдрома на 2 балла |
Клинический случай 3 |
по ВАШ. На 4-е сутки после операции наблюдалось |
|
увеличение мышечной силы в задней группе мышц |
Больной в возрасте 35 лет проведено эндопроте- |
бедра на 1 балл и увеличение объема активных дви- |
зирование тазобедренного сустава по поводу асепти- |
жений в коленном суставе. Включение системы для |
ческого некроза головки бедренной кости. Сразу по- |
хронической нейростимуляции проводилось на 2-е |
сле операции выпали движения в стопе — и развил- |
сутки после операции. При подборе параметров сти- |
ся парез в задней группе мышц бедра со снижением |
муляции добивались возникновения парестезий в зо- |
силы до 3 баллов. Одновременно появился нейро- |
не болевого синдрома — по задней поверхности бе- |
генный болевой синдром по задней поверхности бе- |
дра, голени и в стопе. На фоне хронической стиму- |
дра и голени до стопы (до 9 баллов по ВАШ) с вегета- |
ляции достигнут полный регресс болевого синдрома. |
тивным компонентом — отеком бедра и голени. Кон- |
Этот эффект сохраняется по настоящее время. Мы- |
сервативное и реабилитационное лечение в течение |
шечная сила в задней группе мышц бедра восстано- |
6 мес было полностью неэффективным. При УЗИ |
вилась до уровня нормы, увеличился объем сгибания |
седалищного нерва отмечались диффузные внутри- |
бедра в коленном суставе и движений в стопе. Паци- |
ствольные изменения седалищного нерва на уровне |
ентка продолжает хроническую нейростимуляцию |
вертлужной впадины. В течение первых суток после |
в постоянном режиме. |
операции (20.02.2019) отмечено уменьшение болевого |
|
синдрома в ноге на 2—3 балла. После включения си- |
Клинический случай 2 |
стемы для хронической нейростимуляции в течение |
|
двух суток больная отметила уменьшение болевого |
Пациент в возрасте 65 лет перенес внутримышеч- |
синдрома на 50%. Спустя 3 мес после хирургического |
ную инъекцию клафорана в проекцию прохождения |
лечения отмечено нарастание мышечной силы в зад- |
ствола седалищного нерва. После нее развилась ане- |
ней группе мышц бедра до 4—4,5 балла и в икронож- |
стезия по задней поверхности бедра и голени, выпали |
ной мышце до 2 баллов. Появилось тыльное сгиба- |
движения в стопе, и развился глубокий парез в зад- |
ние пальцев. Увеличился объем сгибания в коленном |
ней группе мышц бедра. Спустя месяц у него поя- |
суставе, а также появились сгибательные движения |
вился нейрогенный болевой синдром по задней по- |
в голеностопном суставе. Тяжесть болевого синдро- |
68 |
ВОПРОСЫ НЕЙРОХИРУРГИИ 5, 2020 |

Оригинальные статьи Original articles
ма на фоне нейростимуляции снизилась до уровня 2 |
лась на степени послеоперационного болевого син- |
баллов. Пациентка продолжает хроническую нейро- |
дрома в ягодичной области. |
стимуляцию в постоянном режиме. |
Хроническая электростимуляция перифериче- |
|
ских нервов применяется с 1967 г. Впервые методику |
Обсуждение |
при болевом синдроме применили P.D. Wall и W.H. |
|
Sweet — электроды имплантированы на срединный |
Впервые эндоскопическая методика в хирургии |
и локтевой нерв [8]. Механизм противоболевого эф- |
периферических нервов применена в 1999 г. при де- |
фекта, предположительно, связан с активацией тол- |
компрессии локтевого нерва на уровне кубитально- |
стых миелинизированных А-волокон, что, в свою |
го канала [4]. Это открыло принципиально новые |
очередь, блокирует вставочные нейроны (интерней- |
возможности выполнения вмешательств на нервных |
роны) в заднем роге спинного мозга, через которые |
стволах из минимально инвазивного доступа. Откры- |
осуществляется передача болевых стимулов по тон- |
тые операции на нервных стволах, требующие боль- |
ким С-волокнам. Помимо этого, электростимуляция |
ших разрезов и значительной травматизации мягких |
может непосредственно изменять возбудимость пе- |
тканей в ходе операции, могут сами по себе приво- |
риферических нервных волокон [9, 10]. |
дить к развитию рубцово-спаечного процесса и ре- |
Наиболее часто периферическая нейростимуля- |
цидива компрессии нерва [5]. Особенно актуально |
ция применяется при мононевропатиях верхних ко- |
применение эндоскопической техники в труднодо- |
нечностей и тригеминальной невралгии [11]. Счи- |
ступных анатомических областях, к примеру, в подъ- |
тается, что периферическая нейростимуляция недо- |
ягодичной области. Хирургический доступ к стволу |
статочно эффективна при невропатиях седалищного |
седалищного нерва в этой области требует глубокого |
нерва. Это связано как с большими размерами ствола |
рассечения и тракции волокон большой ягодичной |
нерва, так и с тем, что сенсорные волокна проходят |
мышцы. Это сопряжено со значительной травмати- |
не по поверхности, а внутри ствола и не могут быть |
зацией мягких тканей. Поэтому открытые операции |
полностью охвачены электрическим полем [12]. По- |
могут приводить к ряду послеоперационных ослож- |
этому при болевых синдромах в результате невропа- |
нений (послеоперационной гематоме, инфекцион- |
тии седалищного нерва прибегают к методике хро- |
ным осложнениям, плохому косметическому резуль- |
нической электростимуляции поясничного утолще- |
тату, прогрессии рубцово-спаечного процесса в отда- |
ния спинного мозга [13]. |
ленном периоде и рецидивам болевого синдрома) [1, |
Имплантация электродов на периферический |
6]. Применение эндоскопической техники позволяет |
нерв чаще всего проводится через иглу под ультра- |
избежать таких осложнений, добиться хорошего кос- |
звуковым контролем [14]. Эта методика имеет су- |
метического результата и сократить период после- |
щественный недостаток, заключающийся в том, что |
операционной реабилитации [7]. В нашей серии на- |
в процессе имплантации невозможно проводить |
блюдений также не было каких-либо послеопераци- |
нейрофизиологическое картирование нерва с це- |
онных осложнений и рецидивов болевого синдрома |
лью определения локализации сенсорных волокон. |
в течение 6 мес. |
В результате электрод может быть размещен над мо- |
Во всех трех случаях седалищный нерв имел вну- |
торными фасцикулами, что может привести, с од- |
триствольные повреждения, что требовало выполне- |
ной стороны, к недостаточному противоболевому |
ния эндоневролиза для достижения оптимального |
эффекту, а с другой стороны, к развитию побочных |
клинического эффекта. В связи с этим нами предло- |
эффектов во время нейростимуляции в виде непро- |
жен модифицированный вариант эндоскопического |
извольных мышечных сокращений. В ходе эндоско- |
доступа к седалищному нерву в подъягодичной об- |
пической имплантации мы проводили нейрофизио- |
ласти. В отличие от стандартного эндоскопического |
логическое картирование нерва после выполнения |
доступа через порты, устанавливаемые под рентге- |
эндоневролиза. Это позволило разместить контакт- |
нологическим контролем, наш доступ требовал вы- |
ные поверхности электрода непосредственно над сен- |
полнения небольшого разреза на уровне ягодичной |
сорными фасцикулами седалищного нерва. Правиль- |
складки. По степени травматичности он сравним со |
ное позиционирование электрода дало возможность |
стандартным эндоскопическим доступом. Создание |
полного охвата зоны боли стимуляцией и во всех слу- |
рабочего пространства при стандартном эндоско- |
чаях привело к уменьшению выраженности болево- |
пическом доступе достигается за счет нагнетания |
го синдрома. |
в подъягодичное пространство физиологического |
Во всех трех случаях отмечены, помимо проти- |
раствора, который рассасывается из мягких тканей |
воболевого эффекта, улучшение двигательных функ- |
в течение 2—3 сут. Это может создавать для больного |
ций и нарастание силы в мышцах нижней конечно- |
дополнительный дискомфорт. Мы использовали ре- |
сти. По результатам данного исследования трудно |
трактор при выполнении эндоскопического доступа |
оценить, какой вклад в восстановление двигательных |
для создания рабочего пространства. Локальная трак- |
функций могла внести хроническая электростимуля- |
ция большой ягодичной мышцы никак не сказыва- |
ция седалищного нерва. В ряде исследований отмече- |
BURDENKO'S JOURNAL OF NEUROSURGERY 5, 2020 |
69 |
