
Pod_red_prof_Nikonova_V_V_dots_Feskova_A_E_3
.pdfМетаболическая терапия гипоксических состояний |
11 |
|
|
Втечение многих десятилетий, если не больше, ученые, практические врачи, фармакологи пытаются разработать лекарственные препараты, которые бы стабилизировали нарушенные функции организма независимо от этиологического фактора, естественно не подменяя этим лекарством определенную специфическую терапию. Основой реализации их терапевтической активности является модуляция обменных процессов, что проявляется усилением адаптационных процессов организма.
Воснове создания этой группы препаратов лежит принцип: метаболические средства в той или иной степени должны быть естественными субстратами или модулировать их синтез de novo и, естественно, что действие средств метаболической направленности должно реализовываться в условиях патологического состояния. Другими словами, указанная группа препаратов («метаболики»; протекторы; антигипоксанты; антиоксиданты) должны в условиях стресса (повреждения, заболевания) предупредить или уменьшить повреждающее действие гипоксии, сохра-
нить целостность окислительного фосфорилирования (выработку АТФ)сохранить орган-мишень и/или организм в целом.
Метаболическая терапия дает возможность поддерживать или замещать некоторые жизненные функции организма до восстановления их ауторегуляции, когда долгий путь выздоровления будут контролировать уже сами восстановленные ауторегулируемые функции.
Вдалекие годы прошлого столетия в качестве «метаболика» использовалась с определенным успехом 40% глюкоза, вводимая внутривенно, потом она сочеталась с введением витаминов группы В, и клиницисты тех времен для лечения истощающих заболеваний использовали большие, а иногда и мегадозы указанных витаминов. И нужно признать, что эти меры действительно значимо улучшали состояние пациентов при инфаркте миокарда, пневмониях, тяжелых стрессах. Не менее интересным и действенным метаболическим препаратом был кагор, настоящее церковное вино. Оно обладало высокой энергетической ценностью, и его использовали еще в дореволюционной России. Мы предвидим скептические и негодующие возгласы приверженцев доказательной медицины, но это работало, и за этими назначениями лежит практический опыт многих тысяч врачей, тысячи спасенных жизней. К этому нужно относиться с уважением!
Необходимо вспомнить и о научных исследованиях алхимиков, которые многие столетия назад в качестве «эликсира жизни» использовали янтарную кислоту, которая в XXI столетии становится ведущим метаболическим препаратом.
12 |
Медицина неотложных состояний. Избранные клинические лекции. Том 4 |
|
|
Несколько десятилетий назад, учитывая патофизиологические процессы, протекающие при гипоксии, Лабори предложил применение поляризующей смеси при критических состояниях. То есть сочетание глюкозы, инсулина, калия и магния значительно уменьшает повреждающее действие гипоксии за счет энергетического субстрата глюкозы, запасы которой быстро истощаются при тяжелых заболеваниях и травмах; восстановление полярности клетки — закачка в нее K+ и Mg+ — способствует нормальному функционированию мембраны, предупреждает/ уменьшает развитие кальциевого парадокса. Плюс анаболическое действие малых доз инсулина… Этот список можно продолжать и дальше.
Но давайте, не отвергая и применяя в дальнейшем опыт наших учителей, вернемся в сегодняшний день.
Одним из самых эффективных и перспективных путей профилактики и терапии гипоксических/ишемических повреждений, следовательно, лечения различной тяжелой патологии в практике интенсивной терапии представляется применение антигипоксантов — фармакологических средств, ослабляющих или ликвидирующих гипоксические нарушения (гипоэргоз) путем поддержания и повышения энергопродукции в системе митохондриального окислительного фосфорилирования. Родоначальником этого направления был В.М. Виноградов, под руководством которого были созданы первые «истинные» антигипоксанты — гутимин и амтизол, которые с успехом применялись при критических состояниях с ишемическими и гипоксическими расстройствами. Эти препараты и препараты, которые применяются сейчас в клинической практике, подавляют или ослабляют активацию ПОЛ-СРО, что также способствует улучшению энергетического потенциала клетки.
Очевидно, вам, дорогие коллеги, понятна суть проблемы, и мы представляем классификацию антигипоксантов и приводим краткую характеристику наиболее широко используемых в практике препаратов.
Классификация антигипоксантов
1. Препараты с поливалентным действием.
1.1.Производные амидинотиомочевины. Эндогенные соединения: гутимин, амтизол.
1.2.Ингибиторы окисления жирных кислот: триметазидин (предуктал), ранолазин, милдронат, пергексилин, этомоксир, карнитин (карнитен).
2. Сукцинатсодержащие и сукцинатобразующие средства: реамберин, мексидол (мексикор, мексифин), оксибутират натрия, цитофлавин, мафусол.
Метаболическая терапия гипоксических состояний |
13 |
|
|
3.Естественные компоненты дыхательной цепи: цитохром С (цитомак), убихинон (убинон), идебенон.
4.Искусственные редокс-системы: олифен (гипоксен).
5.Макроэргические соединения: кислота аденозинтрифосфорная (АТФ), креатинфосфат (неотон).
Еще раз вернемся к механизму противогипоксического действия гутимина и амтизола на молекулярном уровне. Он обусловлен опти-
мизацией функций митохондрий. При гипоксии они стабилизируют митохондриальные мембраны, уменьшают угнетение дегидрогеназ цикла Кребса, предотвращают разобщение окисления и фосфорилирования, увеличивая тем самым продукцию АТФ на единицу потребляемого дефицитного кислорода.
Определенный вклад в антигипоксическое действие гутимина и амтизола вносит их способность снижать кислородный запрос тканей благодаря ингибированию нефосфорилирующих видов окисления микросомального и свободнорадикального. В результате кислород экономится для потребления в энергопродуцирующих окислительных реакциях в митохондриях.
Четко установленным компонентом антигипоксического действия гутимина и амтизола является активация гликолиза с увеличением анаэробного образования АТФ. Данные антигипоксанты помимо уменьшения образования лактата усиливают его утилизацию в реакциях глюконеогенеза, обеспечивая тем самым и ресинтез углеводов, запасы которых в организме невелики. Таким образом, активируя энергопродукцию в процессе гликолиза, гутимин и амтизол не только не усугубляют метаболический ацидоз при гипоксии, но, напротив, ослабляют его проявления и обеспечивают восстановление углеводных источников энергии.
В большом числе экспериментальных и клинических исследований получены доказательства высокой эффективности этих препаратов при шоке различного генеза, инфаркте миокарда, гипоксии и ишемии сердца, почек и печени при хирургических операциях на этих органах, инсультах, внутриутробной гипоксии плода и слабости родовой деятельности, дыхательной недостаточности разной природы, включая хирургические вмешательства на легких, кровопотере, в том числе во время операции, послеоперационных парезах кишечника, менингококковой инфекции.
Средствами, близкими по фармакологическим свойствам (но не по строению) к гутимину и амтизолу, являются препараты — ингибиторы окисления жирных кислот. Среди них особого внимания заслуживает парциальный ингибитор окисления жирных кислот (милдронат).
14 |
Медицина неотложных состояний. Избранные клинические лекции. Том 4 |
|
|
Милдронат обратимо ограничивает скорость биосинтеза карнитина из его предшественника — гамма-бутиробетаина. Вследствие этого нарушается карнитинопосредованный транспорт длинноцепочечных жирных кислот через мембраны митохондрий без воздействия на метаболизм короткоцепочечных жирных кислот. Частичная блокада окисления жирных кислот включает альтернативную систему производства энергии — окисление глюкозы, которая значительно эффективнее использует кислород для синтеза АТФ.
В настоящее время с успехом применяются препараты янтарной кислоты.
Основные элементы механизма действия янтарной кислоты
Ускорение оборота |
|
|
Улучшение тканевого |
дикарбоновой части ЦТК |
|
|
дыхания за счет усиления |
(сукцинат — фумарат — |
|
|
транспорта электронов в |
малат), снижение концен- |
|
|
митохондриях, воссозда- |
трации лактата, увеличе- |
|
|
ния протонного градиента |
ние объема энергии для |
|
|
на их мембранах и смеще- |
химических синтезов |
|
|
ния кривой диссоциации |
за счет восстановления |
|
|
оксигемоглобина вправо — |
пула НАД+ и сукцинатокси- |
|
|
увеличение потребления |
дазного окисления |
ЯК |
кислорода тканями |
|
|
|
||
|
|
||
|
|
|
|
Увеличение пула системы |
|
|
Активация ЯК троп- |
|
|
ного ей фермента — |
|
глутатиона |
|
|
|
|
|
фосфорилирование белков |
|
|
|
|
|
|
|
|
|
|
|
|
|
Участие в ресинтезе эндогенного ГАМК через -кетоглутаровую кислоту и янтарный полуальдегид (в нервной ткани)
Рисунок 3. ЦТК — цикл трикарбоновых кислот; ЯК — янтарная кислота; НАД+ — коферменты дегидрогеназ;
ГАМК — гамма-аминомасляная кислота
Одним из препаратов, созданных на основе янтарной кислоты, является реамберин — 1,5% раствор для инфузий, представляющий собой сбалансированный полиионный раствор с добавлением смешанной натрий-N-метилглюкаминовой соли янтарной кислоты. Осмолярность этого раствора приближена к осмолярности плазмы человека. В/в инфузия реамберина сопровождается повышением рН и буферной емкости крови. В дополнение к антигипоксантной активности реамберин обладает дезинтоксикационным и антиоксидантным действием.

Метаболическая терапия гипоксических состояний |
15 |
|
|
Механизм действия реамберина (В.В. Афанасьев, 2008)
Биохимические основы действия реамберина
—Входящий в состав реамберина сукцинат является естественным эндогенным субстратом клетки. Назначение экзогенного сукцината сопровождается двумя основными изменениями, которые происходят
вуглеводном обмене веществ и окислительном фосфорилировании.
—Янтарная кислота (ЯК) ускоряет оборот дикарбоновой части ЦТК (сукцинат — фумарат — малат) и снижает концентрации лактата, пирувата (в меньшей степени)1 и цитрата, которые накапливаются
вклетках во время гипоксии. Таким образом, она повышает кругооборот ЦТК, следовательно, увеличивает объем энергии, необходимой для синтеза АТФ (и других химических синтезов, например ГАМК).
—Увеличение количества субстрата (сукцината) позволяет осуществлять фосфорилирование белков вследствие активации субстратом тропного ему фермента.
—ЯК увеличивает потребление кислорода тканями и улучшает тканевое дыхание за счет усиления транспорта электронов в митохондриях, воссоздания протонного градиента на их мембранах и смещения кривой диссоциации оксигемоглобина вправо (Розенфельд А.Д., 1983), т.е. усиливает отдачу кислорода тканям.
—Интенсивность окисления сукцината зависит от его концентрации в клетке, а также от присутствия активаторов биотрансформации ЯК (Нарциссов Р.П., 1997), т.е. от наличия предшествующих сукцинату и следующих после него биохимических субстратов. Это очень важное положение для практического применения реамберина в сочетании с препаратами других фармакологических групп. При низких и средних концентрациях сукцината восстанавливается пул НАД+, при высоких — возникает сукцинатоксидазное окисление, возрастает антиоксидантная функция системы глютатиона (Ивницкий Ю.Ю., 1998).
—В условиях гипоксии экзогенно вводимый сукцинат (входящий
всостав реамберина) может поглощаться через альтернативный метаболический путь сукцинатоксидазной системы с последующим потреблением ЯК в дыхательной цепи митохондрий.
—Участие в ресинтезе эндогенного ГАМК через -кетоглютаровую кислоту и янтарный полуальдегид (в нервной ткани). Здесь ЯК обес-
1 По некоторым данным, концентрация ПВК может незначительно возрастать.
16 |
Медицина неотложных состояний. Избранные клинические лекции. Том 4 |
|
|
печивает кругооборот ЦТК, выход -КГ из митохондрий, при наличии которого возможен ресинтез ГАМК. Как холинореактивные системы эволюционно призваны защищать нейроны головного мозга от избытка катехоламинергических воздействий, так ГАМК противодействует НМДА-рецепторам, возбуждение которых сопровождается эксайтотоксичностью. Это свойство ЯК расширяет возможности применения реамберина, так как создает основу для его назначения в терапии хронических дегенеративно-дистрофических неврологических заболеваний, постабстинентных синдромов, в основе которых лежит эксайтотоксичность (таких как демиелинизирующие процессы, сирингомиелия, рассеянный склероз и т.д. или адренергический синдром при алкогольном абстинентном синдроме).
Системные эффекты реамберина
Улучшение микроциркуляции в органах и тканях, которое проявляется:
—снижением зоны некроза в миокарде (Клигуленко Е.Н., 2004);
—редукцией зоны пенумбры при ЧМТ (Цивинский А.Д., 2004);
—сокращением зоны «ишемической» пенубры при инсульте (Румянцева С.А., 2001);
—восстановлением моторной функции кишечника; снижением интенсивности эндогенной интоксикации (Клигуленко Е.Н., 2004);
—снижением интенсивности ацидоза по метаболическим показателям кислотно-основного состояния (КОС), таким как ВВ и BE (Оболенский С.В., 2003).
Введение реамберина сопровождается незначительным ростом центрального венозного давления (ЦВД) (через 12 ч после начала лечения) без признаков гиперволемии (Челнов И.Г., 2002). Среди других явлений отмечают:
—положительную динамику воспаления, которая проявляется улучшением показателей «белой» крови (снижение лейкоцитоза с нормализацией палочкоядерного сдвига в среднем на 5-е сутки от момента введения препарата, нарастание числа лимфоцитов, снижение СОЭ и концентрации провоспалительных цитокинов) (Куликова О.Д., 2002; Челнов И.Г. с соавт., 2002);
—повышение антитоксической функции печени в виде снижения интенсивности гиперферментемии (АЛТ, ACT), билирубинемии; повышение уровня сульфгидрильных групп (Оболенский С.В., 2003);
—редукцию адренергических проявлений абстинентного

Метаболическая терапия гипоксических состояний |
17 |
|
|
синдрома (Афанасьев В.В., 2002) — антистрессорное действие (Романцов М.Г., 2002);
—улучшение функциональной активности головного мозга (при лечении энцефалопатии) (Румянцева С.А., 2001), положительная динамика спектрограмм ЭЭГ (Оболенский С.В., 2003), ускоренное восстановление высшей нервной деятельности (ВНД) за счет снижения клинических проявлений астеновегетативного синдрома (Корнилова Н.Н., 2002), инициацию и поддержание адаптогенных реакций организма (Высочина И.В., 1997; Гаркави Л.X., 1997);
—диуретическое действие (максимально выраженное через 6–12 ч от начала лечения2, сопровождающееся повышением рН мочи (Оболенский С.В., 2003);
—улучшение транспорта кислорода, сдвиг кривой диссоциации оксигемоглобина влево и повышение потребления кислорода различными тканями, включая кожный покров (Розенфельд А.Д., 1983; Куликова О.Д., 2002);
—повышение пула естественных антиоксидантов и торможение процесса пероксидации собственных липидов, улучшение равновесия системы ПОЛ/АОС;
—снижение уровня глюкозы крови в интервале от 48 до 72 ч от начала лечения.
Разнообразие системных эффектов реамберина вытекает из молекулярных механизмов его действия, обобщающими компонентами которого служат антигипоксический и антиоксидантный эффекты препарата. Перечисленные молекулярные и системные эффекты реамберина сопровождаются отчетливым положительным клиническим действием препарата: снижением летальности и сокращением сроков пребывания больных в ОРИТ, в т.ч. наиболее тяжелых пациентов с перитонитом и полиорганной несостоятельностью (ПОН) (Оболенский С.В., 2003; Клигуненко Е.Н., 2004). Эти благоприятные стороны действия реамберина открывают новые возможности интенсивной терапии тяжелых больных.
Мексидол, мексикор — оксиметилэтилпиридина сукцинат — пред-
ставляет собой комплекс сукцината с антиоксидантом эмоксипином, обладающим относительно слабой антигипоксической активностью, облегчает транспорт сукцината через мембраны, что проявляется антигипоксическим эффектом. Подобно эмоксипину, мексидол является ингибитором свободнорадикальных процессов, но оказывает более
2 У детей (Челнов И.Г. и соавт., 2002).
18 |
Медицина неотложных состояний. Избранные клинические лекции. Том 4 |
|
|
выраженное антигипоксическое действие. Клинические испытания подтвердили эффективность мексидола при расстройствах ишемического генеза: острых нарушениях мозгового кровообращения, дисциркуляторной энцефалопатии, вегетососудистой дистонии, атеросклеротических нарушениях функций мозга, абстинентном синдроме при алкоголизме и наркомании, при инфаркте миокарда, ИМТ, сепсисе и множестве других состояний, сопровождающихся гипоксией тканей.
Препаратом комплексного метаболического действия является цитофлавин (рибоксин 200 мг, янтарная кислота 1000 мг, рибофлавин 20 мг, никотинамид 100 мг). Он стимулирует процессы клеточного дыхания и образования энергии, улучшает утилизацию кислорода тканями головного мозга, восстанавливает антиоксидантную активность. Цитофлавин активирует внутриклеточный синтез белка, способствует утилизации глюкозы, жирных кислот и ресинтезу гамма-аминомасляной кислоты в нейронах через шунт Робертса. Препарат обладает оптимальным противогипоксическим эффектом. Наш клинический опыт свидетельствует о высокой клинической эффективности указанных препаратов при различных состояниях, ассоциированных с гипоэргозом.
Со способностью превращаться в сукцинат в цикле Робертса связано, очевидно, и противогипоксическое действие оксибутирата натрия, хотя оно и не очень выражено. Трансаминирование ГАМК с альфакетоглутаровой кислотой является основным путем метаболической деградации ГАМК. Образующийся по ходу нейрохимической реакции полуальдегид янтарной кислоты с помощью семиальдегиддегидрогеназы при участии NAD окисляется в мозговой ткани в янтарную кислоту, которая включается в ЦТК. Такое дополнительное действие весьма полезно при использовании оксибутирата натрия в качестве общего анестетика. В условиях тяжелой циркуляторной гипоксии оксибутират в очень короткие сроки успевает не только запустить клеточные адаптационные механизмы, но и подкрепить их перестройкой энергетического обмена в жизненно важных органах. Поэтому не стоит ожидать сколько-нибудь заметного эффекта от введения малых доз анестетика. Средние дозы для натриевой соли оксибутирата составляют 70– 120 мг/кг (до 250 мг/кг, в этом случае антигипоксическое действие будет выражено максимально). Мононаркоз оксибутиратом натрия представляет собой минимально токсичный вид общей анестезии и поэтому имеет наибольшую ценность для больных в состоянии гипоксии различной этиологии (тяжелая острая легочная недостаточность,
Метаболическая терапия гипоксических состояний |
19 |
|
|
кровопотеря, гипоксические и токсические повреждения миокарда), показан пациентам с различными вариантами эндогенной интоксикации (в состоянии оксидативного стресса).
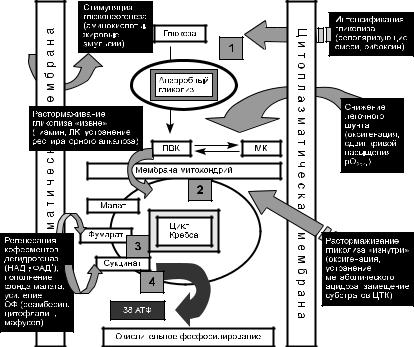
Рисунок 4. Способы воздействия на гликолиз и ЦТК в практике интенсивной терапии. Место цитофлавина (В.В. Афанасьев)
Примечания: расчетная эффективность использования глюкозы в обмене углеводов составляет 38 АТФ, а реальная — 25 АТФ (цит. по М.Я. Малаховой, 2005):
—три реакции субстратного фосфорилирования (№ 7; № 10 и одна в ЦТК) = 3 АТФ;
—пять реакций дегидрирования: акцептор НАД+ = 15 АТФ;
—одна реакция дегидрирования: акцептор убихинон = 20 АТФ. Условные обозначения: ЦТК — цикл трикарбоновых кислот; ПВК —
пировиноградная кислота; МК — молочная кислота; ЛК — липоевая кислота; ОФ – окислительное фосфорилирование; НАД+; ФАД+ — коферменты дегидрогеназ.
1,2,3,4 — точки приложения действия цитофлавина.
20 |
Медицина неотложных состояний. Избранные клинические лекции. Том 4 |
|
|
Мафусол содержит один из компонентов цикла Кребса — фумарат, хорошо проникающий через мембраны и легко утилизируемый в митохондриях. При глубокой гипоксии терминальные реакции цикла Кребса начинают протекать в обратном направлении, и фумарат превращается в сукцинат с накоплением последнего. При этом обеспечивается сопряженная регенерация окисленного НАД из его восстановленной при гипоксии формы и, следовательно, возможность энергопродукции в НАД-зависимом звене митохондриального окисления. При уменьшении глубины гипоксии направление терминальных реакций цикла Кребса меняется на обычное, при этом накопившийся сукцинат активно окисляется в качестве эффективного источника энергии. Антигипоксическое действие мафусола при различных критических состояниях (кровопотеря, шок, травма, интоксикация, острые нарушения мозгового кровообращения по ишемическому и геморрагическому типу) подтверждено в ходе клинических испытаний. Мафусол вводится внутривенно и внутриартериально; вначале вводят струйно, а при нормализации гемодинамических показателей — капельно. При состоянии средней тяжести вводят 2–3 литра, при тяжелом состоянии препарат комбинируют с кровью или коллоидными кровезаменителями, при этом доза мафусола должна быть не менее 1 литра. В случаях кровопотери, не превышающей 15 % объема циркулирующей крови (ОЦК) у взрослых и детей, может быть использован в качестве единственной инфузионной среды. Мафусол можно применять вместо других солевых инфузионных растворов.
Практическое применение в лечении критических состояний нашли и антигипоксанты, представляющие собой естественные для организма компоненты дыхательной цепи митохондрий, участвующие в переносе электронов — цитохром С (цитомак). Данный препарат, в сущности, выполняет функцию заместительной терапии, поскольку при гипоксии из-за структурных нарушений митохондрии теряют часть своих компонентов, включая переносчики электронов. В экспериментальных исследованиях доказано, что экзогенный цитохром С при гипоксии проникает в клетку и митохондрии, встраивается в дыхательную цепь и способствует нормализации энергопродуцирующего окислительного фосфорилирования. Цитохром С может быть полезным средством комбинированной терапии критических состояний. Показана высокая эффективность препарата при отравлении снотворными средствами, окисью угле-
