
Pod_red_prof_Nikonova_V_V_dots_Feskova_A_E_3
.pdf
Кислотно-основное состояние |
131 |
|
|
Фосфатная система
Фосфатная система — основная буферная система внутриклеточного сектора. Она состоит из Na2HPO4 и NaH2PO4.
HPO42– может связывать протоны, превращаясь в H2PO4, последний — наоборот, может освобождать протоны, а также реагировать с гидроксильными ионами:
OH– + H2PO4 HPO42– + H2O.
Белковая система
Белковая система — буферная система обоих водных секторов. Буферные свойства белков обусловлены наличием у них как основной группы (–NH2), так и кислотной (–COOH):
H2N–R–COOH H2N–R–COO– + H+ HOOC–R–NH2 + H+HOOC–R–NH4+.
Гемоглобиновая система
Гемоглобиновая система — буферная система эритроцитов, обеспечивает около половины буферной емкости крови. Буферные свойства этой системы обусловлены тем, что Hb, связанный с кислородом, обладает свойствами кислоты, а восстановленный — свойствами оснований:
HHbO2 H+ + HbO2 H+ +Hb– HHb.
1.3. Методы оценки кислотно-основного состояния
Интегральным показателем КОС является pH плазмы крови (другими словами — концентрация ионов водорода в ней). В норме в артериальной крови paH = 7,35…7,45, в венозной pvH = 7,32…7,42. Как видно из этих данных, реакция среды в плазме, да и во всем внеклеточном секторе, несколько сдвинута в основную сторону, тогда как внутри клетки pH 7, то есть там реакция среды нейтральная. Это состояние выработалось в течение эволюции, поскольку главные жизненные процессы идут в клетках, а в результате этих процессов образуются кислые метаболиты, покидающие клетки. Некоторый сдвиг в основную сторону реакции среды внеклеточного сектора не позволяет закисляться пространству вокруг клетки.
PH, показывая концентрацию протонов во внеклеточной жидкости, не дает представления о механизмах, обеспечивающих эту концентрацию, то есть PH отражает лишь степень компенсации КОС, но не уровень ее напряженности. PH в пределах нормы означает только нормальную

132 Медицина неотложных состояний. Избранные клинические лекции. Том 4
концентрацию ионов водорода, а достигнуто это с помощью нормальной или напряженной работы компенсаторных механизмов, по pH определить нельзя. Если paH < 7,35, то речь идет о декомпенсированном ацидозе, если paH > 7,45 — о декомпенсированном алкалозе, но о характере этих изменений (метаболический или респираторный) по pH также судить невозможно. Для более или менее полной оценки КОС требуются еще 2 показателя, один из которых — pCO2 — отражает респираторный компонент КОС, а другой — BE (base excess — избыток оснований) — метаболический. Все 3 показателя (pH, pCO2 и BE) жестко между собой связаны (как вершины треугольника), поэтому если 2 из них известны, 3-й определяется однозначно. На практике с помощью специальных электродов измеряют pH и pCO2, а BE определяют исходя из этих двух показателей по специальной номограмме. Показатель pCO2 подробно описан в разделе, посвященном ОДН, в норме в артериальной крови он составляет 35–45 мм рт.ст. При pCO2 < 35 мм рт.ст. говорят о респираторном алкалозе, при pCO2 > 45 мм рт.ст. — о респираторном ацидозе.
BE отражает избыток (который может быть и отрицательным, тогда говорят о дефиците) оснований во внеклеточном секторе и в норме составляет ± 2–3 ммоль/л. Таким образом, BE показывает, сколько в каждом литре внеклеточной жидкости не хватает (или каков излишек) всех оснований по сравнению с нормальным их количеством (оно отражается показателем BB, составляющим в норме 40–60 ммоль/л). При BE < –3 ммоль/л речь идет о метаболическом ацидозе, а при BE > 3 ммоль/л — о метаболическом алкалозе.
При развернутой оценке КОС используют еще несколько показателей, среди которых чаще всего следующие:
AB — истинный (актуальный) бикарбонат (19–25 ммоль/л) — действительное содержание HCO3 в крови больного;
SBТ — стандартный бикарбонат (20–27 ммоль/л) — бикарбонат той же крови, помещенный в стандартные условия (pCO2 = 40 мм рт.ст., SO2 = 100 % — то есть полное насыщение гемоглобина кислородом, t = 37 °C); BB — сумма оснований (buffer base) всех четырех буферных систем
(40–60 ммоль/л).
2. Клиническая физиология нарушений КОС
Нарушения КОС проявляются в виде ацидоза или алкалоза, которые могут быть: 1) компенсированными или декомпенсированными; 2) метаболическими или респираторными. Если pH в пределах нормы, говорят о компенсированных ацидозе или алка-

Кислотно-основное состояние |
133 |
|
|
лозе, при выходе pH за пределы нормы — о декомпенсированных. Декомпенсированный ацидоз развивается вследствие превышения скорости накопления протонов над скоростью их связывания или выведения, при декомпенсированном алкалозе наблюдается обратная картина.
2.1. Метаболический ацидоз
Основные причины метаболического ацидоза следующие:
1)гипоксия любого генеза (при ОДН, острой недостаточности кровообращения, шоке и т.п.), из-за которой окисление частично или полностью (например, в случае клинической смерти) переходит на анаэробный путь с образованием молочной и других кислот;
2)почечная недостаточность, в результате которой замедляется выведение протонов, так как задерживаются ионы SO42– и HPO42–;
3)большие потери содержимого тонкого кишечника, желчи, панкреатического сока, так как с ними выводятся бикарбонатные ионы (HCO3) и Na+;
4)сахарный диабет, лихорадка, так как при этих состояниях растет количество кетокислот;
5)выведение мочеточников в сигмовидную кишку, так как экскретируемые почками хлориды всасываются в толстом кишечнике;
6)тяжелая адреналовая недостаточность, поскольку она приводит к острой недостаточности кровообращения, то есть к циркуляторной гипоксии.
Иногда в качестве причины метаболического ацидоза называют гиперкалиемию, однако в данном случае скорее следует говорить о том, что и гиперкалиемия и метаболический ацидоз являются следствиями одной и той же причины (например, ОПН).
При декомпенсированном метаболическом ацидозе pH становится ниже 7,35, а BE — ниже –3 ммоль/л. Поскольку здоровому организму свойственна тенденция к метаболическому ацидозу, механизмы его коррекции достаточно развиты и состоят из дыхательного и почечного путей.
Как известно, излишек протонов стимулирует дыхательный центр,
врезультате чего развивается гипервентиляция, то есть усиливается
выведение CO2. Это ведет к снижению количества H2CO3, которая, как любая кислота, является донатором протонов.
Почечная компенсация происходит медленнее. При этом усилива-
ется экскреция H+ и NH4+, а также задерживается HCO3.
Если компенсация метаболического ацидоза оказывается состоятельной, то pH не выходит за пределы нормы. Так как наиболее бы-

134 |
Медицина неотложных состояний. Избранные клинические лекции. Том 4 |
|
|
стро осуществляется компенсация дыхательным путем, то при компенсированном метаболическом ацидозе снижение BE отмечается на фоне респираторного алкалоза — снижения pCO2. В качестве примера разных вариантов метаболического ацидоза можно привести следующие результаты исследования КОС:
Декомпенсированный |
Компенсированный |
метаболический |
метаболический |
ацидоз |
ацидоз |
|
|
pH = 7,32 |
pH = 7,39 |
pCO2 = 33 мм рт.ст. |
pCO2 = 32 мм рт.ст. |
BE = –11 ммоль/л |
BE = –5 ммоль/л |
|
|
2.2. Респираторный ацидоз
Главная и, пожалуй, единственная причина респираторного ацидоза — гиповентиляция, вследствие которой развивается гиперкапния (pCO2 > 50 мм рт.ст.), что ведет к росту H2CO3. Причины нарушений вентиляции рассмотрены в разделе, посвященном ОДН.
В острой фазе респираторного ацидоза количество бикарбонатов не меняется, поэтому показатель BE остается в пределах нормы, однако при длительно существующем (хроническом) ацидозе, например при бронхиальной астме, включается почечный механизм компенсации, что ведет к задержке HCO3 (и росту BE), а также к усиленному выведению протонов.
Примеры:
Декомпенсированный |
Компенсированный |
респираторный |
респираторный |
ацидоз |
ацидоз |
|
|
pH = 7,25 |
pH = 7,39 |
pCO2 = 80 мм рт.ст. |
pCO2 = 60 мм рт.ст. |
BE = +1 ммоль/л |
BE = +5 ммоль/л |
Без учета клинической картины бывает трудно отличить компенсированный респираторный ацидоз от компенсированного метаболического алкалоза.
2.3. Метаболический алкалоз
Основные причины метаболического алкалоза следующие:
1) потери протонов при массивной рвоте, дренировании желудка;

Кислотно-основное состояние |
135 |
|
|
2)ятрогенные — переливание излишних количеств гидрокарбоната натрия, больших количеств цитратной крови (цитрат метаболизируется в гидрокарбонат);
3)потери организмом K+ и Cl– (гипокалиемический и гипохлоремический метаболический алкалоз);
4)олигурические состояния с задержкой Na+ и HCO3 в послеоперационном и посттравматическом периоде;
5)длительное бесконтрольное введение хлортиазидных диуретиков, приводящее к потере калия и хлоридов;
6)тяжелые формы первичного и вторичного альдостеронизма (задержка натрия и потери калия);
7)длительное введение стероидов (задерживается Na+). Метаболический алкалоз — более тяжелое состояние, чем ме-
таболический ацидоз, так как, как указывалось выше, в организме более развиты механизмы компенсации метаболического ацидоза. Кроме того, метаболический алкалоз связан с нарушением водноэлектролитных соотношений между вне- и внутриклеточным секторами (особенно в случае третьей причины метаболического алкалоза).
Самостоятельная компенсация метаболического алкалоза в организме малоэффективна. Возможности респираторной компенсации ограниченнны, так как гиперкапния при компенсаторной гиповентиляции слабо влияет на характер основных метаболических сдвигов.
Почечная компенсация осуществляется за счет повышения экскреции HCO3. Однако при гипокалиемии канальцевая реабсорбция HCO3 растет, pH мочи сдвигается в кислую сторону, что усиливает алкалоз.
Метаболический алкалоз, который выявляется с помощью вышепредставленных показателей КОС, в подавляющем большинстве случаев имеет место только во внеклеточном секторе, который легко доступен для исследования. При метаболическом алкалозе, связанном с потерями клеткой калия (и эта ситуация встречается, пожалуй, чаще всего), внутри клетки развивается тяжелый метаболический ацидоз. Механизм здесь следующий. Как описано в разделе, посвященном ВЭО, при критических состояниях клетка вследствие гипоксии начинает терять калий, так как из-за гипоксического энергодефицита нарушается работа K+-Na+-насоса. На каждые 3 вышедших иона K+ в клетку заходит 2 иона Na+ и 1 ион H+. В результате во внеклеточном секторе развивается дефицит протонов, то есть алкалоз, а в клетках — их избыток, то есть ацидоз.
136 |
Медицина неотложных состояний. Избранные клинические лекции. Том 4 |
|
|
2.4. Респираторный алкалоз
Главная причина респираторного алкалоза — гипервентиляция легких. Она может развиваться в следующих случаях:
1)испуг, боль, истерическая реакция;
2)гипертермия;
3)ОПН (как компенсация метаболического ацидоза);
4)острая печеночная недостаточность (вследствие накопления NH4OH);
5)гипервентиляция при ИВЛ;
6)ЧМТ, острое нарушение мозгового кровообращения (ОНМК) («раздражение» дыхательного центра);
7)сепсис, особенно грамотрицательный;
8)интоксикация кислыми веществами (например, салицилатами);
9)нарушение диффузии и шунтирование крови слева направо
влегких.
При респираторном алкалозе происходит повышение pH более 7,45 и снижение pCO2 менее 35 мм рт.ст. При изолированном респираторном алкалозе BE остается в пределах нормы, однако при длительном его существовании включается почечная компенсация, в результате чего BE снижается (при этом также задерживаются протоны).
Выраженный респираторный алкалоз протекает очень тяжело, и в первую очередь это связано с тем, что гипокапния приводит к вазоконстрикции, в том числе в головном мозге. Мозговой кровоток снижается на исходной величины, что обусловливает циркуляторную гипоксию мозга. Кроме того, респираторный алкалоз снижает количество ионизированного Ca2+, в результате чего развивается тетания.
3. Связь между ВЭО и КОС
Связь между ВЭО и КОС обусловлена взаимодействием законов электронейтральности и изоосмолярности в средах, разделенных полупроницаемой мембраной, через которую свободно проникает вода и которой задерживаются некоторые ионы. При этом осмолярность вне- и внутриклеточного секторов остается одинаковой (то есть одинакова концентрация частиц в обоих секторах), но из-за того, что эта одинаковая осмолярность обусловлена разными ионами (которые к тому же могут иметь разную валентность), в клетке возникает отрицательный заряд.
Если в организме по какой-либо причине снижается концентрация буферных оснований (ацидоз), то есть снижается BB, и поскольку эти

Кислотно-основное состояние |
137 |
|
|
основания представлены анионами (отрицательно заряженными ионами), то по закону электронейтральности происходят следующие изменения электролитного состава:
1)повышение [Cl–];
2)повышение концентрации остаточных анионов (сульфатов, фосфатов, лактата и др.);
3)снижение [Na+].
Например, при кетоацидозе из-за снижения [HCO3] повышается концентрация остаточных анионов в виде кетокислот и может повышаться [Cl–] и понижаться [Na+]. При метаболическом алкалозе [HCO3], следовательно, по закону электронейтральности падает [Cl–] (чаще всего) или повышается [Na+].
В целом электролитное равновесие в организме можно представить формулой:
[Na+] [Cl–] + [BB–], следовательно, [BB–] [Na+] — [Cl–].
В разделе, посвященном ВЭО, мы говорили, обсуждая вещества, обусловливающие осмолярность внеклеточного сектора, что его основной катион — Na+ (142 ммоль/л), положительный заряд которого уравновешивается Cl– (103 ммоль/л); оставшийся заряд Na+ как раз
иуравновешивается буферными основаниями.
4.Интенсивная терапия нарушений кислотно-основного
состояния
4.1. Интенсивная терапия метаболического ацидоза
Основное направление ИТ метаболического ацидоза — ликвидация причины, его вызвавшей. Однако, если концентрация протонов достигает критического уровня, которому соответствует, по разным данным, pH от 7,1 до 7,2 или превышает его (pH < 7,1), на ликвидацию причины может не хватить времени, поскольку больной может погибнуть раньше, чем будет устранена причина метаболического ацидоза. В этом случае необходимо срочно связать излишек протонов, для чего используется гидрокарбонат (бикарбонат) натрия (пищевая сода, NaHCO3). Правила его введения следующие.
I. pH < 7,1 (7,2).
II. Доза соды (в ммоль) рассчитывается по формуле:
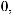
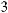
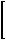
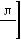

 [
[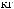 ]
] 
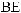
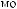
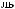



138 |
Медицина неотложных состояний. Избранные клинические лекции. Том 4 |
|
|
BE показывает, сколько ммоль оснований не хватает в каждом литре жидкости организма; количество этой жидкости равно 0,3 л/кг3. Произведение BE и объема жидкости, в котором распределяется сода,
идает общий дефицит оснований в ммоль.
III. Вначале вводят половину расчетной дозы, затем контролируют pH. Если pH становится больше 7,2, от дальнейшего введения соды отказываются. Если результат не достигнут, вводят еще ј расчетной дозы. Если и в этом случае pH не повышается до 7,2, вводят остальную часть расчетной дозы. Такие предосторожности соблюдаются для того, чтобы избежать ятрогенного алкалоза, с которым, как уже говорилось, бороться значительно труднее и который протекает значительно тяжелее.
IV. Для введения NaHCO3 было бы удобно пользоваться, как обычно, молярным раствором (для соды это 8,4% раствор), но такой раствор слишком концентрирован и раздражает стенки вен, поэтому на практике пользуются полумолярным раствором (4,2 %), в каждом миллилитре которого содержится 0,5 ммоль соды.
Пример 1. pH = 7,15, BE = –11 ммоль/л, pCO2 = 30 мм рт.ст., масса тела больного 70 кг. Так как pH ниже нормы, делаем заключение о декомпенсированном ацидозе. Величина BE говорит о его метаболическом характере. Гипокапния свидетельствует о напряжении компенсации за счет респираторного компонента, которая оказывается несостоятельной. Так как pH < 7,2, больной нуждается в срочной коррекции с помощью гидрокарбоната натрия. Его общая доза составляет
0,3 · 70·11 = 231 ммоль, то есть 213 · 2 = 462 мл 4,2% раствора NaHCO3. Вначале вводим половину расчетной дозы (231 мл 4,2% раствора) и далее — по правилу IV.
Пример 2. PH = 7,18, BE = +2 ммоль/л, pCO2 = 75 мм рт.ст., m = 70 кг. Так как pH ниже нормы, речь идет о декомпенсированном ацидозе. Показатели BE и pCO2 свидетельствуют о респираторном характере ацидоза. Хотя pH < 7,2, введение соды противопоказано (категорически!) из-за респираторного характера ацидоза4. Единственный способ лечения в данном случае — нормализация альвеолярной вентиляции способами, определяемыми причинами ее уменьшения (чаще всего — ИВЛ).
3 0,3 л/кг — эмпирический показатель, равный объему, в котором распределяется введенная сода. Как видно, этот объем немного больше объема внеклеточной жидкости, равного 0,2 л/кг (20 % от массы тела).
4 Введение соды увеличит образование CO2, выведение которого и так затруднено из-за гиповентиляции.
Кислотно-основное состояние |
139 |
|
|
4.2. Интенсивная терапия респираторного ацидоза
Лечение респираторного ацидоза заключается в нормализации альвеолярной вентиляции. Методы ее нормализации описаны в разделе, посвященном ИВЛ.
4.3. Интенсивная терапия метаболического алкалоза
Из всех нарушений КОС метаболический алкалоз труднее всего поддается лечению, его гораздо легче предупредить. Поскольку чаще всего метаболический алкалоз является следствием гипокалигистии, то для профилактики метаболического алкалоза необходимо предупреждать потери K+ организмом и вовремя их восполнять. Гипокалигистия является следствием гипоксии, из-за которой не хватает энергии для работы K+-Na+-насоса, поэтому предупреждение и ликвидация гипоксии одновременно являются и профилактикой метаболического алкалоза. При восполнении гипокалигистии особое внимание нужно уделять тому, чтобы калий поступал в клетку. Подробно методы восполнения дефицита калия описаны в разделе, посвященном ВЭО. Если метаболический алкалоз связан с задержкой натрия, вызванной длительным приемом стероидов, их необходимо отменить.
Как правило, метаболическому алкалозу сопутствует и гипохлоремия, поэтому необходимо и введение хлоридов, которые обычно поступают в составе KCl.
Введение слабоконцентрированных кислот при метаболическом алкалозе в настоящее время не используется, так как не является патогенетическим. Как уже указывалось, метаболический алкалоз во внеклеточном секторе обычно сопровождается внутриклеточным ацидозом за счет перехода протонов из внево внутриклеточное пространство.
4.4. Интенсивная терапия респираторного алкалоза
Лечение этого вида расстройства КОС заключается в нормализации вентиляции легких. При респираторном алкалозе необходимо предупредить или ликвидировать причины гипервентиляции, и, как правило, без ИВЛ в этом случае не обойтись.

Утренняя звезда!
Нет среди вишен покоя Облачку на горе.
Кикаку
Острая недостаточность кровообращения. Шок
1. Острая недостаточность кровообращения
Поскольку функция кровообращения (ФКО) — первая функция, восстанавливающаяся в процессе сердечно-легочно-мозговой реанимации (СЛМР), с ее недостаточности мы и начнем рассмотрение синдромов критического состояния. Перед описанием клиникофизиологических механизмов недостаточности той или иной функции мы будем предпосылать некоторые сведения из клинической анатомии и клинической физиологии этой функции.
1.1. Клиническая анатомия системы кровообращения
Система кровообращения состоит из трех составных частей: 1) сердца как насоса, 2) сосудистой системы и 3) объема циркулирующей крови (ОЦК), заключенного в замкнутую систему сердца и сосудов. Принципиальная схема сосудистой системы изображена на рис. 1.
На этой схеме не полностью соблюдены анатомические соотношения в сосудистой системе, однако на ней отображен действительный путь крови по сосудам. Из схемы видно, что кровь циркулирует по единому замкнутому кругу. Участок круга между правым желудочком (ПЖ) и левым пердсердием (ЛП), содержащий, в частности, оксигенатор — легкие (Л), не вполне удачно в свое время был назван малым кругом кровообращения, а участок между левым желудочком (ЛЖ) и правым пердсердием (ПП) — большим кругом кровообращения. Понятно, что в действительности эти участки сосудистой системы кругами не являются, и если об этом помнить, то можно избежать множества недоразумений.
