
- •Методические указания
- •Содержание
- •1 Техника безопасного проведения работ химической лаборатории
- •2 Очистка и подготовка химической посуды
- •3 Техника выполнения основных операций
- •4 Общие указания к работе в лаборатории
- •5 Неорганическая химия (Качественный анализ)
- •Получение и собирание кислорода
- •5.2 Скорость химических реакций. Химическое равновесие
- •5.3 Электролитическая диссоциация
- •5.4 Произведение растворимости
- •5.5 Гидролиз солей
- •5.6 Карбонаты. Жесткость воды
- •5.7 Окислительно-восстановительные реакции
- •5.8 Комплексные соединения
- •5.9 Коррозия металлов
- •6. Аналитическая химия (Количественный анализ)
- •6.1 Определение металлов в растворе комплексонометрическим методом
- •6.3 Определение содержания щавелевой кислоты в растворе перманганатометрическим методом
- •6.6 Определение содержания кислот в растворе методом нейтрализации
- •7.2 Лабораторная работа №2
- •7.3 Лабораторная работа №3
- •8 Размерность
- •9.1 Расчеты массы навески вещества
- •9.2 Щелочи
- •9.3 Кислоты
- •Растворение серной кислоты в воде
- •9.4 Органические вещества
- •9.5 Различные смеси
- •10 Индикаторы
- •11 Демонстрационные опыты Синергетика – теория самоорганизации
- •11.1 «Жук бомбардир»
- •11.2 Реакция Бриггса-Раушера «Йодные часы»
- •11.3 Твёрдофазная колебательная реакция:
- •11.4 Реакция Белоусова-Жаботинского «Химический маятник»
- •11.5 «Фейерверк в жидкости»
- •11.6 Красные призмы.
- •11.7 «Живые капли ртути»
- •11.8 Получение оксалата железа.
- •11.9 "Замерзание" воды при комнатной температуре
- •11.10 Получение оксида хрома (III)
- •11.11 Реакция «Серебряного зеркала»
- •12 Регенерация химических остатков
- •12.1 Регенерация остатков серебра в нитрат серебра
- •12.2 Регенерация остатков серебра в гранулы
- •13 Упаковка и хранение токсичных веществ
- •Список некоторых веществ
- •14 Кристаллография
- •14.1 Кристаллы металлической меди
- •Подсказка
9.2 Щелочи
Баритовая вода (насыщенный раствор Ba(OH)2). В 1л раствора содержится около 80г кристаллогидрата Ba(OH)2*8Н2О. Для приготовления реактива 80г кристаллогидрата растворяют при кипячении в 200мл воды и затем разбавляют водой до 1л. Через сутки после отстаивания прозрачный раствор осторожно сливают в склянки с тубусом или шлифом.
Ba(OH)2 (0.5N), m(1/2) = 0.5н*1л*(1\2)171,342г\моль= 42,835г (85,671г)
Ba(OH)2*8Н2О (0.5N), m(1/2) = 0.5н*1л*(1\2)315,464г\моль=78,866г (157,732г)
KOH (0.5N), m(1/1) = 0.5н*1л*(1\1)56,1056г\моль = 28,053г (56,105г)
KOH (0.1N), m(1/1) = 0.1н*1л*(1\1)56,1056г\моль = 5,611г (11,221г)
KOH (спиртовой), 37г KOH растворяют в 125мл спирта.
KOHКОНЦ, 500г KOH растворяют в 1л воды, т.е. готовят раствор 1:2.
NaOH (0.5N), m(1/1) = 0.5н*1л*(1\1)39,997г\моль = 19,998г (39,997г)
Сухой гидроксид натрия при взвешивании раздражает слизистую оболочку носоглотки. При растворении навески используют фарфоровую посуду, т.к. раствор очень сильно нагревается!!!
NaOHКОНЦ, 500г NaOH растворяют в 1л воды, т.е. готовят раствор 1:2.
NaOHРАЗБАВЛЕННЫЙ, 300г NaOH доводят до 1л водой.
NaOH (2N), 80г NaOH растворяют в 1л воды.
NaOH (15% спиртовой), к 15г NaOH добавляют 85мл спирта (С2Н5ОН). Раствор готовят перед занятием.
NaOH (5%), 50г NaOH растворяют в 1л воды.
NaOH (3N), 120г NaOH растворяют в 1л воды.
NaOH (5% спиртовой), 5г NaOH добавляют к 95мл спирта (С2Н5ОН). Стакан поставить в баню с холодной водой. Раствор готовят перед занятием.
NН4OH (2N), 133мл гидроксида аммония разбавляют в 687мл воды.
9.3 Кислоты
HCl (2N), 67мл HClКОНЦ доливают до 1л водой.
HCl РАЗБАВЛЕННЫЙ, 150мл HClКОНЦ доливают до 1л водой.
HNO3 (плотностью 1,4), 1 часть HNO3КОНЦ на 2 части H2SO4КОНЦ перегоняются при обычном давлении до тех пор, пока идёт разгонка.
HNO3 (2N), 14мл HNO3КОНЦ доводят до 1л водой.
HNO3 (плотностью 1,15), 140мл воды разбавляют в 200мл HNO3КОНЦ.
H2SO4РАЗБАВЛЕННАЯ,1 объём H2SO4КОНЦ на 10 объёмов воды.
H2SO4 (2N), 55мл H2SO4КОНЦ разбавить в 945мл воды.
H2SO4 (5%), 2,6мл H2SO4КОНЦ доливают до 1л водой.
H2SO4 (20%), 108мл H2SO4КОНЦ доливают до 1л водой.
H2SO4 (25%), 159мл H2SO4КОНЦ доливают до 1л водой.
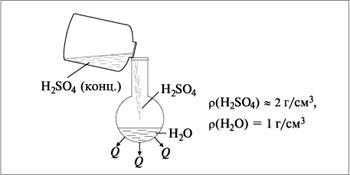
Растворение серной кислоты в воде
HCOOH (N), 0,45мл муравьиной кислоты разводят в 100мл воды
CH3COOH (0,1N), 0,6мл ледяной кислоты CH3COOH разводят в 100мл воды.
H2C2O4 (0,5N), (0.5N), m(1/2) = 0,5н*1л*(1\2)90,35г\моль = 22,509г (45,018г)
H2C2O4*2Н2О (0,5N), m(1/2) = 0,5н*1л*(1\2)126,066г\моль = 31,517г (63,033г)
Хромовая кислота. Для приготовления 0,4н раствора хромовой кислоты необходимо 20г ее растворить в 500мл дистиллированной воды с последующим добавлением 500мл серной кислоты плотностью 1840 кг/м3.
Аспарагиновая кислота. 2г аспарагина растворить в 200мл воды (т.к. нужна кислая среда, добавить 10-15 капель НСl).
Гликоль (глицин, аминоуксусная кислота). 2г гликоля растворяют в 200мл воды (реакция нейтральная).
