
- •Третичная структура белка
- •Структура глобулярных белков
- •Стабилизация пространственной структуры белка
- •Bovine Pancreatic Trypsin Inhibitor (BPTI) - 58 ак
- •Bovine Pancreatic Trypsin Inhibitor (BPTI) - 58 ак
- •Классификация пространственных структур - α/β белки
- •Соотношение между первичной и пространственной структурами белка
- •Доменная структура белков
- •Протяженная структура, формируемая серией линейно расположенных белковых модулей
- •Четвертичная структура белка
- •Стехиометрия и геометрия четвертичной структуры
- •Четвертичная структура лактатдегидрогеназы (ЛДГ)
- •Стабилизация четвертичной структуры белка
- •Способы изучения четвертичной структуры
- •Функциональное значение четвертичной структуры белка
- •Иерархия структурной организации белков
- •Морфины (Morpheeins)
- •Примеры октамерной и гексамерной форм порфобилиногенсинтазы
- •Регуляция активности ПБС с помощью формирования различных морфиновых ансамблей
- •Функции белков (1)
- •Функции белков (2)
- •Функции белков (3)
Доменная структура белков
•Доменами в белках называют области в третичной структуре, которым свойственна определенная автономия структурной организации (II->III).
–Появляются домены у белков начиная с М.м. 14-16 кДа;
–Формируются различными отрезками одной и той же цепи;
–В основном образованы соседними участками п/п цепи;
–Обычно домен состоит из 40-350 ак остатков;
–Домены могут независимо формировать и поддерживать пространственную структуру;
–Домены часто можно разделить ограниченным протеолизом;
–В некоторых белках у доменов есть функциональная автономия;
–Границы доменов чаще всего соответствуют границам экзонов;
–Домены формируются из структурных мотивов;
–Описано около 1000 различных вариантов доменных структур среди 10000 известных белков;
–Предполагается существование около 2000 вариантов доменных структур.
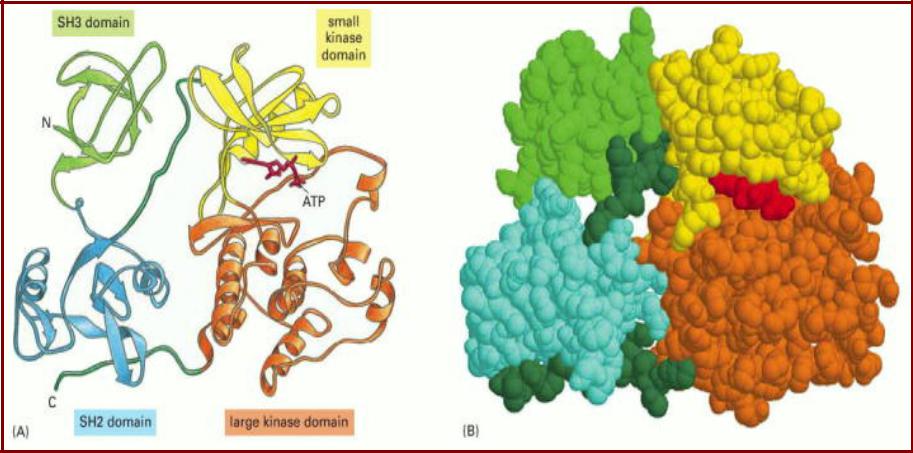
Src–протеинкиназа сформирована четырьмя доменами
Два домена формируют активный центр фермента, два домена - SH2 и SH3 выполняют регуляторные функции
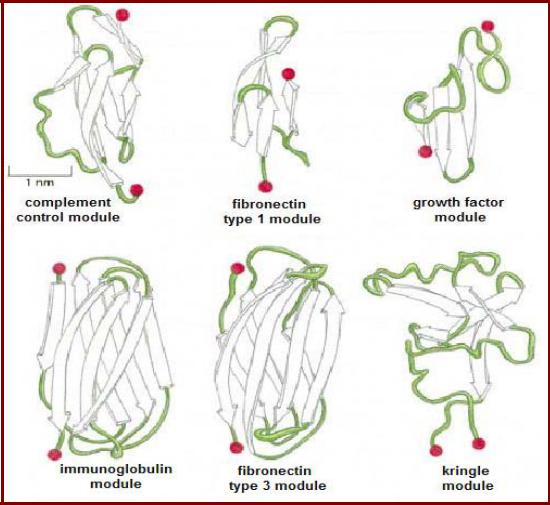
Некоторые белковые домены, называемые модулями (Protein modules), участвуют в формировании
многих различных белков
•Эволюционно наиболее мобильны;
•Размеры 40-200 ак;
•Имеют универсальную структуру:
-Каркасная структура, позволяет формировать центры связывания с различными лигандами путем изменения ак состава в петлях;
-Способны к интеграции в различные белки
(“in-line” – линейный, “plug-in” – сменный);
•Различные доменные структуры белков часто связаны с различными функциями.
Примеры белковых модулей, состоящих из β-слоев
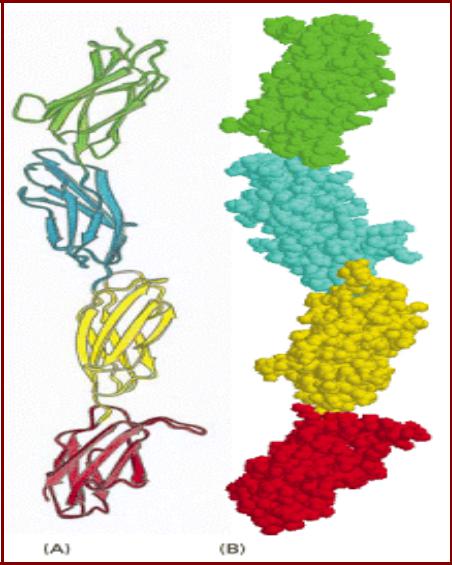
Протяженная структура, формируемая серией линейно расположенных белковых модулей
•Фрагмент молекулы фибронектина
(домены фибронектина типа 3)
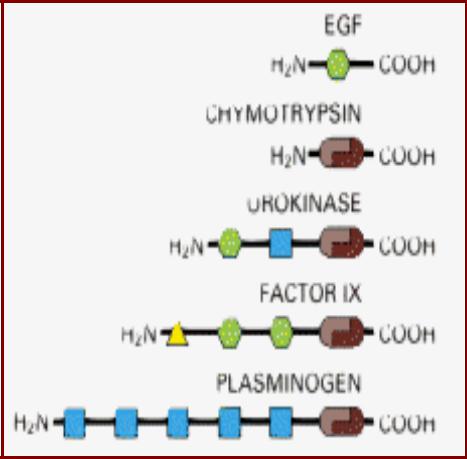
Феномен перетасовки доменов (Domain shuffling) Мозаичные белки
•Структурные модули:
–Домен эпидермального фактора роста EGF (зеленый);
–Два домена, формирующие химотрипсин (коричневые);
–Кальций-связывающий домен (желтый);
–«Kringle» домен (голубой).
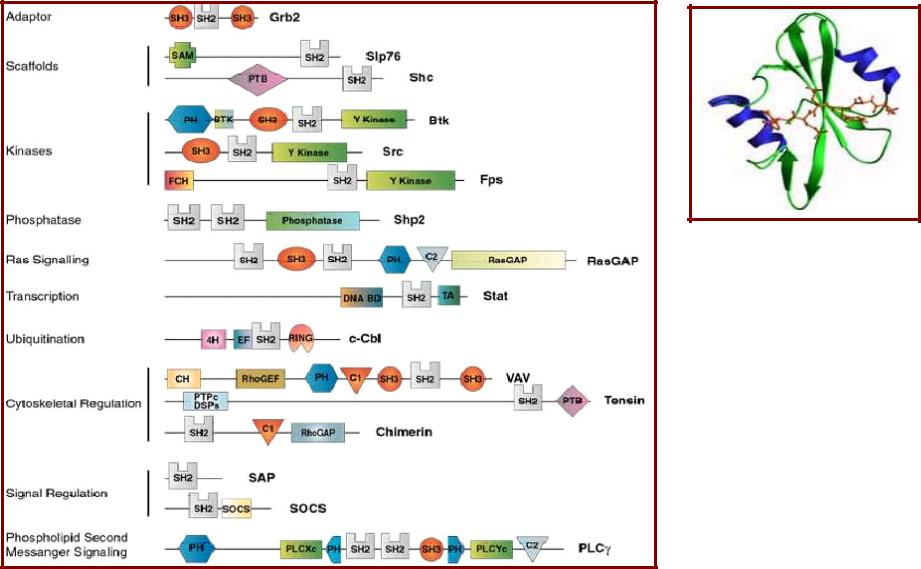
SH2-домен обнаружен во многих регуляторных
белках многоклеточных
SH2-домен:
• (Src-homology 2)
• модуль ~100 ак;
• распознает
специфический мотив, содержащий фосфотирозин (рY).
Методы изучения трехмерной структуры белков:
-Рентгеноструктурный анализ;
-Метод ядерно-магнитного резонанса.
Исследования структуры белков показали, что
•Современная структура белков отражает миллионы лет эволюции;
•Большинство белков принадлежит к большим эволюционирующим семействам;
•Аминокислотная последовательность многих белков сильно менялась в процессе эволюции;
•3D структура белков эволюционно более консервативна, чем первичная структура;
•Сходства между последовательностью или структурой белков могут давать информацию об общих биологических функциях белковых семейств.
