
- •Пути передачи биологической информации
- •Аминокислоты (АК)
- •Трехбуквенные и однобуквенные обозначения аминокислот
- •Кислотно-основные свойства аминокислот
- •Аминокислотный состав белков
- •Заменимые и незаменимые аминокислоты
- •Редкие аминокислоты, входящие в состав белков
- •Аминокислоты, не встречающиеся в белках
- •Что определило такой набор аминокислот в составе белков?
- •Пространственная организация белковой молекулы
- •Первичная структура белка
- •Анализ первичной структуры белковых молекул
- •Вторичная структура белка
- •Особенности пептидной связи, определяющие формирование регулярной пептидной структуры
- •Стерические ограничения, возникающие при формировании полипептидной цепи
- •Типы вторичной структуры белка
- •Альфа спираль
- •Свойства α-спирали (1)
- •Свойства α-спирали (2)
- •Коллагеновая спираль
- •Бета-структуры
- •Параллельный и антипараллельный β-слои
- •Бета-изгиб
- •Методы, применяемые для анализа вторичной структуры белковых молекул
- •Супервторичная структура (мотив)
- •Супервторичные структуры
- •Супервторичные структуры
- •Супервторичные структуры
- •Супервторичные структуры
- •Типы β-бочонков
Строение и функции белков I
Лекция 1 2014г.

Пути передачи биологической информации
ДНК
РНК белок
Ключевые проблемы молекулярной биологии при исследовании белковых молекул:
¾Выяснение законов, управляющих формированием пространственной структуры белков;
¾Анализ соотношения структурных и функциональных свойств
белков;
¾Выяснение механизмов функционирования разнообразных белковых молекул;
¾Изучение способов и путей взаимодействия белков друг с другом;
¾Выявление закономерностей эволюции белковых молекул.

Аминокислоты (АК)
•Пептиды и белки построены из мономеров α-аминокислот (Pro – α-иминокислота);
•Все аминокислоты, встраивающиеся в белки в ходе трансляции, являются
L-изомерами
(исключение – Gly);
•20 аминокислот, встраивающиеся в белковую цепь в ходе трансляции, -
белковые (proteinogenic)
аминокислоты.
H
|
NH2 - C| α – COOH R
Трехбуквенные и однобуквенные обозначения аминокислот
Amino acid 3L code |
1L code |
Amino acid |
3L code |
1L code |
|
Alanine |
Ala |
A |
Methionine |
Met |
M |
Arginine |
Arg |
R |
Phenylalanine |
Phe |
F |
Asparagine |
Asn |
N |
Proline |
Pro |
P |
Aspartic acid |
Asp |
D |
Serine |
Ser |
S |
Cysteine |
Cys |
C |
Threonine |
Thr |
T |
Glutamine |
Gln |
Q |
Tryptophan |
Trp |
W |
Glutamic acid |
Glu |
E |
Tyrosine |
Tyr |
Y |
Glycine |
Gly |
G |
Valine |
Val |
V |
Histidine |
His |
H |
|
|
|
Isoleucine |
Ile |
I |
Any amino acid |
X |
|
Leucine |
Leu |
L |
Asn/Asp |
Asx |
B |
Lysine |
Lis |
K |
Gln/Glu |
Glx |
Z |
Кислотно-основные свойства аминокислот
За счет наличия в молекуле аминокислот одновременно
аминогруппы и карбоксильной группы этим соединениям присущи кислотно-основные свойства. В нейтральной среде
аминокислоты существуют в виде биполярных ионов -
цвиттер-ионов,
т.е. не NH2 – СНR – COOH , а NH3+ – СНR - COO –
Основная классификация аминокислот основана на различии в полярности их R-групп при обычных физиологических условиях

1. Аминокислоты с неполярными или гидрофобными R-группами:
Gly, Ala, Val, Leu, Ile, Met, Phe, Trp, Pro
Характеризуются низкой (по сравнению с другими типами аминокислот) растворимостью в воде
Общие функции:
•Формируют
компактное внутренне ядро, стабилизирующее структуру белка;
•Участвуют в формировании межсубъединичных контактов;
•Организуют
гидрофобные контакты с определенными лигандами.

2. Аминокислоты с полярными незаряженными R-группами:
Tyr, Asn, Gln, Ser, Thr, Cys, (Gly)
Характеризуются относительно высокой растворимостью в воде
Общие функции:
•Участвуют в образовании водородных связей внутри белка.
•Участвуют в образовании водородных связей с другими молекулами.
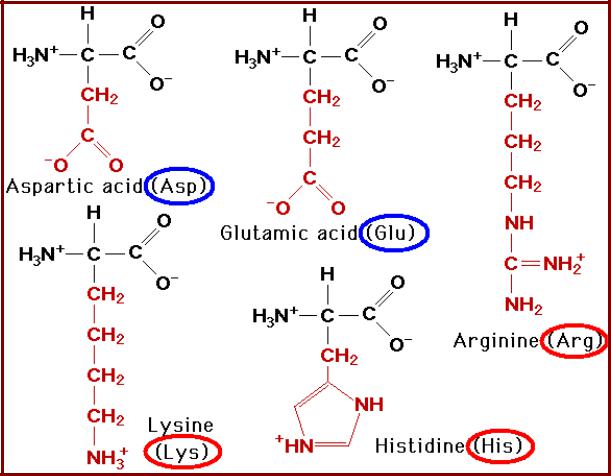
3. Аминокислоты с полярными заряженными R-группами:
Asp, Glu; Lys, Arg, His
Характеризуются наличием заряда при физиологичных рН и высокой растворимостью в воде
Общие функции:
•Участвуют в образовании водородных связей;
•Обеспечивают
ионные
взаимодействия внутри белка;
•Обеспечивают
ионные взаимодействия с другими молекулами.

Различные
способы
группирования аминокислот на основании их физико-
химических
свойств
