
Bilety2
.pdfБилет 28.
1. Липидный состав мембран - фосфолипиды,
гликолипиды, холестерин. Роль липидов в формировании липидного бислоя. Латеральная диффузия липидов и белков. Участие фосфолипаз в обмене фосфолипидов.
Основу мембраны составляет двойной липидный слой, в формировании которого участвуют фосфолипиды и гликолипиды. Липидный бислой образован двумя рядами липидов, гидрофобные радикалы которых спрятаны внутрь, а гидрофильные группы обращены наружу и контактируют с водной средой.
Фосфолипиды - это сложные липиды, производные фосфатидной кислоты. Липидам принадлежит главная роль в образовании мембран клеток. Основная часть липидов в мембранах представлена фосфолипидами, гликолипидами и холестерином.
Вмембранах имеются фосфолипиды двух типов - глицерофосфолипиды и сфингофосфолипиды.
Всостав глицерофосфолипидов входят глицерин, жирные кислоты, фосфорная кислота и обычно азотсодержащие соединения.
Общая формула для фосфолипидов
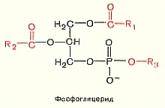 ,
,
где R1 и R2 - радикалы высших жирных кислот (насыщенные и ненасыщенные жирные кислоты соответственно), R3 - радикал азотистого основания, соединенный через гидроксил фосфата эфирной связью с производным фосфатидной кислоты.
В Гликолипидах гидрофобная часть представлена церамидом. Гидрофильная группа - углеводный остаток, присоединённый гликозидной связью к гидроксильной группе у первого углеродного атома церамида. В зависимости от длины и строения углеводной части различают цереброзиды, содержащие моноили олигосахаридный остаток, и ганглиозиды, к ОН-группе которых присоединён сложный, разветвлённый олигосахарид, содержащий N-ацетилнейраминовую кислоту
(NANA).
Холестерол присутствует во всех мембранах животных клеток. Его молекула состоит из жёсткого гидрофобного ядра и гибкой углеводородной цепи, единственная гидроксильная группа является "полярной головкой"
Для мембран характерна асимметричность относительно липидов. Эта асимметричность достигается тем, что липиды могут двигаться вбок в пределах одного монослоя и совершать «флип-флоп» переход, т.е. переход из одного монослоя в другой. Благодаря «флип-флоп» переходу в верхнем монослое концентрируются липиды с насыщенными радикалами жирных кислот, что придает ему особую твердость, а во внутреннем монослое – с ненасыщенными радикалами.
Большинство мембранных белков, так же как и липидов, способны свободно перемещаться в плоскости мембраны. Известно два вида движения белков и липидов в мембране – это так называемые латеральная диффузия и флип-
флоп. Латеральная диффузия – это хаотическое тепловое перемещение молекул липидов и белков в плоскости мембраны. Флип-флоп – это диффузия молекул мембранных фосфолипидов поперек мембраны, но он происходит гораздо реже, чем латеральная диффузия.
Фосфолипаза — фермент, который гидролизует фосфолипиды. В зависимости от положения гидролизуемой связи в фосфолипиде различают 4 основных класса фосфолипаз: A, B, C и D.
2. Аэробный распад глюкозы. Физиологическое
значение аэробного распада глюкозы. Использование глюкозы для синтеза жиров в печени и в жировой ткани.
Аэробный гликолизпроцесс окисления глюкозы до ПВК в присутствии О2. Аэробный гликолиз — основной путь для образования энергии в клетках организма. Он может протекать как прямым (апотомическим или пентозофосфатным), так и непрямым (дихотомическим) путем. В результате непрямого окисления глюкоза полностью распадается на СО2 и Н2О, и при этом выделяется большое количество энергии (2870 кДж/моль).
Реакции гликолиза: Глюкоза под действием гексокиназы и АТФ превращается в глюкозо-6- фосфат, который в свою очередь под действием 6Ф-глюкозоизомеразы превращается в фруктозо-6-фосфат. Фруктозо-6-фосфат фосфорилируется под действием 6- фосфофруктокиназы и АТФ и превращается в фруктозо-1,6-дифосфат, который при участии альдозы расщепляется на 2 изомера: ДАФ(дигидроксиацетонфосфат) и ГАФ(глицеральдегид-3-фосфат ). Затем из ГАФ образуется 1.3-дифосфоглицерат--> 3- фофсфоглицерат--> 2-фосфоглицерат, у которого под действием енолазы отщепляется молекула воды, в результате образуется
ФЕП(фосфоенолпируват). Из ФЕП образуется ПВК. 2 ПВК окисляются в митохондриях в ПДГкомплексе (Пируватдегидрогеназный комплекс) до 2 АцетилКоА с восстановлением 2 НАДНН+. Далее, каждая АцетилКоА окисляется в цикле Кребса до 2СО2, что сопровождается восстановлением 3 НАДНН+, 1 ФАДН2 и синтезом 1 АТФ субстратным фосфорилированием (за счет энергии СукцинилКоА). Далее, восстановленные в ПДГ-комплексе и ц. Кребса НАДНН+ окисляются в ПДЦМХ (Полной Дыхательной цепи митохондрий) и на каждую НАДНН+ синтезируется по 2,5 АТФ, а ФАДН2 окисляется в УДЦМХ (Укороченной Дыхательной цепи митохондрий), что обеспечивает синтез 1,5 АТФ. Также, в аэробных условиях за счет челночных механизмов: малат-аспартатного (сердце, печень, селезенка, почки) или глицерофосфатного (скелетная мускулатура, мозг), синтезируется еще 5 или 3 АТФ, соответственно.
В определённых ситуациях обеспечение кислородом тканей может не соответствовать их потребностям. Например, на начальных стадиях интенсивной мышечной работы при стрессе сердечные сокращения могут не достигать нужной частоты, а потребности мышц в кислороде для аэробного распада глюкозы велики. В подобных случаях включается процесс, который протекает без кислорода и заканчивается образованием лактата из пировиноградной кислоты (аэробное окисление глюкозы)
Использование глюкозы:
В адипоцитах для обеспечения реакций синтеза жира распад глюкозы идёт по двум путям: гликолиз, обеспечивающий образование глицерол-3-фосфата и ацетил-КоА, и пентозофосфатный путь, окислительные реакции которого обеспечивают образование

НАДФН, служащего донором водорода в реакциях синтеза жирных кислот.
3. Строение аргинина и гистидина. Их роль в
обмене веществ.
Аргининчастично незаменимая а/к, образуется в орнитиновом цикле. Ичпользуется для синтеза креатин-фосфата и орнитина. Аргинин, стимулируя синтез мочевины, способствует детоксикации и выведению аммиака.
Гистидин– незаменимая а/к в детском возрасте, является предшественником гистамина, участвует в образовании карнозина и ансерина, в связывании гемоглобином О2. Гистидин учавствует в кроветворении (образование лейкоцитов и тромбоцитов), поэтому при дифиците гистидина снижается образование гемоглабина в костном мозге. Также гистидин спаособствует расширению сосудов и увеличению их проницаемости.
4. Гормоны задней доли гипофиза, их химическая природа и физиологическое значение.
Вазопресси́н, или антидиурети́ческий гормо́н (АДГ) — гормон гипоталамуса, который накапливается в задней доле гипофиза (в нейрогипофизе) и оттуда секретируется в кровь. Секреция увеличивается при повышении осмолярности плазмы крови и при уменьшении объёма внеклеточной жидкости. Вазопрессин
увеличивает реабсорбцию воды почкой, таким образом повышая концентрацию мочи и уменьшая её объём. Имеет также ряд эффектов на кровеносные сосуды и головной мозг. Состоит из 9 аминокислот: цистеин-тирозин- фенилаланин-глутамин-аспарагин-цистеин- пролин(аргинин или лизин)-глицин.
Окситоцин — гормон гипоталамуса, который затем транспортируется в заднюю долю гипофиза, где накапливается (депонируется) и выделяется в кровь. Имеет олигопептидное строение.
БИЛЕТ 29
НАД-зависимая дигидрогиназа.Строение окисленного и востановленного НАД+.Важнейшие субстраты НАД зависимых дигидрогиназ.НАДН дигидрогиназа и др. Переносчики электролитов внутреней мембраны метахондрий.
НАД-зависимые дегидрогеназы. В качестве кофермента содержат НАД и НАДФ. Пиридиновое кольцо никотинамида способно присоединять электроны и протоны водорода.В активном центре фермента НАД+ взаимодействует с субстратом и, отбирая два атома водорода, окисляет субстрат. К атому углерода, расположенному напротив заряженного азота, присоединяются два электрона и протон, т.е. гидрид-ион Н-, взаимодействие НАД+ с двумя электронами и протоном ведет к образованию НАДН. В дыхат. цепи протоны переносятся через мембрану, создавая рН, электроны движутся по цепи переносчиков от убихинола к цитохромоксидазе, генерируя разность электрических потенциалов, необходимую для образования АТФ протонной АТФсинтазой. Таким образом, тканевое дыхание «заряжает» митохондриальную мембрану, а окислительное фосфорилирование «разряжает» ее. Разность эл. потенциалов на митох. мембране, создаваемая дыхат. цепью, к-я выступает в качве молекулярного проводника электронов, является движущей силой для образования АТФ. Разобщение процессов дыхания и окислительного фосфорилирования происходит если протоны начинают проникать через внутреннюю мембрану митохондрий. В этом случае выравнивается градиент рН и исчезает движущая сила фосфорилирования. Хим. в-ва - разобщители называются протонофорами, они способны переносить протоны через мембрану. К таковым относятся 2,4 -динитрофенол,
гормоны щитовидной железы и др. В норме скорость митохондриального транспорта электронов регул-ся содержанием АДФ. Выполнение кл. ф-ций с затратой АТФ приводит к накоплению АДФ, к-й в свою очередь активирует тканевое дыхание. Т. о., клеткам свойственно реагировать на интенс-ть клет. метаболизма и поддерживать запасы АТФ на необходимом уровне. Это свойство называется дыхательным контролем
Свойства и строение гликогена,биосинтез гликогена,мобилизация гликогена(распад),его гормональная регуляция.
Гликоген — (C6H10O5)n, полисахарид, образованный остатками глюкозы, связанными α-1→4 связями (α-1→6 в местах разветвления); основной запасной углевод человека и животных. Гликоген (также иногда называемый животным крахмалом, несмотря на неточность этого термина) является основной формой хранения глюкозы в животных клетках. Откладывается в виде гранул в цитоплазме во многих типах клеток (главным образом печени и мышц) кетоновые тела-структура,механизм образования,окисление.Кетогенез при голодании и диабете.резистентность и склонность к кетозу у детей. При голодании глюкагон усиливает концентрацию жирных к-т вкрови благодаря мобилизации жиров. Активир. глюконеогенез. А также кетогенез, мобилизацию гликогена.
3. Кетоновые тела. Образование, окисление, причины усиления кетогенеза.
Жир. к-ты поступ. в печень в большем кол-ве, чем в норме, поэтому увеличивается скорость β- окисления. Ацетил-КоА накапл. в митохондриях печени и используется для синтеза кетоновых тел. Синтез кетоновых тел происходит только в митохондриях печени. Синтез кет. тел нач. с взаимод. 2 молек ацетил-КоА, под дейст.
тиолазы обр. ацетоацетил-КоА. С ацетоацетилКоА взаимодействует третья молекула ацетилКоА, образуя 3-гидрокси-3-метилглутарил-КоА. Эту реакцию катализирует ГМГ-КоАсинтаза.
Далее ГМГ-КоА-лиаза катализирует расщепление ГМГ-КоА на свободный ацетоацетат и ацетил-КоА. Ацетоацетат может выделяться в кровь или превращаться в печени в другое кетоновое тело - β-гидроксибутират путём восстановления.
Уже через 2-3 дня после начала голодания концция кет. тел в крови достаточна для того, чтобы они проходили в клетки мозга и окислялись, снижая его потребности в глюкозе. β- Гидроксибутират), попадая в клетки, дегидрируется НАД-зависимой ДГ и превращ. в ацетоацетат. Ацетоацетат активируется, взаимодействуя с сукцинил-КоА - донором КоА:
4. Гормоны мозгового вещества надпочечников, их синтез и физиологические функции.
Гормоны мозгового вещества — катехоламины
Гормоны мозгового вещества — катехоламины — образуются из аминокислоты тирозина поэтапно: тирозинДОФАдофамин- норадреналин-адреналин. Хотя надпочечник и секретирует значительно больше адреналина, тем не менее в состоянии покоя в крови содержится в четыре раза больше норадреналина, так как он поступает в кровь и из симпатических окончаний. Секреция катехоламинов в кровь хромаффинными клетками осуществляется с обязательным участием Са+2, кальмодулина и особого белка синексина, обеспечивающего агрегацию отдельных гранул и их связь с фосфолипидами мембраны клетки. Катехоламины называют гормонами срочного приспособления к действию сверхпороговых раздражителей среды.
Физиологические эффекты катехоламинов
Физиологические эффекты катехоламинов, обусловлены различиями в адренорецепторах (альфа и бета) клеточных мембран, при этом адреналин обладает большим сродством к бетаадренорецепторам, а норадреналин — альфа.
Основные функциональные эффекты адреналина
Повышение чувствительности адренорецепторов к адреналину, т.е. пермиссивный эффект, оказывают гормоны щитовидной железы и глюкокортикоиды.
Основные функциональные эффекты
адреналина проявляются в виде:
1)Учащения и усиления сердечных сокращений,
2)Сужения сосудов кожи и органов брюшной полости,
3)Повышения теплообразования в тканях,
4)Ослабления сокращений желудка и кишечника,
5)Расслабления бронхиальной мускулатуры,
6)Стимуляции секреции ренина почкой,
7)Уменьшения образования мочи,
8)Повышения возбудимости нервной системы и эффективности приспособительных реакций.
Адреналин вызывает мощные метаболическе
эффекты в виде усиленного расщепления
гликогена в печени и мышцах из-за активации фосфорилазы, а также подавление синтеза гликогена, угнетение потребления глюкозы тканями, что в целом ведет к гипергликемии. Адреналин вызывает активацию распада жира, мобилизацию в кровь жирных кислот и их окисление. Все эти эффекты противоположны действию инсулина, поэтому адреналин называют контринсулярным гормоном. Адреналин усиливает окислительные процессы в тканях и повышает потребление ими кислорода.
Таким образом, как кортикостероиды, так и катехоламины обеспечивают активацию приспособительных защитных реакций организма и их энергоснабжение, неспецифически повышая устойчивость к неблагоприятных влияниям среды.
Задача
Биохимические признаки атеросклероза. Атеросклероз - наиболее распространенное хроническое заболевание артерий, с формированием одиночных и множественных очагов липидных, главным образом холестериновых отложений — бляшек во внутренней оболочке артерий. Последующие разрастания в ней соединительной ткани (склероз) и отложение кальция в стенки сосуда приводят к деформации и сужению его просвета вплоть до полной закупорки артерии. Тем самым вызывается недостаточность кровоснабжения органа, питаемого через пораженную артерию. Кроме того, возможна острая закупорка (окклюзия) просвета артерии либо тромбом, либо (значительно реже) содержимым распавшейся бляшки, либо и тем и другим одновременно, что ведет к образованию очагов некроза (инфаркт) или гангрены в органе, который питается этой артерией. Атеросклероз возникает при повышении уровень холестерина в крови (>6 ммоль\л ). Кол-во лонп не должно превышать 3,0 ммоль/л и должно составлять не более 75% от общего уровня липопротеидов.
Билет 30.
1. Общая характеристика витаминов, классификация, биологическое значение,
источники, потребность, а-, гипо-,
гиперавитаминозы. Кофакторы и коферменты.
ВИТАМИНЫ - биологически активные низкомолекулярные органические вещества, принимающие участие в биологическом катализе. Являются незаменимыми факторами питания, не синтезируются в организме человека и поступают с растительной пищей и пищей животного происхождения. Исключение составляют: 1) в/р вит.РР – синтезируется в печени из триптофана (н/з а/к); 2) ж/р вит. D3 – синтезируется в коже из 7-дегидрохолестерина под действием УФ; 3) ж/р ретинол – в печени из каротинов. Также витамины синтезируются м/ф кишечника: В1-тиамин, В2-рибофлавин, В6пиридоксин, В12-кобаламин, РР-никотиновая кислота, В9-фолиевая кислота, В5-пантотеновая кислота, К-нафтохинон, Н-биотин.
Витамины делятся на жиро- (ж/р: А, Д, Е, К, F) и водорастворимые (в/р: В1, В2, В3, РР, В6, В9, В12,
Н, С).
Гипервитаминоз– острое расстройство в результате интоксикации сверхвысокой дозой одного или нескольких витаминов, содержащихся в пище или витаминных пилюлях. У взрослых это состояние может быть обусловлено употреблением в пищу большого количества продуктов, богатых тем или иным витамином, или индивидуальной гиперчувствительностью к витаминам - в этом случае достаточно и небольшой дозы витаминного препарата.
Коферменты, или коэнзимы — малые молекулы небелковой природы, специфически соединяющиеся с соответствующими белками,
называемыми апоферментами, и играющие роль активного центра или простетической группы молекулы фермента.
Комплекс кофермента и апофермента образует целостную, биологически активную молекулу фермента, называемую холоферментом
Кофакторнебелковое вещество, которое обязательно должно присутствовать в организме в небольших количествах, чтобы соответствующие ферменты смогли выполнить свои функции. В состав кофактора входят коферменты и ионы металлов (например, ионы натрия и калия).
2. Наследственные нарушения обмена
моносахаридов и дисахаридов: галактоземия, непереносимость фруктозы, непереносимость дисахаридов.
Галактоземия - возникает при нарушении обмена галактозы в рез-те недостатка фермента галактоза-1-фосфатуридилтрансферазы. Проявл. у н/р, питающихся материнским молоком. ранние симптомы - рвота, диарея, дегидратация. уменьш. массы тела. В крови, моче и тканях повышается конц-ция галактозы и галактозо-1-фосфата. В хруст. глаза галактоза восст. альдоредуктазой с образованием спирта галактитола, который накапл. в стекловидном теле глаза, связ. большое кол-во воды. происх. чрезмерная гидратация хрусталика, разв. катаракта. Накопление галактозо-1-фосфата в печени приводит к токсич. возд. на гепатоциты., возн. гепатомегалия и жировая дистрофия печени. В почках накопление галактозо-1- фосфата и галактитола приводит к наруш. работы. Наруш. отмеч. также в кл. гол. мозга. В тяж. случаях набл. отек мозга, задержка умст. развития. Гал-мия м.б. вызвана действием фермента галактокиназы, при этом возн. катаракта но не страдает печень, почки и головной мозг.
Непереносимость фруктозы. Недостаток фруктокиназы клин. не проявляется. Фруктоза
накапливается в крови и выделяется с мочой. где ее можно обнаружить лаб. методами.
Недостаток фруктозо-1-фосфорилазы может возн. при генетич. дефекте. Пока реб. питается груд. молоком., клинич. симпт. не прояв. При изменении рациона после приема пищи появ. рвота, боли в животе, понос, сниж. уровень сахара в крови, может появ. кома. у детей.
Непереносимость дисахаридов — наслед. или приобр. недостат-ть акт-ти дисахаридаз, обуслщая наруш. расщепления и всас. дисахаридов; выз-т непереносимость лактозы, сахарозы и/или мальтозы; проявл.: расстр. пищевар. в виде хронич. фермент. диспепсии.
Недост. лактазы. проявл.: неперенос. материнского и коровьего молока, богатого лактозой. Первич. (врождённая) неперенос. лактозы — сниж. уровня фермента лактазы, Вторич. неперен. лактозы может возникнуть при забол., сопров. пораж. слизистой об-ки киш. (диарея, лямблиоз, резекция кишечника и др.). При вскарм. молоком у ребёнка появл. кишеч. колики, метеоризм, упорная диарея, разв. гипотрофия. Испорожнения водянистые, пенистые, с кислой р-цией. Возм. тяжёлое течение с сепсисом, поражением почек и печени. Безмолочная диета или молоко с исключением лактозы.
Недост. сахаразы — неперен. сахарозы, клин. проявляется диареей после включения в пищу сахарозы, клин. картина зависит от кол-ва принятого дисахарида. Испоражнения водянистые, пенистые, с высоким содержанием молоч к-ты и летучих жирных кислот. Набл. рвота. Гипотрофия, повыш. t.
3. Представление о биосинтезе и катаболизме
фосфолипидов и гликолипидов. Функции фосфолипидов и гликолипидов. Сфинголипидозы.
Катаболизм гликолипидов происходит в лизосомах.
Синтез гликолипидов начинается с присоединения первого моносахаридного остатка к церамиду. Здесь действует фермент — галактозилтрансфераза. Для завершения синтеза требуется еще несколько трансфераз с различной субстратной специфичностью. Гликолипиды встречаются только в мембранах, и, главным образом, в плазматической мембране.
Гликолипиды входят в состав простых липидов растительных масел и жиров. Гликолипидами называется большая и разнообразная по строению группа нейтральных липидов, в состав которых входят остатки моноз. Они широко (обычно в небольших количествах) содержатся в растениях (липиды пшеницы, овса, кукурузы, подсолнечника), животных и микроорганизмах. Гликолипиды выполняют структурные функции, участвуют в построении мембран, им принадлежит важная роль в формировании клейковинных белков пшеницы, определяющих хлебопекарное достоинство муки. Чаще всего в построении молекул гликолипидов участвуют D- галактоза, D-глюкоза, D-манноза.
Фосфолипиды могут синтезироваться во многих тканях организма,. но в плазму почти целиком поступают из печени и слизистой оболочки кишечника. Фосфолипиды пищи как таковые не всасываются, а подвергаются гидролизу фосфолипазами в кишечном соке с образованием как лизофосфатидов, так и основного компонента; фосфорсодержащего амина, двух молекул жирных кислот и глицерина. Фосфолипиды разрушаются, находясь в составе соответствующих липопротеинов, и столь же легко обмениваются между липопротеинами и клеточными мембранами. Катаболизм отдельных фосфолипидов может происходить либо до их

распада на основные компоненты, либо в ходе реакций деацилирования—реацилирования с изменением их жирокислотного состава.
Фосфолипиды играют важную роль в организме человека. Входя в состав клеточных оболочек, они имеют существенное значение для их проницаемости и обмена веществ между клетками и внутриклеточным пространством. Фосфолипиды пищевых продуктов различаются по химическому составу и биологическому действию. В пищевых продуктах в основном встречаются лецитин, в состав которого входит холин, а также кефалин, в состав которого входит этаноламин.
Сфинголипидозы - врожденные нарушения метаболизма липидов, главным образом сфинголипидов, обусловленные отсутствием лизосомных ферментов , катализирующих процессы распада сфинголипидов.
Сфинголипиды — это класс липидов, относящихся к производным алифатических аминоспиртов. Они играют важную роль в передаче клеточного сигнала и в клеточном распознавании. Особенно богата сфинголипидами
4. Пути обезвреживания аммиака в организме.
Цикл мочевинообразования. Механизмы обезвреживания в нервной и мышечной ткани.
Из организма аммиак выводится в виде конечных продуктов азотистого обмена: мочевины, аммонийных солей. Основной р- цией обезвреживания явл.синтез глутамина.
Глутамин можно считать транспортной формой аммиака, он явл. нейтр.ам-к и способен легко проникать в кл.мембраны путем облегченной диффузии. В печени аммиак обезвреживается путем связывания с СО2 и образования карбамоилфосфата, используется 2АТФ. Затем карбамоилфосфат исп. в орнитиновом цикле.
Мочевая кислота является фракцией остаточного азота и конечным продуктом обмена пуриновых оснований (аденина и гуанина). М.к-та, выводимая с мочой отражает поступление пуринов с пищей и распад эндогенных пуриновых нуклеотидов. Орнитиновый цикл в печени выполняет 2 ф-ции
– превращение азота ам-к в мочевину, кот.экскретируется и помогает избежать накопления аммиака в организме.; синтез аргинина и пополнение его фонда в организме.
