
Bilety2
.pdfсвязываются в цитоплазме с рецепторными белками. После связывания рецептора с гормоном резко повышается его сродство к ядерному хроматину.
Взаимодействие стероидных рецепторов с ДНК осуществляется через ДНКсвязывающие участки рецептора . С другой стороны, в составе ДНК имеются специфические гормончувствительные элементы, примыкающие, как правило, с 5 - конца к гормон-зависимым генам.
5. В результате анализа сыворотки крови, взятой натощак, было обнаружено высокое содержание кетоновых тел. Ваш комментарий.
Кетоновые тела — группа органических соединений, являющихся промежуточными продуктами жирового, углеводного и белкового обменов.Появление повышенных количеств К. т.
БИЛЕТ 15
1. Уровни организации белковых молекул. Первичная, вторичная, третичная и четвертичная структура белка и их краткая характеристика.
Белкивысокомолекулярные биологич полимеры, составленные из 21 различн.мономераальфа- а/к остатков, соединенных пептидной связью. Если аминокислотная цепь содержит менее 10-20 остатков а/к, ее называют пептидом, если более полипепептидом. Полипептиды состоят из 50 и более а/к остатков. назбелками. Общая формула а/к: пептидные связи соедин аминогруппой одной а/к с карбоксильной
группой др а/к. Пептидные связи очень прочные
для их разрушения вне организма организма требуются высокая температура и и давление, сильно кислая или сильно щелочная среда и длительное время. В клетках организма пептидная связь разрывается
в крови и моче является важным диагностическим признаком, свидетельствующим о нарушении углеводного и жирового обменов (так как не образуется оксалоацетат)
Из печени К. т. поступают в кровь и с нею во все остальные органы и ткани, где они включаются в универсальный энергообразующий цикл — цикл трикарбоновых кислот, в котором окисляются до углекислоты и воды.
Кетонемию и кетонурию наблюдают при сахарном диабете, углеводном голодании, лихорадочных состояниях, общем голодании и истощении (повышен кетогенез), приеме богатой кетогенными веществами пищи (усилен кетогенез),и др.
протеолитическими ферментами. Вращение вокруг связи С-N требует больших затрат энергии и затруднено. Пептидная цепь имеет одно направление и 2 разных конца-N конец несет свободную аминогруппу первой а/к и C- конец несет карбоксильную группу последнего а/ к остатка.
Уровни организации бел молекул. Структура
белка и их характеристика:
Б. представляют собой сложные полипептиды, а/к в кот связаны пептидн связями, обращающимися при взаимодейтвии альфакарбоксильных и альфа-аминогрупп а/к.
К дипептидн могут могут присоединиться другие а/к, образуя три-, тетра-, пентапептиды и тд вплоть до образования крупного полипептида. Последовательность расположения а/к в полипептиде представляет собой первичную структуру белка. Всего существует 4 уровня структурной организации белкапервичная, вторичная, третичная, четвертичная структура.
Большинство белков состоят из 3 уровней. Первичная:
Последовательность расположения а/к остатков в полипептиде. Особенности:
-первичная структура Б. Генетически детерминирована и уникальна, замена а/к внутри полипептидной цепи приводит к изменению структуры и функции белка
-она стабильна, это обеспечивается дипептидными и дисульфидными связями
-число комбинаций а/ к в полирхпептиде оч велико, повторяющихся последовательности а/к редки. Идентичная последовательность а/к в обл активных центров ферментов
-она детерминирует вторичную, третичную и четвертичную структуру белк молекулы Вторичная:
-конфигурация полипептидной цепи, более компактно упакована в спиральную или какую либо другую конфирмацию. Процесс конфирмации идет в соответствии с программой заложенной в первичной структуре Б. Существуют 2 осн конфигурации полипептидной цепи: альфаспераль и бета-складчатый слой. Третичная:
-это пространственная ориентация полипептидной спирали, следующая за вторичной структурой способ компактизации белк. молекулы. Процесс укладки полипептидной цепифолдинг. Третичная структура белка формируется самопроизвольное полностью детерминир-яс первичную структуру Б. Основной движущий моментвзаимодействие радикалов а/ к с мол воды, сост в том, что гидрофобные радикалы а/ к ориентируются внутри мол Б. В то время как гидрофильные радикалы ориентируются снаружи Четвертичная:
-пространственная ориентация нескольких полипептидных цепей, обладают собственной первичной, вторичной, или третичной
структурой, с образованием макромолекулярного образования
2. Пентозофосфатный путь превращения глюкозы. Значение этого пути для эритроцитов и жировой ткани
(формула на листке!)
Схематически пентозофосфатный путь выглядит так: глюкоза→глюкозо-6-фосфат → 6- фосфатглюконолактон → рибулозо-5-фосфат → рибозо-5-фосфат. В Эритроцитах для восстановления глутатиона-SH (инактивирует активный кислород, вызывающего преджевременный лизиз) В Жирных кислотах для синтеза жтрных кислот
3. Образование желчных кислот и их роль в переваривании жиров. Конъюгирование желчных кислот, первичные и вторичные желчные кислоты
Образование: синтезированные в гепатоцитах
первичные желчные:холевая и хенодезоксихолева, кислоты экскретируются в
желчь конъюгированными с глицином или таурином и по желчевыводящим путям поступают в желчный пузырь, где и накапливаются. Вторичные желчные кислоты
(дезоксихолевая и литохолевая) образуются из первичных (холевой и хенодезоксихолевой соответственно) под воздействием анаэробных бактерий толстой кишки Жёлчные кислоты синтезируются в печени из холестерола и секретируются в жёлчный пузырь. Содержимое жёлчного пузыря - жёлчь. Это вязкая жёлтозелёная жидкость, содержащая главным образом жёлчные кислоты; в небольшом количестве имеются фосфолипиды и холестерол.
Роль в переваривании:Жёлчные кислоты представляют собой в основном конъюгированные жёлчные кислоты: таурохолевую, гликохолевую и другие. После
приёма жирной пищи жёлчный пузырь сокращается и жёлчь изливается в просвет двенадцатиперстной кишки. Жёлчные кислоты действуют как детергенты, располагаясь на поверхности капель жира и снижая поверхностное натяжение. В результате крупные капли жира распадаются на множество мелких, т.е. происходит эмульгирование жира. Эмульгирование приводит к увеличению площади поверхности раздела фаз жир/вода, что ускоряет гидролиз жира панкреатической липазой. Эмульгированию способствует и перистальтика кишечника.
Конъюгирование - присоединение ионизированных молекул глицина или таурина к карбоксильной группе жёлчных кислот; усиливает их детергентные свойства, так как увеличивает амфифильность молекул.
Конъюгация происходит в клетках печени и начинается с образования активной формы жёлчных кислот - производных КоА
Затем присоединяется таурин или глицин, и в результате образуется 4 варианта конъюгатов: таурохолевая и таурохенодезоксихолевая, гликохолевая или гликохенодезоксихолевая кислоты (они значительно более сильные эмульгаторы, чем исходные жёлчные кислоты).
Конъюгатов с глицином образуется в 3 раза больше, чем с таурином, так как количество таурина ограничено.
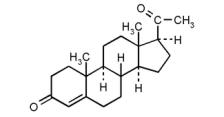
4.Эстрогены, их химическое строение, механизм действия и физиологическая роль.
Стероидные г., в основном синт-ся в фоллик.
Плацента также продуц эстрогены. Прогестерон
сост из 18 ат. С. Эти горм выз. разв. вторич. пол. признаков., прог. подгот. слиз. об. матки к имплант. яйцекл., сохр. берем., торм. овуляцию и стимул. разв. тк. молоч. ж-зы. Эстрогены оказ. анаболич. дейст., стимул. синтез белка. Связ. с
внутриклет. рецеп. и регулир. транскрип. генов подобно стер. горм. Эстрогены повышают концентрации в крови тироксина, железа, меди. Оказывают антиатеросклеротическое действие, увеличивают содержание ЛПВП, уменьшает ЛПНП и холестерина (уровень триглицеридов возрастает).
5. В суточной моче у пациента было обнаружено 10-кратное превышение содержания уропорфирина 1 и копропорфирина 1. Ваш комментарий
Эритропоэтическая уропорфирия — редкое врожденное тяжелое заболевание, наследуется аутосомно по рецессивному типу.
Заболевание может проявляться у новорожденных, появляется моча красного цвета. Освобождающийся из эритроцитов уропорфириноген окисляется в уропорфирин и откладывается в коже, спустя несколько недель или месяцев после рождения на теле ребенка появляются пузыри с последующим развитием язв, которые на фоне антибиотикотерапии рубцуются, оставляя участки склерозированной кожи на лице и другой локализации. У ребенка нередко возникают контрактура суставов и слепота, отсутствуют волосы, ногти. У больных обнаруживается увеличение селезенки. Выявляется гемолитическая анемия с внутриклеточным гемолизом, повышен уровень свободного билирубина сыворотки крови. Укорочена продожительность жизни эритроцитов, часто снижена их осмотическая
резистентность. Повышен уропорфирин и копропорфирин мочи и эритроцитов.
БИЛЕТ 16
Зависимость скорости ферментативных реакций от факторов окружающей среды.
Скорость ферм. р-ции опр. изм. кол-ва субстрата или прод. р-ции за ед. времени. Зав. от конц. субст, ферм., кофактора, прод. р-ции, от рН обусл. влиянием на ионизацию функ. гр. в акт. центре ферм., функ. гр. субст. При значит откл рН от опт. знач. фермент. акт. утрач. из-за денатур. от температуры - с ростом t увелич. скть р-ции, т.к. увелич. ск-ть достижения перех. сост. субстр., с повыш t увелич вероятн. денатур. ферм. и разруш. струк. акт. центра. При увелич. конц. ферм. ск-ть р-ции увелич. линейно. При пост. конц. ферм. скорость р-ции при увелич. кол-ва субст. увелич. гиперболически.
Биосинтез глюкозы из аминокислот, глицерина и молочной кислоты. Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори).
Аминокислоты и глицерин используются для синтеза глюкозы главным образом при голодании или при низком содержании углеводов в рационе (углеводное голодание). В этих условиях глюконеогенез служит для обеспечения глюкозой мозга, в то время как другие органы обеспечиваются энергией за счет окисления жирных кислот.Физиологическая роль глюконеогенеза из лактата существенно иная. Молочная кислота не является конечным продуктом обмена, но ее образование — это тупиковый путь метаболизма: единственный способ использования молочной кислоты связан с ее превращением вновь в пируват при участии той же лактатдегидро-геназы:Из клеток, в которых происходит гликолиз, образующаяся молочная кислота поступает в кровь и улавливается в основном печенью, где и превращается в пируват. Пируват в печени частично окисляется, частично превращается в глюкозу — цикл Кори, или глюкозо-лактатный
цикл (рис. 9.24). Часть пирувата в мышцах путем трансаминирования превращается в аланин, который транспортируется в печень, и здесь снова образует пируват — глюкозо-аланиновый цикл.
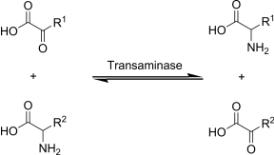
Трансаминирование, химизм процесса, специфичность аминотрансфераз. Диагностическое значение определения аминотрансфераз.
Трансаминирование - пренос а-аминогруппы с аминоксилоты на а-кетокислоту. Р-ции катализ. ферм. аминотрансферазы, коферм. к-х служит пиридоксальфосфат.
Пиридоксальфосфат явл. простетич. гр. декарбоксилазы аминокислот.
Кофермент аминотрансфераз, синтетаз, гидроксилаз и других ферментов, уч. в метаб. аминок-т; особенно важна его роль в метаб. триптофана, глицина, серина, глутамата. Пиридоксальфосфат необходим также для синтеза предшественника гема . Кроме того, он стабилизирует структуру мышечной фосфорилазы (в составе этого фермента сосредоточе на значительная часть запасов витамина В6).
Андрогены, основные представители, физикохимическая характеристика, их биологическое значение.
Андрогены— общее собирательное название группы стероидных гормонов, производимых

половыми железами (семенниками у мужчин и яичниками у женщин) и корой надпочечников и обладающих свойством в определённых концентрациях вызывать андрогенез, вирилизацию организма — развитие мужских вторичных половых признаков — у обоих полов. Понижают уровень глюкозы в крови. Увеличивают мышечную массу и силу. Способствуют снижению общего количества подкожного жира и уменьшению жировой массы по отношению к мышечной массе, но могут увеличить отложения жира по мужскому типу (на животе) при одновременном уменьшении отложений жира в типично женских местах (ягодицы и бедра, грудь). Понижают уровень холестерина и липидов в крови, тормозят развитие атеросклероза и сердечно-сосудистых заболеваний, но в меньшей степени, чем эстрогены (отчасти именно поэтому у мужчин продолжительность жизни меньше и сердечно-сосудистые заболевания чаще и развиваются в более молодом возрасте, чем у женщин).Андрогены вызывают появление или развитие мужских вторичных половых признаков: понижение и огрубление голоса, рост волос на лице и теле по мужскому типу, превращение пушковых волос на лице и теле в терминальные, усиление секреции пота и изменение его запаха.
У пациента в моче было обнаружено 10кратное увеличение содержания гомогентизиновой кислоты. Ваш комментарий.
Выпадение функций оксидазы гомогентизиновой кислоты, характеризующееся расстройством обмена тирозина и экскрецией с мочой большого количества гомогентизиновой кислоты – алкаптонурия. Данная патология характеризуется аутосомно-рецессивным типом наследования. Алкаптонурией чаще болеют мужчины. В нормальных условиях гомогентезиновая кислота — промежуточный продукт распада тирозина и фенилаланина — переводится в фумарат и ацетоацетон, вступающие в другие биохимические циклы. Ранний признак алкаптонурии — выделение у ребенка мочи, быстро темнеющей при стоянии на воздухе. В дальнейшем может присоединиться мочекаменная болезнь, осложняющаяся пиелонефритом.
БИЛЕТ 17
1. Строение нуклеиновых кислот. Азотистые основания и сахара, входящие в состав ДНК и
РНК. Нуклеозиды и нуклеотиды. Адениловые динуклеотиды (НАД, НАДФ, ФАД). Связи, формирующие первичную структуру ДНК и РНК, –5`-фосфатный и 3`- гидроксильный концы полинуклеотидных цепей. Вторичная структура ДНК и РНК. Денатурация и ренатурация ДНК
(Формулы отдельные!)
Встречаются два типа нуклеиновых кислот: рибонуклеиновая кислота (РНК) и дезоксирибонуклеиновая кислота (ДНК), различающиеся между собой по нуклеотидному составу. Углеводным компонентом РНК является рибоза, а ДНК — дезоксирибоза. В составе РНК встречаются четыре основных азотистых основания — аденин, гуанин, цитозин и урацил. Нуклеотиды, образующие ДНК, также содержат четыре основных азотистых основания — аденин, гуанин, цитозин и тимин.
Один конец РНК заканчивается свободным остатком фосфорной кислоты, который присоединен к пятому атому углерода сахара. Этот конец считают началом полинуклеотидной
Цепи и называют 5-концом. На другом конце РНК у третьего атома углерода сахара оказывается свободной гидроксильная группа (3-конец). Соединения азотистых оснований с рибозой или 2-дезоксирибозой носят название нуклеозиды.
НАД – никотинамидадениндинуклеотид;
НАДФ – никотинамидаденин динуклеотид фосфат. Молекулы НАД и НФДФ способны к обратимому окислению и восстановлению
(благодаря окислительно-восстановительной
способности никотинамида), поэтому они участвуют в качестве переносчиков водорода; в реакциях биологического окисления НАД и НАДФ являются кофакторами ферментов дегидрогеназ.
Структурными единицами нукл кислот явл нуклеотиды,сост из азотист основания,углевода(заним центр место) и фосфорной к-ты. Нуклеозиды- соединения, сост из остатка азотистого основания и углевода — рибозы (рибонуклеозиды) или дезоксирибозы (дезоксирибонуклеозиды):
ДНК — Дезоксирибонуклеиновая к-та. Сахар — дезоксирибоза, азотистые основания: пуриновые — гуанин (G), аденин (A), пиримидиновые — тимин (T) и цитозин (C).
ДНК часто состоит из двух полинуклеотидных цепей, направленных антипараллельно
Вторичная структура ДНК и РНК образ-ся за счет взаимод нуклеотидов (в большей степени азотистых оснований) между собой, водородных связей. Классич пример вторичн структуры ДНК - двойная спираль ДНК – это сам распростр в природе форма ДНК, сост из двух полинуклеотидных цепей ДНК. Построение каждой новой цепи ДНК осуществл по принципу комплементарности, т.е. каждому азотистому основанию одной цепи ДНК соотв строго опред основание др цепи: в комплемнтарной паре напротив A стоит T, а напротив G располагается C и т.д. Молекула ДНК имеет форму спирали,образованную двумя полинуклеотидными цепями,закрученными вокруг друг другва и вокруг общей оси.Двойная спирать правозакрученная,полунуклеотидные цепи в ней антипараллельны(одна3-5,другая 5- 3)На кождом из концов молекулы ДНК расположены 5 и 3 конец.Полинуклеиновые цепи удерживаются относительно друг друга за счет водородных связец между комплементарнымми пуриновыми и пиримидиновыми основаниями.Так последовательеость нуклеотидов одной цепи комплементара последовательности другой.
Вторичная структура матричных и рибосомных РНК Она построена из одной нуклеотидной цени.Отдельные участки цепи РНК образуют спирализованные петли-«шпильки»,за счет водородных связей между комплементарными азотистыми основаниями.
Особенности вторичной структуры ДНК:
1)молекула ДНК построена из двух полинуклеотидных цепей, связанных между собой водородными связями и ориентированных антипараллельно (то есть 3'- конец одной цепи расположен напротив 5'- конца другой цепи и наоборот);
2)водородные связи образуются между комплементарными парами азотистых оснований.
3)обе цепи ДНК закручены в спираль, имеющую общую ось. Азотистые основания обращены внутрь спирали; кроме водородных, между ними возникают также гидрофобные взаимодействия. Рибозофосфатные части расположены по периферии, образуя остов спирали.
Денатурация-расхождение ДНК,в результате
разрыва водородных и гидрофобных связей цепи ДНК,под дейстпием различных окружающих факторов(температура)
Ренатурация — процесс, обратный денатурации, при котором белки возвращают свою природную структуру.
2. Гликолиз, его биологическое значение, последовательность реакций гликолиза в анаэробных условиях. Энергетический выход или КПД гликолиза. (на формулы “гликолиз” до образования ПВК!)
Аэробный путь окисления глюкозы происходит в 3 этапа:
1.окисление молекулы глюкозы до 2 молекул пирувата;
2.окислительное декарбоксилирование пирувата (с образованием 2 молекул ацетилКоА);
3.реакции цикла Кребса, где каждая молекула ацетил-КоА сгорает с образованием 12 АТФ.
1-ый этап. Окисление молекулы глюкозы до
2молекул пирувата - это первые 10 реакций гликолиза. Суммарная реакция 1 этапа: Глюкоза + 2 НАД+ + 2 АДФ ^ 2 пирувата + 2 НАДН + Н+ + 2 АТФ
2-ой этап. Окислительное декарбоксилирование пирувата (с образованием 2 молекул ацетил-КоА) происходит в матриксе митохондрий и осуществляется мультиферментным комплексом пируватдегидрогеназой. В его состав входят 3 фермента и 5 коферментов:
1.Пируватдекарбоксилаза - кофермент тиаминпирофосфат (активная формавитамина В1).
2.Дегидролипоилацетилтрансфераза - кофермента: в активном центре - липоевая кислота (витаминоподобное вещество), из матрикса митохондрий используется Коэнзим А
(КоА~8Н).
3.Дигидролипоилдегидрогеназа - коферменты: в активном центре - ФАД, из матрикса митохондрий используется - НАД.
Суммарная реакция: 2 Пируват + 2 НАД+ + КоА ^
2ацетил-КоА + 2 НАДН + Н+ Каждый восстановленный НАД в митохондриях
отдает протоны и электроны в полную ц.п.э., где образуется 2 х 3 АТФ = 6 АТФ. Таким образом, ценность второго этапа - 6 АТФ. Эти реакции происходят только в аэробных условиях!
3-ий этап. Реакции цикла Кребса, где каждая молекула ацетил-КоА сгорает с
образованием 12 АТФ. Следовательно, энергетический выход третьего этапа (в расчете на молекулу глюкозы) - 2 х 12 АТФ = 24 АТФ.
3. Фосфолипиды, разновидности, структура, роль в построении биомембран и в формировании их функциональных особенностей.
Фосфолипиды (фосфоглицериды) - это сложные липиды, производные фосфатидной кислоты. Липидам принадлежит главная роль в образовании мембран клеток. Основная часть липидов в мембранах представлена фосфолипидами, гликолипидами и холестерином.
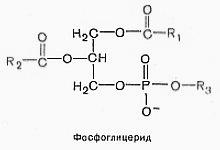 (лецитин, кефалин, глицерофосфатиды – класс-ия)
(лецитин, кефалин, глицерофосфатиды – класс-ия)
Вмембранах имеются фосфолипиды двух типов - глицерофосфолипиды и сфингофосфолипиды.
Всостав глицерофосфолипидов входят глицерин, жирные кислоты, фосфорная кислота и обычно азотсодержащие соединения.
Вклеточной мембране фосфолипиды образуют двойной слой, в котором гидрофобные цепи жирных кислот направлены внутрь мембраны, а гидрофильные полярные группы кнаружи.
Основной структурой мембраны клетки
является двойной слой фосфолипидных молекул. За счет гидрофобных взаимодействий углеводные цепочки липидных молекул удерживаются друг возле друга в вытянутом
состоянии. Благодаря тому, что большинство липидных компонентов бислоя находится в жидком состоянии, мембрана обладает подвижностью, совершает волнообразные движения. Ее участки, а также белки, погруженные в липидный бислой, перемешаются из одной ее части в другую.
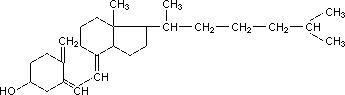
1.4.Витамины группы D, их строение и физиологическая роль. Образование 1,25дигидроксихолекальциферола и его роль в регуляции обмена кальция и фосфора.
Витамины группы D (кальциферолы)
Кальциферолы - группа химически родственных соединений, относящихся к производным стеринов. Наиболее биологически активные витамины - D2 и D3. Витамин
D2 (эргокалыщферол), производное эргостерина - растительного стероида, встречающегося в некоторых грибах, дрожжах и растительных маслах. При облучении пищевых продуктов УФО из эргостерина получается витамин D2, используемый в лечебных целях. Витамин D3, имеющийся у человека и животных, - холекальциферол, образующийся в коже человека из 7-дегидрохолестерина под действием УФ-лучей
Витамины D2 и D3 - белые кристаллы, жирные на ощупь, нерастворимые в воде, но хорошо растворимые в жирах и органических растворителях.
Провитамины D2 и D3 - стерины, у которых в кольце В две двойные связи. При воздействии света в процессе фотохимической реакции происходит расщепление кольца В. А - 7- дегидрохолестерин, провитамин D3, (синтезируется из холестерина); Б - эргостерин - провитамин D2.
Биологическая роль. В организме человека витамин D3 гидроксилируется в положениях 25 и 1 и превращается в биологически активное соединение 1,25дигидроксихолекальциферол (калыщтриол). Калыщтриол выполняет гормональную функцию, участвуя в регуляции обмена Са2+ и фосфатов, стимулируя всасывание Са2+ в кишечнике и кальцификацию костной ткани, реабсорбцию Са2+и фосфатов в почках. При низкой концентрации Са2+ или высокой концентрации D3 он стимулирует мобилизацию Са2+ из костей (см. раздел 11).
Недостаточность. При недостатке витамина D у детей развивается заболевание "рахит", характеризуемое нарушением кальцификации растущих костей. При этом наблюдают деформацию скелета с характерными изменениями костей (Х- или о-образная форма ног, "чётки" на рёбрах, деформация костей черепа, задержка прорезывания зубов).
Гипервитаминоз D. Это состояние характеризуется избыточным отложением солей кальция в тканях лёгких, почек, сердца, стенках сосудов, а также остеопорозом с частыми переломами костей.
5. В крови пациента было обнаружено высокое содержание лактатдегидрогеназы (ЛДГ1) и тропонина Т. Ваш комментарий
Это фермент, который участвует в процессе окисления глюкозы и образовании молочной кислоты. Лактат образуется в клетках в процессе дыхания. Лактатдегидрогеназа содержится почти во всех органах и тканях человека, особенно много его в мышцах.
При полноценном снабжении кислородом лактат в крови не накапливается, а разрушается до нейтральных продуктов и выводится. В условиях гипоксии (недостатка кислорода) накапливается, вызывает чувство мышечной усталости, нарушает процесс тканевого дыхания. Тропонины — небольшие белки, включённые в процесс регуляции мышечного сокращения. Два вида тропонинов, тропонин-I и тропонин-T(миокард), структурно различаются в скелетной и сердечной мышцах. Для тропонинов отношение концентрации внутри мышечных клеток к концентрации в плазме крови намного выше, чем для ферментов и миоглобина, что делает эти белки высокочувствительными маркёрами поражения миокарда. Можно говорить в данном случае, об инфаркте миокарда
БИЛЕТ 18
Дыхательная цепь. Строение и основные принципы. Теория содержания окисления и фосфорилирования.
Дыхательная цепь - это переносчики протонов и электронов от окисляемого субстрата на О2. Дыхат. цепь состоит из: НАД-зависимой дегидрогеназы; ФАД-зависимой дегидрогеназы; Убихинона (КоQ); Цитохрмов b, c, a+a3. Соединение может отдавать электроны только соед-ю с более высоким ок-восст. потенциалом. В дых. цепи каждое последующее звено имеет
