Лиофильные дисперсные системы (1)
Особенности строения молекул ПАВ
Молекула ПАВ имеет дифильное строение, то есть состоит из полярной (функциональной) группы и углеводородного радикала:
Гидрофильная группа |
|
Гидрофобный радикал |
|
|
Классификация ПАВ
По химическому строению |
По коллоидно-химическим свойствам |
Ионные |
|
Неионные |
|
Истинно растворимые |
|
Коллоидные |
|
|
|
|
|
|
|
Лиофильные дисперсные системы (2)
Классификация ПАВ (продолжение)
C12H25SO3Na
R1(R2)3NBr
C12H25(CH3)3NBr
|
Ионные |
Анионные |
Амфотерные Катионные |
|
Анионные ПАВ: |
а) карбоновые кислоты и их соли – |
RCOOH, RCOOM (M-катион); |
б) алкилсульфаты ROSO2OM; |
в) алкиларилсульфонаты RArSO2OM; |
г) др. классы ПАВ, содержащие |
поверхностноактивный анион. |
|
Катионные ПАВ: |
а) соли алифатических и ароматиче- |
ских аминов; |
б) соли алкилзамещенных четвер- |
тичных аммониевых оснований |
Неионные ПАВ:
ROH+nH2C CH2 RO(OCH2CH2)nH
RO(OCH2CH2)nH
O
Коллоидные ПАВ – все типы ПАВ, способные к мицеллообразованию при достижении ККМ.
Истинно растворимые ПАВ – ни при каких концентрациях не образуют мицелл.
|
|
Амфотерные ПАВ: |
|
|
|
|
|
ОН- |
Н+ |
|
|
8 |
|
RNH(CH ) COO- RNH(CH ) COOH |
RN+H (CH ) COOH |
|
|
|
2 n |
2 n |
2 |
2 |
n |
|
Лиофильные дисперсные системы (3)
Мицеллообразование в растворах ПАВ. Солюбилизация
Строение мицелл (схемы)
Прямые мицеллы: |
Обратные мицеллы: |
полярные раство- |
неполярные раство- |
рители; числа аг- |
рители; числа агре- |
регации 50-500; |
гации 3-40; |
H < T S; S > 0, |
водородные связи; |
H ~ 0. |
H < T S; H < 0. |
|
|
ККМ – критическая концентрация мицеллообразования.
Изменение формы прямых мицелл
Мицеллы сферические (а), дискообразные (б) и цилиндрические (в).
Солюбилизация – явление растворения веществ в мицеллах ПАВ.
9
Лиофильные дисперсные системы (4)
Элементы термодинамики мицеллообразования
В соответствии с законом действия масс, процесс мицеллообразования можно представить так:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
mK + + nR− |
|
|
|
M (n−m)− |
|
Константа равновесия: |
|
K = |
|
aM |
= |
cM |
|
|
M |
|
|
am+ an− |
cm+ |
cn |
_ m+ |
n− |
|
|
|
|
|
K |
R |
|
K |
R |
|
|
K |
R |
Принимая, что
сПАВ = ККМ ; 1;
cK + = cR− = KKM ; aM =1
можно записать:
|
K = |
1 |
= ККМ −(n+m) |
|
ККМ n ККМ m |
|
|
|
Стандартная энергия Гиббса
мицеллообразования (на 1 моль ПАВ):
GM = − RTn ln K
|
|
|
|
|
|
|
|
|
|
|
|
|
|
G0 = |
RT |
ln KKM m+n = (1+ |
m |
)RT ln KKM |
|
|
|
|
M |
n |
|
|
|
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
d ln K |
|
|
|
m d ln KKM |
|
HM0 |
|
|
|
= − 1 |
+ |
|
|
|
= |
|
2 |
|
dT |
|
|
RT |
|
|
|
|
n dT |
|
|
|
|
|
m |
|
|
H 0 |
|
|
|
1 |
+ |
|
|
ln KKM = |
|
M + const |
|
|
|
|
|
|
|
n |
|
|
RT |
|
|
0 |
|
|
0 |
|
0 |
|
0 |
= |
HM0 |
− GM0 |
GM |
= HM |
−T SM |
; SM |
|
T |
|
|
|
|
|
|
|
|
|
|
S = −(1+ m)R[ln KKM +T ( d ln KKM )m ] |
n |
dT |
1.Неионное ПАВ: m = 0.
2.Ионное ПАВ, полная диссоциация: m = 0.
3.Ионное ПАВ, полная ассоциация в мицелле, но полная диссоциация в растворе: m = n.
4.Ионное ПАВ, реальный случай; 0,6<m/n<0,9.
10
Лиофильные дисперсные системы (5)
Методы определения ККМ
Все методы определения ККМ базируются на анализе зависимости какого-либо свойства раствора ПАВ от его концентрации.
τ – мутность; n – коэффициент преломления; π – осмотическое давление; λ – эквивалентная электропроводность; σ – поверхностное натяжение.
Зависимость удельной электропроводности раствора ионного ПАВ от концентрации.
ККМ2 соответствует концентрации, при которой меняется форма мицелл.
11
Лиофильные дисперсные системы (6)
Факторы, влияющие на величину ККМ
• длина углеводородного радикала;
R 
 KKM
KKM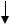
RT ln KKM = a −b n
•характер полярной группы (ионная или неионная);
•температура;
•введение неэлектролитов;
•введение индифферентных электролитов:
ln KKM = a − b n − k ln c
Определение мицеллярной массы методом Дебая
H (c − KKM ) |
= |
1 |
+ 2A (c − KKM ) |
|
|
− KKM |
2 |
МM |
12
Агрегативная устойчивость и коагуляция
дисперсных систем
(Лиофобные системы)
Лиофобные системы (1)
Процессы, которые могут протекать в дисперсных системах
Лиофобные системы (2)
Снижение Gs за счет уменьшения площади межфазной поверхности s

 Процессы укрупнения частиц
Процессы укрупнения частиц 

Изотермическая перегонка |
Коагуляция |
(перенос вещества от мелких |
(потеря агрегативной устойчивости |
частиц к крупным) |
из-за слипания или слияния частиц) |
Коалесценция – слияние частиц (характерно для капель эмульсий)
Гетерокоагуляция – слипание частиц различной природы
Флокуляция – образование агрегатов из частиц, разделенных прослойками среды (например, в присутствии полимеров)
Адагуляция – адгезионное взаимодействие |
|
частиц дисперсной фазы с макроповерхностью |
3 |
Лиофобные системы (3)
Факторы агрегативной устойчивости
Лиофобная дисперсная система, будучи термодинамически неустойчивой, может быть кинетически устойчивой благодаря наличию энергетического
барьера |
|
между |
частицами |
(барьера |
отталкивания). |
|
|
|
|
Из теории бинарных столкновений: |
|
|
d |
|
|
E |
|
|
|
− |
= Pk 2 exp − |
|
|
|
kБT |
|
|
d |
|
|
1. Быстрая (диффузионная) коагуляция: P = 1, Е = 0.
2. Медленная (барьерная) коагуляция: Е ≠ 0.
Все факторы, ведущие к снижению межфазного натяжения и возникновению энергетического (потенциального) барьера, являются факторами устойчивости.
Факторы устойчивости:
1.Электростатический (ионносольватный).
2.Адсорбционно-сольватный
3.Структурно-механический
4.Энтропийный
5.Гидродинамический
Агрегативная устойчивость реальных систем обеспечивается, как правило, несколькими факторами одновременно.
4




 RO(OCH
RO(OCH




 KKM
KKM




 Процессы укрупнения частиц
Процессы укрупнения частиц 

