
- •3. Вопросы для контрольной работы
- •4. Экзаменационные вопросы
- •История развития экологии.
- •Предмет и задачи экологии. Взаимосвязь с другими биологическими науками.
- •Уровни организации живых систем. Принцип эмерджентности.
- •Клеточные Системы Экосистемы
- •Основные разделы экологии.
- •Методы экологических исследований.
- •6. Математические методы и моделирование. Системный подход к изучению экологии.
- •7. Экология как теоретическая основа охраны природы. Классификация природных ресурсов.
- •8. Экология и здоровье человека.
- •9. Экология как элемент мировоззрения. Экология и политика.
- •10. Экология как теоретическая основа сельского хозяйства.
- •Среда и условия существования особей.
- •12. Классификация экологических факторов.
- •13. Закон толерантности Шелфорда.
- •14. Экологическая пластичность видов.
- •15. Взаимодействие экологических факторов. Закон минимума Либиха.
- •16. Правило Алехина.
- •17. Законы Коммонера.
- •18. Свет как экологический фактор.
- •19. Отношение животных и растений к свету.
- •20. Фотопериодизм.
- •21. Температура как экологический фактор.
- •22. Отношение растений и животных к температуре.
- •23. Правило Бергмана. Правило Аллена.
- •24. Влажность как экологический фактор.
- •25. Отношение растений и животных к влаге.
- •26. Эдафический фактор.
- •27. Физические и химические свойства почв и их экологическое значение.
- •28. Отношение растений и животных к почве.
- •29. Воздух как экологический фактор.
- •30. Биологические ритмы.
- •31. Термопериодизм.
- •32. Приспособленность организмов к неблагоприятным природным факторам.
- •33. Представление об экологической нише. Правило обязательного заполнения экологических ниш.
- •34. Понятие о популяциях.
- •35. Численность и плотность популяций.
- •36. Рождаемость и смертность популяций.
- •37. Скорость роста популяций.
- •39. Причины колебания численности популяций.
- •40. Этологическая структура популяций.
- •41. Экологическая структура популяций.
- •42. Эффект группы. Принцип Олли.
- •43. Полиморфизм популяций.
- •Типы взаимодействия между видами.
- •Конкуренция.
- •Аменсализм.
- •Комменсализм.
- •Паразитизм.
- •Протокооперация.
- •Мутуализм.
- •Хищничество.
- •Математические модели Лотки – Вольтерры. Принцип конкурентного исключения Гаузе.
- •Основные понятия синэкологии.
- •Видовое разнообразие биоценозов и факторы, его определяющие. Правило Дарлингтона.
- •Меры видового разнообразия.
- •Экотоны и понятие краевого эффекта.
- •Видовая структура биоценоза.
- •Понятие о консорциях.
- •Пространственная структура биоценозов.
- •Экологическая структура биоценозов.
- •Простые и сложные экосистемы.
- •Энергетика экосистем.
- •Цепи и циклы питания.
- •Экологическая пирамида.
- •Правило 10 %. Правило 1 %.
- •Биологическая продуктивность экосистем.
- •Сукцессии. Концепции климакса.
- •Стабильные и нестабильные экосистемы.
- •Энергетическая классификация экосистем.
- •Жизненные формы растений.
- •Жизненные формы животных.
- •Наземные экосистемы.
- •Тундра.
- •Хвойные леса.
- •Листопадные леса умеренной зоны.
- •Пустыни.
- •Саванны.
- •Чапараль.
- •Полувечнозеленый тропический лес.
- •Вечнозеленый тропический лес.
- •Лентические экосистемы.
- •Лотические экосистемы.
- •Заболоченные угодья.
- •Открытый океан.
- •Воды континентального шельфа.
- •Районы апвеллинга.
- •Эстуарии.
- •Понятие об ареале. Типы ареалов.
- •Космополиты. Эндемики. Реликты.
- •Химический состав биосферы.
- •Круговорот воды.
- •Круговорот углерода.
- •Круговорот кислорода.
- •Круговорот фосфора.
- •Круговорот азота.
- •Учение в. И. Вернадского о биосфере.
- •Роль живого вещества в биосфере.
- •Возникновение и состав биосферы.
- •Возникновение и развитие ноосферы.
- •Современные экологические проблемы Республики Беларусь.
- •Биоразнообразие Республики Беларусь.
Круговорот углерода.
Восполнение
ресурсов
СОа
процессе
человеческой
Равновесие
атмосфера - вода
Рис.
23.
Круговорот углерода в биосфере![]()



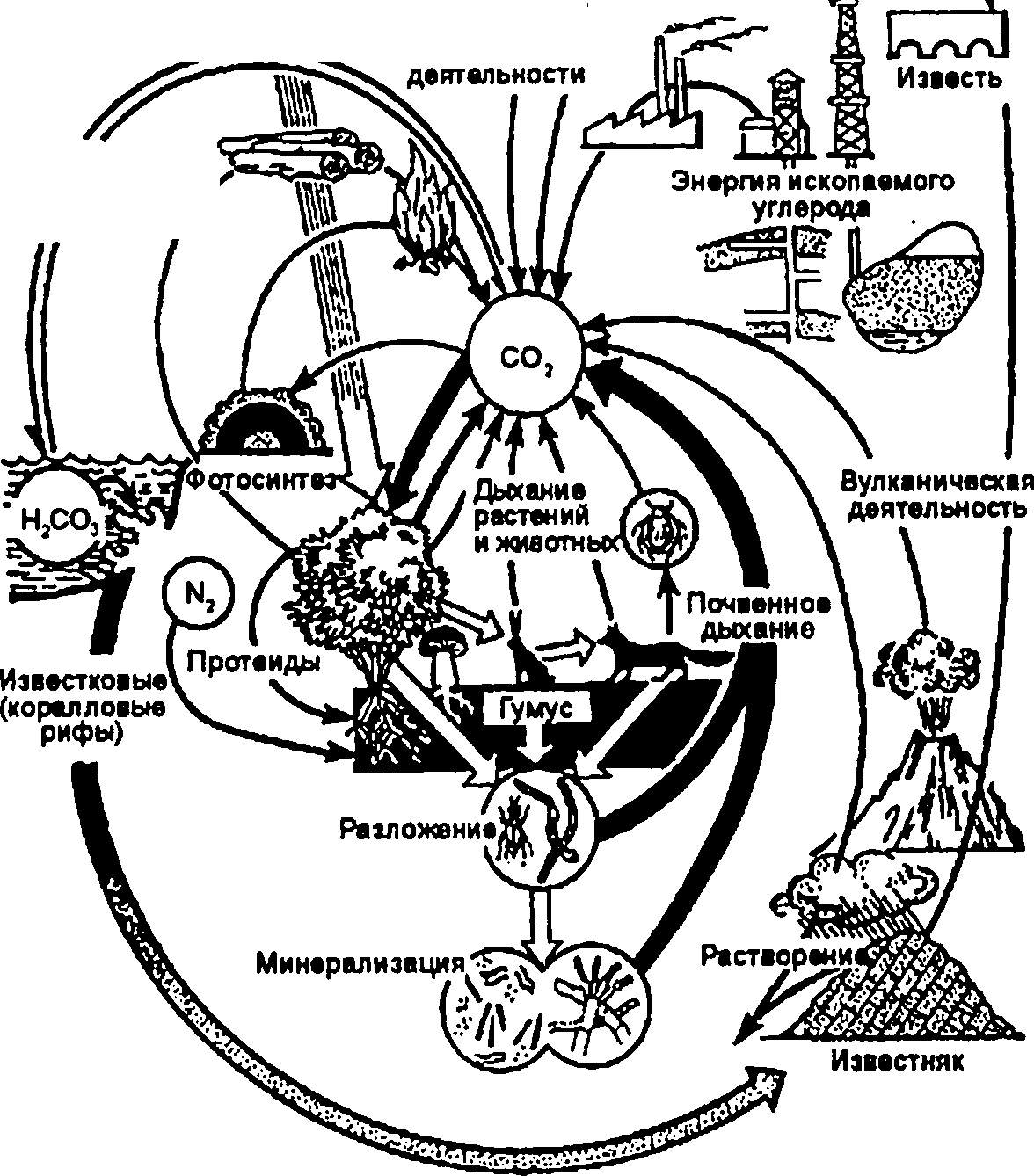
В.И. Вернадский в своем труде о биосфере писал: «Преобладающее, особое значение атомов углерода свойственно не только живым организмам, это свойство биосферы, ее живой и косной материи, до известной степени всей земной коры». С углеродом связан процесс возникновения и развития жизни на Земле. В атмосфере его содержится 0,046 % в форме углекислого газа и 0,00012 % в форме метана; в земной коре - 0,35 % и в живом веществе - около 18 %. Он вовлекается в цепь непрерывных реакций и биогеохимических круговоротов, соединяясь с большинством элементов самыми разнообразными способами. В то же время связь атомов углерода между собой и с другими атомами (кислорода, водорода, серы, фосфора и др.) может быть разрушена под воздействием природных факторов.
Предполагается, что углерод распределен в довольно тонком слое земной коры, в атмосфере в виде диоксида и оксида углерода и в животной и растительной биомассах. Основные запасы углерода в природе содержатся в минералах и горных породах главным образом в форме карбонатов (СаС03) и гидрокарбонатов (Са(НС03))2, представляющих собой растворимые и нерастворимые донные отложения в Мировом океане, накопившиеся за миллионы лет геологической истории Земли. Этот процесс продолжается и в настоящее время.
В несвязанном состоянии углерод встречается в виде алмазов (наибольшие месторождения в Южной Африке и Бразилии) и графита (наибольшие месторождения в Германии, Шри-Ланке и России). Каменный уголь содержит до 90 % углерода. В связанном состоянии углерод входит также в разные горючие ископаемые, в карбонатные минералы, например в кальцит и доломит, а также в состав всех биологических веществ.
Углекислый газ, содержащийся в воздухе и воде, составляет запас углерода, участвующего в создании биомассы. Содержание С02 в атмосфере нестабильно (менее 1 %), и подвержено сезонным изменениям. В настоящее время наблюдается его увеличение, связанное с антропогенным воздействием. Если 100 лет назад содержание углекислого газа составляло примерно 270 частей на 1 млн, то сегодня эта цифра выросла до 350 частей на 1 млн.
Также постепенно растет (на 1-2 % ежегодно) содержание в атмосфере метана и оксида углерода, что тоже связано с сельским хозяйством и энергетикой. В тех районах, где в процессе выработки энергии потребляется большое количество ископаемого топлива, зарегистрирован небольшой, но неуклонный рост концентрации оксидов азота и серы.
Если сравнить содержание диоксида углерода в водах (реки, озера, моря), атмосфере и океане, то окажется, что Мировой океан содержит более 98 % общего запаса углерода атмосферы и гидросферы.
Следует подчеркнуть, что цикл биологического круговорота углерода не замкнут. Углерод может выходить из него на довольно длительный срок в виде карбонатов, торфов, сапро- пелей, гумуса и других органических осадков. В разных циклах биологического круговорота участвует около 98-99 % ассимилированного углерода.
Если в круговороте кислорода зеленые растения являются его поставщиком в атмосферу, то в круговороте углерода они являются мощным механизмом, улавливающим его из атмосферы в виде углекислого газа и связывающим в органические соединения. В процессе фотосинтеза углерод ассимилируется растениями и переводится в углеводы. В процессе же дыхания происходит обратный процесс: углерод органических соединений превращается в диоксид углерода.
Ежегодно наземные растения связывают около 18 млрд т углерода, растения морей - 25 млрд т. Еще одним мощным утилизатором углерода являются морские организмы, которые используют его для образования своих скелетов. В дальнейшем остатки отмерших морских организмов опускаются на дно морей и океанов и образуют мощные отложения известняков. Между углекислым газом атмосферы и водой океана существует подвижное равновесие. Организмы поглощают углекислый кальций, создают свои скелеты, а затем из них образуются пласты известняков.
Наличие углерода непосредственно связано с наличием кислорода, поскольку на каждую молекулу кислорода должна где-то существовать и молекула восстановленного углерода. Это позволяет оценивать запасы углерода в биосфере величиной порядка 2-1015—2-1016 т. Казалось бы, такого количества углерода должно хватить на многие миллионы лет. Так оно и есть. Сложность, однако, в том, что большая часть этого элемента распылена. А то, что мы извлекаем на поверхность Земли в виде угля, нефти и других полезных ископаемых, это лишь малая доля общего количества восстановленного углерода в осадочных породах.
В воде углекислый газ растворяется в 35 раз лучше кислорода. От его содержания зависит количество растворенных гидрокарбонатов, т.е. жесткость воды. Если содержание С02 в воде уменьшается, то выпадает осадок нерастворенного карбоната, который будет растворен при восстановлении равновесия между углекислым газом и гидрокарбонатом.
В технике и быту нарушение углекислотного равновесия приводит к образованию накипи в котлах ТЭЦ и других системах, использующих воду. В природных условиях результатом этой реакции является образование полостей в земной коре, сталактитов и сталагмитов.
