
- •Глава 1. Основы металловедения
- •Кристаллизация и структура металлов
- •Строение металла
- •1.1.2. Кристаллизация металла
- •1.1.3. Изменение структуры металла
- •1.1.4. Изучение структуры металла
- •1.2. Строение сплавов
- •1.2.1. Правило фаз
- •1.2.2. Сплав - механическая смесь
- •1.2.3. Сплав - твердый раствор
- •1.2.4. Сплав - химическое соединение
- •1.2.5. Тройные сплавы
- •1.2.6. Электролитические сплавы
- •1.3. Свойства сплавов
- •Глава 2. Коррозия металлов
- •2.1. Определение и методы исследования коррозии
- •2.1.1. Классификация коррозионных процессов
- •2.1.2. Методы оценки коррозии
- •2.1.3. Методы коррозионных исследований
- •2.2. Химическая коррозия
- •2.2.1. Внешние факторы газовой коррозии
- •2.2.2. Оксидные пленки
- •2.2.3. Методы защиты от газовой коррозии
- •2.2.4. Коррозия в неэлектролитах
- •2.3. Электрохимическая коррозия
- •2.3.1. Причины возникновения коррозии
- •2.3.2. Коррозионная диаграмма Эванса
- •2.3.3. Коррозия с водородной и кислородной деполяризацией
- •2.3.4. Влияние внешних факторов на скорость коррозии
- •2.3.5. Влияние внутренних факторов на скорость коррозии
- •2.3.6. Атмосферная коррозия
- •2.3.7. Морская коррозия
- •2.3.8. Подземная коррозия
- •2.3.9. Электрокоррозия
- •2.4. Методы защиты от электрохимической коррозии
- •2.4.1. Обработка коррозионной среды
- •2.4.2. Катодная защита
- •2.4.3. Протекторная защита
- •2.4.4. Анодная защита
- •Глава 3. Коррозионные процессы в нефтегазовом комплексе и методы предотвращения коррозии
- •3.1. Особенности эксплуатации металлов в процессе транспортировки и хранения нефти, нефтепродуктов и газа
- •3.2. Коррозия металлов при контактировании с нефтепродуктами
- •3.3. Рациональный выбор конструкционных материалов
- •3.4. Применение органических покрытий с целью предотвращения коррозии газонефтепроводов
- •3.5. Методы электрохимической защиты трубопроводов
- •3.6. Защита трубопроводов от блуждающих токов
- •3.7. Методы защиты трубопроводов от внутренней коррозии
- •Глава 1. Основы металловедения…………………….4
- •Глава 2.Коррозия металлов……………………………...41
- •Глава 3. Коррозионные процессы в нефтегазовом комплексе и методы предотвращения коррозии……………………………………………….……109
- •394026 Воронеж, Московский просп., 14
1.2.4. Сплав - химическое соединение
Этот тип сплавов характеризуется во всех случаях определенным химическим составом и дает упорядоченную решетку замещения (рис. 13, в). Химические соединения по сравнению с твердыми растворами обладают, как правило, повышенной твердостью и хрупкостью. Они образуются, если химические свойства, параметры решеток, природа компонентов имеют достаточно большие различия.
Далеко не всегда химические соединения образуются по законам валентности, которые соблюдены в таких соединениях, как FеО, Cu3Р, Мg2Si. Так называемые электронные соединения (или фазы Юм - Розери) имеют лишь определенное соотношение числа валентных электронов к числу атомов z/n. Так, сплавы CuZn, АlСu3, Сu5Sn имеют отношение 3/2 и решетку объемноцентрированного куба, сплавы CuZn3, Cu3Sn - отношение 7/4 и гексагональную решетку. Эти сплавы имеют не вполне упорядоченную решетку замещения.
Соединения с фазами внедрения не подчиняются ни правилу валентности, ни правилу образования фаз Юм - Розери. Соединения этого типа образуют большую группу карбидов (Fе3С, ТiС, NbС, WС и др.) и нитридов (ТiN, ZrN, WN и др.).
Если компоненты системы образуют химическое соединение, его составу будет соответствовать максимум на диаграмме состояния и вертикальная линия превращения. Химическое соединение, устойчивое в интервале температуры от комнатной до температуры плавления, играет роль самостоятельного компонента и способно давать диаграммы состояния любого типа.
В качестве примера на рис. 17 дана диаграмма состояния системы А—В с химическим соединением состава АmВn. Диаграмма по существу состоит из двух систем: А - АmВn с образованием механической смеси с эвтектикой и АmВn - В, образующей твердый раствор с неограниченной растворимостью компонентов.

Рис. 17. Диаграмма состояния системы А-В с химическим соединением АmВn
Важно отметить, что химические соединения, как тела кристаллические, дают структуру, по существу не отличающуюся от структуры чистого металла.
1.2.5. Тройные сплавы
При построении диаграммы состояния тройной системы приходится иметь дело с тремя переменными - температурой и концентрациями двух компонентов А и В (концентрация третьего компонента выражена формулой С=100 – А - В). Следовательно, такая диаграмма должна быть пространственной.
Существует не одна система графического построения диаграммы. Идея каждой из них заключается в том, что на поверхности геометрической фигуры (прямоугольный треугольник, равносторонний треугольник) строятся точки, отвечающие тому или иному составу сплава, а на перпендикулярах к поверхности откладываются значения температуры того или иного фазового превращения в сплаве. Геометрическое место точек образует соответствующую поверхность раздела областей превращения. Наиболее распространенный метод использует в качестве основания равносторонний треугольник, который называется концентрационным (рис.18).
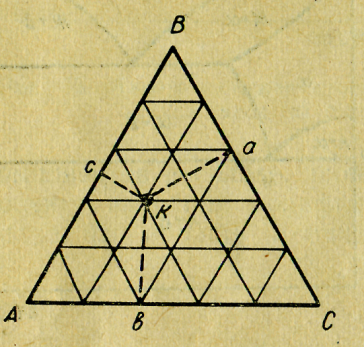
Рис. 18. Концентрационный равносторонний треугольник
Каждая из вершин треугольника отвечает чистым компонентам А, В и С. Точки, лежащие на сторонах треугольника, соответствуют частным случаям двухкомпонентных систем А - В, В - С или А - С. Точки, лежащие внутри треугольника, обозначают состав тройного сплава.
Для определения концентрации компонентов за 100% принимают высоту треугольника. Если теперь из данной фигуративной точки опустить перпендикуляр на каждую из сторон, то концентрация каждого из компонентов определится как длина перпендикуляра, опущенного на противоположную по отношению к определяемому компоненту сторону. Этот прием основан на теореме, согласно которой в равностороннем треугольнике сумма перпендикуляров, опущенных из любой точки на его стороны, равна высоте треугольника.
Диаграммы состояния тройных сплавов весьма сложны и в построении, и в изучении. Простейшая диаграмма состояния сплава - твердого раствора с неограниченной взаимной растворимостью компонентов показана на рис. 22. Из рисунка видно, что сферические поверхности ликвидуса и солидуса имеют переменную кривизну. Найти точку начала и конца кристаллизации сплава произвольного состава при этом весьма трудно. Поэтому для практического использования строят плоскостные диаграммы. Для этого на концентрационный треугольник наносят проекции изотермических сечений плоскостей ликвидуса и солидуса. На рис. 19 показан принцип построения таких изотерм. Линия a1b1 - проекция изотермы ликвидуса ab при t1; линия с1d1 - проекция изотермы ликвидуса cd при t2.
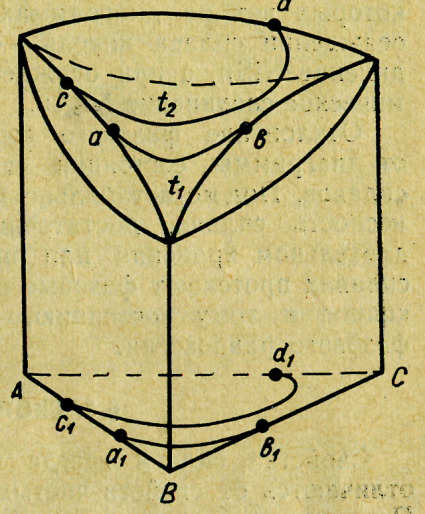
Рис. 19. Объемная диаграмма состояния тройного сплава твердого раствора с неограниченной растворимостью компонентов
Изучение тройных и более сложных систем позволяет решать важные практические задачи. В частности, именно благодаря изучению диаграмм состояния удалось раскрыть секрет легкоплавких сплавов.
Так, тройной сплав Розе (50% висмута, 31% свинца и 19% олова) плавится при 95°С, хотя компоненты имеют температуру плавления соответственно 271, 327 и 232°С, Оказалось, что этому составу отвечает эвтектический сплав системы, образующей механическую смесь. Незначительный сдвиг состава уводит от эвтектической температурой точки, и температура плавления резко возрастает.
