
- •Глава 1. Основы металловедения
- •Кристаллизация и структура металлов
- •Строение металла
- •1.1.2. Кристаллизация металла
- •1.1.3. Изменение структуры металла
- •1.1.4. Изучение структуры металла
- •1.2. Строение сплавов
- •1.2.1. Правило фаз
- •1.2.2. Сплав - механическая смесь
- •1.2.3. Сплав - твердый раствор
- •1.2.4. Сплав - химическое соединение
- •1.2.5. Тройные сплавы
- •1.2.6. Электролитические сплавы
- •1.3. Свойства сплавов
- •Глава 2. Коррозия металлов
- •2.1. Определение и методы исследования коррозии
- •2.1.1. Классификация коррозионных процессов
- •2.1.2. Методы оценки коррозии
- •2.1.3. Методы коррозионных исследований
- •2.2. Химическая коррозия
- •2.2.1. Внешние факторы газовой коррозии
- •2.2.2. Оксидные пленки
- •2.2.3. Методы защиты от газовой коррозии
- •2.2.4. Коррозия в неэлектролитах
- •2.3. Электрохимическая коррозия
- •2.3.1. Причины возникновения коррозии
- •2.3.2. Коррозионная диаграмма Эванса
- •2.3.3. Коррозия с водородной и кислородной деполяризацией
- •2.3.4. Влияние внешних факторов на скорость коррозии
- •2.3.5. Влияние внутренних факторов на скорость коррозии
- •2.3.6. Атмосферная коррозия
- •2.3.7. Морская коррозия
- •2.3.8. Подземная коррозия
- •2.3.9. Электрокоррозия
- •2.4. Методы защиты от электрохимической коррозии
- •2.4.1. Обработка коррозионной среды
- •2.4.2. Катодная защита
- •2.4.3. Протекторная защита
- •2.4.4. Анодная защита
- •Глава 3. Коррозионные процессы в нефтегазовом комплексе и методы предотвращения коррозии
- •3.1. Особенности эксплуатации металлов в процессе транспортировки и хранения нефти, нефтепродуктов и газа
- •3.2. Коррозия металлов при контактировании с нефтепродуктами
- •3.3. Рациональный выбор конструкционных материалов
- •3.4. Применение органических покрытий с целью предотвращения коррозии газонефтепроводов
- •3.5. Методы электрохимической защиты трубопроводов
- •3.6. Защита трубопроводов от блуждающих токов
- •3.7. Методы защиты трубопроводов от внутренней коррозии
- •Глава 1. Основы металловедения…………………….4
- •Глава 2.Коррозия металлов……………………………...41
- •Глава 3. Коррозионные процессы в нефтегазовом комплексе и методы предотвращения коррозии……………………………………………….……109
- •394026 Воронеж, Московский просп., 14
2.3.4. Влияние внешних факторов на скорость коррозии
Из внешних факторов, влияющих на скорость, вид и распространение коррозионного процесса, рассмотрим следующие: рН коррозионной среды, состав и концентрацию нейтральных растворов, концентрацию растворенного кислорода, скорость движения металла относительно среды, температуру среды.
Влияние рН среды. В каждом конкретном случае вероятность коррозионного поведения того или иного металла в зависимости от рН среды можно проследить по соответствующей' диаграмме равновесный потенциал - рН при комнатной температуре (диаграмма Пурбэ). Диаграммы обычно строят для ряда значений активности ионов металла (1, 10-2, 10-4 и 10-6 моль/л). Область потенциалов широка настолько, чтобы, на диаграмму можно было нанести все ионные равновесия, как окислительно-восстановительные, так и гидратообразования, отражающие образование всех возможных ионов или соединений с участием металла, в том числе при взаимодействии его с ионами Н+ и ОН-.
Диаграмма Пурбэ позволяет однозначно определить область коррозионной устойчивости, в которой металл термодинамически не способен окисляться; она позволяет также прогнозировать области пассивного и коррозионно активного состояния металла. Вместе с тем диаграмма далеко не всегда способна дать однозначный ответ о коррозионном поведении металла в силу того, что характеризует равновесное состояние системы, тогда как коррозионный процесс - всегда процесс неравновесный, подверженный влиянию многих кинетических факторов.
В общем случае коррозии с водородной деполяризацией повышение концентрации Н+ смещает катодный потенциал в положительную сторону, что должно увеличивать скорость коррозии. Но в сильнокислых растворах многое зависит от природы кислоты. Кислота может играть роль окислителя, вызывая пассивацию металла, как это происходит с железом в концентрированной Н2SО4. В других случаях кислота взаимодействует с металлом с образованием труднорастворимой защитной пленки соли. По причине образования МgF2 магний стоек в плавиковой кислоте, из-за образования Fе3(РО4)2 железо не корродирует в фосфорной кислоте.
Природа металла также достаточно четко проявляется во влиянии рН на скорость коррозии. По характеру этой зависимости при комнатной температуре металлы можно разбить на 5 групп (рис. 31).
Группа - благородные металлы (Pt, Au, Ag и др.) и в известной мере титан, на коррозию которых рН не оказывает влияния (рис. 31, а).
Группа II - амфотерные металлы, достаточно устойчивые в нейтральной области, но нестойкие в кислой и щелочной средах. Это цинк, алюминий, олово, свинец (рис. 31, б).
Группа III - молибден, вольфрам, тантал, вполне устойчивые в кислой и нейтральной областях рН, но заметно корродирующие в щелочной (рис. 31, в).
Группа IV - никель, кобальт, кадмий, скорость коррозии которых невелика и не зависит от рН в нейтральной и щелочной средах. В области малых значений рН подкисление увеличивает скорость коррозии (рис. 31, г).
Наконец,
металлы V
группы нестойки в кислой среде и умеренно
стойки в нейтральной. В нейтральной
области рН не влияет на скорость коррозии,
но при дальнейшем подщелачивании
скорость коррозии падает, достигая
минимума при рН 12![]() 14.
Это магний, марганец, хром, медь, железо
(рис. 31, д).
Особенность
железа проявляется в том, что при рН
выше 14 стойкость резко падает из-за
образования растворимого гипоферрита
НFеО2-.
14.
Это магний, марганец, хром, медь, железо
(рис. 31, д).
Особенность
железа проявляется в том, что при рН
выше 14 стойкость резко падает из-за
образования растворимого гипоферрита
НFеО2-.

Рис. 31. Влияние рН среды на скорость коррозии ряда металлов: a — благородные металлы; б — амфотерные металлы; в — молибден, вольфрам, тантал; г — никель, кобальт, кадмий; д — железо, марганец, хром
Влияние состава и концентрации нейтральных солей. Чаще всего в нейтральной среде протекает коррозия с кислородной деполяризацией. Влияние нейтральных солей на скорость коррозии проявляется через свойства образующихся продуктов коррозии. При образовании трудно растворимых соединений происходит частичное или полное экранирование поверхности металла, скорость коррозии падает. Например, углекислые соли калия или натрия образуют на поверхности цинка или железа осадок солей ZnСО3 или FеСО3; свинец в растворе сернокислой соли покрывается плотным слоем PbSО4. Соли могут образовывать на металле и оксидные слои, пассивирующие поверхность. К пассиваторам относятся KCrO4, K2Cr2O7, KMnO4 и др.
Нитраты, хлориды и нередко сульфаты, наоборот, обычно образуют растворимые соединения, не способные замедлять процесс. Хлориды, кроме того, наряду с другими солями галогеноводородных кислот обладают способностью активировать поверхность, что ускоряет скорость коррозии. Активирующий эффект возрастает в ряду J- - Br- - Cl- - F-.
Влияние состава солей, склонных к гидролизу (например, АlСl3, СН3СОONa) определяется тем, в какую сторону в результате гидролиза будет изменяться рН среды.
Концентрация нейтральных солей также влияет на скорость коррозии. Как видно из рис. 32 и 33, повышение концентрации до некоторых значений увеличивает скорость процесса.
.

Рис. 32. Влияние концентрации нейтральных солей на скорость коррозии стали
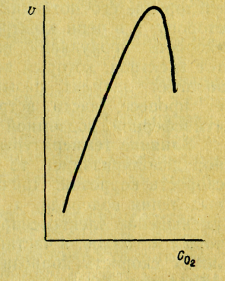
Рис. 33. Влияние концентрации кислорода на скорость коррозии железа в дистиллированной воде
Влияние кислорода. Скорость коррозии металлов в нейтральной среде существенно зависит от концентрации растворенного в коррозионной среде кислорода, который обеспечивает протекание катодного процесса. Источником кислорода в подавляющем большинстве случаев является воздух. Влияние кислорода на коррозию косвенно наблюдается на рис. 32. Более четко эта связь видна на рис. 33, на котором показана зависимость скорости коррозии стали в дистиллированной воде от содержания в ней кислорода. Скорость коррозии прямо пропорциональна концентрации кислорода, что отвечает механизму диффузионной кинетики электрохимического процесса. Прямая зависимость наблюдается до тех пор, пока слишком высокая концентрация кислорода не приводит к пассивации поверхности металла. Содержание кислорода в коррозионной среде в свою очередь зависит как от состава и концентрации солей, так и от температуры, условий перемешивания и других факторов, определяющих растворимость кислорода.
Неравномерное поступление кислорода к поверхности металла (неравномерная или дифференциальная аэрация) способно вызвать энергичную местную коррозию, скорость которой будет определяться степенью неравномерности. Эффект неравномерной аэрации демонстрирует знаменитый опыт Эванса. Два совершенно одинаковых стальных электрода, соединенных миллиамперметром, помещаются в сосуд с 3%-ным раствором хлористого натрия. Электроды отделены один от другого пористой диафрагмой. Если теперь у поверхности одного из электродов при помощи барботера воздуха повышать концентрацию кислорода, его потенциал начнет смещаться в положительную сторону, а в цепи электродов появится ток коррозии. Чем выше скорость продувания воздуха, тем энергичнее корродирует тот электрод, который не подвергается аэрации. Такой коррозионный элемент называется аэрационным. Он моделирует процесс, часто встречающийся на практике в условиях атмосферной, подземной или морской коррозии.
Влияние температуры. Если коррозия протекает с водородной деполяризацией, то рост температуры должен увеличивать скорость коррозии. Причина этому снижение перенапряжения выделения водорода, а также ускорение диффузии, уменьшение электросопротивления среды. При коррозии некоторых металлов, в частности стали, в азотной или соляной кислотах скорость коррозии связана с температурой уравнением Аррениуса.
Скорость коррозии с кислородной деполяризацией, как сильно зависящая от концентрации кислорода, с ростом температуры может замедляться. Повышение температуры настолько снижает растворимость кислорода в электролитах, что это обстоятельство оказывается решающим.
В отдельных случаях повышение температуры может привести к пассивации металла. Так, цинк в дистиллированной воде до 50°С достаточно хорошо защищен пленкой гидроксида цинка, при температуре около 60 °С происходит депассивация поверхности, но в дальнейшем, в интервале 90 - 100 °С, снова наступает устойчивая пассивация, и коррозия почти прекращается.
Влияние скорости движения коррозионной среды. Влияние скорости движения коррозионной среды на скорость разрушения металла особенно четко проявляется при коррозии с кислородной деполяризацией. Движение раствора способствует повышению концентрации кислорода в приэлектродном слое, а также удалению продуктов коррозии, способных пассивировать поверхность. Все это увеличивает скорость коррозии. При значительных скоростях возможна и пассивация поверхности за счет слишком высокой концентрации кислорода. Наконец, при еще большем повышении скорости движения среды появляются очаги коррозионной эрозии как результат комбинированного воздействия процессов электрохимического и механического разрушения металла. При этом безразлично, идет ли речь о движении коррозионной среды относительно металла (транспортировка электролита по трубопроводу) или о движении металла относительно коррозионной среды (движущееся судно).
