
- •Лекции №35-37 Карбонильные соединения. Альдегиды и кетоны
- •Изомерия и номенклатура предельных альдегидов и кетонов
- •Методы получения альдегидов и кетонов
- •Физические свойства
- •Химические свойства альдегидов и кетонов
- •Реакции нуклеофильного присоединения по карбонильной группе
- •Реакционная способность карбонильных соединений
- •Кето–енольная таутомерия, катализируемая основаниями и кислотами
- •1. Галогенирование.
- •2. Альдольная конденсация
- •Альдольная конденсация кетонов
- •3. Реакции изотопного обмена.
- •4. Рацемизация оптически активных кетонов
- •Реакции восстановления
- •Реакции окисления карбонильных соединений
- •Реакции окислительно-восстановительного диспропорционирования
- •Аминометилирование по Манниху
Реакционная способность карбонильных соединений
в реакциях нуклеофильного присоединения
Скорость-определяющей
стадией реакций нуклеофильного
присоединения по карбонильной группе
является бимолекулярная атака реакционного
центра субстрата нуклеофилом. Поэтому
успех реакции определяется величиной
частичного положительного заряда на
карбонильном углероде и его пространственной
доступностью. Поэтому реакционная
способность карбонильных соединений
падает по мере увеличения длины и
разветвленности алкильного радикала
при к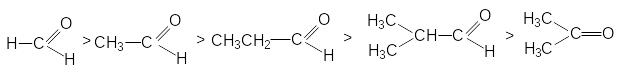 арбонильном
углероде, а также при переходе от
альдегидов к кетонам:
арбонильном
углероде, а также при переходе от
альдегидов к кетонам:
Можно видеть, что такое влияние связано с увеличением в этом ряду положительного индуктивного эффекта алкильных групп и с возрастанием пространственных препятствий для атаки на карбонильный углерод.
Кето–енольная таутомерия, катализируемая основаниями и кислотами
Кето-енольная таутомерия – форма изомерии, в которой изомеры (таутомеры) отличаются между собой расположением атомов водорода и кратностью связей между другими атомами.
Для карбонильных соединений характерна таутомерия в связи с кислотными свойствами атомов водорода при -углеродном атоме и основностью карбонильного кислорода. Исходная карбонильная форма называется кето-формой, а его таутомер – енольной формой.
R-CH2CHO R-CH=CH-OH
кето-форма енольная форма
Взаимный переход таутомеров также называется кето-енольной таутомерией. Эта реакция катализируется основаниями и кислотами.
Основно-каталитическая реакция:
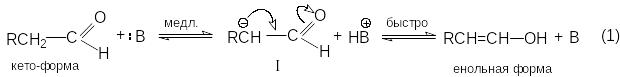
Кислотно-каталитическая реакция
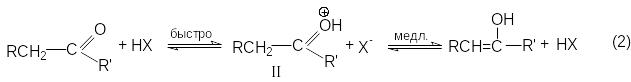
Присоединение протона к кислороду карбонильной группы резко облегчает отрыв протона от -углеродного атома вследствие большей электроноакцепторной способности положительно заряженного кислорода.
Кето-енольная таутомерия играет важную роль во многих превращениях альдегидов и кетонов, так как енолы, а также интермедиаты I и II являются важнейшими интермедиатами в реакциях альдегидов и кетонов.
Рассмотрим некоторые из этих реакций:
1. Галогенирование.
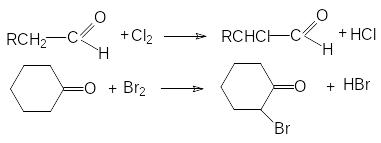 Результатом
галогенирования является замещение
водорода при -углеродном
атоме по отношению к карбонильной группе
Результатом
галогенирования является замещение
водорода при -углеродном
атоме по отношению к карбонильной группе
Важнейшими особенностями этих реакций являются:
– одно и то же карбонильное соединение реагирует со всеми галогенами с одинаковой скоростью при прочих равных условиях;
– скорость галогенирования не зависит от концентрации галогена;
– реакции катализируются кислотами и основаниями.
В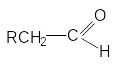 этой связи можно предположить, что
скорость-определяющей стадией этих
реакций является енолизация. Так как в
этой стадии галоген не участвует,
скорость реакции не зависит от природы
и концентрации галогена. В то же время
чувствительность реакции к ускорению
кислотами и основаниями является
признаком кето-енольной таутомерии.
этой связи можно предположить, что
скорость-определяющей стадией этих
реакций является енолизация. Так как в
этой стадии галоген не участвует,
скорость реакции не зависит от природы
и концентрации галогена. В то же время
чувствительность реакции к ускорению
кислотами и основаниями является
признаком кето-енольной таутомерии.
На примере альдегида основно-каталитическое галогенирование может быть представлено следующими стадиями
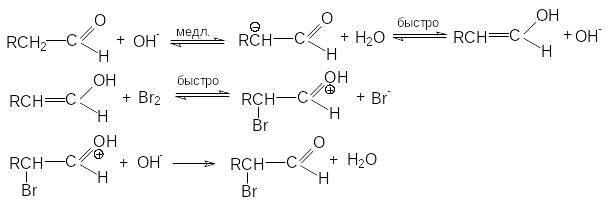
С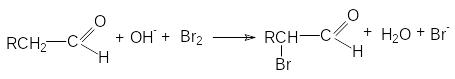 уммирование
левых и правых частей уравнения реакций
механизма приводит к стехиометрическому
уравнению
уммирование
левых и правых частей уравнения реакций
механизма приводит к стехиометрическому
уравнению
и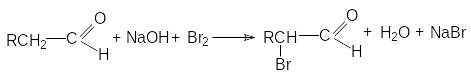 ли
ли
В результате введения в -положение карбонильного соединения электроноакцепторного атома галогена, следующий атом водорода при -углеродном атоме приобретает более высокую кислотность. Поэтому образующиеся моногалогенпроизводные реагируют быстрее в системе последовательных реакций
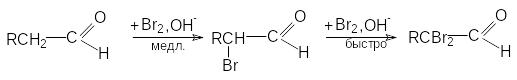
и реакцию трудно остановить на стадии образования моногалогенпроизводного в условиях основного катализа. Чтобы решить задачу получения моногалогенкарбонильного соединения реакцию необходимо проводить в условиях кислотного катализа.
Если объектом галогенирования является метилкетон или ацетальдегид, то из-за активирующего действия галогенов-заместителей на последующее галогенирование быстро образуется ,,-тригалогенпроизводное, которое легко расщепляется основанием:
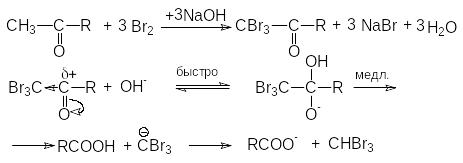
или суммарно:
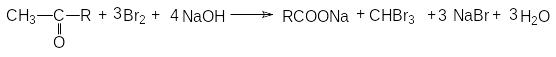
Приведенная последовательность реакций называется галоформной реакцией, поскольку в результате ее образуется хлороформ, бромоформ или иодоформ в зависимости от галогена, используемого при галогенировании. Галоформная реакция служит удобной качественной пробой на присутствие кетонов, особенно в случае иодирования, так как иодоформ представляет собой плохо растворимое вещество ярко-желтого цвета. Реакция оказывается удобной для синтеза карбоновых кислот в тех случаях, когда метилкетон более доступен, чем другие реагенты для синтеза кислот.
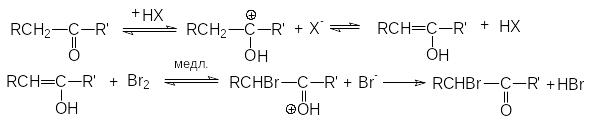
Кислотно-каталитическое галогенирование карбонильных соединений может быть представлено следующим механизмом:
Скорость-определяющая стадия этой реакции –электрофильное взаимодействие молекулярного брома с енольной формой карбонильного соединения. Очевидно, что введение в молекулу карбонильного соединения электроакцепторного атома галогена снижает реакционную способность енольной формы в реакциях электрофильного присоединения. Поэтому в условиях кислотного катализа можно с высоким выходом получать моногалогенпроизводные карбонильных соединений.
