
ХИНОНЫ
1. Классификация и номенклатура
Хиноны по своей структуре являются циклогексадиенонами, но их названия происходят от ароматических углеводородов: бензохинон от бензола, толухинон от толуола, нафтохинон от нафталина и т.д. Цифры в начале названия обозначают положение двух карбонильных групп.


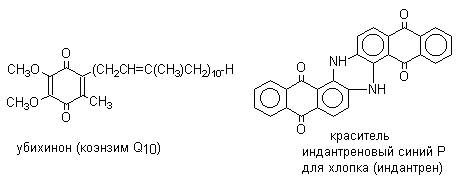
Многие производные хинонов составляют важную группу природных веществ - красителей, пигментов, антибиотиков, витаминов и т.д.
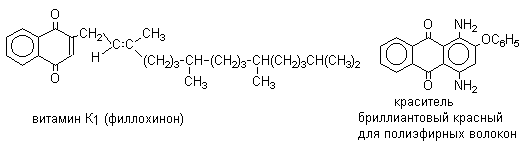
2. Методы получения
Хиноны получают окислением одно- и двухатомных фенолов, аминов и диаминов ароматического ряда. Самый удобный способ получения хинонов заключается в окислении одноатомных фенолов солью Фреми - нитрозодисульфонатом калия. Эта реакция осуществляется в исключительно мягких условиях в водном спирте или ацетоне, выход обычно превышает 90%.
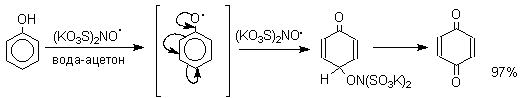
Приведенный на этой схеме циклогексадиеноновый интермедиат был выделен, что доказывает механизм одноэлектронного окисления фенолов солью Фреми. Другим одноэлектронным окислителем фенолов является карбонат серебра. Этот реагент, согласно данным последних лет, особенно пригоден для окисления 1,2-дигидроксибензола и его производных до орто-хинона.

Для окисления фенолов, ароматических аминов и гидрохинонов до 1,4-бензохинонов и 1,4-нафтохинонов часто используют реагенты на основе хрома (YI). К ним относятся оксид хрома (YI) в уксусной кислоте или реагент Килиани (дихромат натрия в серной кислоте), однако выходы хинонов, как правило, ниже, чем при окислении солью Фреми или карбонатом серебра.
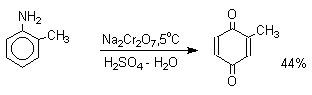

1,4-нафтохинон, 9,10-антрахинон и 9,10-фенантренхинон могут быть получены прямым окислением углеводородов оксидом хрома (YI) в уксусной кислоте или бихроматом натрия в серной кислоте.
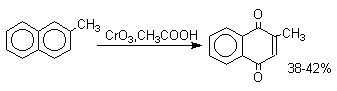
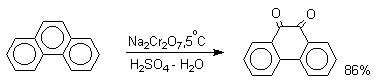
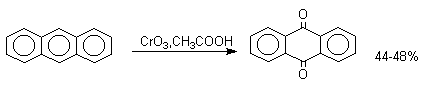
В промышленности тот же самый результат достигается при окислении кислородом в присутствии оксида ванадия (Y) как катализатора. Таким способом можно получать антрахинон и фенантренхинон.
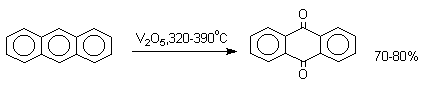
9,10-Антрахинон получают также ацилированием бензола фталевым ангидридом по Фриделю-Крафтсу с последующей циклизацией орто-бензоилбензойной кислоты.


Этот один из самых простых и старых способов промышленного получения антрахинона.
3. Физические свойства и строение
Хиноны – окрашенные кристаллические вещества. п-Бензохиноны окрашены в желтый цвет, о-бензохиноны – в красный, антрахиноны и фенантрахиноны – светло-желтые вещества.
Карбонильные группы оказывают значительное электроноакцепторное влияние, поэтому хиноны обладают электроноакцепторными свойствами. Электроноакцепторные свойства хинонв характеризуются сродством к электрону и восстановительным потенциалом (см. ниже). Сродство к электрону возрастает при введении электроноакцепторных заместителей и уменьшается при увеличении числа конденсированных циклов. о-Хиноны более сильные акцепторы, чем п-хиноны.
4. Химические свойства Восстановление и образование семихинонов
Наиболее важной реакцией хинонов является их восстановление до двухатомных фенолов. Восстановление хинонов осуществляется в две стадии. На первой стадии в результате одноэлектронного восстановления образуются анион-радикалы, которые называют семихинонами. Эти частицы могут быть легко зарегистрированы с помощью ЭПР-спекроскопии. На второй стадии анион-радикал присоединяет еще один электрон с образованием дианиона двухатомного фенола.
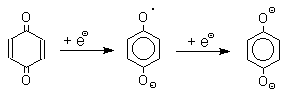
Способность хинона восстанавливаться до двухатомного фенола, т.е. свойство его как окислителя, оценивается с помощью нормального редокс-потенциала, определяемого из уравнения Нернста для реакции:

Величина Ео представляет собой нормальный потенциал, характерный для каждой системы хинон-гидрохинон, при равных концентрациях хинона и гидрохинона и концентрации ионов водорода, равной единице. Таким образом, Ео является количественной характеристикой окислительной способности хинона.
Величины нормальных редокс-потенциалов Ео некоторых хинонов в воде при 25оС
Хинон |
Ео в мв |
Хинон |
Ео в мв |
1,2-бензохинон |
783 |
2,3-дихлор-1,4-нафтохинон |
499 |
1,4-бензохинон |
700 |
9,10-антрахинон |
130 |
2-метил-1,4-бензохинон |
645 |
1,4-антрахинон |
400 |
2-хлор-1,4-бензохинон |
713 |
9,10-фенантренхинон |
440 |
1,2-нафтохинон |
566 |
1,4-фенантренхинон |
520 |
1,4-нафтохинон |
470 |
1,6-пиренхинон |
610 |
2,6-нафтохинон |
758 |
3,4,5,6-тетрахлор-1,4-бензохинон |
740 |
2-метил-1,4-нафтохинон |
422 |
дифенохинон |
954 |
Из данных, представленных в таблице следует, что 1,2-хиноны более сильные окислители, чем 1,4-хиноны, а бензохиноны превосходят по окислительной способности хиноны нафталинового ряда, которые в свою очередь превосходят антрахиноны и фенантренхиноны. Электроноакцепторные группы усиливают окислительные свойства хинонов. Высокие редокс-потенциалы хинонов определяются тем, что восстановление хинона в двухатомный фенол сопровождается превращением ненасыщенного кетона в ароматическое соединение.
Восстановление хинонов до двухатомных фенолов осложняется образованием хингидрона - аддукта состава 1:1 между хиноном и двухатомным фенолом. Хингидрон может быть окислен до хинона или нацело восстановлен до гидрохинона.
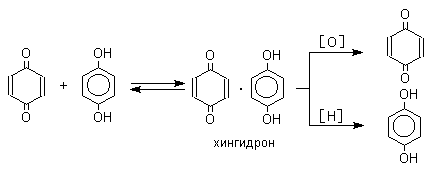
Окрашенный в темно-зеленый цвет хингидрон представляет собой классический пример молекулярных комплексов, где один компонент служит донором, а другой - является акцептором электрона. Такие комплексы, где происходит перекрывание ВЗМО донора и НСМО акцептора, получили название комплексов с переносом заряда. В кристаллах хингидрона молекулы хинона и гидрохинона чередуются и располагаются в двух параллельных плоскостях друг над другом. Комплексы с переносом заряда часто интенсивно окрашены. Окраска комплексов обусловлена переносом заряда от ароматического донора к акцептору, хотя степень переноса заряда невелика и редко превышает 0,1 заряда электрона.
Восстановление хинонов до двухатомных фенолов проводят с помощью самых разнообразных восстановителей, среди которых в лабораторных условиях предпочтение отдается дитиониту натрия Na2S2O4 в щелочной среде.

Помимо дитионита натрия в качестве восстановителей употребляются алюмогидрид лития и боргидрид натрия, хлорид олова (II) в соляной кислоте, цинк в уксусной кислоте и др. В промышленности восстановление 1,4-бензохинона до гидрохинона осуществляется с помощью оксида серы (IY) и железа в воде при 70-80оС.
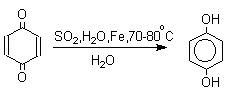
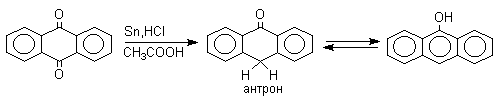
9,10-Антрахинон при восстановлении дитионитом натрия образует 9,10-антрадиол (антрагидрохинон).

При восстановлении 9,10-антрахинона оловом в смеси соляной и уксусной кислот получается антрон - простейший кетон ряда антрацена.
Производные 9,10-антрахинона широко используются в качестве синтетических антрахиноновых красителей для хлопка, шерсти и синтетических волокон. Эти красители отличаются яркостью цвета, высокой термической и фотохимической устойчивостью. Выше в качестве примера приведены формулы некоторых антрахиноновых красителей. Эти красители получают из 2-аминоантрахинона и его производных, например:
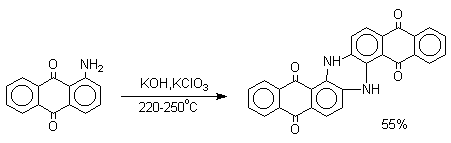
Восстановление антрахиноновых и других кубовых красителей дитионитом натрия в щелочной среде используется для перевода этих нерастворимых в воде соединений в так называемую лейкоформу, которая в виде динатриевой соли хорошо растворима в воде. Таким образом, например, упомянутый выше индантрен восстанавливают в тетрагидропроизводное, имеющее четыре фенольных гидроксила. Это лейкопроизводное хорошо растворимое в воде. Хлопчатобумажную ткань пропитывают раствором лейкоформы и выдерживают на воздухе. Лейкоформа окисляется кислородом до исходного красителя. Такой способ крашения гарантирует однородность окраски ткани.
Легкость восстановления хинонов до фенола открывает возможность для использования хинонов в качестве дегидрирующих агентов. Для этой цели выбирают хиноны с высоким окислительно-восстановительным потенциалом, такие как 2,3,5,6-тетрахлор-1,4-бензохинон (хлоранил); 2,3-дихлор-5,6-дициано-1,4-бензохинон (ДДХ), дифенохинон. 1,2-Хиноны ввиду нестабильности практически не используются в качестве дегидрирующих агентов. Дегидрированию подвергаются дигидроароматические соединения ряда бензола и тетрагидропроизводные ряда нафталина, антрацена, гетероциклических соединений, тропилиден и т.д.
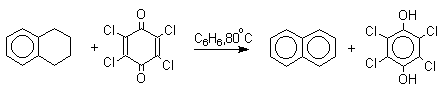
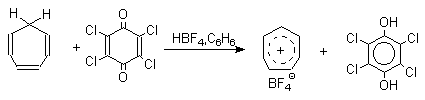
Механизм дегидрирования углеводородов заключается в отщеплении хиноном гидрид-иона с образованием карбокатиона, который стабилизируется отщеплением протона. Поэтому дегидрированию подвергаются углеводороды, которые при отщеплении гидрид-иона образуют сравнительно стабильные карбокатионы.
